El síndrome de Takotsubo es un importante diagnóstico diferencial en pacientes con síndrome coronario agudo y se asocia a un riesgo significativo de complicaciones potencialmente mortales. Afecta principalmente a las mujeres posmenopáusicas y a menudo existe un acontecimiento desencadenante previo. El pronóstico es comparable al de un infarto agudo de miocardio.
El síndrome de Takotsubo es un importante diagnóstico diferencial en pacientes con síndrome coronario agudo y se asocia a un riesgo significativo de complicaciones potencialmente mortales. En este artículo se resumen los aspectos esenciales de la enfermedad.
El síndrome de Takotsubo (STT) se caracteriza por una disfunción ventricular izquierda aguda pero completamente reversible que no se debe a una estenosis significativa de las arterias coronarias [1]. Es característica la llamativa distribución de las anomalías del movimiento de la pared con “abombamiento” regional del ventrículo izquierdo [1–3]. La enfermedad se describió por primera vez en Japón en 1990. Siguieron series de casos de Europa y Norteamérica más de diez años después de la primera descripción. Como resultado, la concienciación y el interés por el TTS aumentaron, lo que provocó un incremento significativo de artículos científicos en los últimos años. Aunque el término STT está bien establecido en la actualidad, en la literatura aún pueden encontrarse términos anteriores como “miocardiopatía de Takotsubo”, “síndrome del corazón roto”, “síndrome de abombamiento apical” o “miocardiopatía de estrés”.
Los pacientes con STT suelen presentar síntomas de angina de pecho y/o disnea y, por lo tanto, son indistinguibles de los pacientes con síndrome coronario agudo (SCA) en función de los síntomas [1,2]. Se supone que alrededor del 2% de todos los pacientes cuyos síntomas clínicos iniciales apuntan a un SCA padecen un TTS. Las mujeres se ven afectadas con mucha más frecuencia que los hombres [1–3]. En algunos colectivos, la proporción de mujeres supera el 90%, y las mujeres posmenopáusicas, en particular, corren un mayor riesgo de padecer TTS. Una característica particular del STT es un acontecimiento precipitante en el período previo al episodio, que puede encontrarse en aproximadamente dos tercios de los pacientes [1–3]. Este factor estresante puede ser tanto de naturaleza física como emocional, por lo que incluso los acontecimientos agradables pueden provocar un TTS (Tab. 1).
Aclaración diagnóstica
Debido a la presentación clínica de los pacientes con STT, el registro de un ECG es el primer paso en la elaboración del diagnóstico diferencial. Aquí, de forma similar a los pacientes con SCA, son posibles elevaciones del segmento ST, depresiones del segmento ST o negativizaciones de T [1]. Sin embargo, las alteraciones también pueden ser inespecíficas y un ECG sin alteraciones no descarta la STT. En algunos colectivos, los pacientes mostraron cambios periódicos en el ECG con elevaciones iniciales del segmento ST seguidas de negativizaciones T y prolongación QT en la fase subaguda.

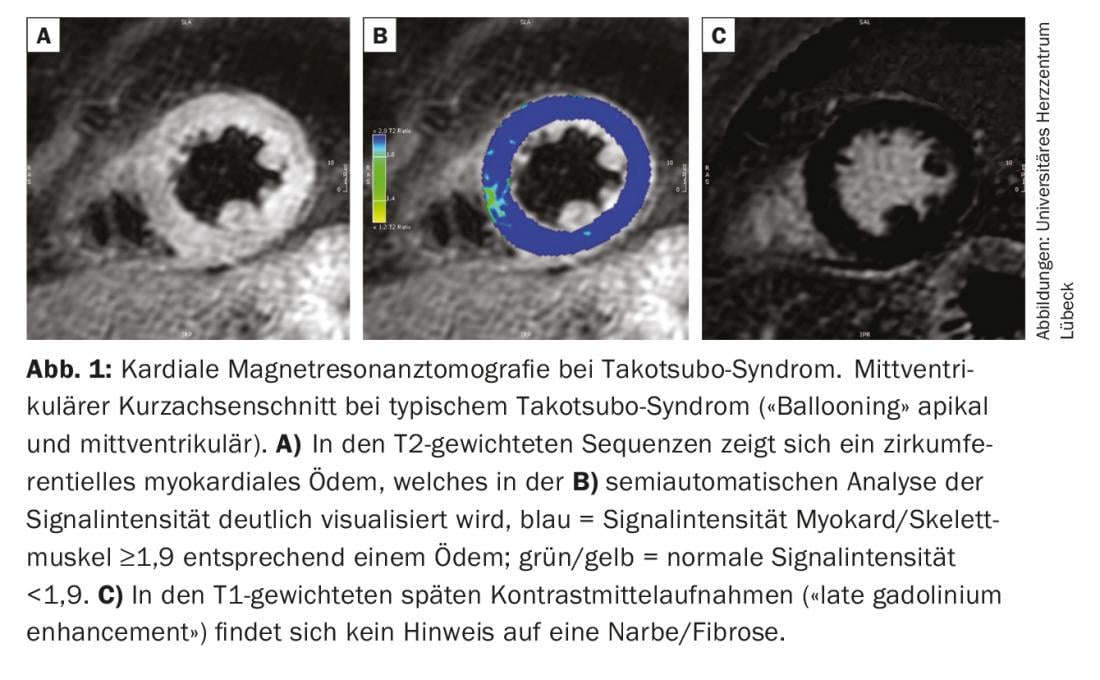
Los biomarcadores cardiacos (troponina, creatina cinasa) pueden estar moderadamente elevados en el contexto del STT, con niveles máximos que suelen ser significativamente inferiores a los de los pacientes con infarto agudo de miocardio [1]. Por el contrario, los pacientes con STC suelen tener concentraciones significativamente más elevadas de péptidos natriuréticos. Sin embargo, una diferenciación fiable entre un TTS y un ACS no es posible ni siquiera sobre la base de los parámetros químicos de laboratorio. Para ello, es absolutamente necesaria la realización de una angiografía coronaria. A diferencia del SCA, en los pacientes con STT no se encuentran estenosis coronarias que puedan explicar la magnitud de las alteraciones cinéticas [1]. El diagnóstico suele guiarse por la visualización de las anomalías características del movimiento de la pared ventricular izquierda mediante laevocardiografía o ecocardiografía. Los criterios necesarios para confirmar el STT se establecieron en una declaración de la Sociedad Europea de Cardiología y se resumen en la tabla 2 [1]. Dado que la reversibilidad de la disfunción ventricular izquierda forma parte explícitamente de la definición, el diagnóstico sólo puede hacerse definitivamente en el curso con la documentación de un retorno a la función sistólica normal. Sin embargo, esto puede llevar algunas semanas. La resonancia magnética cardiaca proporciona información adicional importante para confirmar el diagnóstico ya en la fase aguda. En el caso de la ETT, ésta suele mostrar edema miocárdico regional con signos de inflamación difusa sin evidencia de daño irreversible en forma de fibrosis o necrosis (Fig. 1) [2]. Así pues, la resonancia magnética proporciona una información diagnóstica diferencial importante para diferenciar el infarto de miocardio con lisis espontánea o la miocarditis y, por lo tanto, debe realizarse en todos los pacientes con STT dudosa si existe la posibilidad.
Formas del síndrome de Takotsubo
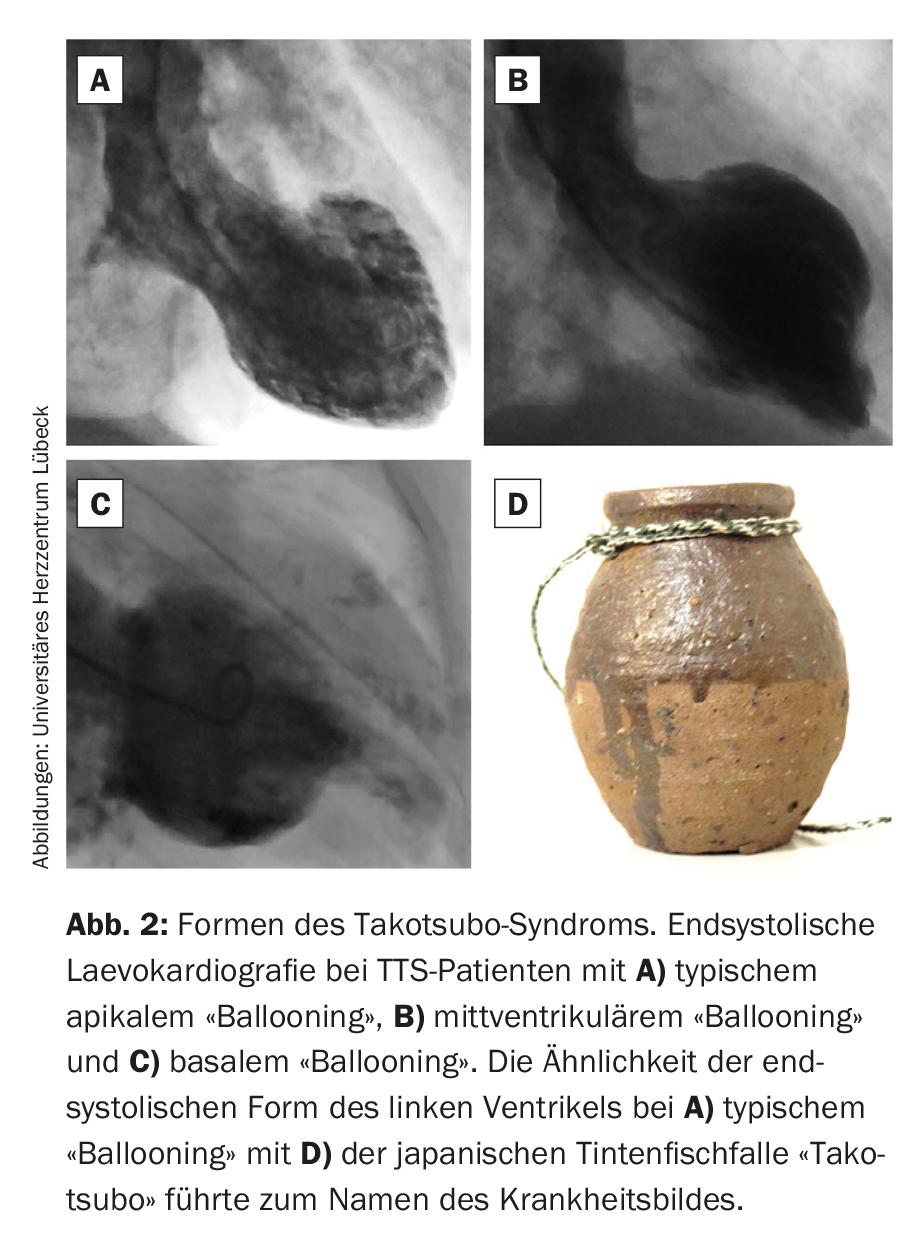
Basándose en la distribución de las alteraciones cinéticas del ventrículo izquierdo, se distinguen tres formas principales de STT (Fig. 2). La forma clásica, que es la más frecuente (aprox. 75%), se caracteriza por una hipercontractilidad basal con acinesia medioventricular y apical (típico “abombamiento” apical). El contorno telesistólico recordó al primer descriptor una trampa japonesa para pulpos con forma de jarra de fondo redondo y cuello corto (“takotsubo”). Esto dio lugar al nombre de la enfermedad. En las formas atípicas de STT, los tramos medioventriculares (“abombamiento” medioventricular, aproximadamente el 20% de los casos de STT) o basales (“abombamiento” basal, aproximadamente el 5% de los casos de STT) son hipo o acinéticos. Además, recientemente se ha descrito una forma focal muy poco frecuente de STT [3]. Sin embargo, debido a su extensión no circular, difiere fundamentalmente de las formas establecidas y requiere absolutamente un esclarecimiento diagnóstico diferencial preciso mediante resonancia magnética. Además del ventrículo izquierdo, el ventrículo derecho también se ve afectado por trastornos cinéticos en aproximadamente un tercio de los pacientes con STT, y también se han descrito formas aisladas del ventrículo derecho [1,2].
Fisiopatología
Se han propuesto numerosas teorías sobre la patogénesis del STT. Sin embargo, a pesar de los crecientes esfuerzos científicos, aún no se han aclarado definitivamente los mecanismos subyacentes. La observación de factores estresantes desencadenantes en un gran número de pacientes hizo suponer que el aumento de la actividad del sistema nervioso simpático y los niveles elevados de catecolaminas podrían desempeñar un papel protagonista en la fisiopatología [4]. Esta teoría se vio respaldada por la demostración de un aumento de los niveles de catecolaminas en el plasma de los pacientes con STT, por la observación de disfunción ventricular izquierda tras la administración externa de catecolaminas así como en pacientes con tumores productores de catecolaminas y por cambios morfológicos en los exámenes histológicos comparables a los efectos cardiotóxicos conocidos de las catecolaminas. Sin embargo, después de que no se encontraran acontecimientos desencadenantes y niveles elevados de catecolaminas en todos los pacientes con STT, también surgieron dudas sobre este modelo fisiopatológico. Además, los niveles sistémicamente elevados de catecolaminas no explican la sorprendente distribución de las anomalías del movimiento de la pared con afectación ocasional del ventrículo derecho.
Un concepto alternativo ve la causa principal del STT en los trastornos de la microcirculación coronaria, que se han demostrado en varios estudios de pacientes con STT utilizando una amplia gama de métodos. Así pues, aunque la aparición de alteraciones microcirculatorias en el contexto de la ETT es en gran medida indiscutible, sigue sin estar claro si la reducción del flujo coronario es causante de la enfermedad o es un fenómeno secundario debido a la disfunción ventricular izquierda. Estudios recientes también apuntan a una posible predisposición genética a la aparición del STT [5]. Sin embargo, para ello se necesitan más estudios sobre grandes colectivos de pacientes. Debido a su aparición predominante en mujeres posmenopáusicas, la posible influencia de los estrógenos también es objeto de investigación científica. Otros conceptos fisiopatológicos postulados, como la obstrucción del tracto de salida del ventrículo izquierdo, el vasoespasmo coronario, el puente muscular o la rotura de la placa con lisis espontánea del trombo, han sido refutados en estudios posteriores o parecen muy improbables debido a la baja prevalencia en pacientes con STT [6].
Terapia
Dado que no existen recomendaciones basadas en pruebas sobre la terapia para los pacientes con STT, las decisiones sobre el tratamiento se toman de forma individual. En la fase aguda de la enfermedad, la atención se centra en la monitorización cardiovascular continua y el tratamiento de cualquier complicación [1]. En la mayoría de los casos, el tratamiento de la insuficiencia cardiaca se inicia en función de los síntomas clínicos (inhibidores de la ECA, betabloqueantes, diuréticos si es necesario). En el curso, la normalización de la función ventricular izquierda así como los cambios del ECG se documentan mediante controles regulares. Es necesario un ajuste constante de la terapia farmacológica a la clínica actual.
Previsión
Debido a la regresión completa de las alteraciones cinéticas del ventrículo izquierdo, en un principio se consideró que los pacientes tras un TTS tenían un buen pronóstico. Sin embargo, esta suposición ha sido refutada por varios estudios en los últimos años. Éstos muestran tasas de mortalidad a corto y largo plazo similares o incluso superiores tras un TTS en comparación con los pacientes con infarto agudo de miocardio [3,7,8]. Pueden producirse complicaciones graves, especialmente durante la fase aguda de la enfermedad. Estos incluyen, entre otros, insuficiencia cardiaca grave con edema pulmonar hasta shock cardiogénico o arritmias cardiacas potencialmente mortales [9,10]. El riesgo de arritmias no debe subestimarse incluso en la fase subaguda hasta la completa normalización de la función ventricular izquierda y los cambios en el ECG (especialmente un tiempo QT posiblemente prolongado). En la evolución a largo plazo, las enfermedades concomitantes no cardiovasculares (por ejemplo, las neoplasias malignas) también contribuyen de forma decisiva al pronóstico [11]. Se han identificado numerosos factores de riesgo de acontecimientos adversos para la evaluación del pronóstico [1,7]. Entre ellos se incluyen la edad, el sexo masculino, los factores estresantes físicos, el grado de disfunción del ventrículo izquierdo y la afectación del ventrículo derecho. La tasa de recurrencia tras un episodio de TTS se sitúa entre el 5 y el 10%. Curiosamente, en el caso de episodios recurrentes de STT, un paciente puede mostrar diferentes formas de “abombamiento”.
Mensajes para llevarse a casa
- El STT es un importante diagnóstico diferencial en pacientes con sospecha de síndrome coronario agudo sin estenosis coronarias causales y se diagnostica mediante criterios específicos.
- Afecta principalmente a las mujeres posmenopáusicas y a menudo existe un acontecimiento desencadenante previo.
- La resonancia magnética cardiaca proporciona valiosa información adicional para confirmar el diagnóstico.
- El aumento de la actividad simpática y de los niveles de catecolaminas, las alteraciones de la microcirculación coronaria y una predisposición genética parecen desempeñar un papel fisiopatológico. Sin embargo, los mecanismos exactos de la enfermedad no se han aclarado definitivamente.
- A pesar de la normalización completa de la función ventricular izquierda, el pronóstico tras un TTS es comparable al de un infarto agudo de miocardio.
Literatura:
- Lyon AR, et al: Current state of knowledge on Takotsubo syndrome: a Position Statement from the Taskforce on Takotsubo Syndrome of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2016; 18: 8-27.
- Eitel I, et al: Características clínicas y hallazgos por resonancia magnética cardiovascular en la miocardiopatía de estrés (takotsubo). JAMA 2011; 306: 277-286.
- Templin C, et al: Características clínicas y resultados de la miocardiopatía de Takotsubo (por estrés). N Engl J Med 2015; 373: 929-938.
- Wittstein IS, et al: Características neurohumorales del aturdimiento miocárdico debido al estrés emocional súbito. N Engl J Med 2005; 352: 539-548.
- Eitel I, et al: Estudio de asociación de todo el genoma en el síndrome de takotsubo – Resultados preliminares y direcciones futuras. Int J Cardiol 2017; 236: 335-339.
- Eitel I, et al: Tomografía de coherencia óptica para evaluar la carga y la morfología de la placa en pacientes con síndrome de Takotsubo. J Am Heart Assoc 2016; 5(12). pii: e004474.
- Stiermaier T, et al: Exceso de mortalidad a largo plazo en la miocardiopatía takotsubo: predictores, causas y consecuencias clínicas. Eur J Heart Fail 2016; 18: 650-656.
- Redfors B, et al: La mortalidad en el síndrome de takotsubo es similar a la mortalidad en el infarto de miocardio – Un informe del registro SWEDEHEART. Int J Cardiol 2015; 185: 282-289.
- Stiermaier T, et al: Prevalencia e importancia clínica de las arritmias potencialmente mortales en la miocardiopatía de Takotsubo. J Am Coll Cardiol 2015; 65: 2148-2150.
- Stiermaier T, et al: Incidencia, factores determinantes y relevancia pronóstica del shock cardiogénico en pacientes con miocardiopatía de Takotsubo. Eur Heart J Acute Cardiovasc Care 2016; 5: 489-496.
- Moller C, et al.: Prevalencia e impacto pronóstico a largo plazo de la malignidad en pacientes con síndrome de Takotsubo. Eur J Heart Fail 2017. doi: 10.1002/ejhf.868. [Epub ahead of print].
CARDIOVASC 2018; 17(1): 4-7











