La epidemiología de las bacterias multirresistentes ha cambiado en Suiza: descenso significativo del SARM y fuerte aumento de las enterobacterias productoras de BLEE. Los gérmenes ESBL pueden adquirirse a través de los alimentos (carne de ave, verduras, etc.). Los viajeros que regresan y los pacientes repatriados del extranjero tienen un mayor riesgo de contraer microorganismos multirresistentes. Si no hay respuesta a la terapia antibiótica empírica, está indicado el esclarecimiento microbiológico debido a la posible resistencia. E. coli, incluidos los aislados ESBL, siguen siendo bien sensibles a la fosfomicina y la nitrofurantoína.
El aumento de la resistencia a los antibióticos amenaza muchos logros de la medicina moderna. Las autoridades sanitarias de la UE y de EE.UU. calculan cada una unas 25.000 muertes al año atribuibles a la resistencia a los antibióticos. Los pacientes están inquietos por las noticias de los medios de comunicación sobre infecciones bacterianas que ya no pueden tratarse.
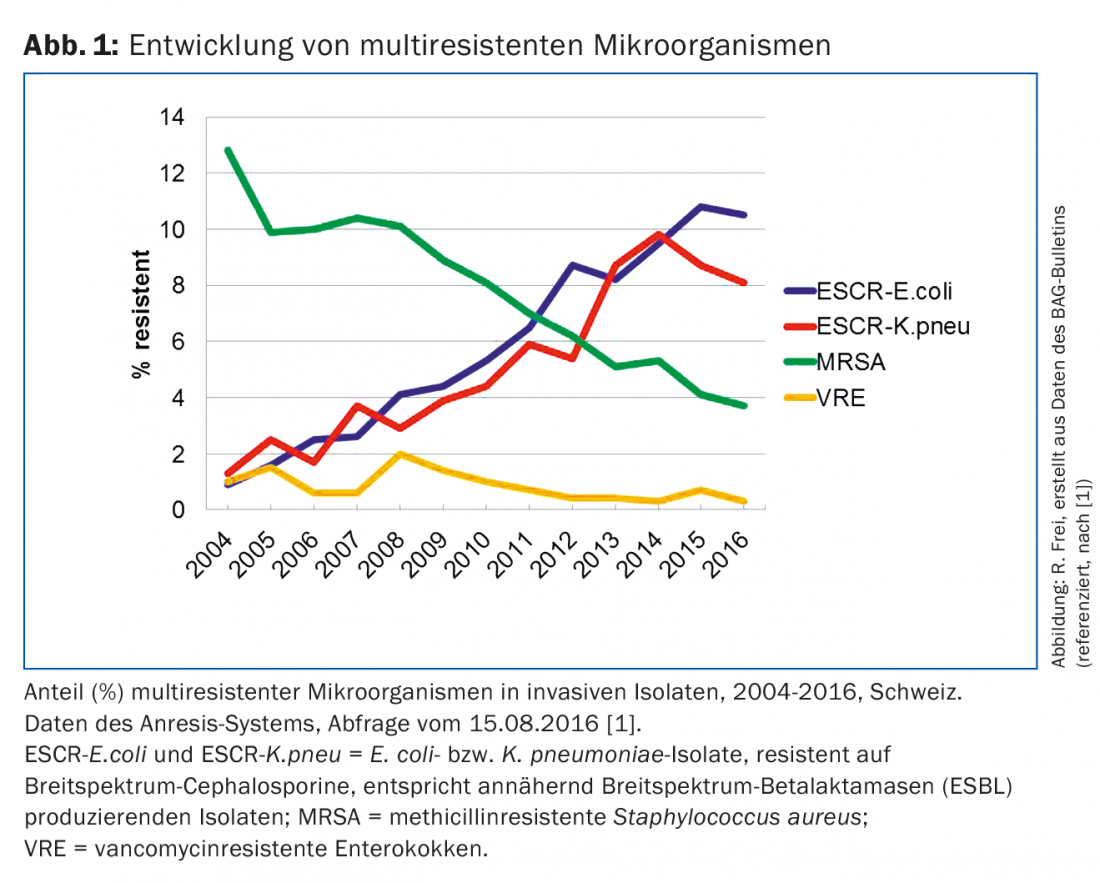
Las bacterias multirresistentes son resistentes a varias clases de antibióticos. Los microorganismos multirresistentes están causando grandes problemas en los hospitales de todo el mundo, entre ellos diversas enterobacterias, Pseudomonas aeruginosa, Acinetobacter baumannii, Staphylococcus aureus y enterococos. En comparación con muchos otros países, la mayoría de las tasas de resistencia en Suiza son más bajas. Un médico de atención primaria de este país se enfrenta principalmente a la Escherichia coli multirresistente , con menos frecuencia a otros aislados de enterobacterias resistentes y al S. aureus resistente a la meticilina (SARM). Sólo ocasionalmente entra en contacto con otros gérmenes multirresistentes, incluidos los patógenos resistentes campylobacter, gonococos y tuberculosis. Según el sistema de vigilancia suizo Anresis (www.anresis.ch), la prevalencia de bacterias multirresistentes ha evolucionado de forma diferente en los últimos 12 años [1]. Mientras que la proporción de aislados de SARM ha disminuido significativamente, las enterobacterias con resistencia a las cefalosporinas de amplio espectro y a otras clases de sustancias han aumentado de forma constante y pronunciada (Fig. 1) [1].
SARM
En 2015, algo menos del 6% de los aislados de S. aureus analizados en pacientes ambulatorios de la Suiza alemana seguían siendo resistentes a la meticilina (SARM). En cambio, en los países del sur y centro de Europa, la tasa de SARM fue significativamente superior, por ejemplo en Francia del 17%, en Italia del 34% y en Portugal incluso del 47%. En el pasado, el SARM se propagaba principalmente en hospitales y otras instituciones médicas (SARM asociado a la atención sanitaria). Desde hace varios años, están apareciendo nuevas cepas con características diferentes que pueden causar infecciones agresivas en pacientes ambulatorios, incluso en pacientes jóvenes sin contacto previo con el sistema sanitario (SARM asociado a la comunidad). En los últimos años, también se ha observado que las personas en estrecho contacto con animales tienen un mayor riesgo de ser portadoras del SARM. El SARM puede encontrarse en varios animales, especialmente en caballos y perros, pero sobre todo en animales de granja como pollos y cerdos [2]. En Suiza, la tasa de colonización por SARM en cerdos de engorde en el matadero ha aumentado desde 2009 del 2% al 26,5% en 2014. El responsable es una línea clonal de SARM (CC398), que también se encuentra con frecuencia en animales de granja de otros países europeos. Pertenece al SARM “asociado al ganado”, que afecta sobre todo a personas con contacto laboral con cerdos, como granjeros y veterinarios [3]. Otras personas que corren el riesgo de contraer infecciones por SARM son las personas y viajeros que regresan del sur de Europa o de EE.UU., los pacientes y empleados de centros sanitarios como centros de rehabilitación o residencias de ancianos con tasas elevadas de SARM.
Medidas para el SARM
En los casos de infecciones agresivas de la piel y los tejidos blandos y/o de falta de respuesta a los antibióticos betalactámicos (como la amoxicilina-ácido clavulánico), debe sospecharse la presencia de SARM e iniciarse el diagnóstico microbiológico. Los portadores se detectan mejor con un frotis de la nariz y la garganta. Tras el contacto con el paciente en la consulta del médico, es importante desinfectar las manos y las superficies de contacto con preparados a base de alcohol. Para un contacto más estrecho, por ejemplo durante un examen, son útiles los abrigos, las mascarillas y los guantes. Los pacientes hospitalizados deben ser aislados del contacto. Debido a la resistencia cruzada a las penicilinas y cefalosporinas, todos los antibióticos betalactámicos perorales disponibles actualmente son ineficaces. La clindamicina, el cotrimoxazol o el linezolid (Zyvoxid®) por vía peroral son adecuados como monoterapia en la clínica ambulatoria si se demuestra sensibilidad. La clindamicina sólo debe utilizarse si la cepa también ha resultado sensible a los macrólidos o se ha descartado la resistencia a la MLSB. Para los pacientes inmunodeprimidos colonizados o los trabajadores sanitarios, el tratamiento de descolonización del SARM puede llevarse a cabo previa consulta con un centro.
Enterobacteriáceas productoras de ESBL
En Suiza, el 7% de los aislados de Escherichia coliprocedentes del tracto urogenital de pacientes ambulatorios son actualmente resistentes a las cefalosporinas de tercera generación (Tab. 1) . Alrededor del 95% de estas cepas producen betalactamasas de amplio espectro (BLEE), cuyos genes son móviles y están localizados en plásmidos. Esto les permite transferirse a otras células, especies y géneros bacterianos y propagarse rápidamente. Estas cepas suelen ser multirresistentes.
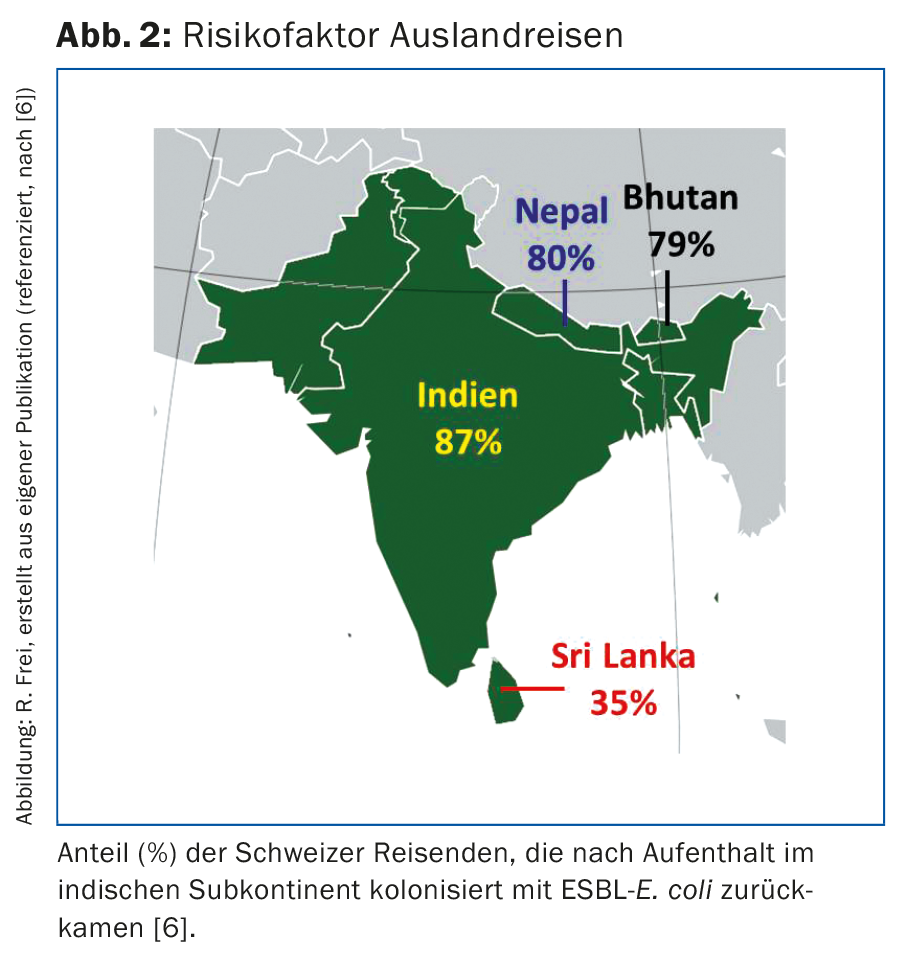
Antes del año 2000, los aislados de E. coli y Klebsiella pneumoniae productores de BLEE se encontraban principalmente en pacientes de hospitales y residencias de ancianos. En la actualidad, la mayoría de las E. coli ESBL se adquieren fuera de las instituciones médicas. Las bacterias productoras de ESBL pueden encontrarse en diversos alimentos [2,4]. Por ejemplo, se detectaron E. coli ESBL en el 66% de las muestras de carne de pollo de producción suiza, y en la carne de pollo de origen extranjero incluso en el 86% de las muestras [2]. Estas cepas también se encontraron en muestras de otras aves de corral, carne de cerdo y vacuno, así como en varias muestras de verduras. El uso de antibióticos en medicina veterinaria favorece la selección, multiplicación y propagación de bacterias resistentes en los animales de granja y en la agricultura. En 2014, se vendieron en Suiza casi 50.000 kg de antibióticos destinados a la medicina veterinaria [2]. En EE.UU. se utilizan cuatro veces más antibióticos para los animales que para los humanos. Aunque un calentamiento suficiente de los alimentos elimine las bacterias, los gérmenes pueden transmitirse a los humanos a través de utensilios de cocina, manos y alimentos crudos contaminados. Nuestras propias investigaciones demostraron que el 8% de las tablas de cocina de los hogares y el 16% de las cocinas de los hospitales estaban contaminadas con gérmenes ESBL tras procesar carne de pollo [5]. Los guantes de los cocineros fueron incluso ESBL-positivos en un 50%. Viajar al extranjero supone un riesgo adicional: El 87% de los viajeros suizos a la India estaban colonizados por vía rectal con E. coli ESBL a su regreso, después de que sólo el 3% fueran portadores de ESBL antes de la salida (Fig. 2) [6]. Se encontró una tasa de portadores de al menos el 30% entre los viajeros procedentes de otros países del subcontinente indio, Asia Próxima y Sudoriental, África y Sudamérica [7]. Otras personas con mayor riesgo de ESBL son los trabajadores de los mataderos, los cocineros, los residentes de residencias de ancianos y asilos, los pacientes mayores de 65 años o aquellos con tratamiento previo con antibióticos [8].
Tratamiento de las infecciones por BLEE
Las E. coli ESBL también han aumentado drásticamente en Suiza [1]. De 2004 a 2014, su proporción de aislados de E. coli invasiva se multiplicó por diez (del 1 al 10%). Se han notificado tasas similares o superiores en la mayoría de los países europeos, con tasas incluso superiores al 25% en Italia, Rumanía y Bulgaria. La elevada prevalencia de los formadores de BLEE en toda Suiza, tanto en niños como en pacientes adultos y ancianos, ha dificultado la terapia de las infecciones por E. coli y K. pneumoniae. La tabla 1 resume la resistencia actual de los aislados de E. coliprocedentes de pacientes ambulatorios. La tabla también muestra la multirresistencia de los aislados ESBL con tasas de resistencia en torno al 70% a las quinolonas y al cotrimoxazol. En cambio, la fosfomicina, la nitrofurantoína y los carbapenems tienen tasas de resistencia bajas, entre el 0 y el 4%, por lo que pueden utilizarse terapéuticamente para las infecciones urinarias no complicadas. El tratamiento de otras infecciones por cepas ESBL puede ser difícil y requiere pruebas de resistencia a los antibióticos. Para las infecciones graves, los carbapenems se consideran el tratamiento de elección. Dado que el ertapenem (Invanz®) sólo debe administrarse una vez al día (1 g i.v.), también puede utilizarse en la clínica ambulatoria. El efecto clínico de la amoxicilina-ácido clavulánico es incierto, incluso con susceptibilidad probada del patógeno ESBL, excepto en las infecciones del tracto urinario. Los portadores de ESBL se detectan con mayor fiabilidad mediante hisopos rectales o muestras de heces, orina y muestras de lugares clínicamente infectados [8]. Hasta ahora, sin embargo, ningún plan de descolonización ha demostrado desgraciadamente un éxito a largo plazo. Como la transmisión de E.coli BLEE se ha desplazado del hospital a la comunidad y la tasa de transmisión en los hospitales de agudos es baja, muchos hospitales de agudos han abandonado el aislamiento estricto de los contactos para E.coli BLEE [8]. Se sigue recomendando el aislamiento por contacto para los pacientes colonizados o infectados por otras enterobacterias productoras de BLEE (por ejemplo, K. pneumoniae).
Carbapenemasas de pesadilla
Hoy en día se conocen más de 1000 betalactamasas bacterianas diferentes. Entre ellas, las carbapenemasas son las más temidas, ya que inactivan no sólo los carbapenems sino prácticamente todos los antibióticos betalactámicos. La mayoría de los bacilos gramnegativos productores de carbapenemasas son también extremadamente multirresistentes. Incluso una prueba ampliada de resistencia a los antibióticos suele mostrar sólo 1 ó 2 sustancias activas, como la colistina. A veces, ninguno de los preparados disponibles en el mercado es ya eficaz in vitro. Hasta ahora, este tipo de cepas sólo se han dado esporádicamente en Suiza y casi siempre eran importadas de otros países. Las carbapenemasas del tipo KPC se dan con frecuencia en Italia, Grecia, Israel y EE.UU. y son el tipo más común en Suiza hasta la fecha (aproximadamente el 45% de las carbapenemasas identificadas) [9]. Las carbapenemasas de tipo NDM se han propagado principalmente en la India y los países balcánicos y se han trasladado a otros países con viajeros, pacientes y emigrantes. Las enzimas del grupo OXA-48 se introdujeron en los países europeos desde Turquía, el norte de África y Oriente Próximo y representan aproximadamente un tercio de las carbapenemasas en Suiza. Recientemente, se descubrió un mecanismo de resistencia a la colistina (MCR-1) en aislados de China y otros países, incluida Suiza, que se propaga con plásmidos [10]. A un profesional que atienda a un paciente con bacterias productoras de carbapenemasas se le aconsejaría consultar con un departamento de enfermedades infecciosas.
Literatura:
- Oficina Federal de Salud Pública. Anresis.ch: Informes sobre microorganismos multirresistentes seleccionados en Suiza. Boletín 2016;(35): 530.
- Oficina Federal de Seguridad Alimentaria y Veterinaria FSVO: ARCH-Vet. Informe sobre la distribución de antibióticos en medicina veterinaria y el seguimiento de la resistencia a los antibióticos en animales de granja en Suiza. Informe General 2014. www.blv.admin.ch/blv/de/home/tiere/tierseuchen/tierarzneimittel/antibiotika/vertrieb.html
- Larsen J, et al: Pruebas de adaptación humana y transmisión alimentaria del Staphylococcus aureus resistente a la meticilina asociado al ganado. Clin Infect Dis 2016; Sep 20. pii: ciw532. [Epub ahead of print]
- Zogg AL, et al.: Characteristics of ESBL-producing Enterobacteriaceae and methicillin-resistant Staphylococcus aureus (MRSA) isolated from Swiss and imported raw poultry meat collected at retail level. Schweiz Arch Tierheilkd 2016; 158(6): 451-456.
- Tschudin-Sutter S, et al.: Enterobacteriaceae productoras de β-lactamasa de espectro extendido (ESBL): una amenaza desde la cocina. Infect Control Hosp Epidemiol 2014; 35(5): 581-584.
- Kuenzli E, et al: Altas tasas de colonización de Escherichia coli productora de β-lactamasa de espectro extendido (ESBL) en viajeros suizos al sur de Asia: un estudio de cohortes multicéntrico observacional prospectivo que analiza la epidemiología, la microbiología y los factores de riesgo. BMC Infect Dis 2014; 14:528.
- Ostholm-Balkhed A, et al.: Travel-associated faecal colonization with ESBL-producing Enterobacteriaceae: incidence and risk factors. J Antimicrob Chemother 2013; 68(9): 2144-2153.
- Tissot F, et al.: Enterobacteriaceae con betalactamasas de amplio espectro (BLEE) en hospitales: nuevas recomendaciones Swissnoso 2014. www.swissnoso.ch/wp-content/uploads/pdf/v18_2_de.pdf
- Babouee B, et al: Aparición de cuatro casos de Klebsiella pneumoniae portadora de KPC-2 y KPC-3 introducidos en Suiza, 2009-10. Euro Surveill 2011; 16(11). pii: 19817.
- Nordmann P, et al.: Resistencia a la colistina mediada por plásmidos: una amenaza adicional a la resistencia a los antibióticos. Clin Microbiol Infect 2016; 22(5): 398-400.
PRÁCTICA GP 2016; 11(12): 16-19