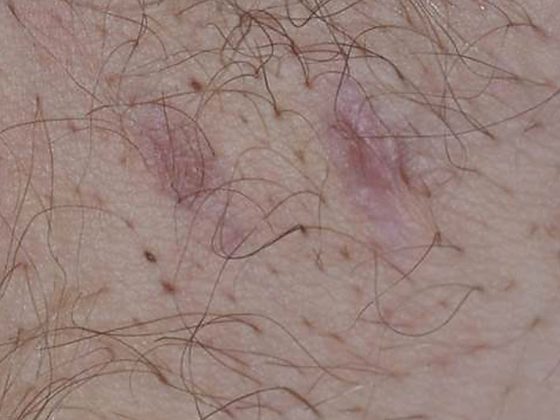
La proporción de mujeres de 18 a 24 años vacunadas contra el VPH está estancada en torno al 50%. La cobertura de la vacunación debe mejorar significativamente si se quiere reducir la circulación del virus del papiloma a largo plazo. Una posibilidad, por ejemplo, es la vacunación planificada de chicos adolescentes y hombres jóvenes. La ventana adolescente del calendario de vacunación de dos dosis contra el VPH finaliza a partir del 15º cumpleaños. Después de esta ventana juvenil, se requieren tres dosis en lugar de dos. No obstante, casi dos tercios de todos los casos de VPHVacunas administradas después de los 15 años, lo que reduce la eficacia (un tercio ya había mantenido relaciones sexuales en el momento de la vacunación). Además, el riesgo de coincidencia temporal con enfermedades autoinmunes raras aumenta con la edad.
El desarrollo de las vacunas contra el VPH y de los métodos de detección del VPH ha estado marcado por el trabajo de investigación sobre el VPH de Harald zur Hausen, por el que fue galardonado con el Premio Nobel de Medicina en 2008. En Suiza están autorizadas dos vacunas contra el VPH, que tienen un alto efecto protector contra dos (bivalente, bHPV, 2vHPV) o cuatro tipos de VPH (cuatrivalente, qHPV, 4vHPV). El lanzamiento al mercado de una vacuna contra el VPH que inmuniza contra nueve tipos de VPH (novem-valente, 9vHPV) está previsto para el próximo año (2016). Tanto el 4vHPV como el 9vHPV protegen al >90% contra los condilomas puntiformes. El 9vHPV abarca otros tipos de VPH oncogénicos (los denominados tipos de “alto riesgo”), aunque su frecuencia varía a escala internacional [1]: Por ejemplo, los tipos oncogénicos 51 (en cuarto lugar) y 59, que son relativamente frecuentes en Suiza, no están incluidos en el 9vHPV. Además, se dice que los efectos secundarios en el lugar de la inyección (ardor/dolor, eritema, hinchazón) son aún más frecuentes, con un 91% (9vHPV) frente a un 85% (4vHPV) [2] – las AMP vacunadoras y los médicos tendrán que intensificar su labor educativa en consecuencia.
La vacuna novem-va^lente contra el VPH sólo podrá demostrar su contribución teóricamente posible de un máximo del 20% de reducción adicional de los carcinomas cervicales si sustituyera por completo a las vacunas bi- y tetravalentes contra el VPH y la tasa de cobertura de vacunación aumentara notablemente.
Planes de vacunación
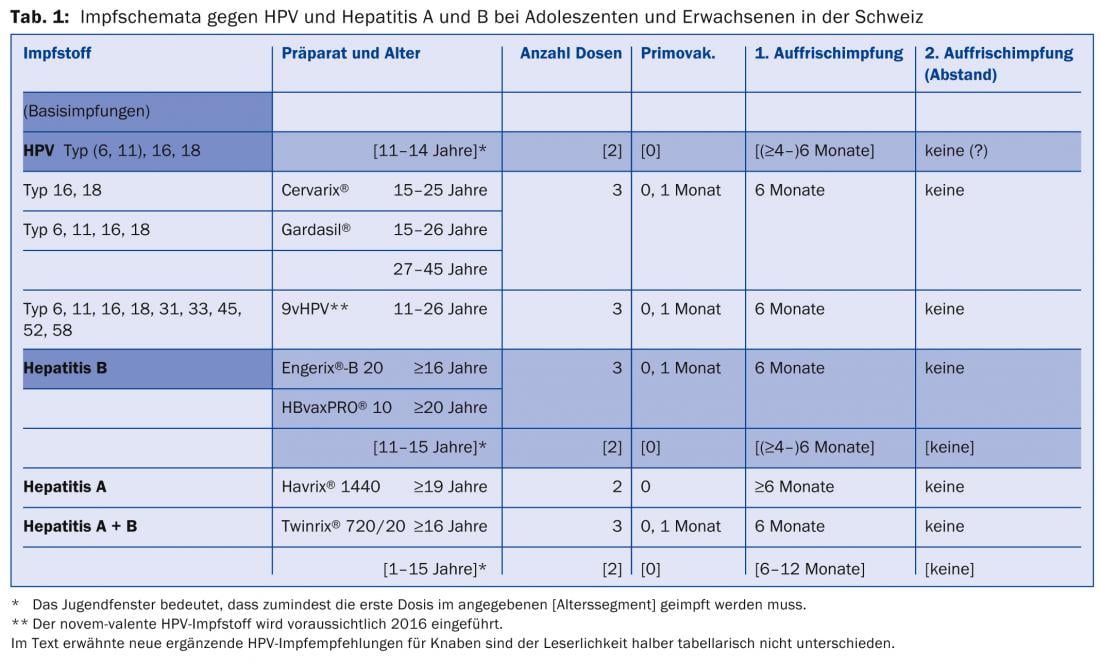
Para la vacunación contra el VPH, existe un calendario de vacunación de dos dosis en Suiza, con el inicio de la llamada ventana de vacunación de dos dosis para adolescentes a partir de los 11 años y hasta los 15 años (fecha límite de la primera dosis; recomendada desde febrero de 2012). Del mismo modo, los esquemas de dos dosis existen desde octubre. 2000 en la ventana juvenil para la vacunación contra la hepatitis B entre el 11º y el 16º cumpleaños, y desde agosto de 2001 para la vacunación combinada contra la hepatitis A+B entre el 1º y el 16º cumpleaños. Es obvio e inmunológicamente posible tratar contra el VPH y la hepatitis (A y) B al mismo tiempo en dos sesiones separadas por seis meses en la ventana adolescente de 11-15 meses. Una inyección en el músculo deltoides izquierdo y otra en el derecho (Tab. 1).
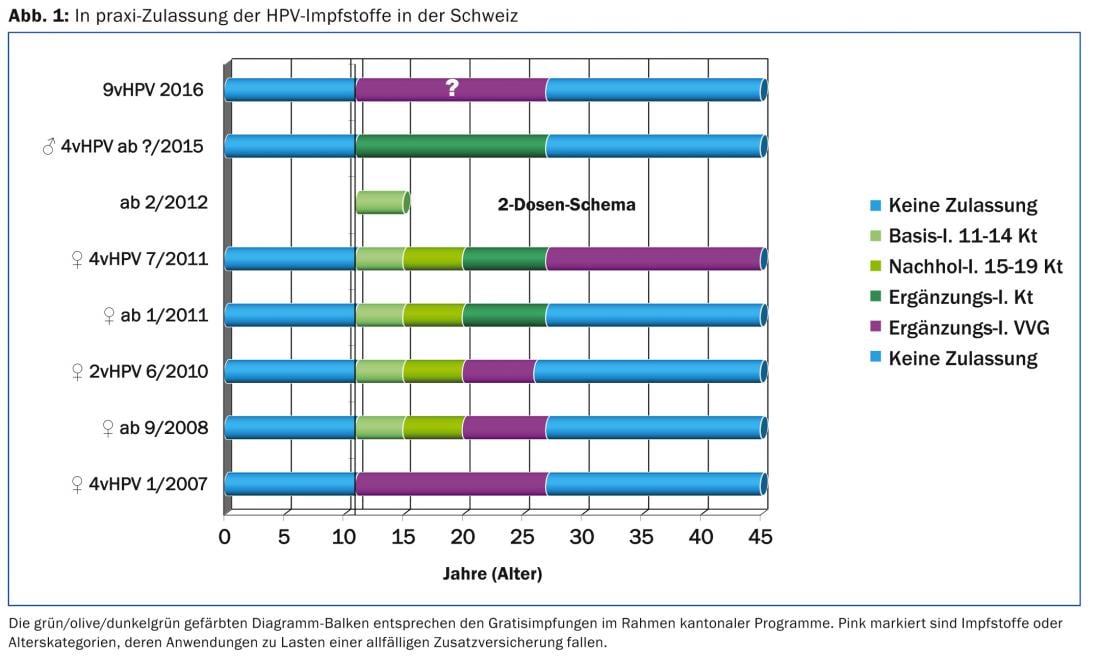
En los programas cantonales, la posibilidad de “vacunación gratuita” de las jóvenes nacidas entre 1984 y 2003 existe desde septiembre de 2008 (Fig. 1). Una evaluación de la vacunación contra el VPH encargada por la Oficina Federal de Salud Pública [3] mostró unas tasas de cobertura de vacunación de las jóvenes de 18 a 24 años de un buen 50%. Se considera que esto es insuficiente para reducir la circulación viral de los tipos oncogénicos 16 y 18 del VPH y también para proteger a las personas no inmunizadas (el llamado efecto rebaño). Dado que el estado de infección de la pareja actual es el factor de riesgo más importante para la transmisión del VPH, la vacunación suplementaria contra el VPH de los chicos adolescentes y los hombres jóvenes prevista este año, también en el marco de los programas cantonales, no es sólo una “equidad de acceso” corregida [4], sino también una posible protección contra la transmisión del virus. Un estudio canadiense [5] demostró que la prevalencia del VPH era mayor en las personas con parejas infectadas (85%) que en los pacientes cuyas parejas eran negativas al VPH (19%). Los preservativos ejercieron un mayor efecto protector en los hombres que en las mujeres. En un estudio epidemiológico observacional estadounidense, la prevalencia del VPH fue del 38% (prueba del VPH ocho meses después de cohabitar) a pesar del uso sistemático del preservativo [6]. Por supuesto, existe el mismo esquema de dos dosis para los varones en la ventana de la adolescencia, que es el momento óptimo para la vacunación. En teoría, la única distinción que se hace en las recomendaciones de vacunación suizas de 2015 es que las vacunas contra el VPH para los varones adolescentes no se denominan vacunas básicas o de puesta al día como en el caso de las chicas, sino “vacunas suplementarias”. En el caso de las vacunaciones complementarias, no existen requisitos para alcanzar una tasa mínima de cobertura de vacunación con la ayuda de las campañas correspondientes.
Impacto de la vacunación contra el VPH y de la investigación sobre el cribado del cáncer de cuello de útero
Las vacunas bivalente y tetravalente pueden prevenir teóricamente hasta el 70% de los carcinomas cervicales cuando se vacuna antes de la cohabitación; la vacuna novem-valente contra el VPH incluso hasta el 90% [2]. Dado que esta prevención primaria del carcinoma de cuello de útero no ofrece una protección completa, deben continuarse las medidas de prevención secundaria (citologías cervicales). De las mujeres vacunadas menores de 25 años, una cuarta parte (25,2%) declaró que se les seguía recomendando hacerse una citología, pero que era necesaria con menos frecuencia [3]. Aunque este cambio en el comportamiento de cribado no está exento de polémica, es importante tener en cuenta que la sensibilidad de la prueba única de citología vaginal (50-70%) podría disminuir en cohortes de mujeres jóvenes con una cobertura de vacunación elevada. La displasia cervical severa (denominada HSIL, High-grade Squamous Intraepithelial Lesion) es diagnosticada por los citotecnólogos en aproximadamente el 0,2% de todas las citologías cervicales; una disminución de la proporción positivo-patológica podría dar lugar a que se detectaran menos citologías positivas. La cobertura máxima de vacunación puede reducir teóricamente los cambios de HSIL entre un 50% (2vHPV y 4vHPV) y un 80% (9vHPV) [2], lo que significa que aún puede detectarse una única citología vaginal HSIL positiva por cada 1000 envíos.
Además, el cribado del cuello uterino en Suiza debe adaptarse a las recomendaciones internacionales. Se recomienda preferentemente (sociedades de cáncer/colposcopia/patología de EE.UU.: ACS, ASCCP, ASCP) la co-prueba cervical a intervalos de 5 años a partir de los 30-65 años. La prueba conjunta significa que los resultados citológicos (prueba de Papanicolaou microscópica) y los resultados biológicos moleculares (prueba del VPH totalmente automatizada) se obtienen a partir de la misma citología cervical (citología de “base líquida”). Para no desestabilizar a una de cada diez mujeres con las pruebas conjuntas (pruebas de ADN del VPH positivas debido, por ejemplo, a infecciones transitorias por VPH, especificidad de la prueba del 90%), probablemente se debería dar preferencia a las pruebas de ARNm del VPH con una especificidad hacia el 95% [7]. Las pruebas del VPH y la vacunación contra el VPH son los temas principales de los congresos internacionales bienales EUROGIN. El autor en ejercicio consiguió convencer a su laboratorio extranjero, gracias a la información del congreso y a su propia publicación [8], para que incluyera por primera vez esta prueba denominada Aptima® de ARNm del VPH en el programa de análisis en Suiza (Fig. 2).

La detección del genoma del grupo ARNm del papilomavirus se carga con la posición 3133.00 (CHF 54). En Estados Unidos, el ensayo Aptima® HPV mRNA fue aprobado por la FDA en octubre de 2011 (FDA approved). Este ensayo detecta específicamente las proteínas oncogénicas E6/E7 de 14 tipos de VPH de alto riesgo (16, 18, 31, 33, 35, 45, 51, 56, 58, 59, 66, 68) que se sobreexpresan como resultado de la persistencia de la infección basada en la traducción ribosómica del ARNm del VPH. Esta desregulación celular es el resultado de la integración del genoma vírico en los núcleos celulares del epitelio cervical basal. Los posibles cambios dentro de las diferentes prevalencias de tipos de VPH (“de alto riesgo”) debidos a la vacunación abogan por una prueba de ARNm del VPH de alto riesgo con una amplia cobertura de tipos, es decir, que incluya los tipos 51 y 59, que no están incluidos en la vacuna 9vHPV y son relativamente comunes en Suiza.
Mensajes para llevarse a casa
- Las tasas de cobertura de la vacunación básica y de puesta al día (niñas adolescentes de 11 a 19 años) contra el virus del papiloma humano (VPH) deberían haberse optimizado desde 2011 con programas cantonales de vacunación suplementaria para mujeres de 20 a 26 años. Sin embargo, la proporción de mujeres de 18 a 24 años vacunadas se estanca en torno al 50% [3].
- Para reducir de forma duradera la circulación del virus del papiloma y conseguir así un efecto rebaño, es necesario lograr una mayor cobertura de vacunación, por ejemplo mediante la vacunación planificada de los adolescentes varones y los hombres jóvenes.
- Aunque los ginecólogos son los vacunadores más frecuentes contra el VPH, con un 32% de todas las vacunaciones contra el VPH (principalmente vacunaciones de puesta al día y suplementarias [3]), y están haciendo un seguimiento de esta nueva competencia básica, hay que recordar que la vacunación contra el VPH se utiliza principalmente como una Vacunación básica de los niños de 11 a 14 años se recomienda y, por lo tanto, sería antes del momento de la primera relación sexual o al mismo tiempo en el 99,5% de los casos.
- El hecho de que casi dos tercios de todas las vacunaciones contra el VPH se realicen después de los 15 años reduce la eficacia, por un lado (un tercio de las adolescentes tardías ya habían mantenido relaciones sexuales en el momento de la vacunación) y, por otro, con el aumento de la edad, conlleva el riesgo de coincidencia temporal con enfermedades autoinmunes raras como la esclerosis múltiple o enfermedades neurológicas (síndrome de Guillain-Barré) [9]. Además, el calendario de vacunación contra el VPH después de la ventana de la adolescencia (a partir de los 15 años) requiere tres dosis en lugar de dos.
Dr. Daniel Brügger
Literatura:
- Krech T, et al: Virus del papiloma humano urogenital y clamidia. Schweiz Med Forum 2010; 10(12): 230-232.
- Luxemburgo A (CDC/NCIRD): Resultados clave del programa de vacunación contra el VPH 9-valente (9vHPV). www.cdc.gov/vaccines/acip/meetings/downloads/slides-2014-10/HPV-02-Luxembourg.pdf
- Mäusezahl-Feuz M: Evaluación de la vacunación contra el VPH. VIII. Congreso de Vacunación, 06.11.2014 Biel.
- Stronski-Huwiler S: Vacunación contra el VPH en Suiza: ¿niñas Y niños? VIII. Congreso de Vacunación, 06.11.2014 Biel
- Burchell AN, et al: Influencia del estado de infección de la pareja en la prevalencia del virus del papiloma humano entre las personas con una nueva pareja sexual. Sex Transm Dis 2010; 37(1): 34-40.
- Winer RL, et al: El uso del preservativo y el riesgo de infección genital por el virus del papiloma humano en mujeres jóvenes. N Engl J Med 2006; 354(25): 2645-2654.
- Monsonego J, et al: Evaluación de las pruebas oncogénicas de ARN y ADN del virus del papiloma humano con la citología de base líquida en el cribado primario del cáncer de cuello uterino: el estudio FASE. Int J Cancer 2011; 129(3): 691-701.
- Brügger D: ¿Qué será del cribado del cáncer ginecológico? Ginecología 2010; 5: 6-8.
- Siegrist CA: Enfermedades autoinmunes tras la vacunación de adolescentes o adultos: ¿Qué debemos esperar? CMAJ 2007; 177(11): 1352-1354.
PRÁCTICA GP 2015; 10(2): 17-20