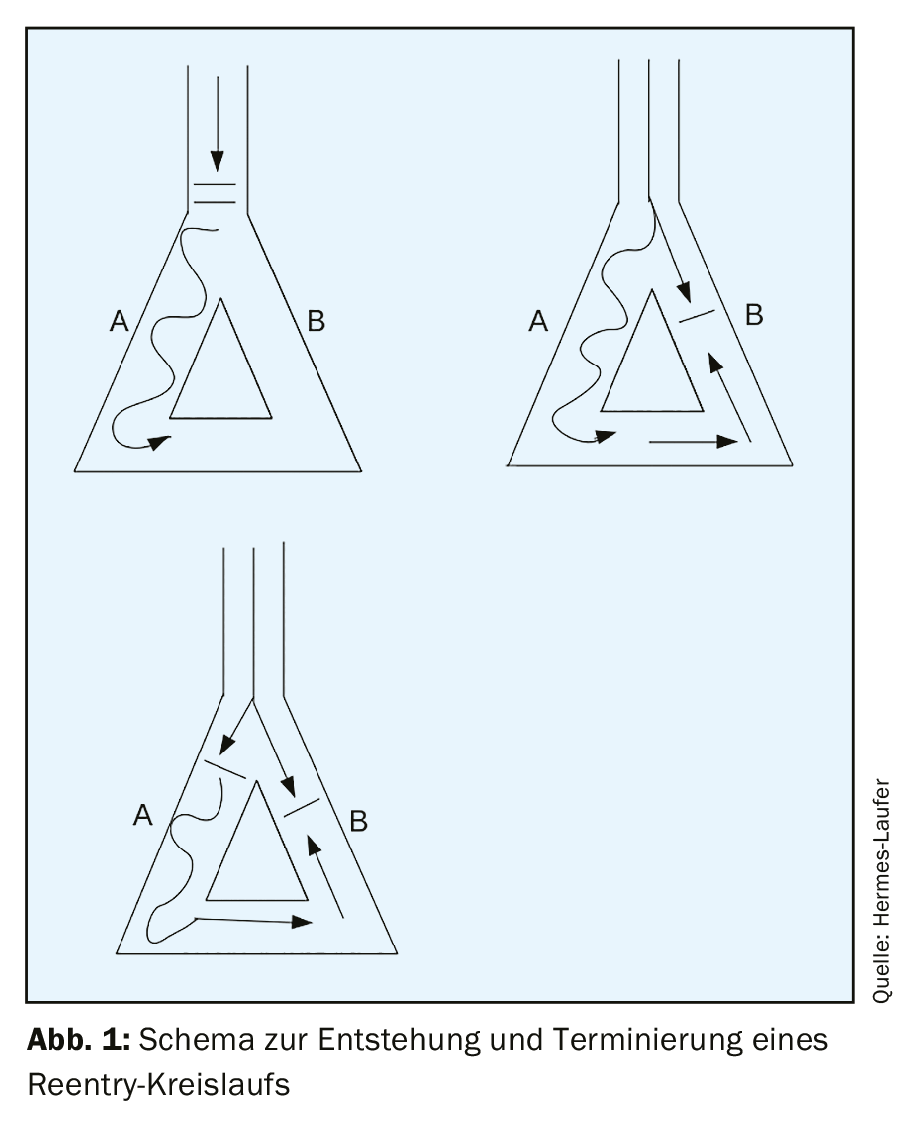
La taquicardia de complejo estrecho es una presentación clínica frecuente. La reentrada, en particular, provoca una taquicardia persistente. El requisito previo para el desarrollo de una taquicardia de reentrada es un sustrato con dos vías de conducción diferentes, que tengan velocidades de conducción y periodos refractarios distintos. La taquicardia supraventricular no está asociada a una cardiopatía estructural en la mayoría de los casos.
La taquicardia regular de complejo estrecho es una presentación clínica común con una prevalencia de 2,25/1000 pacientes [1]. Los tres mecanismos subyacentes de la taquicardia en general son el automatismo, la reentrada y la actividad desencadenada. Con mucho, el más común de estos tres mecanismos en la taquicardia sostenida es la reentrada. La automaticidad se produce focalmente y es bastante rara (menos del 10% de todas las taquicardias). La actividad desencadenada es una alteración de la repolarización, por la que durante la fase III o la fase IV del potencial de acción se producen postdespolarizaciones y, en cuanto se alcanza el valor umbral, se produce un potencial de acción renovado y, por tanto, una taquicardia. Las taquicardias por reentrada supraventricular se dividen en taquicardias por reentrada nodal AV, taquicardias por reentrada AV y taquicardias por reentrada auricular focal, con una distribución de frecuencias del 60%, el 30% y el 10% [2]. El requisito previo para el desarrollo de una taquicardia de reentrada es un sustrato con dos vías de conducción diferentes, que tengan velocidades de conducción y periodos refractarios distintos. Si se produce un desencadenante, como una extrasístole, al mismo tiempo que la vía de conducción con el periodo refractario más largo sigue siendo refractaria, pero la vía con el periodo refractario más corto ya se ha recuperado, se produce inicialmente un bloqueo unidireccional y puede dar lugar a una excitación en círculo si la excitación llega en el momento en que la segunda vía de conducción es capaz de conducir de nuevo (brecha excitable). (Fig. 1). La taquicardia supraventricular no está asociada a una cardiopatía estructural en la mayoría de los casos.
Diagnóstico diferencial
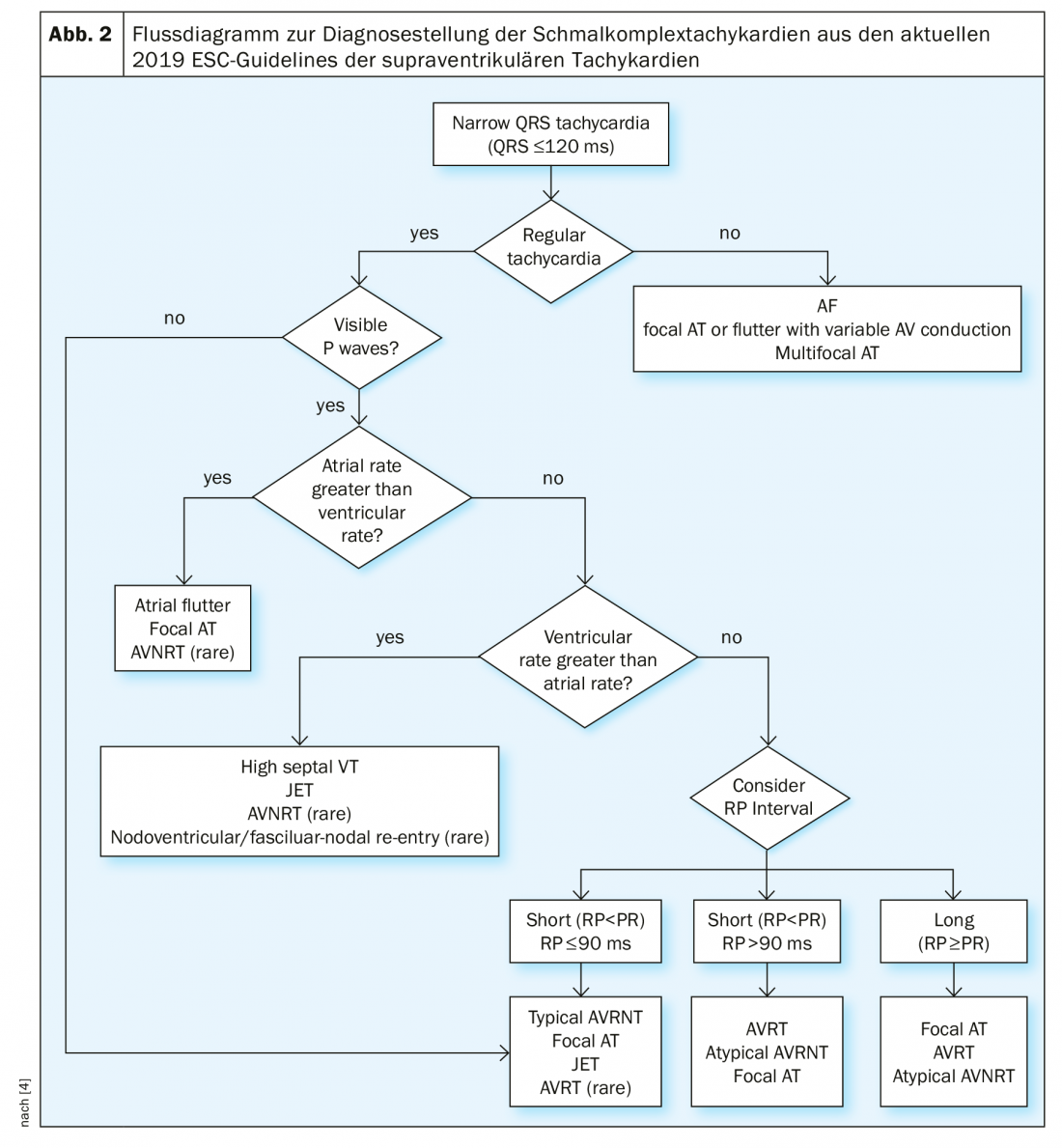
Si no está clara la taquicardia de complejo estrecho con una duración del QRS <120 ms, en primer lugar debe comprobarse la estabilidad hemodinámica del paciente y, siempre que sea posible, debe obtenerse un ECG de 12 derivaciones. Se recomienda la vigilancia monitorizada, así como análisis de laboratorio que incluyan hemograma, electrolitos, función renal y función tiroidea. En la derivación 12, debe comprobarse la regularidad de la taquicardia y la presencia de ondas P. La frecuencia ventricular irregular suele ser fibrilación auricular, aleteo auricular con conducción variable o taquicardia auricular focal. En particular, el inicio y el final de la taquicardia son de gran importancia, por ejemplo, si se trata de un inicio y un final súbitos o progresivos. Si hay ondas P presentes, verifique que cada complejo QRS tiene una onda P asociada, que la distancia PR es mayor que la distancia RP (PR>RP o RP>PR) y que la frecuencia auricular es mayor, menor o igual que la frecuencia ventricular. En el diagrama de flujo de las directrices actuales de la ESC se ofrece una visión general del diagnóstico diferencial de la taquicardia de complejo estrecho (Fig. 2) . En casos poco claros y estabilidad hemodinámica, debe considerarse una maniobra vagal diagnóstica y/o la administración de adenosina intravenosa. Así, en el aleteo auricular, las ondas de aleteo se manifiestan y el AVNRT o AVRT se interrumpe en la mayoría de los casos mediante la administración adecuada de adenosina. Si la adenosina no tiene ningún efecto sobre la taquicardia de complejo estrecho, o bien se inyectó en una dosis y/o modo de administración inadecuados (se inyectó demasiado despacio o sin enjuague de NaCl) o, en casos raros, se trata de una taquicardia ventricular septal alta.
AVNRT
La forma más común de taquicardia supraventricular paroxística, la taquicardia por reentrada nodal AV (TRNAV), se caracteriza por un inicio repentino y una terminación igualmente repentina. Aproximadamente el 95% de los casos son AVNRT típicos del tipo lento-rápido, en los que la conducción anterógrada se realiza a través de la vía de conducción lenta y la retrógrada a través de la vía de conducción rápida. En la anamnesis debe preguntarse si existe un aumento de la diuresis durante/después de la taquicardia, así como una sensación de “golpeteo en la garganta” (signo de la rana), que son síntomas típicos de la TRNAV debido a la contracción simultánea de la aurícula y el ventrículo con las válvulas cerradas y la liberación de PNA asociada. El ECG de superficie muestra una taquicardia regular de complejo estrecho (excepto con bloqueo de rama del haz preexistente) sin ondas P visibles o con ondas P retrógradas con un intervalo RP muy corto, inferior a 70 ms (Fig. 3) [4]. En las TRNAV atípicas (alrededor del 5% de las TRNAV) de tipo rápido-lento o lento-lento, las ondas P retrógradas suelen ser visibles antes del complejo QRS posterior, porque la excitación retrógrada discurre por la vía lenta.

La TRNAV puede manifestarse en la infancia o en los primeros años de la edad adulta, así como en la cuarta o quinta década de la vida o incluso más tarde [3,4]. La fisiología de la conducción dual es innata, pero la probabilidad de aparición de TRNAV se modula con la edad, en parte debido a extrasístoles de frecuencia variable y en parte debido a modificaciones estructurales relacionadas con la edad de las propiedades de las dos vías de conducción, que también pueden conducir a una manifestación tardía de la TRNAV [3]. Otros factores que pueden influir en la probabilidad de manifestación de la TRNAV mediante desencadenantes agrupados son los factores hormonales, como en el hipertiroidismo, y el consumo excesivo de cafeína y alcohol.
AVRT
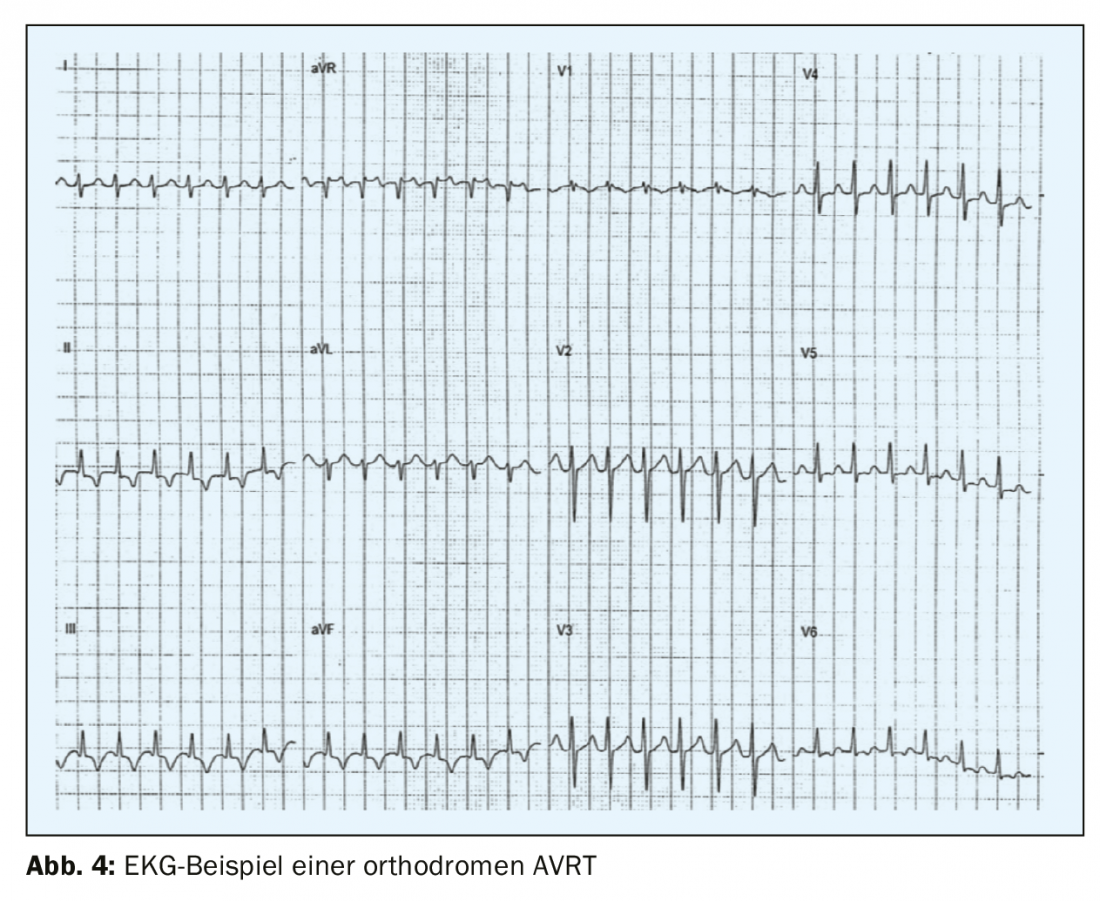
La segunda forma más común de taquicardia supraventricular paroxística – AVRT – está causada por una vía accesoria entre la aurícula y el ventrículo, que se encuentra fuera del sistema de conducción específico. El síndrome de preexcitación o síndrome Wolff-Parkinson-White fue descrito por primera vez a principios de la década de 1930 por los tres cardiólogos que le dieron su nombre, Louis Wolff, John Parkinson y Paul Dudley White, y casi simultáneamente por Max Holzmann en Zúrich. Lo más habitual es que la vía accesoria se localice a lo largo de la válvula mitral en la pared libre izquierda (aproximadamente el 60-70% de las vías accesorias), seguida de las vías localizadas septalmente en el anillo mitral o tricúspide (aproximadamente el 25%) y sólo el 15% se localizan en la pared libre del VD [5]. Algunos pacientes (<12%) tienen múltiples vías accesorias, lo que debe tenerse en cuenta, por ejemplo, en pacientes con anomalía de Ebstein [6]. En el síndrome de preexcitación, existe una vía accesoria manifiesta, arritmias frecuentes y un cuadro típico de preexcitación en el ECG con la típica onda delta, un trazo ascendente o descendente aplanado del complejo QRS y un complejo QRS ensanchado de más de 120 ms. En la mayoría de los casos, los pacientes con síndrome de WPW tienen un corazón estructuralmente normal y se encuentran en la infancia o la adolescencia en el momento de la primera manifestación. Los hombres se ven afectados con más frecuencia que las mujeres. En la TRAV ortodrómica (>90% de las TRAV y 20-30% de todas las taquicardias supraventriculares sostenidas), el circuito va primero de la aurícula al ventrículo a través del sistema de conducción normal y vuelve del ventrículo a la aurícula a través de la vía accesoria. El ECG convulsivo muestra una taquicardia regular de complejo estrecho con una frecuencia mayoritaria de 160-220/min con ondas P retrógradas con un intervalo RP de >70 ms (RP<PR) (Fig. 4) .
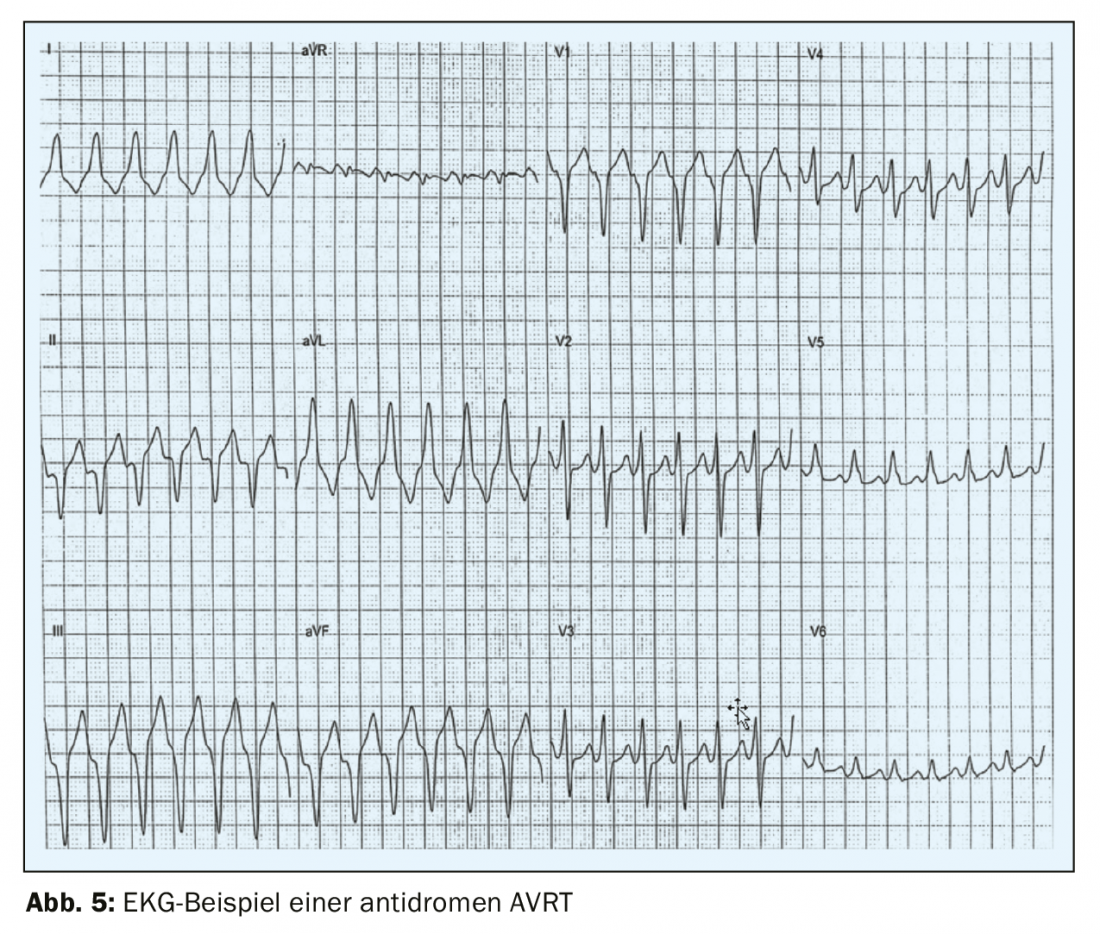
El AVRT antidrómico, mucho más raro, sólo se produce en el 3-8% de los pacientes con WPW [7], con una excitación que inicialmente va de la aurícula al ventrículo a través de la vía accesoria y de vuelta a través del nodo AV. El ECG de superficie muestra un complejo QRS ancho, lo que dificulta distinguir la AVRT antidrómica de la taquicardia ventricular (Fig. 5) . La fibrilación auricular paroxística se produce en el 50% de los pacientes con síndrome de WPW. [8,4]que puede ser potencialmente mortal y degenerar en fibrilación ventricular si se conduce a través de la vía accesoria y a una frecuencia ventricular rápida. En el ECG de superficie, esta arritmia se reconoce por una frecuencia rápida e irregular y un complejo QRS ancho con preexcitación [9] (FBI – rápido, ancho, irregular). Por este motivo, es crucial que incluso los hallazgos incidentales de un ECG de preexcitación en pacientes asintomáticos se aclaren siempre rítmicamente y se traten en la mayoría de los casos. En la denominada “WPW oculta”, sólo existe una vía accesoria de conducción retrógrada, normalmente en la pared libre del VI, pero la preexcitación no es visible en el ECG de superficie y la manifestación inicial es una AVRT ortodrómica. Dado que la vía accesoria no puede conducir anterógradamente en este caso, los pacientes con un WPW oculto no corren un mayor riesgo de muerte súbita cardiaca.
Taquicardia auricular
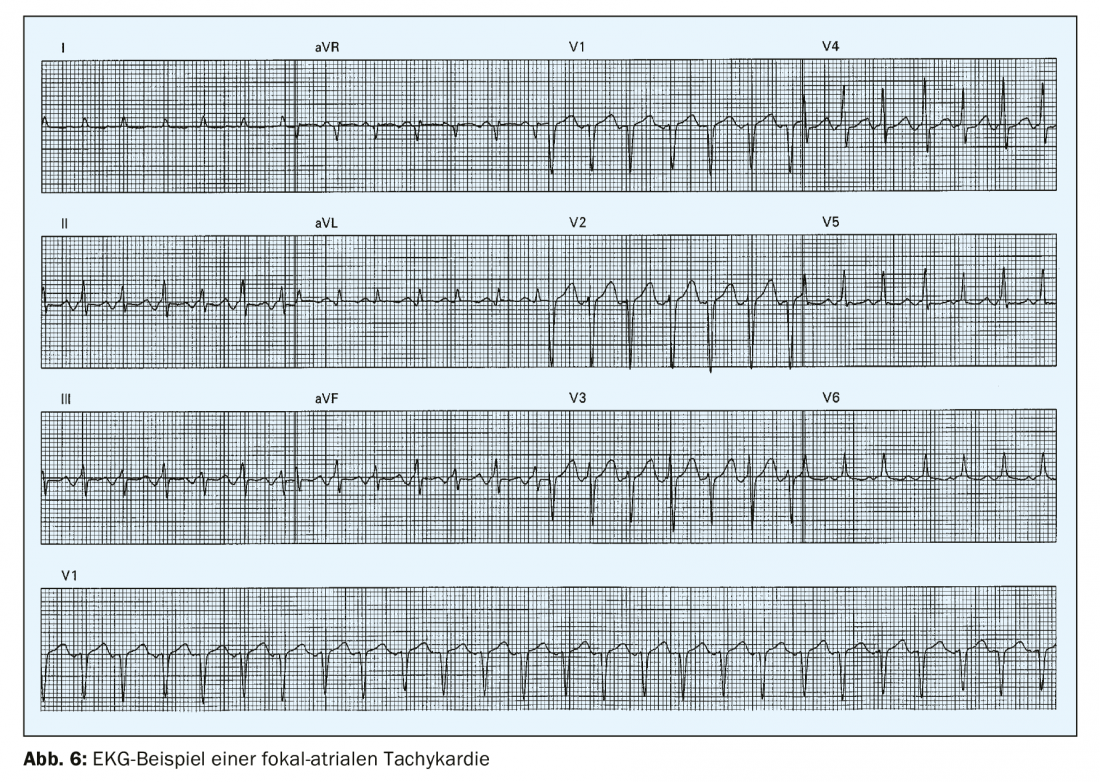
La taquicardia auricular focal es un ritmo auricular organizado >100/min originado fuera del nodo sinusal (Fig. 6) . Es poco frecuente, con una prevalencia del 0,34% en adultos jóvenes [4] y representa menos del 10% de todas las TSV. En el ECG de superficie, se encuentran ondas P monomórficas con una longitud de ciclo estable. El mecanismo desencadenante puede ser una microrreentrada o un automatismo. La taquicardia auricular focal suele originarse en la zona de las uniones venoauriculares, por ejemplo en el seno coronario, en la zona de la crista terminalis o en el anillo mitral o tricúspide. La configuración de la onda P en el ECG de 12 derivaciones puede proporcionar información sobre el origen de la taquicardia auricular focal.
Aleteo auricular
El aleteo auricular debe distinguirse entre el aleteo auricular típico dependiente del istmo (90%) con macrorreentrada en sentido horario o antihorario alrededor del istmo cavotricuspídeo (anillo tricúspide) y el aleteo atípico. En el aleteo auricular típico, se distingue entre el tipo I con una macrorreentrada en el sentido contrario a las agujas del reloj alrededor del istmo cavotriscópico y el tipo II con una macrorreentrada en el sentido de las agujas del reloj. Los ECG respectivos del aleteo auricular típico de tipo I y de tipo II pueden ser muy diferentes; por ejemplo, las típicas “ondas en diente de sierra” aparecen en el aleteo de tipo I y pueden estar completamente ausentes en el de tipo II, ya que aquí suelen quedar ocultas en el complejo QRS y las ondas T. El aleteo auricular atípico puede originarse tanto en la aurícula derecha como en la izquierda y suele observarse en pacientes preoperados, pacientes con defectos cardíacos congénitos o tras intervenciones como las ablaciones de fibrilación auricular, en las que existe un sustrato apropiado alrededor del cual gira el circuito del aleteo. En el ECG de superficie, el aleteo típico se observa en las ondas de aleteo en diente de sierra del ECG, que suelen tener una frecuencia de alrededor de 300/min y se presentan negativamente en las derivaciones inferiores y positivamente en V1 en el caso del aleteo auricular típico dependiente del istmo en sentido antihorario. La transición AV suele ser 2:1 pero puede ser 3-4:1, 1:1 o variable. Por lo tanto, en el caso de una TSV regular con una frecuencia de alrededor de 150/min, el aleteo auricular debe considerarse siempre un diagnóstico diferencial, independientemente de si las ondas de aleteo son visibles o no en el ECG de superficie. El nodo AV entra fisiológicamente en un bloqueo 2:1 o superior durante el aleteo auricular, debido a su periodo refractario y a su propiedad de conducción decremental. Clínicamente, el aleteo auricular se asocia a menudo con la fibrilación auricular, por lo que los pacientes deben someterse a pruebas de detección.
Una discusión de la fibrilación auricular está más allá del alcance de este artículo, excepto para mencionar que la taquicardia irregular con arritmia absoluta sin ondas P claras es fibrilación auricular y debe buscarse documentación en el ECG para su posterior tratamiento.
Gestión
Gestión de la TRNAV: En la terapia aguda, la cardioversión sincronizada debe realizarse en pacientes hemodinámicamente inestables, lo que es extremadamente raro que sea necesario en la práctica (indicación de clase IB). Las maniobras vagales como la maniobra de Valsalva con presión abdominal, el masaje unilateral del seno carotídeo o beber rápidamente agua fría pueden acabar a menudo con la taquicardia por reentrada (indicación de clase IB). El masaje del seno carotídeo debe ir siempre precedido de una auscultación para identificar la estenosis carotídea y, en general, debe realizarse con precaución en pacientes ancianos con aterosclerosis. Si fracasan las maniobras vagales, el paciente está estable y no hay contraindicaciones, deben administrarse 6-18 mg de adenosina rápidamente y con lavado i.v. con NaCl (indicación de clase IB). La aplicación de fármacos antiarrítmicos como los betabloqueantes iv o el verapamilo o el diltiazem se incluye como opción terapéutica en las directrices actuales (indicación de clase IIa), pero puede provocar hipotensión y bloqueo AV transitorio y en la práctica actual sólo es necesaria en contadas ocasiones. La regla de oro para el tratamiento a largo plazo de la TRNAV, tanto típica como atípica, es la ablación con catéter, que conduce a la curación en el 97% de los casos y a complicaciones graves [10] como el bloqueo AV y la dependencia del marcapasos sólo en el 0,3%. La tasa de complicaciones depende de la experiencia de los electrofisiólogos. No hay límite de edad para la ablación con catéter, incluso los ancianos de edad avanzada con comorbilidades deberían someterse a la ablación con catéter.
Gestión de la AVRT: En terapia aguda, la cardioversión sincronizada debe realizarse en pacientes hemodinámicamente inestables (indicación de clase IB). Las maniobras vagales, como la AVNRT, también están indicadas y pueden terminar con la taquicardia (indicación de clase IB). En el tratamiento farmacológico, hay que distinguir entre AVRT ortodrómica y antidrómica.
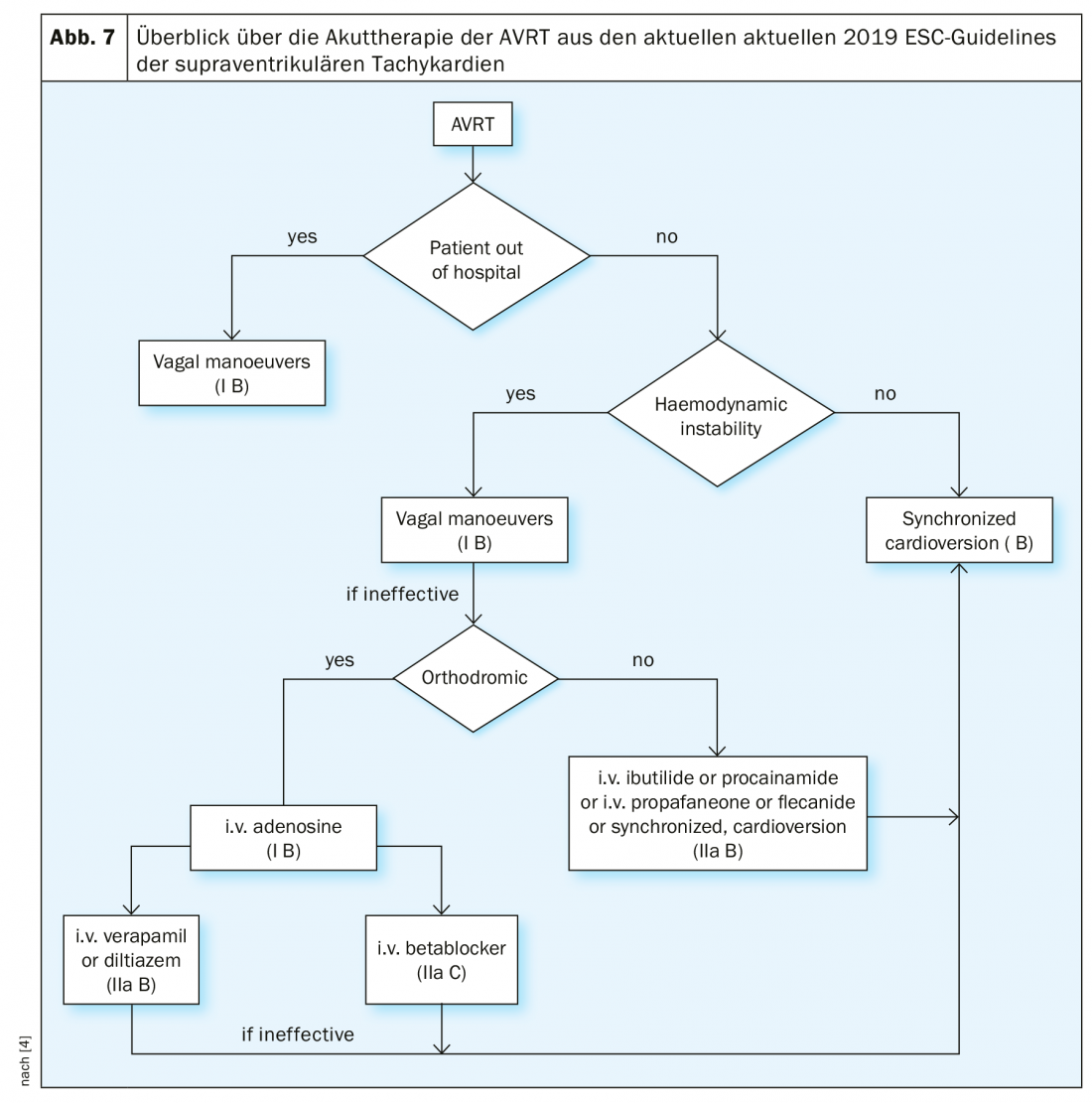
En la AVRT ortodrómica, debe administrarse adenosina 6-18 mg iv (indicación de clase IB), que es aún más eficaz en la AVRT que en la AVNRT. Los fármacos cronotrópicos negativos deben evitarse en la AVRT antidrómica. Las opciones terapéuticas, además de la cardioversión sincronizada, son la flecainida, la procainamida o la propafenona, como en la fibrilación auricular con preexcitación. El diagrama de flujo de las directrices actuales sobre TSV ofrece una visión general de la terapia aguda de la AVRT (Fig. 7).
Tras el tratamiento agudo, la regla de oro, como en el caso de la TRNAV, es la ablación de la vía accesoria. La tasa de complicaciones de la ablación depende de la localización de la vía accesoria; entre las principales complicaciones se incluyen el bloqueo AV completo (0,17-2,7%) y el taponamiento pericárdico (0,1-1,1%) [4]. Las vías accesorias izquierdas pueden ablacionarse mediante un abordaje aórtico transeptal o retrógrado. Si el paciente no desea la ablación con catéter, pueden utilizarse betabloqueantes, diltiazem o verapamilo para el WPW oculto y antiarrítmicos de clase IC para el WPW manifiesto, “abierto”. En el WPW manifiesto, los antagonistas del calcio de tipo verapamilo (y los fármacos digitálicos) están contraindicados porque ralentizan la conducción a través del nodo AV, favoreciendo una conducción rápida a través de la vía accesoria y, por tanto, una frecuencia ventricular amenazadoramente rápida.
Tratamiento del aleteo auricular: El control farmacológico no siempre es fácil de conseguir en el aleteo auricular, las combinaciones de fármacos cronotrópicos negativos (betabloqueantes, antagonistas del calcio, digoxina) pueden utilizarse con precaución. La anticoagulación debe iniciarse según los mismos criterios que para la fibrilación auricular (puntuación CHA2DS2-VASc ≥1 punto). No es infrecuente que la cardioversión sincronizada sea necesaria en la terapia aguda porque el control de la frecuencia inducido por fármacos es insuficiente. La amiodarona también puede utilizarse para el control de la frecuencia, pero sólo puede lograr el control del ritmo en el 29% de los casos [11], por lo que la estrategia principal para el control del ritmo en el aleteo auricular es la cardioversión sincronizada. La cardioversión del aleteo auricular requiere menos energía que la cardioversión de la fibrilación auricular y es más eficaz. En pacientes con un marcapasos y un cable auricular presente, la sobreestimulación auricular puede provocar la terminación del aleteo. La adenosina sólo debe utilizarse para confirmar el diagnóstico y desenmascarar las ondas de aleteo cuando el ECG no sea claro y pueda provocar fibrilación auricular. El patrón oro de la terapia a largo plazo es la ablación con catéter, que conduce a un 90% de libertad de recurrencia en el aleteo auricular dependiente del istmo. La ablación del aleteo auricular atípico es más difícil, ya que a menudo es necesario cartografiar y ablacionar múltiples circuitos eléctricos en torno a sustratos individuales. En la fibrilación auricular, el objetivo debe ser lograr un control del ritmo adecuado a la situación general del paciente. Es imperativo que se sigan las directrices de anticoagulación para todas las medidas de control del ritmo y la frecuencia del aleteo auricular y la fibrilación auricular.
Tratamiento de la taquicardia auricular focal: En la terapia aguda, pueden utilizarse betabloqueantes o antagonistas del calcio para reducir la frecuencia ventricular [4]. La adenosina puede provocar la terminación o incluso bradicardia en cerca del 50% de los casos, por lo que no siempre ayuda en el diagnóstico y el tratamiento [12]. En pacientes sintomáticos con taquicardia auricular focal recurrente, debe realizarse una ablación con catéter.
Mensajes para llevarse a casa
- La cardioversión sincronizada debe realizarse en pacientes hemodinámicamente inestables, independientemente de la forma de la TSV.
- La documentación de la taquicardia mediante un ECG de 12 derivaciones es de gran importancia para el manejo posterior y debe buscarse siempre.
- Las maniobras vagales y la adenosina (6-18 mg en bolo i.v.) están indicadas con estabilidad hemodinámica tanto para confirmar el diagnóstico como para
- Terapia aguda si no hay contraindicaciones.
- La ablación con catéter es una terapia segura y eficaz a largo plazo para el AVNRT, el AVRT y el aleteo auricular típico, con altas tasas de ausencia de recidivas y bajas tasas de complicaciones en centros especializados.
- En la taquicardia auricular, la terapia inicial es la medicación, pero en los pacientes sintomáticos con recurrencias debe considerarse también la indicación de la ablación con catéter.
Literatura:
- Delacretaz E: Taquicardia supraventricular. New England Journal of Medicine, 2006; 354(10): 1039-1051.
- Wellens HJ: Electrofisiología, 25 años de conocimientos sobre los mecanismos de las arritmias supraventriculares: SERIE HISTORIA NASPE. 2003; 26(9): 1916-1922.
- Pentinga ML, et al: Taquicardia nodal auriculoventricular de aparición tardía. 1993; 38(3): 293-298.
- Brugada J, et al: 2019 ESC Guidelines for the management of patients with supraventricular tachycardiaThe Task Force for the management of patients with supraventricular tachycardia of the European Society of Cardiology (ESC). 2019.
- Jackman WM, et al: Ablación con catéter de las vías auriculoventriculares accesorias (síndrome de Wolff-Parkinson-White) mediante corriente de radiofrecuencia. 1991; 324(23): 1605-1611.
- Cappato R, et al: Ablación con catéter de corriente de radiofrecuencia de las vías auriculoventriculares accesorias en la anomalía de Ebstein. 1996; 94(3): 376-383.
- Brembilla-Perrot B, et al: Incidencia e importancia pronóstica de la taquicardia antidrómica espontánea e inducible. 2013; 15(6): 871-876.
- Gemma LW, et al: Desarrollo de una respuesta ventricular preexcitada rápida a la fibrilación auricular en un paciente con preexcitación intermitente. 2013; 24(3): 347-350.
- Etheridge SP, et al: Riesgo de acontecimientos potencialmente mortales en niños con síndrome de Wolff-Parkinson-White: un estudio internacional multicéntrico. 2018; 4(4): 433-444.
- Spector P, et al: Metaanálisis de la ablación del aleteo auricular y la taquicardia supraventricular. 2009; 104(5): 671-677.
- Kafkas NV, et al: Eficacia de conversión de la ibutilida intravenosa en comparación con la amiodarona intravenosa en pacientes con fibrilación auricular y aleteo auricular de inicio reciente. 2007; 118(3): 321-325.
- Eidher U, et al: Eficacia y seguridad de la ibutilida para la conversión de la taquicardia auricular monomórfica. 2006; 29(4): 358-362.
CARDIOVASC 2020; 19(2): 6-11