La diabetes mellitus progresiva de tipo 2 se caracteriza por una disminución continua de la secreción endógena de insulina. La insulina sigue siendo un fármaco antidiabético probado y muy eficaz. La elección del tratamiento con insulina se basa en diversos factores como el estadio de la diabetes, el control metabólico y los recursos del paciente. Inicialmente, la gran mayoría de los diabéticos de tipo 2 pueden tratarse con una terapia de insulina basal. Presenta el menor riesgo de hipoglucemia y de aumento de peso en comparación con otros regímenes de insulina (insulinoterapia prandial, insulinoterapia mixta). En la práctica clínica, la combinación de insulina y análogos de GLP 1 es cada vez más popular.
Desde el punto de vista patogénico, la diabetes mellitus tipo 2 se caracteriza por una resistencia a la insulina y una restricción progresiva de la secreción de insulina. Como resultado, se suelen encontrar niveles elevados de glucosa en sangre en ayunas y picos de glucosa en sangre posprandiales. Por lo tanto, para mantener un control metabólico adecuado, la mayoría de los pacientes requieren tratamiento con insulina durante el curso de la enfermedad. La terapia con insulina aún se inicia a menudo o se considera demasiado tarde. Las razones para ello son múltiples e incluyen el miedo a los efectos secundarios (aumento de peso, hipoglucemia), así como otros numerosos factores (por ejemplo, inhibición de la autoinyección, miedo al deterioro de la calidad de vida, etc.) [1,2].
Desde un punto de vista puramente terapéutico, la insulina ofrece numerosas ventajas: La insulina es el fármaco antidiabético con mayor eficacia terapéutica y es fácilmente controlable, no tiene un potencial de interacción relevante con otros fármacos, no está contraindicada incluso en la insuficiencia cardiaca, renal o hepática más grave y, además, tiene un efecto positivo sobre los lípidos plasmáticos [3]. Los efectos secundarios como la hipoglucemia y el aumento de peso a menudo pueden controlarse bien o evitarse en gran medida con un entrenamiento adecuado y el ajuste de la dosis o la elección del régimen terapéutico apropiado (por ejemplo, la combinación con agonistas de los receptores GLP 1). Por lo tanto, la insulinoterapia moderna sigue representando una opción terapéutica muy eficaz y moderna en el concepto de tratamiento multimodal para los diabéticos de tipo 2.
Este artículo pretende ofrecer una visión general actualizada y práctica del tratamiento con insulina en personas con diabetes mellitus tipo 2.
Valores objetivo de HbA1c y algoritmos terapéuticos
El intervalo objetivo de HbA1c se establece individualmente para cada paciente. Se tienen en cuenta diversos factores, como la edad o la esperanza de vida, las comorbilidades y el riesgo de hipoglucemia [4]. La importancia de un buen control metabólico con respecto al desarrollo y la progresión de secuelas microvasculares como la retinopatía diabética o la nefropatía es indiscutible. Por otro lado, la influencia de un buen control de la glucemia sobre las complicaciones macrovasculares aún no se ha aclarado de forma concluyente. Aunque el estudio UKPDS mostró cierto beneficio del control glucémico precoz y bueno en el resultado cardiovascular al cabo de los años [5], el estudio no mostró ningún beneficio del control glucémico precoz y bueno en el resultado cardiovascular al cabo de los años. Sin embargo, en ensayos posteriores (ADVANCE, ACCORD, VADT), realizados principalmente en pacientes con diabetes de larga evolución, el control intensivo de la glucemia con el objetivo de alcanzar niveles de HbA1c inferiores al 7% no redujo la mortalidad cardiovascular [6–8]. En general, la mayoría de las sociedades profesionales especifican una HbA1c en torno o por debajo del 7%, pero con la opción de valores objetivo de HbA1c más altos (por ejemplo, pacientes mayores con comorbilidades) o más bajos (por ejemplo, pacientes más jóvenes con diabetes de corta duración y bajo riesgo de hipoglucemia).
En las recomendaciones actuales de la ADA/EASD para el tratamiento de la hiperglucemia en pacientes con diabetes de tipo 2, el tratamiento con insulina básica aparece como una opción terapéutica con la mayor potencia terapéutica a la par que los fármacos antidiabéticos orales. Dado que la insulinoterapia tiene posibles efectos secundarios, pero también implica un esfuerzo en términos de formación y aplicación de la medicación, en la práctica tiene sentido sopesar la indicación de la insulinoterapia frente a las demás opciones terapéuticas antidiabéticas, teniendo en cuenta la potencia y los efectos secundarios.
Indicaciones para el tratamiento con insulina
Además de las indicaciones dependientes del metabolismo (deterioro del control metabólico en combinación doble o triple con antidiabéticos orales con aumento de la HbA1cvalor), hay una serie de situaciones independientes del metabolismo en las que la terapia con insulina tiene sentido (Tab. 1). A menudo, en la situación aguda con hiperglucemia pronunciada (“glucotoxicidad”), además de los síntomas correspondientes con poliuria y polidipsia, se produce una especie de “rigidez secretora” de la secreción de insulina y una disminución de la acción de la insulina. En este caso, la terapia con insulina -que a menudo sólo es necesaria temporalmente- ayuda a reducir el azúcar en sangre de forma rápida y eficaz para que la función de las células beta y la resistencia a la insulina mejoren de nuevo. Además, se ha demostrado que en pacientes con diabetes mellitus de tipo 2 recién diagnosticada, una terapia insulínica precoz e intensificada (en comparación con los antidiabéticos orales) conduce a una recuperación significativamente mejor de la función de las células beta y a una remisión glucémica más prolongada [9]. En una proporción considerable de pacientes, la diabetes mellitus de tipo 1 no se manifiesta hasta después de los 35 años [10], y hasta un 14% de todos los pacientes que se presentan fenotípicamente como diabéticos de tipo 2 tienen autoanticuerpos detectables de las células de los islotes como expresión de una patogénesis autoinmune de la diabetes [11]. Si existen indicios de una deficiencia absoluta de insulina o de diabetes mellitus de tipo 1, el inicio de la terapia con insulina también está indicado en esta situación.

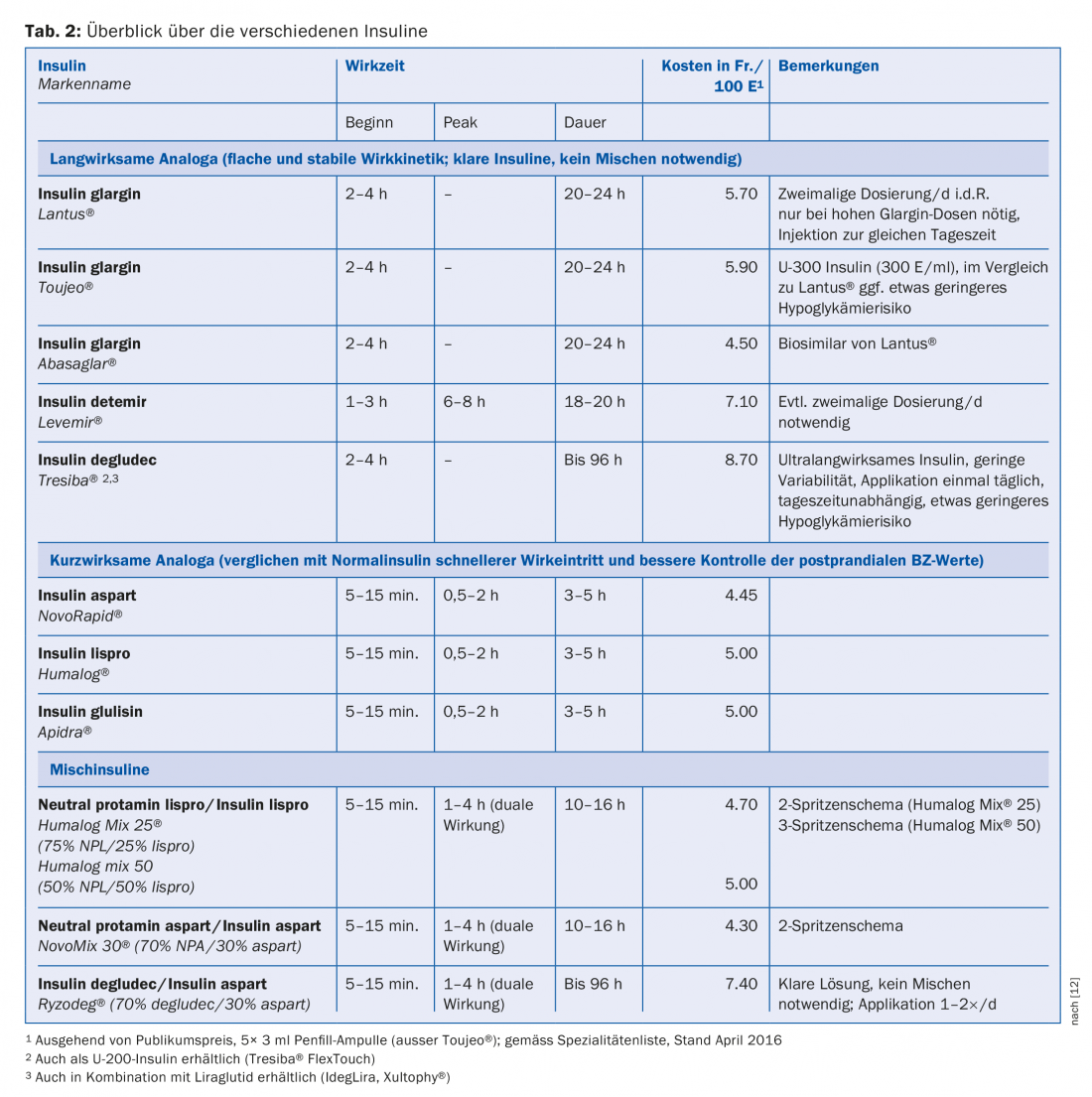
Los diferentes tipos de insulina
En función de su duración de acción, las insulinas se dividen en insulinas de acción rápida (prandiales), insulinas de acción prolongada (basales) e insulinas mixtas [12]. En una comparación directa, no existen diferencias en la reducción de la HbA1c entre los análogos de insulina y las insulinas regulares o NPH. Sin embargo, en la vida cotidiana y debido a aspectos prácticos (aplicación, menor intervalo inyección-comida, mejor control de los valores de glucemia posprandial, menor riesgo de hipoglucemia), los análogos de insulina se han impuesto tanto para la terapia basal como para la prandial. Los análogos se diferencian de la insulina humana por una estructura molecular modificada. Al sustituir ciertos aminoácidos o añadir ácidos grasos, se modifican las propiedades farmacodinámicas y farmacocinéticas, como la duración de la acción o el inicio de la misma. En la tabla 2 se muestra un resumen de los análogos de insulina (incluidas las insulinas mixtas) que se utilizan con frecuencia en la actualidad.
Información general sobre la aplicación práctica de la insulinoterapia
La terapia ideal con insulina normaliza los niveles de glucosa en sangre pre y posprandiales sin provocar hipoglucemia ni aumento de peso. Los regímenes de insulina conocidos (tab. 3) difieren en su complejidad y esfuerzo para el paciente.
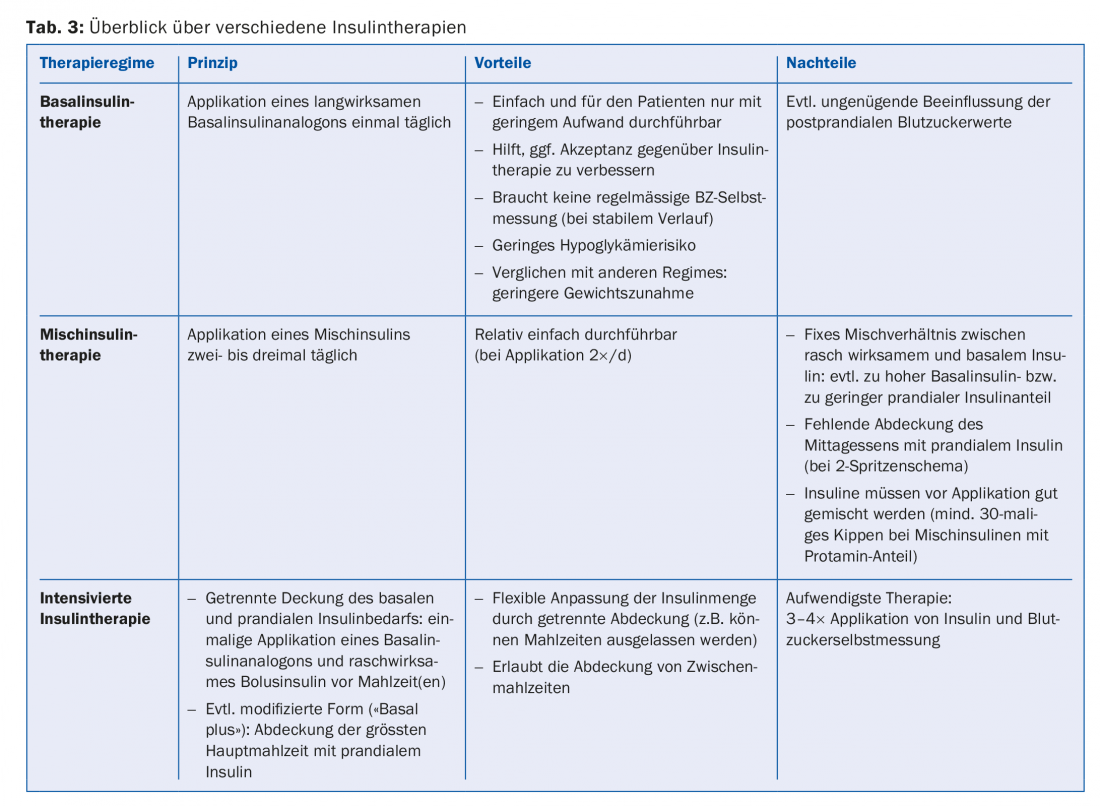
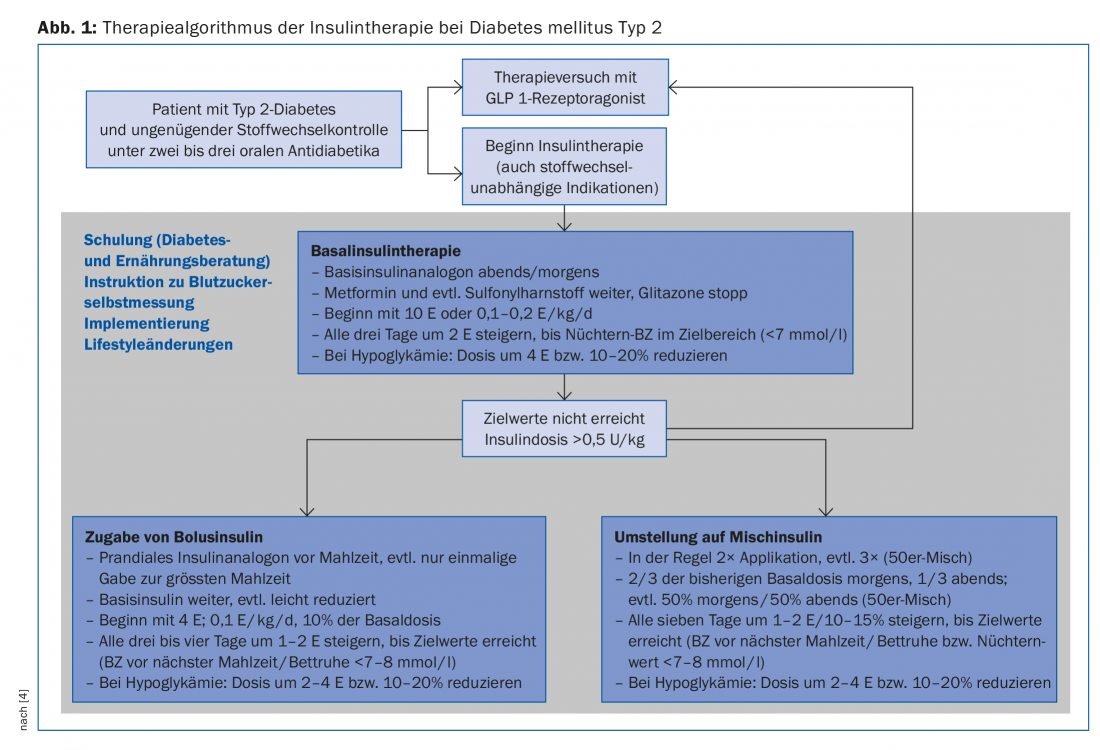
Por lo tanto, en un primer paso se suele optar por una terapia de insulina basal, que sólo se intensificará si no se alcanzan los valores objetivo o si la insulinoterapia vuelve a deteriorarse (Fig. 1).
La motivación o adherencia a las terapias inyectables contra la diabetes es fundamental para el éxito del tratamiento. La terapia con insulina supone a menudo un cambio drástico en el concepto de tratamiento para el paciente; la terapia debe adaptarse a los recursos específicos del paciente y requiere una formación considerable por parte de un equipo interdisciplinar.
Los efectos secundarios pueden empeorar significativamente la adherencia y deben evitarse en la medida de lo posible desde el principio y comentarse con el paciente incluso antes de iniciar la terapia. El riesgo de hipoglucemia puede reducirse de forma decisiva mediante el ajuste de la dosis y el entrenamiento (por ejemplo, prevención de situaciones de riesgo, reducción de la dosis de insulina tras un esfuerzo físico, titulación lenta de la dosis). El aumento de peso es, por un lado, una expresión de la mejora del control metabólico (reducción de la glucosuria), pero también puede tener otras razones, por ejemplo la ingesta de tentempiés para prevenir la hipoglucemia. En la práctica clínica, este efecto secundario es probablemente una de las razones más frecuentes del fracaso de la insulinoterapia o uno de los factores más importantes por los que se rechaza la insulinoterapia o se inicia demasiado tarde. Las terapias combinadas con antidiabéticos más recientes -además de subrayar la importancia de los cambios en el estilo de vida en esta situación- pueden ser un apoyo adicional en este caso.
Terapia de insulina basal
Con diferencia, la terapia más fácil de llevar a cabo es la insulinoterapia basal (Fig. 2), que se realiza como terapia añadida a la terapia existente con fármacos antidiabéticos orales. Los fármacos antidiabéticos orales -a excepción de las glitazonas- se suelen pasar; en concreto, la combinación con metformina tiene un efecto ahorrador de insulina [13]. Las sulfonilureas ayudan a controlar los niveles de glucemia postprandial, pero pueden aumentar el riesgo de hipoglucemia en combinación con la insulina. Además, se vuelven cada vez más ineficaces a medida que aumenta la duración de la diabetes y disminuye la función de las células beta.
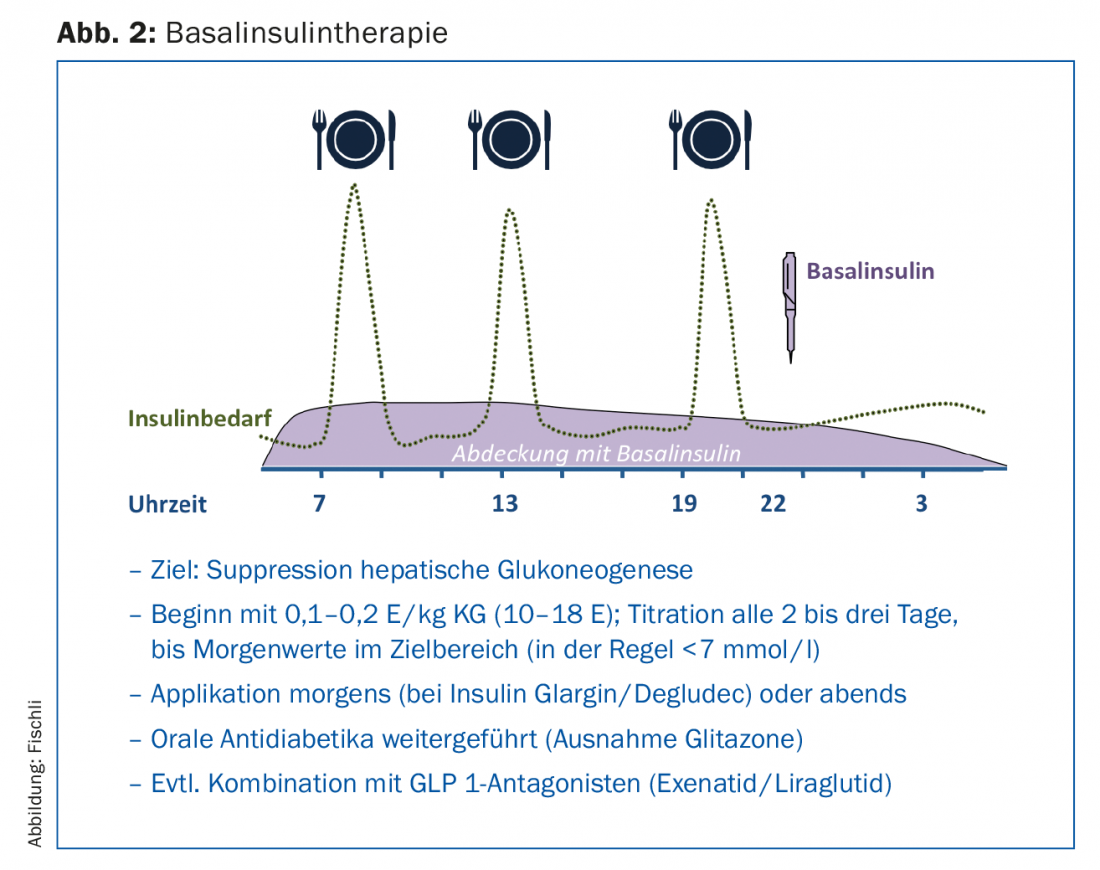
La aplicación de un análogo de insulina basal de acción prolongada inhibe principalmente la gluconeogénesis hepática y reduce así los niveles elevados de glucosa en sangre en ayunas, así como los niveles en la fase postabsortiva. Con valores de HbA1c superiores al 8,5%, los valores elevados de glucemia en ayunas influyen especialmente en la situación metabólica [14], por lo que el tratamiento con insulina basal mejora decisivamente el control de la glucemia también en estas situaciones. En los estudios, la glargina [15] o la insulina detemir [16] en combinación con metformina consiguieron un valor de HbA1c inferior al 7% en aproximadamente dos tercios de los pacientes. Al dosificar, debe tenerse en cuenta que la insulina se aumenta gradualmente hasta alcanzar los valores objetivo (estrategia “tratar hasta el objetivo”). Este aumento puede realizarlo el propio paciente con la formación adecuada (Fig. 1).
En comparación con la insulinoterapia prandial o mixta, la insulinoterapia básica ofrece las ventajas de un menor aumento de peso y el menor riesgo de hipoglucemia [17]. Especialmente para los conductores de vehículos a motor, este último punto es crucial. En 2015, un grupo de trabajo interdisciplinar revisó las directrices sobre la aptitud para conducir y la capacidad de conducción en la diabetes mellitus [18]. Las personas sin factores de riesgo (es decir, sin trastorno de sensibilización a la hipoglucemia y sin antecedentes de hipoglucemia grave) que son tratadas exclusivamente con un análogo de insulina basal (por ejemplo, insulina glargina o detemir) tienen un riesgo global bajo de hipoglucemia, razón por la cual ya no es necesaria la medición rutinaria de la glucemia antes de cada viaje en coche.
Combinación con otros fármacos antidiabéticos
Combinar la terapia de insulina con inhibidores de la DPP IV o agonistas de los receptores GLP 1 es posible y ofrece varias ventajas [19]. La combinación de insulina y análogo GLP 1 es cada vez más popular. La secuencia, es decir, qué clase de sustancia se da primero, no importa realmente. La insulina basal puede iniciarse en primer lugar, o la insulina puede combinarse con agonistas de los receptores GLP 1 como terapia añadida.
Farmacológicamente, ambas sustancias tienen un efecto hipoglucemiante y sinérgico a través de diferentes mecanismos [20]. Sin embargo, la influencia del agonista del receptor GLP 1 en la regulación central del apetito y la saciedad ayuda a prevenir el aumento de peso bajo tratamiento insulínico. Cada vez hay más datos que respaldan los beneficios de esta terapia combinada en términos de progresión de peso, control metabólico y riesgo de hipoglucemia [21].
En Suiza, la exenatida (Byetta®) y la liraglutida (Victoza®) están aprobadas para su combinación con insulina básica; la liraglutida también está disponible en combinación fija con insulina degludec (Xultophy®). El más nuevo dulaglutida una vez a la semana (Trulicity®) está aprobado en combinación con insulina prandial. El grupo más reciente de fármacos antidiabéticos, los inhibidores de SGLT 2, también tienen un efecto ahorrador de insulina o reductor de peso en combinación con la insulina [22].
Intensificación de la terapia con insulina
Debe considerarse la intensificación o el cambio de la terapia con insulina si el control metabólico se deteriora aún más o los efectos secundarios (hipoglucemia, aumento de peso) complican la terapia (Fig. 1). Antes de añadir una insulina prandial o cambiar a una insulina mixta, merece la pena probar un agonista del receptor GLP 1 en combinación con la insulina básica.
La intensificación de la terapia con insulina se realiza añadiendo un análogo de insulina de acción rápida antes de las comidas como un régimen clásico de bolo básico o cambiando a una terapia de insulina mixta. Sin embargo, esta última presenta algunas desventajas (tab. 3), y en comparación directa con la insulina básica en bolo, las insulinas mixtas obtienen peores resultados en términos de control metabólico [23].
Literatura:
- Polonsky WH, et al: Resistencia psicológica a la insulina en pacientes con diabetes tipo 2: el alcance del problema. Diabetes Care 2005; 28(10): 2543-2545.
- Nakar S, et al: Transición a la insulina en la diabetes de tipo 2: la idea errónea de los médicos de familia sobre los temores de los pacientes contribuye a las barreras existentes. J Diabetes Complications 2007; 21(4): 220-226.
- Romano G, et al.: Tratamiento con insulina y sulfonilureas en pacientes con DMNID. ¿Son diferentes los efectos sobre el metabolismo de las lipoproteínas incluso con un control similar de la glucemia? Diabetes 1997; 46(10): 1601-1606.
- Inzucchi SE, et al: Gestión de la hiperglucemia en la diabetes tipo 2, 2015: un enfoque centrado en el paciente: actualización de una declaración de posición de la Asociación Americana de Diabetes y la Asociación Europea para el Estudio de la Diabetes. Diabetes Care 2015; 38(1): 140-149.
- Holman RR, et al: Seguimiento durante 10 años del control intensivo de la glucosa en la diabetes tipo 2. N Engl J Med 2008; 359(15): 1577-1589.
- Gerstein HC, et al: Efectos de la reducción intensiva de la glucosa en la diabetes tipo 2. N Engl J Med 2008; 358(24): 2545-2559.
- Patel A, et al: Control intensivo de la glucemia y resultados vasculares en pacientes con diabetes tipo 2. N Engl J Med 2008; 358(24): 2560-2572.
- Duckworth W, et al: Control de la glucosa y complicaciones vasculares en veteranos con diabetes tipo 2. N Engl J Med 2009; 360(2): 129-139.
- Weng J, et al: Efecto de la terapia intensiva con insulina sobre la función de las células beta y el control glucémico en pacientes con diabetes tipo 2 recién diagnosticada: un ensayo multicéntrico aleatorizado de grupos paralelos. Lancet 2008; 371(9626): 1753-1760.
- Harris MI, Robbins DC: Prevalencia de la IDDM de inicio en la edad adulta en la población estadounidense. Diabetes Care 1994; 17(11): 1337-1340.
- Laugesen E, et al: Diabetes autoinmune latente del adulto: conocimientos actuales e incertidumbre. Diabet Med J Br Diabet Assoc 2015; 32(7): 843-852.
- Wallia A, Molitch ME: Terapia con insulina para la diabetes mellitus tipo 2. JAMA 2014; 311(22): 2315-2325.
- Hemmingsen B, et al: Comparación de metformina e insulina frente a insulina sola para la diabetes tipo 2: revisión sistemática de ensayos clínicos aleatorizados con metaanálisis y análisis secuenciales de ensayos. BMJ 2012; 344: e1771.
- Monnier L, et al.: Contribuciones de los incrementos de glucosa plasmática en ayunas y postprandial a la hiperglucemia diurna global de los pacientes diabéticos de tipo 2 Variaciones con el aumento de los niveles de HbA1c. Diabetes Care 2003; 26(3): 881-885.
- Riddle MC, et al: The treat-to-target trial: randomized addition of glargine or human NPH insulin to oral therapy of type 2 diabetic patients. Diabetes Care 2003; 26(11): 3080-3086.
- Hermansen K, et al: A 26-week, randomized, parallel, treat-to-target trial comparing insulin detemir with NPH insulin as add-on therapy to oral glucose-lowering drugs in insulin-naive people with type 2 diabetes. Diabetes Care 2006; 29(6): 1269-1274.
- Holman RR, et al: Eficacia a tres años de los regímenes complejos de insulina en la diabetes tipo 2. N Engl J Med 2009; 361(18): 1736-1747.
- http://sgedssed.ch/fileadmin/files/6_empfehlungen_fachpersonen/61_richtlinien_fachaerzte/Neue-Auto-Richtlinien_SGED_15-11-24_DE-DEFkorr.pdf
- Yki-Järvinen H, et al: Efectos de la adición de linagliptina a los regímenes de insulina basal para la diabetes tipo 2 controlada inadecuadamente. Diabetes Care 2013; 36(12): 3875-3881.
- Del Prato S: Combinación de relación fija de insulina basal y agonista del receptor GLP-1: ¿dos mejor que uno? Lancet Diabetes Endocrinol 2014; 2(11): 856-858.
- Eng C, et al: Glucagon-like peptide-1 receptor agonist and basal insulin combination treatment for the management of type 2 diabetes: a systematic review and meta-analysis. Lancet 2014; 384(9961): 2228-2234.
- Nauck MA: Actualización sobre la evolución de los inhibidores de SGLT2 en el tratamiento de la diabetes de tipo 2. Drug Des Devel Ther 2014; 8: 1335-1380.
- Giugliano D, et al.: Eficacia de los análogos de insulina para alcanzar el objetivo de hemoglobinaA1c de <7% en la diabetes tipo 2: metaanálisis de ensayos controlados aleatorizados. Diabetes Care 2011; 34(2): 510-517.
PRÁCTICA GP 2016; 11(5): 8-14