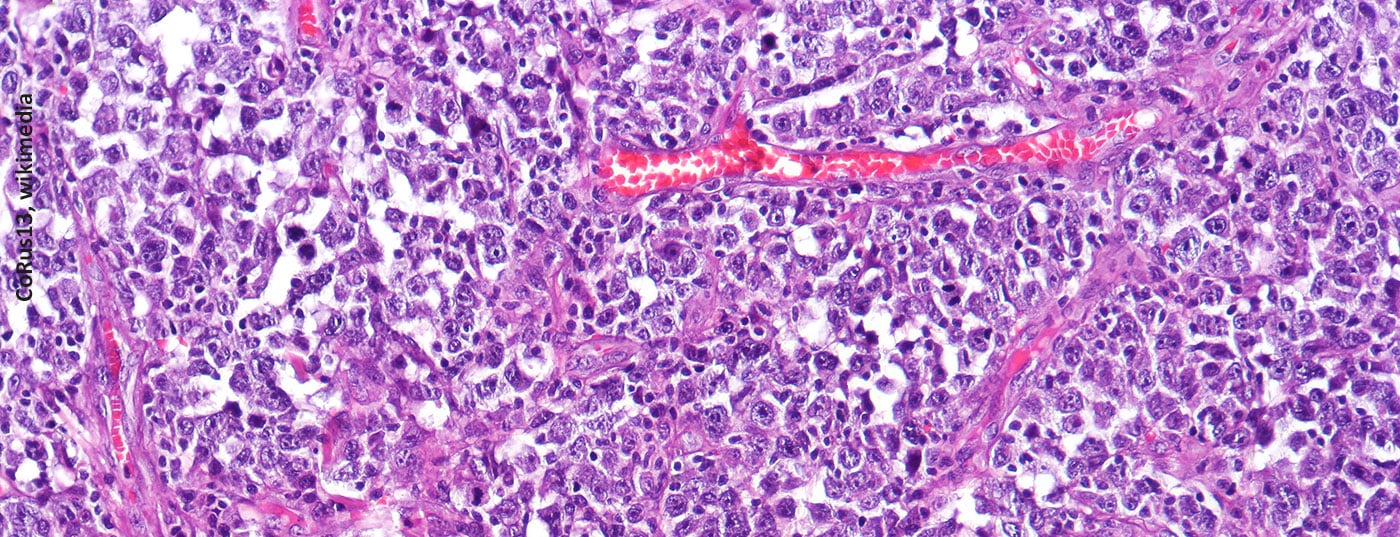
El linfoma difuso de células B grandes es la forma más común de linfoma no hodgkiniano. Si no se tratan, las acumulaciones de células de linfoma dificultan la función de los órganos afectados y provocan la muerte de los pacientes en pocos meses. La estrategia de tratamiento depende del estadio de la enfermedad y de la evolución hasta el momento, así como de las características generales del paciente. Para los adultos con LDCBG en recaída o refractario que no reúnen los requisitos para un trasplante de células madre hematopoyéticas, desde el año pasado se dispone de un conjugado anticuerpo-fármaco como opción de tratamiento adicional.
En Suiza, cada año se diagnostica un linfoma no hodgkiniano (LNH) a unas 1.500 personas [1]. La frecuencia aumenta de forma correlacionada con la edad y es de aproximadamente 2-3 por 100.000 habitantes en el grupo de 30 años, mientras que es de 70-120 por 100.000 habitantes en el grupo de 80 años. Histológicamente, el LNH se divide en los linfomas de células B, más comunes, y los linfomas de células T, menos comunes. Se desconoce la etiología del LNH, pero hay indicios de una conexión con enfermedades víricas (por ejemplo, el virus de Epstein-Barr, el VIH, la hepatitis B, la hepatitis C). Bacterias como la Helicobacter pylori también aumentan el riesgo de linfoma. Dado que el linfoma difuso de células B grandes (LDCBG) progresa rápidamente y disemina las células linfomatosas en el organismo incluso en las primeras fases de la enfermedad, es uno de los linfomas agresivos [2,3]. La clasificación REAL se utiliza para definir las linfomentidades según marcadores morfológicos, clínicos, inmunofenotípicos y genéticos moleculares [3,4].
Clasificación diagnóstica según los criterios de Lugano
Clínicamente, la enfermedad suele manifestarse como una linfadenopatía rápidamente progresiva, manifestaciones extraganglionares y síntomas generales [6]. Por lo general, los ganglios linfáticos agrandados no son dolorosos, a diferencia de los ganglios sensibles que suelen aparecer con las infecciones víricas. Si hay hallazgos palpatorios positivos de ganglios linfáticos superficiales agrandados junto con pruebas de laboratorio patológicas (por ejemplo, recuento anormal de leucocitos y deshidrogenasa láctica patológica [LDH]-valor), la sospecha puede confirmarse mediante un examen ecográfico de los ganglios linfáticos superficiales o una tomografía computarizada (TC) [3]. Estos dos métodos de obtención de imágenes también son muy adecuados para la biopsia selectiva de ganglios linfáticos, siempre que no se vaya a realizar una resección de ganglios linfáticos. Posteriormente, se realizan otros diagnósticos principalmente mediante procedimientos de imagen transversal, en particular el [18F]FDG-PET/CT. La PET/TC ha sustituido en gran medida a la TC con contraste como medida recomendada y está firmemente anclada en las directrices clínicas, como la clasificación de Lugano de la ICML (Conferencia Internacional sobre Linfoma Maligno) [3,7,8].

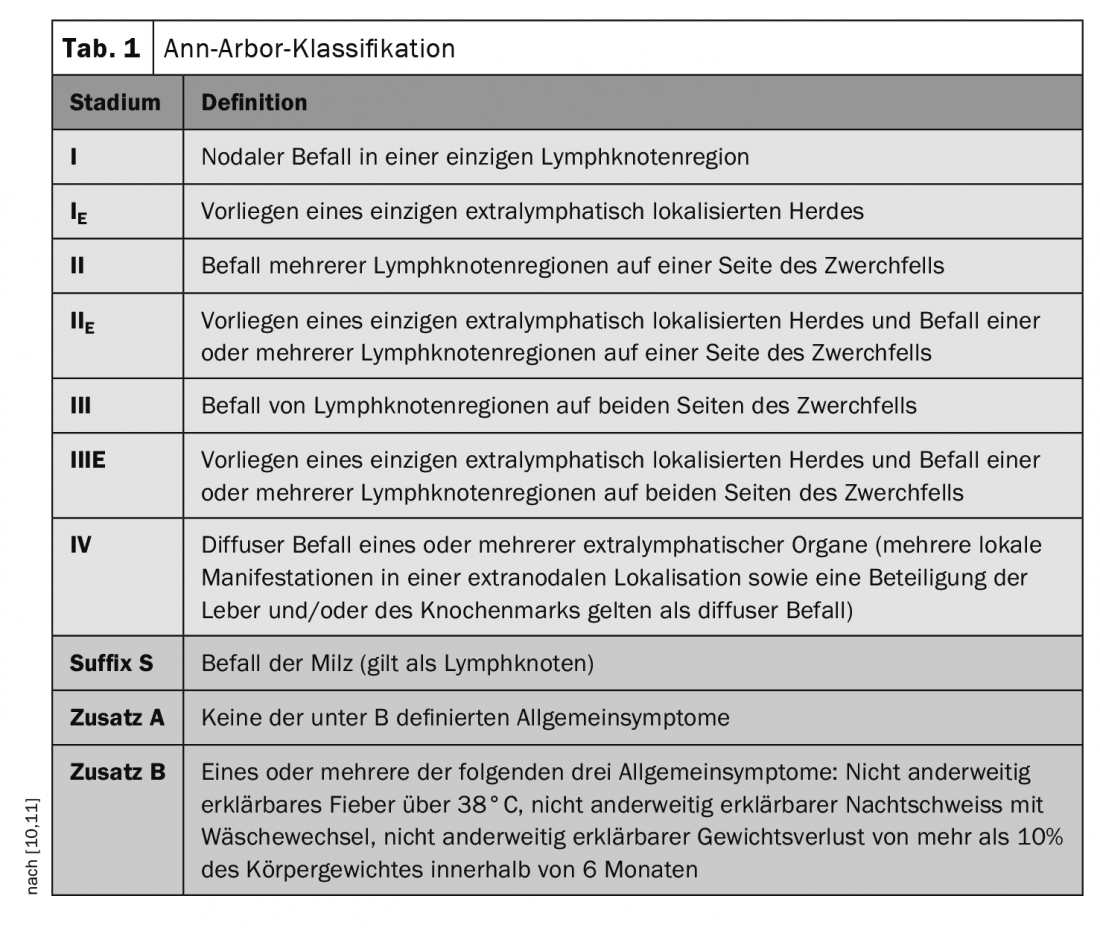
El diagnóstico por imagen no sólo es importante en el diagnóstico patológico de los ganglios linfáticos y las manifestaciones orgánicas de los linfomas Hodgkin y no Hodgkin, sino que también desempeña un papel importante en el curso de la enfermedad y en los cuidados de seguimiento (recuadro) [9]. El DLBCL se asigna a un estadio de la enfermedad (estadios I a IV) según la clasificación de Ann-Arbor (Tab. 1) [10,11]. Desde un ganglio linfático, las células malignas pueden migrar a través de los vasos linfáticos a los ganglios linfáticos vecinos y seguir multiplicándose allí. Sólo en las últimas fases del curso de la enfermedad las células del DLBCL invaden el sistema sanguíneo y entonces pueden afectar también a órganos no linfáticos.
El grupo de trabajo “Linfomas agresivos” de la Alianza Alemana contra el Linfoma ha publicado un folleto revisado sobre el linfoma difuso de células B grandes bajo la dirección del Prof. Björn Chapuy, Charité Universitätsmedizin Berlin.
Puede descargarse gratuitamente para médicos y pacientes en https://lymphome.de [5].
Tratamiento complementario con conjugado anticuerpo-fármaco
Si no se trata, el DLBCL es rápidamente mortal, por lo que el diagnóstico es una indicación para iniciar la terapia. La intención de la terapia es principalmente curativa, incluso en pacientes de edad avanzada y/o con comorbilidad. El tratamiento estándar es la quimioinmunoterapia R-CHOP (rituximab, ciclofosfamida, doxorrubicina, vincristina, prednisona). Sin embargo, alrededor del 40% de los pacientes presentan enfermedad refractaria o recurrente [6]. Para ellos, el conjugado anticuerpo-fármaco polatuzumab vedotin (Polivy®) está disponible desde el año pasado. Se trata de un anticuerpo contra CD79b, una subunidad del receptor de células B, unido al inhibidor de la mitosis monometil auristatina-E. En combinación con bendamustina y rituximab, el polatuzumab vedotin está indicado para el tratamiento de adultos con LDCBG en recaída o refractario que no sean elegibles para un trasplante de células madre hematopoyéticas [12].

Mayor SLP y SG en el brazo de estudio con polatuzumab vedotin
La aprobación de Polivy® se basa en el estudio aleatorizado y abierto de fase Ib/II GO29365 [13–15]. El estudio comparó la eficacia, seguridad y tolerabilidad del polatuzumab vedotin como complemento de la bendamustina más rituximab (BR) con la BR sola. El estudio incluyó una cohorte aleatorizada de pacientes con LDCBG pretratados que no reunían los requisitos para un trasplante autólogo de células madre hematopoyéticas y presentaban una enfermedad recidivante o refractaria tras al menos un régimen previo de quimioterapia sistémica. Entre los 80 pacientes aleatorizados al tratamiento con Polivy más BR (n=40) o BR sola (n=40), la mediana de edad era de 69 años (rango: 30-86 años). El 98% de los pacientes tenían un LDCBG no especificado (NOS). En conjunto, el 48% de los pacientes tenían un LDCBG ABC (de células B activadas) y el 40% un LDCBG GCB (similar a las células B del centro germinal).

Las participantes en el estudio aleatorizado 1:1 recibieron Polivy® más BR o BR sola durante seis ciclos de 21 días [9] (recuadro). El criterio de valoración principal del estudio fue la tasa de respuesta completa (RC) al final del tratamiento (6-8 semanas después del día 1 del 6º ciclo de tratamiento o del último tratamiento del estudio). Esto fue evaluado mediante PET-TC por un Comité de Revisión Independiente (IRC). Los resultados muestran que el 40% de las pacientes tratadas con Polivy® más BR lograron una respuesta completa (n=16/40), lo que significa que no se detectaron células cancerosas en el momento del estudio, en comparación con el 17,5% (n=7/40) tratadas sólo con BR. Además, se alcanzó una mediana de supervivencia libre de progresión (SLP) de 7,6 meses en el brazo del estudio con polatuzumab vedotin como tratamiento complementario en comparación con 2,0 meses en el brazo de control (IC 95%: 6,0-17,0 e IC 95%: 1,5-3,7, respectivamente). La mediana de la supervivencia global (SG) fue de 12,4 meses en los participantes tratados con polatuzumab vedotin más BR frente a 4,7 meses en el brazo de control.
Literatura:
- Kantonsspital Wintertur, www.ksw.ch/gesundheitsthemen/lymphsystem/non-hodgkin-lymphom-nhl/, (último acceso 03.03.2022)
- Red de Competencia en Linfoma Maligno,https://lymphome.de/diffus-grosszelliges-b-zell-lymphom (último acceso 03.03.2022)
- Mayerhöfer ME, Haug A: Imagen híbrida en el linfoma. Radiologist 2020; 60: 376-385.
- Harris NL, et al: Una clasificación euroamericana revisada de las neoplasias linfoides: una propuesta del Grupo Internacional de Estudio del Linfoma. Sangre 1994; 84: 1361-1392.
- “Nuevo: Folleto sobre “Linfoma difuso de células B grandes (DLBCL)” con las estrategias de tratamiento actuales”, Informationsdienst Wissenschaft, 05.01.2022; https://nachrichten.idw-online.de (última consulta: 03.03.2022).
- Siegmund-Schultze N: Linfoma difuso de células B grandes avanzado: polatuzumab vedotin prolonga la supervivencia libre de progresión en el contexto de primera línea. Dtsch Arztebl 2022; 119(5): A-190/B-157
- Cheson BD, et al: Recomendaciones para la evaluación inicial, la estadificación y la valoración de la respuesta del linfoma Hodgkin y no Hodgkin: la clasificación de Lugano. J Clin Oncol 2014; 32: 3059-3068.
- Barrington SF, et al: Papel de la imagen en la estadificación y evaluación de la respuesta del linfoma: consenso del Grupo de Trabajo de Imagen de la Conferencia Internacional sobre Linfomas Malignos. J Clin Oncol 2014; 32: 3048-3058.
- Centro de Tumores de Alta Austria, Guía médica, www.tumorzentrum.at/fileadmin/user_upload/20210928_Leitlinie_DLBCL.pdf (última consulta: 03.03.2022)
- Onkopedia, www.onkopedia.com/de/onkopedia/guidelines/diffuses-grosszelliges-b-zell-lymphom/@@guideline/html/index.html
- Lister TA, et al: Informe de un comité convocado para debatir la evaluación y estadificación de los pacientes con enfermedad de Hodgkin: Reunión de Cotswolds. J Clin Oncol 1989; 7: 1630-1636.
- Swissmedicinfo: Información sobre medicamentos, www.swissmedicinfo.ch (último acceso 03.03.2022)
- Sehn L, et al: Polatuzumab vedotin más bendamustina y rituximab en el linfoma difuso de células B grandes recidivante/refractario: resultados actualizados de un estudio aleatorizado de fase Ib/II y resultados preliminares de una extensión de un solo brazo. ASH Diciembre 2020 Abstract #3020 y Póster
- Agencia Europea de Medicamentos (EMA), Product information: Polivy® www.ema.europa.eu/en (última consulta: 03.03.2022)
- “Swissmedic concede la autorización de comercialización de Polivy de Roche para pacientes con linfoma agresivo pretratado”, Roche, 20.07.2021
- Revisión del CAD. ¿Qué son los conjugados anticuerpo-fármaco? https://adcreview.com/adc-university/adcs-101/antibody-drug-conjugates-adcs (última llamada 03.03.2022)
PRÁCTICA GP 2022, 17(3): 44-46
InFo ONCOLOGÍA Y HEMATOLOGÍA 2022, 10(2): 38-39