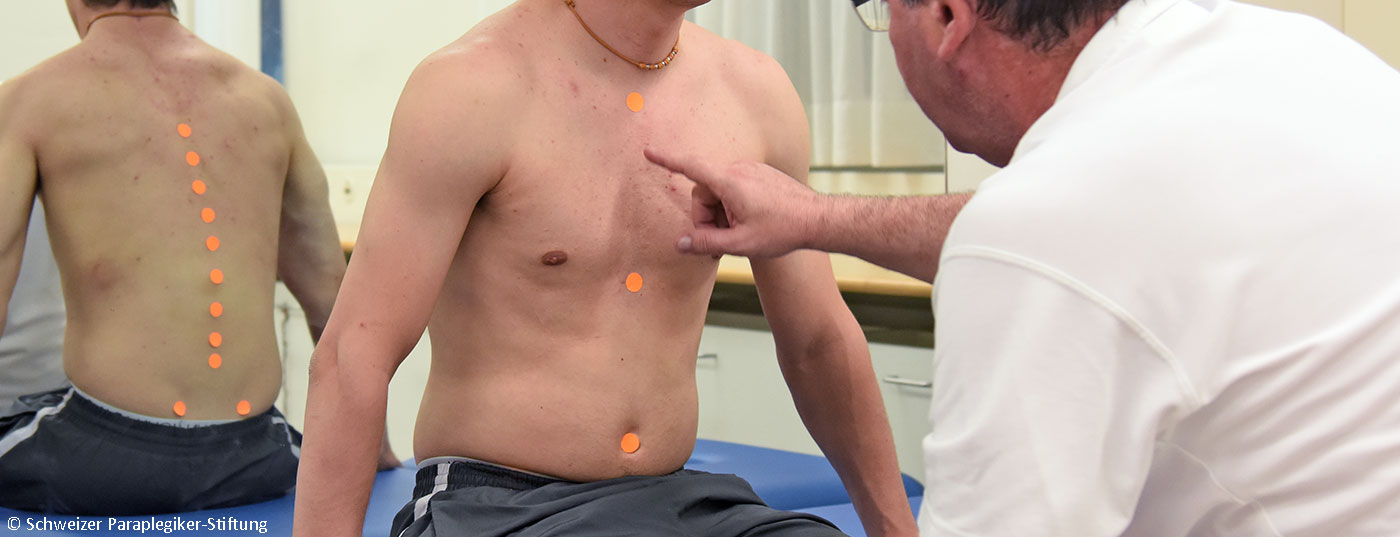
El dolor crónico es el problema de salud más común entre los pacientes con paraplejia. Debido a la aparición de diferentes tipos de dolor y mecanismos del dolor en el marco del modelo de enfermedad bio-psico-social, la terapia del dolor en este grupo de pacientes constituye un reto especial.
El dolor crónico es el problema de salud más común entre los pacientes con paraplejia. Debido a la aparición de diferentes tipos de dolor y mecanismos del dolor en el marco del modelo de enfermedad bio-psico-social, la terapia del dolor en este grupo de pacientes constituye un reto especial. Como demuestran datos recientes, esto puede tener éxito en un equipo interdisciplinar. A continuación se analizan la aparición, la importancia y la fisiopatología del dolor crónico en la paraplejia, así como los enfoques diagnósticos y terapéuticos.
Ocurrencia e importancia
Entre los cinco problemas de salud notificados con más frecuencia en pacientes con parálisis espinal en Suiza, el dolor ocupa el primer lugar [1], por delante de los problemas con la función de la vejiga, la higiene personal, el vaciado intestinal o la marcha. Una revisión pone de manifiesto la amplitud con la que el dolor afecta a diversos niveles somáticos, psicológicos y sociales [2]. Por ejemplo, el dolor crónico puede persistir y empeorar con el tiempo, repercutir negativamente en la participación y los resultados de la rehabilitación, provocar una discapacidad funcional con pérdida de movilidad, reducir la calidad de vida, alterar el sueño, interferir en la participación en las actividades cotidianas y dificultar la reincorporación al trabajo. La presencia de dolor neuropático en la fase temprana de tres a seis meses tras la lesión hace probable la persistencia de este dolor después de tres a cinco años.
Datos suizos recientes informan de una alta prevalencia del 74% de dolor crónico en pacientes con lesión medular, así como de factores de riesgo como el sexo femenino, la edad avanzada, las situaciones de penuria económica y los problemas de salud secundarios [3]. Los elevados datos de prevalencia también están en consonancia con los datos conocidos internacionalmente, con una prevalencia del dolor en parapléjicos del 84% [4]. Entre ellos, además del dolor musculoesquelético, que muestra una prevalencia del 59%, el dolor neuropático también ocupa una posición elevada (dolor neuropático a nivel de la lesión 41%, por debajo del nivel de la lesión 34%). Entre los dolores musculoesqueléticos, el dolor de espalda es el más frecuente con un 43-55% [5] y el dolor de hombro con un 35% [6]. La elevada prevalencia de la espasticidad en la paraplejia, del 71% [7], es significativa debido a los vínculos existentes entre la espasticidad y el dolor [8].
Clasificación del dolor en la paraplejia
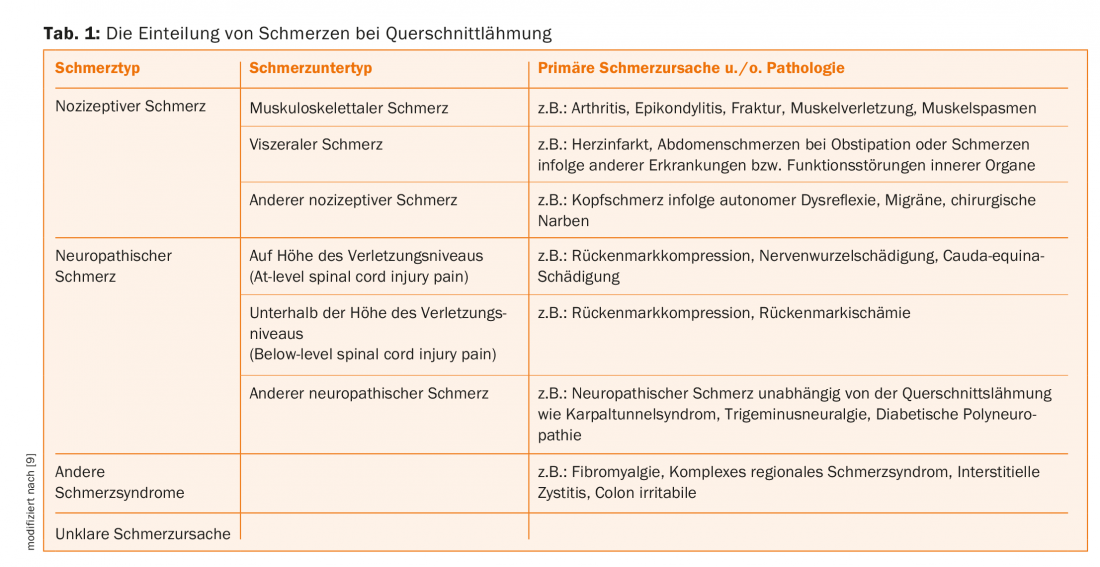
Según la clasificación del dolor por paraplejia actualizada por la Sociedad Internacional de la Médula Espinal en 2012, distinguimos entre dolor nociceptivo, neuropático, otros síndromes de dolor definidos y dolor no asignable [9]. (Tab. 1). En consecuencia, el dolor nociceptivo se divide en dolor musculoesquelético debido a patologías musculares, óseas o articulares, dolor visceral debido a enfermedades y disfunciones de los órganos internos y otros dolores nociceptivos como el dolor de cabeza debido a la disreflexia autonómica. El dolor debido a la espasticidad también se clasifica como dolor nociceptivo. En el grupo del dolor neuropático, se distingue entre el dolor neuropático debido a una lesión nerviosa, que está directamente relacionado con la lesión de la médula espinal o la lesión de la cauda equina, por un lado, y el dolor neuropático, que es independiente de las lesiones mencionadas, por otro. Los primeros se dividen en dolor por lesión medular a nivel y dolor por lesión medular por debajo del nivel. Los dolores neuropáticos independientes de la paraplejia, como el síndrome del túnel carpiano, la neuralgia del trigémino, la polineuropatía diabética, etc., se denominan “otros dolores neuropáticos”. Los síndromes de dolor definidos como la fibromialgia, el síndrome de dolor regional complejo o el colon irritable se cuentan entre los denominados otros síndromes de dolor. Por último, no siempre es posible clasificar etiológicamente el síndrome doloroso. En este caso, el síndrome de dolor se denomina “dolor no atribuible” [9,10]. Las características clínicas para distinguir los tipos de dolor mencionados se muestran en el cuadro 1.

Diagnóstico del dolor en parapléjicos
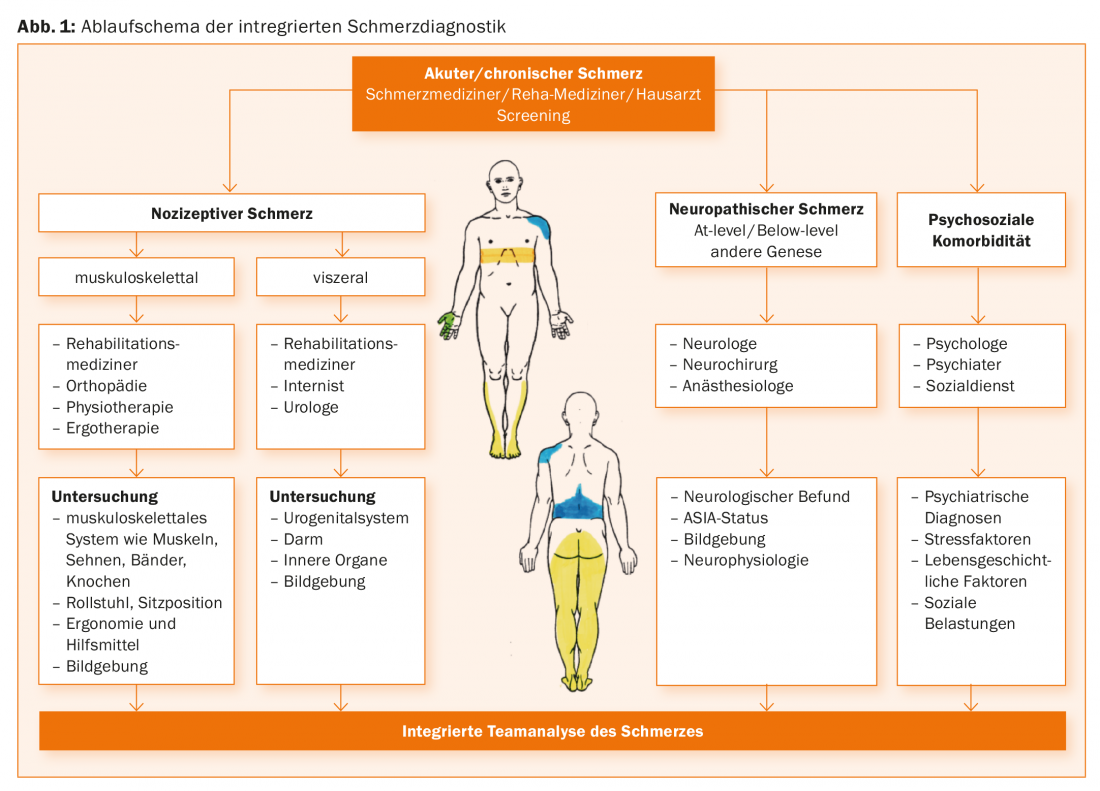
Para una descripción detallada de los pasos del diagnóstico, consulte la bibliografía [10]. Como se detalla más adelante, el tratamiento interdisciplinar multimodal del dolor también incluye el diagnóstico integrado del dolor en todos los equipos [11]. En la figura 1 se muestra un algoritmo de diagnóstico. En consecuencia, cualquier persona implicada en el cuidado de pacientes parapléjicos, idealmente un médico especialista en dolor, debería considerar la presencia de diferentes tipos de dolor basándose en las características clínicas presentadas en la visión general 1 y, según la sospecha diagnóstica de dolor nociceptivo o neuropático, consultar las disciplinas individuales paso a paso, dependiendo de la presentación clínica. Clínicamente, deben registrarse las localizaciones del dolor (es útil dibujar el dolor), información sobre el carácter del dolor, la intensidad del dolor, el curso del dolor durante el día y la dependencia de la actividad física y las funciones orgánicas. Al final, lo ideal es que todos los médicos y terapeutas implicados discutan juntos los resultados de los exámenes y emitan diagnósticos que todos los miembros del equipo puedan respaldar en esencia.
El dolor nociceptivo, tal y como lo define la Asociación Internacional para el Estudio del Dolor (IASP) [12], es el resultado de la activación de los nociceptores debido a un daño real o inminente en el tejido no neuronal. Aquí, a diferencia del dolor neuropático, existe una función normal del sistema somatosensorial. Dependiendo del cuadro clínico, los médicos rehabilitadores, los cirujanos ortopédicos, los internistas, los urólogos, los fisioterapeutas y los terapeutas ocupacionales deben participar en el diagnóstico para descubrir las causas del sistema musculoesquelético, como los músculos, los tendones, los ligamentos y los huesos. También suele ser necesaria una evaluación de la silla de ruedas y de su ergonomía, incluida la posición sentada. En cuanto al sistema visceral, el examen del sistema urogenital, del sistema intestinal y de los órganos internos desempeña un papel importante. En general, también deben incluirse las técnicas de imagen.
El dolor neuropático es definido por la IASP como el dolor causado por una lesión o enfermedad del sistema somatosensorial [12]. Se recomienda un esquema de clasificación para el diagnóstico del dolor neuropático [13], que está disponible de forma adaptada para el diagnóstico del dolor neuropático debido a la paraplejia [14]. En este caso, se requiere la presencia de una paraplejia y dolor a nivel de la lesión o por debajo de ella anamnésicamente, la evidencia de una lesión de la médula espinal o de la cauda equina por aparatos y la exclusión de otras causas de dolor para el diagnóstico diferencial. Si sólo se cumple la información anamnésica, como los antecedentes de paraplejia y dolor en el nivel de la lesión o por debajo de éste, se trata de un posible dolor neuropático. Si además se cumplen todos los criterios diagnósticos siguientes, como la demostración de signos sensoriales positivos o negativos, la evidencia aparente de una lesión de la médula espinal o la cauda equina y la exclusión de otras causas de dolor, existe un dolor neuropático definitivo. Si sólo se cumplen dos de los tres criterios mencionados, sólo puede diagnosticarse un probable dolor neuropático debido a una paraplejia.
Como ya se ha mencionado, el nivel de la lesión desempeña un papel importante en la clasificación del dolor neuropático en la paraplejia. El nivel neurológico de la lesión se define como el segmento más caudal de la médula espinal con sensibilidad normal al tacto leve y sensación aguda y función motora normal [15]. En consecuencia, se habla de dolor neuropático a nivel de la lesión (dolor a nivel de la lesión medular) cuando se produce en el dermatoma del nivel de la lesión neurológica, incluida la médula espinal. hasta tres de los dermatomas subyacentes. Por otro lado, el dolor neuropático por debajo del nivel de la lesión medular es un dolor que se extiende más de tres dermatomas por debajo del nivel de la lesión o que, en general, está por debajo del nivel de la lesión. Mientras que el dolor neuropático a nivel de la lesión puede ser de origen neuropático central en el caso de una lesión de la médula espinal, así como de origen neuropático periférico en el caso, por ejemplo, de una lesión traumática de la raíz nerviosa a nivel de la lesión, el dolor neuropático por debajo del nivel de la lesión es siempre, por definición, un dolor neuropático generado centralmente. El dolor neuropático en el síndrome de la cauda equina representa una forma especial, ya que corresponde a una causa neuropática periférica del dolor debido a la lesión de la raíz nerviosa de la cauda equina y, por lo tanto, se clasifica por definición en el grupo del dolor neuropático a nivel de la lesión, aunque la extensión del dolor se encuentre más allá de tres segmentos por debajo del nivel de la lesión neurológica [9]. La aparición de dolor neuropático más tarde de un año tras la lesión o el cambio del síndrome doloroso tras un intervalo estable, entonces posiblemente asociado también a un cambio del estado neurológico, puede ser una expresión de siringomielia u otra patología espinal. En cualquier caso, la toma de imágenes debe realizarse aquí, si procede, mediante resonancia magnética (RM). Si es necesario, hay que implicar a los neurocirujanos en el diagnóstico. La siringomielia se produce con mayor frecuencia después de una media de 15 años tras un traumatismo, predominantemente en casos de paraplejia completa y a nivel de la columna cervical [16].
Diagnóstico neurofisiológico e instrumental
Según el esquema diagnóstico mencionado, el diagnóstico de lesión de la médula espinal o de la cauda equina se realiza mediante resonancia magnética como procedimiento estándar [17]. Aquí, en la mayoría de los casos, pueden detectarse lesiones tanto en pacientes con dolor neuropático debido a la paraplejia como sin él. En este caso, la neurofisiología clínica tiene una importancia secundaria en el diagnóstico del dolor neuropático, ya que los pacientes sin dolor neuropático también muestran hallazgos patológicos. Los exámenes electrofisiológicos pueden complementar el examen clínico y mejorar el diagnóstico de la paraplejia. Entre ellos se incluyen los potenciales evocados somatosensoriales (SEP) como prueba de la función de la médula posterior, los potenciales evocados láser (LEP) y los potenciales evocados térmicos de contacto (CHEPS) como prueba de la función del tracto espinotalámico anterior, los potenciales evocados motores tras la estimulación magnética transcraneal como prueba del tracto corticoespinal y la respuesta simpática cutánea como prueba de las vías simpáticas de la médula espinal [18].
Como ya se ha explicado, el diagnóstico del dolor neuropático implica el examen del sistema somatosensorial [13]. En el caso de una lesión dudosa (por ejemplo, debido a artefactos metálicos en la resonancia magnética) o una lesión atípica en la resonancia magnética (lesión fuera de las vías sensoriales), el uso de procedimientos especiales sólo disponibles en centros como el LEP y las pruebas sensoriales cuantitativas (QST) pueden apoyar el diagnóstico de dolor neuropático debido a una paraplejia [19]. Las pruebas sensoriales cuantitativas crean un perfil de fenómenos sensoriales positivos y negativos [20]. La QST ha demostrado que el desarrollo de dolor neuropático debido a la paraplejia está asociado a un aumento de la sensibilidad, como la hiperalgesia por pinchazo y la alodinia [21,22], por lo que la QST puede ser capaz de identificar a los pacientes con riesgo de sufrir dolor neuropático en una fase temprana.
En cuanto a los amplios mecanismos en el desarrollo del dolor neuropático debido a la paraplejia, remitimos a [10].
[24]Los factores psicológicos desempeñan un papel central en el procesamiento del dolor según el modelo bio-psico-social de la enfermedad [23]. Según esto, factores como la catastrofización del dolor, la ansiedad relacionada con el dolor, la tensión y la evitación del dolor, así como la impotencia, pueden conducir a una intensificación del dolor y a un peor afrontamiento del mismo. Entre los factores que pueden reducir la intensidad del dolor y mejorar su tratamiento se incluyen la autoeficacia, las estrategias de tratamiento del dolor, la disposición al cambio y la aceptación del dolor. La implicación de los factores mencionados también pudo confirmarse en pacientes con dolor crónico en la paraplejia [3,25,26]. Para evaluar los factores psicológicos mencionados que pueden contribuir a la cronificación o el mantenimiento del dolor, siempre debe realizarse una evaluación psicológica si se sospecha de los mismos. Los indicios de factores psicosociales acompañantes relevantes pueden incluir síntomas depresivos, trastornos del apetito, baja motivación o participación con respecto a las actividades diarias, indicios de catastrofismo o sesgo con respecto al diagnóstico del dolor, síntomas de ansiedad y pánico, trastornos del sueño, falta de apoyo familiar o indicios de abuso o dependencia del alcohol, las drogas o los medicamentos [27].
Enfoque terapéutico multimodal interdisciplinar
De acuerdo con el modelo bio-psico-social de la enfermedad [23], se ha establecido un enfoque terapéutico multimodal interdisciplinar en el tratamiento del dolor crónico [11]. Esto implica un enfoque integrado de todo el equipo que incluya disciplinas médicas, fisioterapéuticas, psicológicas y de otro tipo. El núcleo de este enfoque son las reuniones periódicas del equipo y la comunicación interprofesional estructurada. Este enfoque puede tener lugar en un entorno de paciente individual, en el que todos los médicos y terapeutas implicados tratan al paciente sobre la base de citas individuales, o en el marco de programas de grupo firmemente establecidos. En el mejor de los casos, un parapléjico con dolor debe ser tratado en un centro con la experiencia adecuada. Por el contrario, un equipo ambulatorio de terapeutas individuales también puede lograr buenos resultados con una buena comunicación.
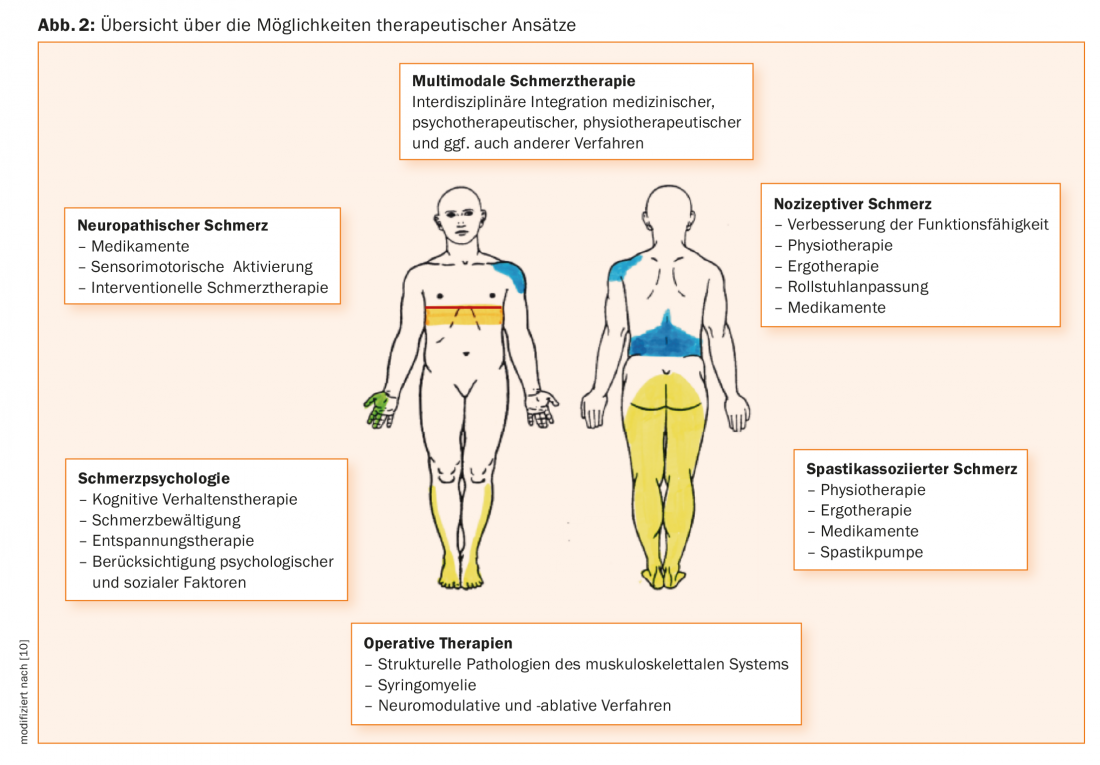
Dado que el dolor aparece pronto en los pacientes con paraplejia y tiende a persistir, se recomienda un tratamiento precoz [28]. Un enfoque terapéutico interdisciplinar se considera en una revisión reciente [29]. Visión general 2 ofrece una visión general de las opciones terapéuticas actuales que deben aplicarse en un equipo interdisciplinar.
Terapia médica
Terapia farmacológica antinociceptiva: La terapia farmacológica para el dolor nociceptivo incluye analgésicos no opiáceos (por ejemplo, paracetamol, metamizol, antiinflamatorios no esteroideos [NSAR]) y también opiáceos. Sin embargo, según una directriz terapéutica para pacientes con dolor de espalda crónico sin parálisis espinal, esos medicamentos son sólo una opción terapéutica de apoyo y deben revisarse en cuanto a su efecto y efectos secundarios cada cuatro semanas o en cuanto a la continuación de la terapia cada tres meses [30]. Si el dolor y la espasticidad interactúan, también debe intentarse optimizar la terapia de la espasticidad. En caso de dolor visceral relacionado con la actividad intestinal, debe considerarse la optimización de los movimientos intestinales mediante laxantes.
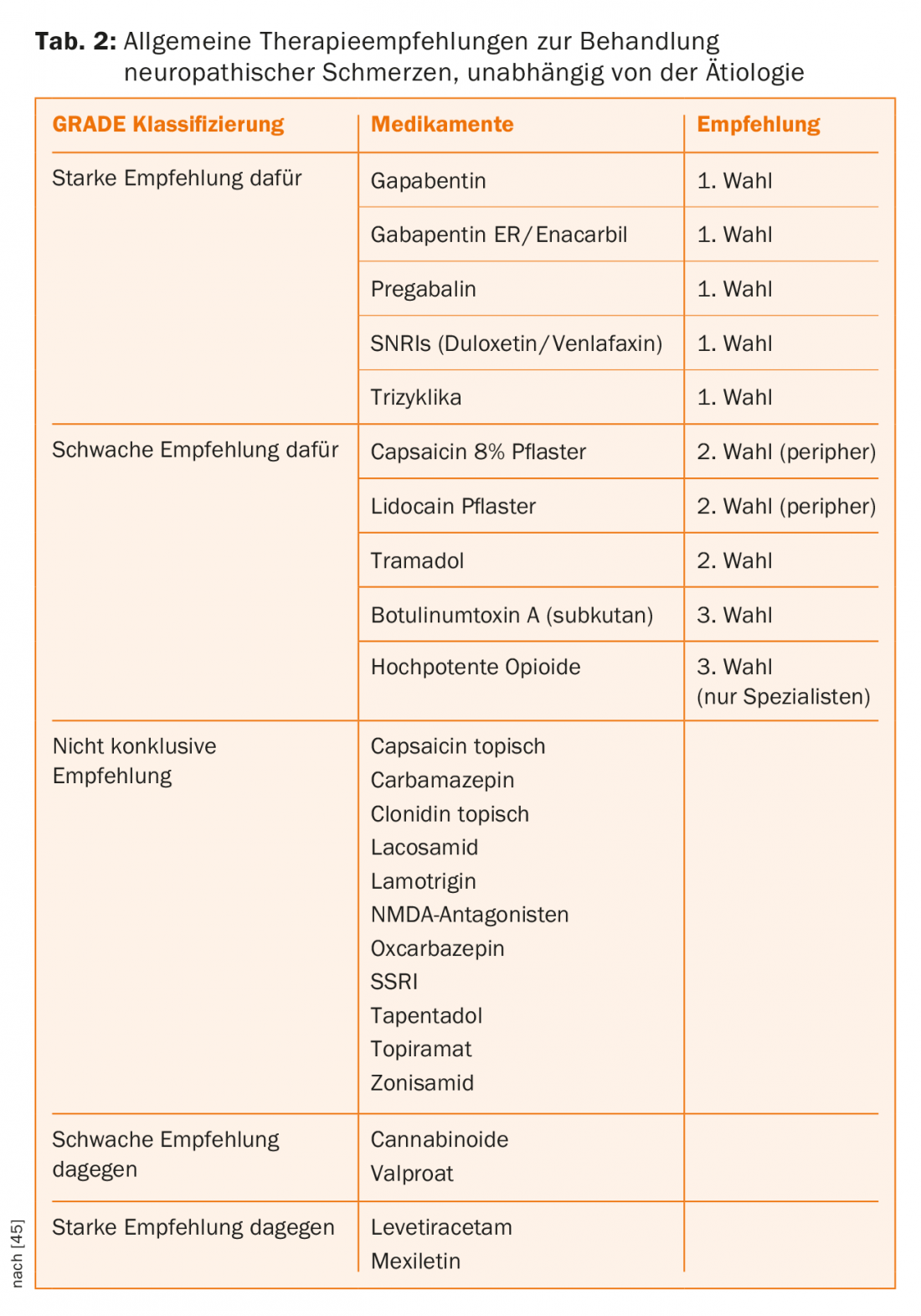
Tratamiento farmacológico antineuropático: El tratamiento farmacológico del dolor neuropático debido a la paraplejia se resume en una directriz actual [31]. En este caso, se recomiendan la pregabalina, la gabapentina y la amitriptilina como fármacos de primera línea, y el tramadol y la lamotrigina como fármacos de segunda línea, esta última sólo en casos de paraplejia incompleta. Los opiáceos se consideran la terapia de cuarta línea (Tabla 2). Si no se consigue el éxito con estas opciones de medicación, se puede recurrir a las recomendaciones terapéuticas generales de la IASP (Tabla 2).
Tratamiento intervencionista/neuroquirúrgico del dolor: Para el dolor neuropático debido a la paraplejia, las pruebas de procedimientos como la estimulación epidural de la médula espinal (EME), la estimulación cerebral profunda (ECP), la estimulación de la corteza motora (ECM), la cirugía de lesión de la zona de entrada de la raíz dorsal (DREZ) y la mielotomía son limitadas, por lo que estas opciones no pueden recomendarse de forma general. En casos individuales, se necesitan centros experimentados para una evaluación de dichos procedimientos [31] (véase también el Panorama 2).

Fisioterapia/terapia ocupacional: Los enfoques fisioterapéuticos se utilizan predominantemente en la terapia del dolor nociceptivo. Dependiendo del cuadro clínico, los objetivos de la fisioterapia pueden ser el desarrollo del control postural, el control del movimiento o el control del tronco alcanzable, el tratamiento de los desequilibrios musculares y las adaptaciones de transferencia. Por ejemplo, pueden aplicarse aquí los conceptos de terapia según Bobath o Vojta. En particular, las técnicas manuales y los tratamientos de los tejidos blandos pueden tener un efecto positivo. Estrechamente relacionado con los enfoques fisioterapéuticos está la adaptación óptima de la silla de ruedas. Su objetivo es el ajuste ergonómico de la silla de ruedas y del entorno a las circunstancias y necesidades individuales del parapléjico. La optimización de la posición del asiento mejora la estabilidad del mismo y, por tanto, reduce la tensión sobre los hombros, el cuello y la espalda.
Psicológico: En la terapia psicológica del dolor, la terapia cognitivo-conductual (TCC) es un método utilizado con frecuencia para los problemas psicosociales [32]. La TCC muestra efectos positivos sobre el dolor y las variables conductuales en pacientes con síndromes de dolor crónico, incluido el dolor de espalda [33]. Además, se ha podido demostrar la influencia positiva de la TCC en la salud psicológica de las personas con parálisis medular [34]. Otros procedimientos pueden incluir, por ejemplo, técnicas de relajación, hipnosis, métodos basados en la atención plena y ejercicios de psicología positiva [35–37], algunos de los cuales también se han estudiado en el tratamiento del dolor en la paraplejia.
Programas interdisciplinarios de terapia multimodal: La superioridad de las terapias multidisciplinares sobre los tratamientos unidisciplinares está reconocida desde hace tiempo [38]. Estos enfoques terapéuticos pueden conducir a una mejora del dolor y del estado de ánimo, a la reincorporación al trabajo y a una reducción de los costes sanitarios. En particular, se ha demostrado la eficacia de los programas terapéuticos interdisciplinarios basados en la terapia cognitivo-conductual [39]. Actualmente se dispone de pruebas de programas interdisciplinarios multimodales de tratamiento del dolor para pacientes con dolor neuropático crónico debido a una paraplejia, que demuestran mejoras en la ansiedad y la depresión, la calidad del sueño, la intensidad del dolor, la discapacidad relacionada con el dolor, la participación y el afrontamiento del dolor [40–43].
Utilizando nuestro propio programa interdisciplinar de terapia multimodal del dolor para peatones con dolor de espalda crónico [44], que sólo duró una semana pero incluyó una alta intensidad de tratamiento de 34 horas, pudimos demostrar efectos positivos duraderos en el deterioro del dolor, la calidad de vida, la discapacidad relacionada con el dolor, la depresión y la aceptación del dolor durante un año. Ahora hemos establecido un programa semanal de este tipo para parapléjicos con dolor crónico, que actualmente está siendo evaluado. Los puntos centrales de este programa corresponden esencialmente a los de los estudios sobre la paraplejia mencionados anteriormente, como la educación médica sobre cuestiones específicas de la paraplejia o el dolor, la fisioterapia del dolor nociceptivo y la espasticidad, la terapia de entrenamiento médico, la atención plena, la terapia ocupacional con respecto a la posición sentada, la adaptación de la silla de ruedas y la ergonomía, así como contenidos psicológicos como los fundamentos de la psicología del dolor, la aceptación del dolor, la gestión del estrés, la terapia de relajación y otros (Fig. 3).

Mensajes para llevarse a casa
- Debido a la aparición de diferentes tipos de dolor y mecanismos del dolor dentro del modelo biopsicosocial de la enfermedad, la terapia del dolor para pacientes con parálisis espinal es un reto especial.
- Según el modelo de enfermedad bio-psico-social, se recomienda un enfoque terapéutico multimodal interdisciplinar en la terapia del dolor crónico.
- La superioridad de las terapias multidisciplinares sobre los tratamientos unidisciplinares se conoce desde hace mucho tiempo. En particular, podría demostrarse la eficacia de los programas terapéuticos interdisciplinarios basados en la terapia cognitivo-conductual.
Literatura:
- Rubinelli S, Glassel A, Brach M: Desde la perspectiva de la persona: Problemas percibidos en el funcionamiento entre personas con lesión medular en Suiza. J Rehabil Med. 2016; 48(2):235-243.
- Siddall PJ: Tratamiento del dolor neuropático tras una lesión medular: ahora y en el futuro. Médula espinal. 2009; 47(5): 352-359. Epub 2008/11/13.
- Muller R, Landmann G, Bechir M, et al: Dolor crónico, depresión y calidad de vida en individuos con lesión medular: Papel mediador de la participación. J Rehabil Med 2017; 49(6): 489-496. Epub 2017/06/10.
- Siddall PJ, McClelland JM, et al: Un estudio longitudinal de la prevalencia y las características del dolor en los primeros 5 años tras una lesión medular. Dolor 2003; 103(3): 249-57. Epub 2003/06/07.
- Michailidou C, Marston L, De Souza LH, Sutherland I: Una revisión sistemática de la prevalencia del dolor musculoesquelético, de espalda y lumbar en personas con lesión medular. Discapacidad y rehabilitación. 2014; 36(9): 705-715. Epub 2013/07/12.
- Bossuyt FM, Arnet U, et al: Dolor de hombro en la comunidad suiza de lesionados medulares: prevalencia y factores asociados. Discapacidad y rehabilitación 2018; 40(7): 798-805. Epub 2017/01/14.
- Andresen SR, Biering-Sorensen F, et al: Dolor, espasticidad y calidad de vida en individuos con lesión medular traumática en Dinamarca. Médula espinal 2016; 54(11): 973-979. Epub 2016/11/05.
- Finnerup NB: Dolor neuropático y espasticidad: intrincadas consecuencias de la lesión medular. Médula espinal 2017; 11(10): 70. Epub 2017/07/12.
- Bryce TN, Biering-Sorensen F, et al: Clasificación internacional del dolor en la lesión medular: parte I. Antecedentes y descripción. 6-7 de marzo de 2009. médula espinal 2012; 50(6): 413-417. epub 2011/12/21.
- Landmann G, Chang EC, et al: [Pain in patients with paraplegia]. Dolor 2017; 31(5): 527-545. Epub 2017/09/25.
- Kaiser U, Treede RD, Sabatowski R: Terapia multimodal del dolor en el dolor crónico no oncológico: ¿estándar de oro o necesidad de más aclaraciones? Dolor 2017; 158(10): 1853-1859.
- Loeser JD, Treede RD: El protocolo de Kioto de la terminología básica del dolor de la IASP. Dolor 2008; 137(3): 473-477. Epub 2008/06/28.
- Finnerup NB, Haroutounian S, et al: Dolor neuropático: un sistema de clasificación actualizado para la investigación y la práctica clínica. Pai. 2016; 157(8):1599-1606.
- Finnerup NB: Dolor en pacientes con lesión medular. Dolor 2013; 154 Suppl 1(1): S71-76. Epub 2013/02/05.
- Kirshblum SC, Burns SP, et al: Normas internacionales para la clasificación neurológica de las lesiones medulares (revisadas en 2011). The journal of spinal cord medicine 2011; 34(6): 535-546. Epub 2012/02/15.
- Krebs J, Koch HG, et al: Las características de la siringomielia postraumática. Médula espinal. 2015; 1(10): 218. Epub 2015/12/02.
- Watts J, Box GA, et al: Resonancia magnética de las lesiones intramedulares de la médula espinal: una revisión pictórica. Revista de imagen médica y oncología radioterápica 2014; 58(5): 569-581. Epub 2014/07/06.
- Curt A, Ellaway PH: Neurofisiología clínica en el pronóstico y seguimiento de la lesión medular traumática. Manual de neurología clínica 2012; 109: 63-75. Epub 2012/10/27.
- Landmann G, Berger MF, et al: Utilidad de los potenciales evocados por láser y las pruebas sensoriales cuantitativas en el diagnóstico del dolor neuropático por lesión medular: un estudio de casos múltiples. Médula espinal 2017; 55(6): 575-582. Epub 2017/01/25.
- Rolke R, Magerl W, et al: Pruebas sensoriales cuantitativas: un protocolo exhaustivo para ensayos clínicos. Revista europea del dolor 2006; 10(1): 77-88. Epub 2005/11/18.
- Zeilig G, Enosh S et al: La naturaleza y el curso de los cambios sensoriales tras una lesión medular: propiedades predictivas e implicaciones en el mecanismo del dolor central. Brain: a journal of neurology 2012; 135(Pt 2): 418-430. Epub 2011/11/19.
- Finnerup NB, Norrbrink C, et al: Fenotipos y predictores del dolor tras una lesión medular traumática: un estudio prospectivo. La revista del dolor: revista oficial de la Sociedad Americana del Dolor 2014; 15(1): 40-48. Epub 2013/11/26.
- Engel GL: La necesidad de un nuevo modelo médico: un reto para la biomedicina. Science 1977; 196(4286): 129-136. Epub 1977/04/08.
- Keefe FJ, Rumble ME, et al: Aspectos psicológicos del dolor persistente: estado actual de la ciencia. La revista del dolor: revista oficial de la Sociedad Americana del Dolor 2004; 5(4): 195-211. Epub 2004/05/27.
- Jensen MP, Moore MR, et al: Factores psicosociales y adaptación al dolor crónico en personas con discapacidades físicas: una revisión sistemática. Arch Phys Med Rehabil 2011; 92(1): 146-160.
- Craig A, Tran Y, Middleton J: Morbilidad psicológica y lesión medular: una revisión sistemática. Médula espinal 2009; 47(2): 108-114. Epub 2008/09/10.
- Mehta S, Guy SD, Bryce TN, et al: The CanPain SCI Clinical Practice Guidelines for Rehabilitation Management of Neuropathic Pain after Spinal Cord: screening and diagnosis recommendations. Médula espinal 2016; 54 Suppl 1(1): S7-S13. Epub 2016/07/23.
- Finnerup NB, Jensen MP, et al: Un estudio prospectivo del dolor y el funcionamiento psicológico tras una lesión medular traumática. Médula espinal 2016; 54(10): 816-821. Epub 2016/03/02.
- Loh E, Guy SD, et al: The CanPain SCI Clinical Practice Guidelines for Rehabilitation Management of Neuropathic Pain after Spinal Cord: introduction, methodology and recommendation overview. Médula espinal 2016; 54 Suppl 1(1): S1-6. Epub 2016/07/23.
- Bundesärztekammer (BÄK) KBK, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF): Nationale Versorgungsleitlinie Nicht-spezifischer Kreuzschmerz – Langfassung. www.versorgungsleitlinien.de, www.awmf.org
- Guy SD, Mehta S, Casalino A, et al: The CanPain SCI Clinical Practice Guidelines for Rehabilitation Management of Neuropathic Pain after Spinal Cord: Recommendations for treatment. Médula espinal 2016; 54 Suppl 1(1): S14-23. Epub 2016/07/23.
- Butler AC, Chapman JE, et al: El estado empírico de la terapia cognitivo-conductual: una revisión de los metaanálisis. Revisión de psicología clínica. 2006; 26(1): 17-31. epub 2005/10/04.
- Ostelo RW, van Tulder MW, et al: Tratamiento conductual para el dolor lumbar crónico. La base de datos Cochrane de revisiones sistemáticas 2005; 25(1): CD002014. Epub 2005/01/28.
- Mehta S, Orenczuk S, et al: Una revisión basada en pruebas de la eficacia de la terapia cognitivo-conductual para los problemas psicosociales tras una lesión medular. Psicología de la rehabilitación 2011; 56(1): 15-25. Epub 2011/03/16.
- Muller R, Gertz KJ, et al: Efectos de una intervención de psicología positiva adaptada sobre el bienestar y el dolor en individuos con dolor crónico y una discapacidad física: Un ensayo de viabilidad. The Clinical journal of pain 2016; 32(1): 32-44. Epub 2015/02/28.
- Jensen MP, Barber J, et al: El efecto de la sugestión hipnótica en el dolor de las lesiones medulares. Journal of Back and Musculoskeletal Rehabilitation 2000; 14(1,2): 3-10.
- Kabat-Zinn J: Intervenciones basadas en la atención plena en contexto: pasado, presente y futuro. Psicología clínica: ciencia y práctica 2003; 10(2): 144-156.
- Flor H, Fydrich T, Turk DC: Eficacia de los centros multidisciplinares de tratamiento del dolor: una revisión metaanalítica. Dolor 1992; 49(2): 221-230. Epub 1992/05/01.
- Morley S, Eccleston C, Williams A: Revisión sistemática y metaanálisis de ensayos controlados aleatorizados de terapia cognitivo-conductual y terapia conductual para el dolor crónico en adultos, excluida la cefalea. Dolor 1999; 80(1-2): 1-13.
- Norrbrink C, Lindberg T, et al: Efectos de un programa de ejercicios sobre el dolor musculoesquelético y neuropático tras una lesión medular: resultados de un estudio con ergómetro de doble cuerda sentado. Médula espinal 2012; 50(6): 457-461. Epub 2012/02/01.
- Heutink M, Post MW, et al: The CONECSI trial: results of a randomized controlled trial of a multidisciplinary cognitive behavioural program for coping with chronic neuropathic pain after spinal cord injury. Dolor 2012; 153(1): 120-128. Epub 2011/11/22.
- Perry KN, Nicholas MK, Middleton JW: Comparación de un programa de tratamiento del dolor con la atención habitual en un centro de tratamiento del dolor para personas con dolor crónico relacionado con una lesión medular. Revista clínica del dolor 2010; 26(3): 206-216. Epub 2010/02/23.
- Burns AS, Delparte JJ, et al: Evaluación de un programa interdisciplinar para el dolor crónico tras una lesión medular. PM & R: la revista de lesiones, función y rehabilitación 2013; 5(10): 832-838. Epub 2013/05/21.
- Reck T, Dumat W, Krebs J, Ljutow A: [Terapia del dolor multimodal ambulatoria: Resultados de un programa intensivo de grupo multimodal ambulatorio de 1 semana para pacientes con dolor de espalda crónico inespecífico – evaluación retrospectiva a los 3 y 12 meses]. Dolor 2017; 31(5): 508-515. Epub 2017/03/05. Terapia del dolor multimodal ambulatoria: resultados de un programa intensivo de grupo multimodal ambulatorio de 1 semana para pacientes con dolor de espalda crónico inespecífico – evaluación retrospectiva a los 3 y 12 meses.
- Finnerup NB, Attal N, et al: Farmacoterapia para el dolor neuropático en adultos: una revisión sistemática y metaanálisis. Lancet Neurol 2015; 14(2): 162-173. Epub 2015/01/13.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2018; 16(3): 16-24.