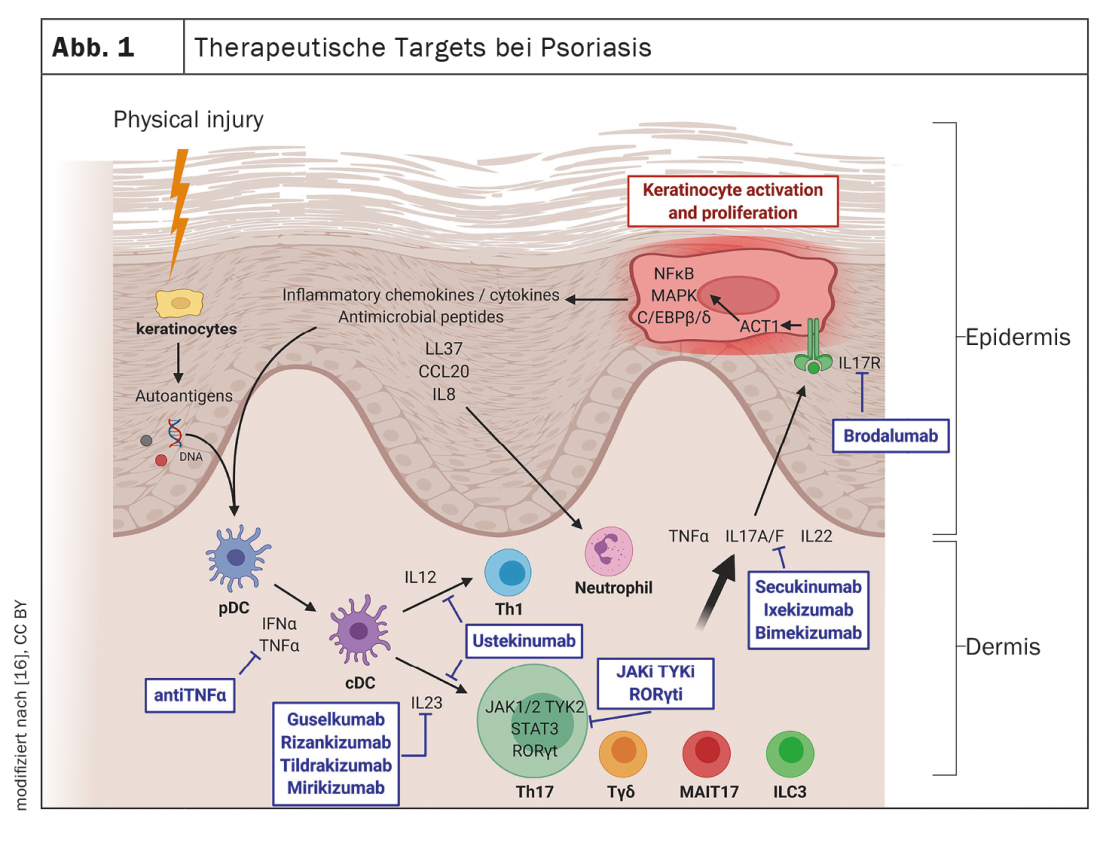
Hoy en día, la psoriasis se considera una enfermedad sistémica inflamatoria en la que las citocinas proinflamatorias desempeñan un papel importante. Varios circuitos inflamatorios están implicados en la patogénesis de la psoriasis. Las citocinas de las familias IL-23 e IL-17 son dianas probadas, pero también se están investigando otras dianas terapéuticas.
La eficacia y la seguridad de la inmunoterapia sistémica han mejorado significativamente en los últimos años con la introducción de nuevos agentes de las clases de inhibidores de la IL-17 y la IL-23. “En los últimos años hemos asistido a un rápido aumento del número de preparados”, afirma la Dra. med. Sylvie Haase, especialista en enfermedades cutáneas y venéreas en una consulta de un grupo dermatológico de Constanza [2]. En la actualidad se dispone de una amplia gama de agentes sistémicos dirigidos contra diferentes dianas y, a medida que se sigan descifrando los patomecanismos moleculares, se espera que esta tendencia continúe en el futuro (Fig. 1). Cada vez más, el reto consiste en adecuar a los pacientes a las opciones de tratamiento apropiadas. Resulta que entre los pacientes con psoriasis de moderada a grave, hay quienes responden muy bien a la primera opción de terapia sistémica y permanecen con el mismo tratamiento durante años, pero también algunos en los que la psoriasis resulta refractaria a la terapia, explicó el ponente.
Análisis de la respuesta a los biológicos: ¿Qué se puede deducir de ellos?
Se considera que la característica patológica central de la psoriasis es la inflamación crónica de la piel, que conduce a una proliferación incontrolada y una diferenciación disfuncional de los queratinocitos. A nivel molecular, el papel fisiopatológico central del eje TNF-α-IL-23-Th17 está muy bien caracterizado. Los anticuerpos monoclonales aprobados actualmente en Suiza para el tratamiento de la psoriasis están dirigidos contra las siguientes citocinas: TNF-α, interleucina(IL)-12/IL-23, IL-23, IL-17A o IL-17A/F [1]. Según los metaanálisis en red, los grupos del inhibidor de la IL-17 (IL-17-i) y del inhibidor de la IL-23 (IL-23-i) muestran una mayor eficacia en términos de PASI*-90 y PASI-100 en comparación con el TNF-α-i [8]. En cuanto a la IL-23-i, el Dr. Haase explica: “El efecto se produce algo más lentamente en comparación con los inhibidores de la IL-17, pero los preparados no tienen un espectro específico de efectos secundarios”. En Suiza, los IL-17A-i secukinumab e ixekizumab están actualmente aprobados, así como recientemente el IL17A/F-i bimekizumab, y entre los IL-23-i, guselkumab, risankizumab y tildrakizumab están en el mercado.
* PASI = Índice de área y gravedad de la psoriasis
En un estudio de cohortes, un equipo de investigación de Dinamarca analizó la respuesta a diferentes biológicos [3]. Los 2022 resultados publicados en el Journal of the European Academy of Dermatology and Venereology muestran que del total de 3280 pacientes incluidos (edad media de 45,0 años, 37% mujeres), el 6,3% se clasificaron como superrespondedores y el 6,5% como refractarios al tratamiento. Estos últimos tenían un IMC medio superior al de los demás pacientes (32,2 frente a 29,4, p<0,0001), mientras que los superrespondedores tenían menos comorbilidades y un estatus socioeconómico más alto.
El inhibidor de la IL-17A/F bimekizumab es un nuevo actor
Que la IL-17A desempeña un papel central en la patogénesis de la psoriasis se ha demostrado varias veces mediante el uso con éxito de los anticuerpos inhibidores correspondientes. Sin embargo, la IL-17F también se sobreexpresa en la piel y el tejido sinovial de los enfermos de psoriasis [4]. El bimekizumab, un anticuerpo monoclonal IgG1 que inhibe selectivamente la interleucina IL-17F y la IL-17A, está disponible desde hace poco en Suiza. En los tres estudios pivotales, el bimekizumab mostró una buena eficacia y obtuvo mejores resultados que el antagonista de la IL-12/IL-23 ustekinumab y el inhibidor del TNF-α adalimumab en los criterios de valoración coprincipales PASI-90 e IGA# 0/1 en la semana 16 [5–7]. El perfil de seguridad del bimekizumab se caracteriza por los efectos de clase conocidos de la inhibición de la IL-17, entre los efectos secundarios comunes se incluye la candidiasis oral. Un nuevo nanoanticuerpo trivalente contra la IL-17A y la IL-17F que se está investigando actualmente para su uso en la psoriasis es el sonelokimab. Se han obtenido resultados prometedores en estudios de fase I y II [4]. Los nanocuerpos son anticuerpos recombinados, específicos de antígeno, que constan únicamente del dominio variable necesario para la unión al antígeno y son, por tanto, comparativamente pequeños.
# IGA=Evaluación Global del Investigador: Pacientes con IGA: 0 = piel sin apariencia, 1 = síntomas cutáneos leves.
También están en proyecto varios agentes de aplicación oral o tópica
La búsqueda de nuevos agentes antipsoriásicos es un campo de investigación en rápido desarrollo. Los siguientes agentes sistémicos han sido recientemente aprobados para la psoriasis en placas por la Administración de Alimentos y Medicamentos de EE.UU. (FDA) este año (tabla 1):
- El deucravacitinib (BMS-986165) es un inhibidor altamente selectivo de TYK2 en forma de dosificación oral para uso una vez al día en la psoriasis en placas de moderada a grave (aprobación de la FDA 09/09/22) [9,10].
- El roflumilast (ARQ-151) es un inhibidor tópico de la PDE-4 para el tratamiento de la psoriasis en placas en pacientes ≥12 años de edad (aprobación de la FDA 29/07/22) [11–13].
- Tapinarof-Crème 1% (Vtama) es un modulador de los receptores de aril hidrocarburos para el tratamiento de la psoriasis en placas en adultos (aprobación de la FDA 24/05/22) [18,19].
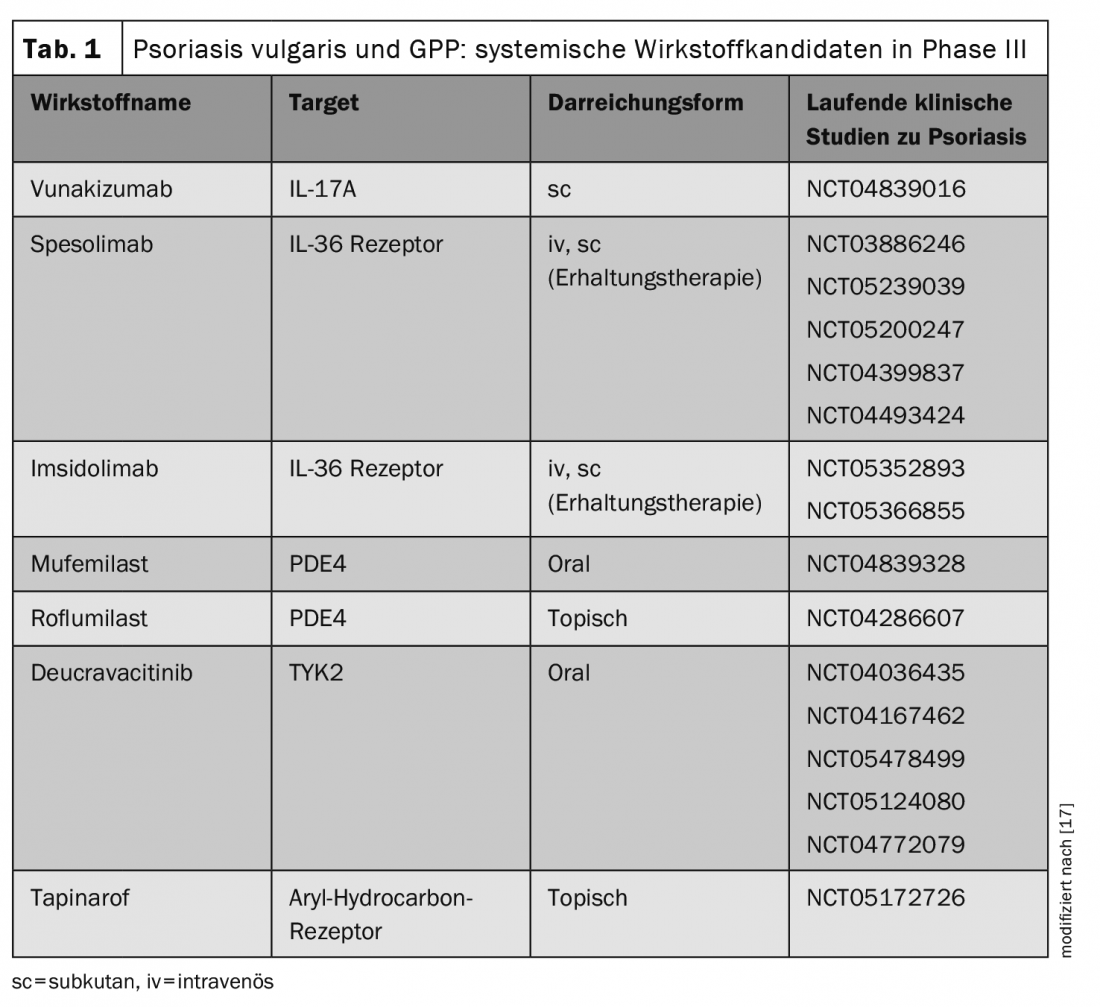
Además, el espesolimab, un anticuerpo monoclonal humanizado contra la IL36-R fue aprobado por la FDA para el tratamiento de los brotes de GPP (psoriasis pustular generalizada) (aprobación de la FDA 01.09.22). La decisión de aprobación se basa en el estudio de fase II Effisayil-1 [14,15]. Otros agentes sistémicos innovadores se encuentran actualmente en fases avanzadas de desarrollo clínico (Tab. 1) [17]. Por lo tanto, es posible que el espectro terapéutico también se amplíe en Europa en un futuro no muy lejano para incluir otros sistemas terapéuticos. Especialmente para los pacientes refractarios, las nuevas alternativas de tratamiento son bienvenidas. En cuanto a los perfiles de efectos secundarios, el Dr. Haase señala que los efectos de clase de sustancia conocidos de los inhibidores de JAK incluyen un número ligeramente mayor de infecciones del tracto respiratorio superior y herpes simple, y que ocasionalmente puede producirse un exantema similar al acné. Se necesitan datos a largo plazo para comprender mejor las diferencias entre las distintas opciones de tratamiento y poder hacer una elección orientada al paciente.
Congreso: Bodensee Dermaconsil
Literatura:
- Lauffer F, et al: Citocinas de la familia IL-17 en la psoriasis. JDDG; 1610-0379/2020/1807
- “Psoriasis – ¿hay algo nuevo?”, Dra. med. Sylvie Haase, 3ª Dermaconsil Bodensee, 22.10.2022.
- Loft N, et al: Prevalencia y caracterización de la psoriasis refractaria al tratamiento y de los superrespondedores al tratamiento biológico: un estudio a escala nacional. J Eur Acad Dermatol Venereol 2022; 36(8): 1284-1291.
- Iznardo H, Puig L: Inhibición dual de IL-17A e IL-17F en la enfermedad psoriásica. Ther Adv Chronic Dis 2021 Ago 12;12:20406223211037846
- Warren RB, et al: Bimekizumab frente a adalimumab en la psoriasis en placas. N Engl J Med 2021; 385: 130-141.
- Reich K, et al: Bimekizumab frente a ustekinumab para el tratamiento de la psoriasis en placas de moderada a grave (BE VIVID): eficacia y seguridad de un ensayo de fase 3 de 52 semanas, multicéntrico, doble ciego, con comparador activo y controlado con placebo. Lancet 2021; 397: 487-498.
- Gordon KB, et al: Bimekizumab efficacy and safety in moderate to severe plaque psoriasis (BE READY): a multicentre, double-blind, placebo-controlled, randomised withdrawal phase 3 trial. Lancet 2021; 397: 475-486.
- Yasmeen N, et al: Terapias dirigidas para pacientes con psoriasis de moderada a grave: revisión sistemática y metaanálisis en red de la respuesta PASI a 1 año. J Dermatolog Treat 2022; 33(1): 204-218.
- Boerner LK. Una reunión híbrida divulga las estructuras de los fármacos candidatos [Internet]. Noticias de Química e Ingeniería. 2022. Disponible en: https://cen.acs.org/acs-news/acs-meeting-news/Hybrid-meeting-divulges-st…,(último acceso 15.11.2022)
- Chimalakonda A, et al.: Perfil de selectividad del inhibidor de la tirosina quinasa 2 deucravacitinib en comparación con los inhibidores de la Janus quinasa 1/2/3. Dermatol Ther (Heidelb) 2021; 11(5): 1763-1776.
- Lebwohl MG, et al: Ensayo de roflumilast en crema para la psoriasis crónica en placas. N Eng J Med 2020; 383(3): 229-239.
- Arcutis Biotherapeutics. La FDA aprueba ZORYVE (roflumilast) Crema 0,3% de Arcutis Para el tratamiento de la psoriasis en placas en individuos de 12 años o más [Internet]. 2022. Disponible en: www.arcutis.com/fda-approves-arcutis-zoryve-roflumilast-cream-0-3-for-th…,(último acceso 15.11.2022)
- Lebwohl M, et al.: Seguridad y eficacia de roflumilast crema una vez al día al 0,3%, un potente inhibidor de la fosfodiesterasa-4 para el tratamiento de la psoriasis en los ensayos de fase 3 DERMIS-1 y DERMIS-2. Póster presentado en:30º Congreso de la EADV, del 29 de septiembre al 2 de octubre de 2021; virtual
- Boehringer Ingelheim. La FDA aprueba la primera opción de tratamiento para los brotes de psoriasis pustulosa generalizada en adultos [Internet]. 2022. Disponible en: www.boehringer-ingelheim.us/press-release/fda-approves-first-treatment-o…,(último acceso 15.11.2022)
- Bachelez H, et al: Ensayo de espesolimab para la psoriasis pustulosa generalizada. N Engl J Med 2021; 385(26): 2431-2440.
- Bugaut H, Aractingi S: El importante papel del eje IL17/23 en la psoriasis respalda el desarrollo de nuevas terapias dirigidas. Front Immunol 2021;12:621956. www.frontiersin.org,(última consulta: 15 de noviembre de 2022).
- Drakos A, Vender RA: Review of the Clinical Trial Landscape in Psoriasis: An Update for Clinicians. Dermatol Ther (Heidelb) 2022, https://doi.org/10.1007/s13555-022-00840-9,(última consulta: 15 de noviembre de 2022).
- Keam SJ: Tapinarof crema 1%: primera aprobación. Fármacos 2022; 82(11): 1221-1228.
- Lebwohl MG, et al: Ensayos de fase 3 de la crema tapinarof para la psoriasis en placas. N Engl J Med 2021; 385(24): 2219-2229.