La Sociedad Europea de Nutrición Clínica y Metabolismo (ESPEN) define la ME como un estado nutricional en el que las deficiencias energéticas, proteínicas y de micronutrientes provocan una alteración de la composición corporal (reducción de la masa muscular) y una disminución de las funciones tanto físicas como mentales. En los países industrializados, uno de cada tres pacientes corre el riesgo de padecer ME o tiene ME manifiesta en el momento de su ingreso en el hospital. La EM se describe como “una de las causas ocultas más importantes del aumento de los costes de la atención sanitaria”.
Hipócrates de Kos, el padre de la medicina moderna, atribuía gran importancia a la nutrición ya en el siglo IV a.C.: “[…] que tu alimento sea tu medicina y tu medicina sea tu alimento”. Hoy en día, los efectos clínicos negativos de la desnutrición asociada a la enfermedad (ME) están bien estudiados: mayor estancia hospitalaria, menor calidad de vida, mayores tasas de morbilidad y mortalidad. La EM se describe como “una de las razones ocultas más importantes del aumento de los costes en el sistema sanitario” [Neue Zürcher Zeitung, 11.06.2002].
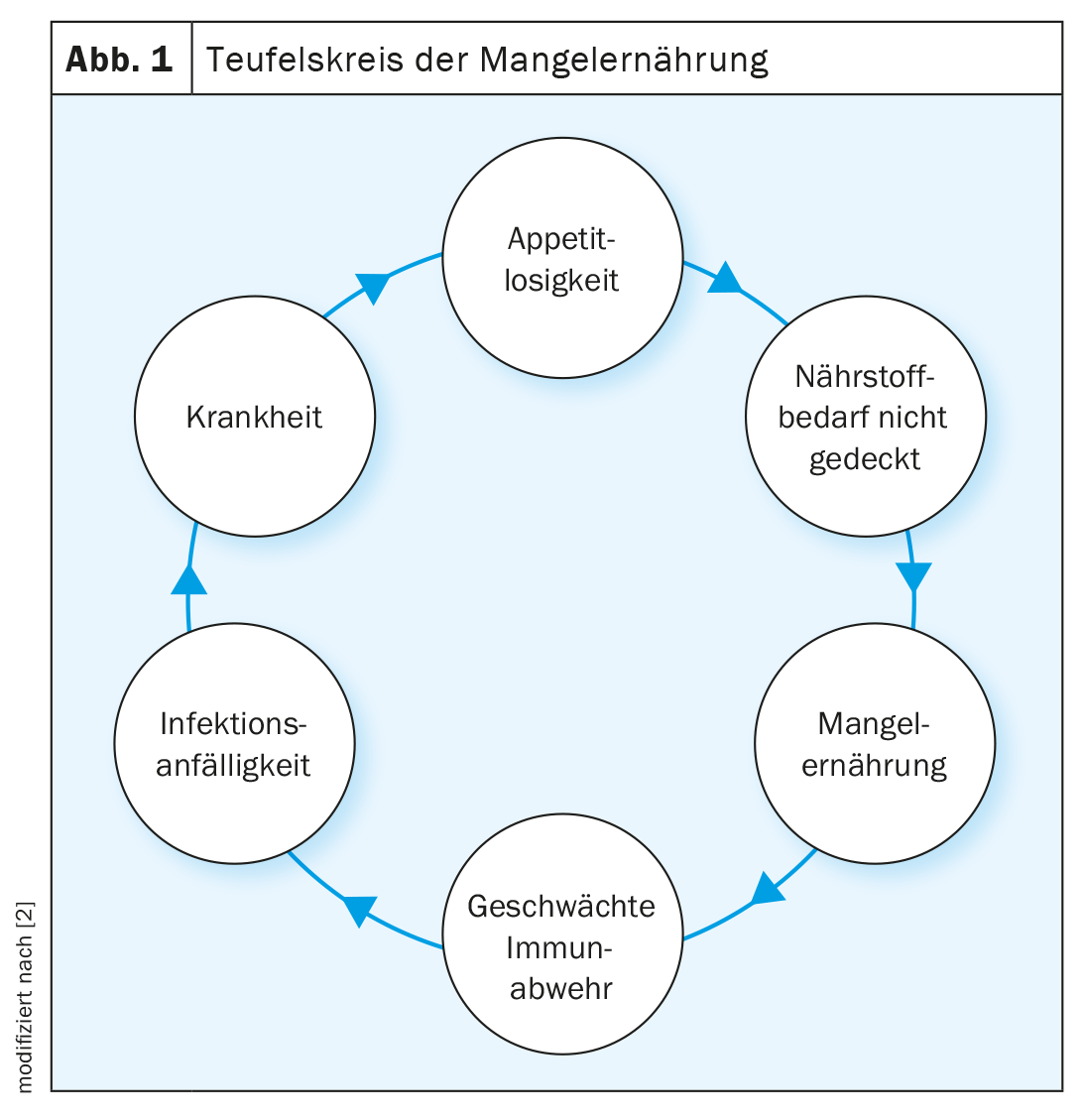
La Sociedad Europea de Nutrición Clínica y Metabolismo (ESPEN) define la ME como un estado nutricional en el que las deficiencias energéticas, proteínicas y de micronutrientes provocan una alteración de la composición corporal (reducción de la masa muscular) y una disminución de las funciones tanto físicas como mentales [1]. En los países industrializados, uno de cada tres pacientes corre el riesgo de padecer ME o tiene ME manifiesta en el momento de su ingreso en el hospital. Estos pacientes suelen seguir perdiendo peso en el transcurso de la hospitalización, lo que empeora su estado nutricional. Los múltiples factores que influyen en esta pérdida de peso progresiva y no deseada incluyen la pérdida de apetito, el estado inflamatorio, el catabolismo proteico, la disfunción hormonal, el malestar gastrointestinal, la inactividad física y la fatiga psicológica (Fig. 1). Por término medio, el 2% de la población anciana está desnutrida y el 24% corre el riesgo de padecer ME. En las personas frágiles, la prevalencia fue significativamente mayor, del 9% y el 45%, respectivamente [3]. La pérdida de apetito es una respuesta fisiológica a una enfermedad aguda, pero puede provocar déficits energéticos y proteicos potencialmente drásticos. La ME y la enfermedad se influyen mutuamente, de modo que, por un lado, la enfermedad puede dar lugar a la ME y, por otro, la ME puede influir negativamente en el curso de la enfermedad. Combinadas con una respuesta endocrina e inflamatoria al estrés, las deficiencias energéticas, proteínicas y de micronutrientes pueden provocar una pérdida muscular y de fuerza y una reducción de la función corporal, especialmente en los enfermos crónicos. En cambio, en las enfermedades agudas, la pérdida de apetito puede actuar como mecanismo de protección y aumentar la autofagia (mecanismo del organismo para descomponer los orgánulos celulares dañados y los productos tóxicos), lo que puede ayudar a la recuperación. Así pues, la supresión de la autofagia por la terapia nutricional en la enfermedad aguda produce efectos potencialmente negativos. Sin embargo, en pacientes crónicamente enfermos, este mecanismo fisiológico de protección puede conducir a una ME asociada a la enfermedad. En pacientes con múltiples enfermedades crónicas de gravedad leve y deterioro del estado nutricional, una terapia nutricional adecuada tiene un efecto positivo en el resultado clínico. Estos pacientes pueden tener un metabolismo y una utilización de los nutrientes más eficientes debido a una baja resistencia a la insulina que los pacientes agudamente enfermos [4]. Para mejorar los resultados clínicos y aumentar el bienestar, debe aplicarse una terapia nutricional individualizada y personalizada. Los aspectos importantes son el momento de la terapia nutricional, la forma en que se administra, así como la cantidad y la elección de los nutrientes.
Situación actual de las pruebas
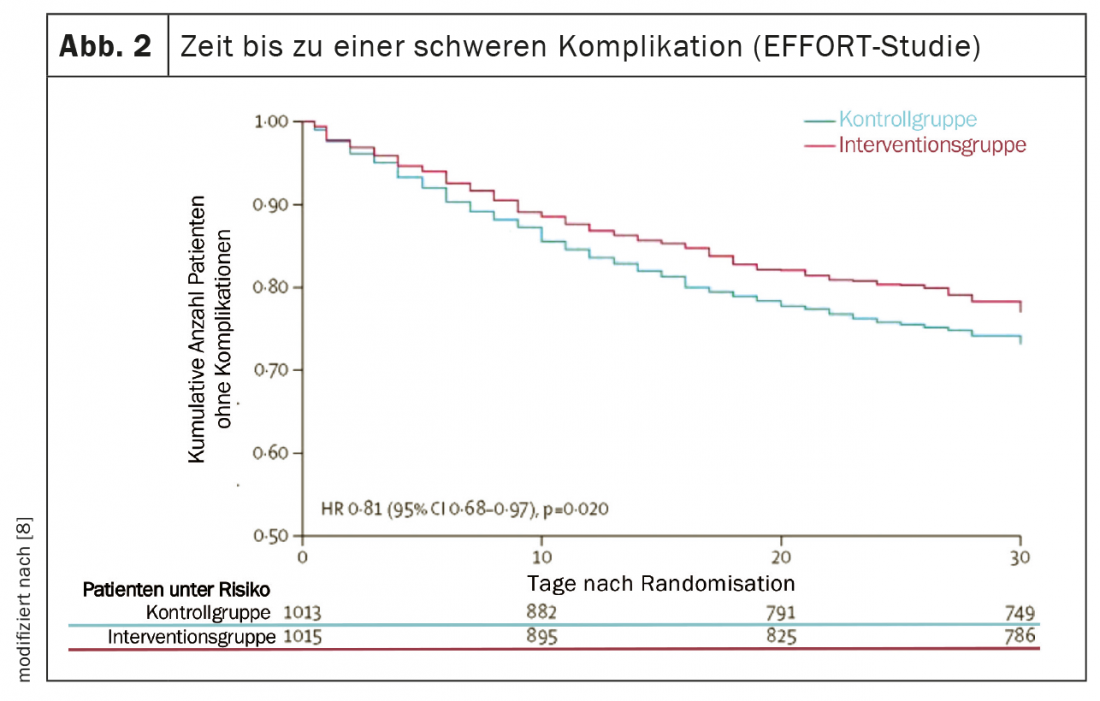
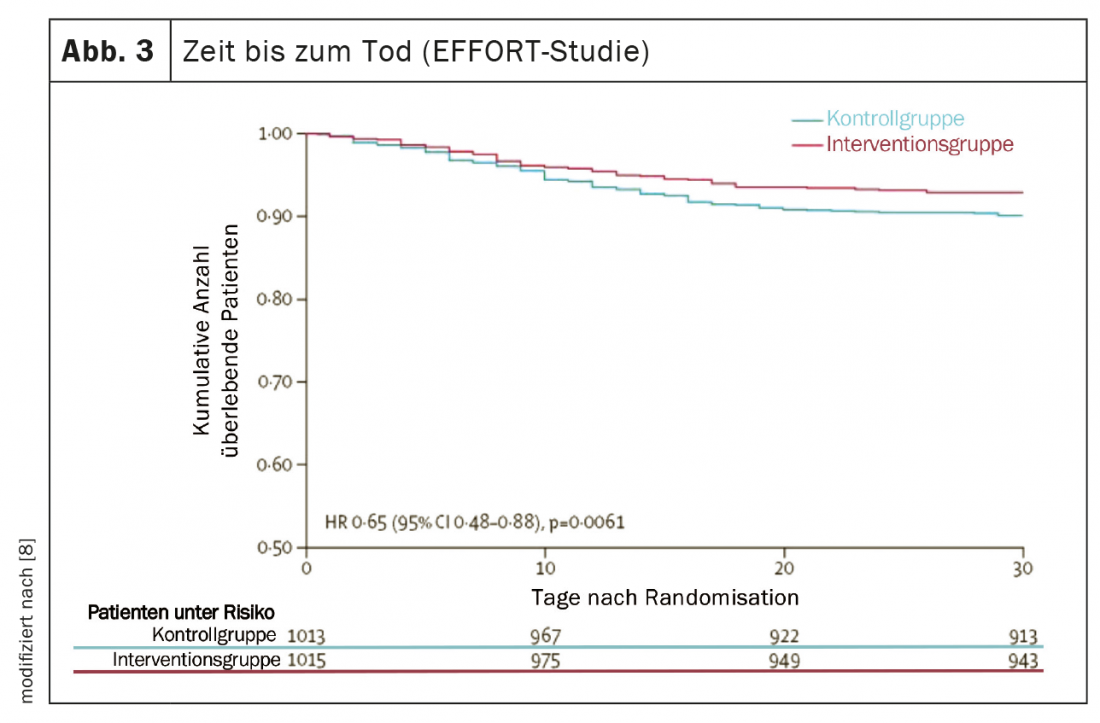
En los últimos cinco años, varios estudios de gran calidad han aportado nuevos e importantes conocimientos que han hecho avanzar significativamente la medicina nutricional y han trasladado a la práctica los resultados de la investigación nutricional [5]. El estudio PREDIMED (Prevención con Dieta Mediterránea) proporcionó pruebas sólidas de que una dieta mediterránea suplementada con aceite de oliva virgen extra o frutos secos mixtos reducía el riesgo de enfermedades cardiovasculares y metabólicas en aproximadamente un 30% a lo largo de cinco años [6]. Dos ensayos controlados aleatorios multicéntricos demostraron la gran eficacia de una terapia nutricional adecuada en pacientes desnutridos tanto en el hospital como tras el alta [7,8]. En primer lugar, el ensayo controlado con placebo NOURISH (Nutrition effect On Unplanned Readmissions and Survival in Hospitalized patients) con 652 adultos mayores desnutridos demostró que la suplementación oral con alto contenido en proteínas puede reducir significativamente la mortalidad a los 90 días con un Número Necesario a Tratar (NNT) de 20 [7]. Por otro lado, el estudio EFFORT (Effect of early nutritional support on Frailty, Functional Outcomes and Recovery of malnourished medical patients Trial) con 2028 pacientes hospitalizados que sufrían desnutrición en ocho hospitales suizos demostró la eficacia de una terapia nutricional individualizada y controlada por algoritmos. En comparación con la nutrición hospitalaria estándar, la terapia nutricional dirigida a alcanzar los objetivos proteínicos y energéticos redujo significativamente la tasa de complicaciones graves (NNT=25) y la tasa de mortalidad (NNT=37) (Figs. 2 y 3). Además, los trastornos funcionales se produjeron con una frecuencia significativamente menor y la calidad de vida mejoró notablemente [8]. Un metaanálisis reciente, que incluyó estos dos estudios, concluyó que una terapia nutricional adecuada en pacientes desnutridos reduce el riesgo tanto de mortalidad como de rehospitalizaciones electivas en aproximadamente un 25% [5].
Gestión de la nutrición
El objetivo de la terapia nutricional es mantener o mejorar el estado nutricional y la calidad de vida mediante la administración adecuada de nutrientes. Para evitar un deterioro del estado nutricional, es necesario un tratamiento nutricional rápido y eficaz (Tab. 1 ). En vista de la creciente necesidad de terapia nutricional en el ámbito ambulatorio – más pacientes ancianos y polimórbidos que necesitan cuidados – tiene sentido desarrollar un campo especializado de cuidados para la terapia nutricional en estrecha colaboración con una Enfermera de Práctica Avanzada. En nuestra opinión, la utilización de profesionales sanitarios en funciones de práctica avanzada, especialmente en la gestión de la nutrición, es prometedora. Poseen profundos conocimientos clínicos y actúan de acuerdo con las pruebas científicas actuales. Así, pueden asesorar, tratar o acompañar de forma independiente a pacientes con cuadros clínicos complejos. Esto conduce a un desarrollo eficaz y sostenible de la terapia nutricional.
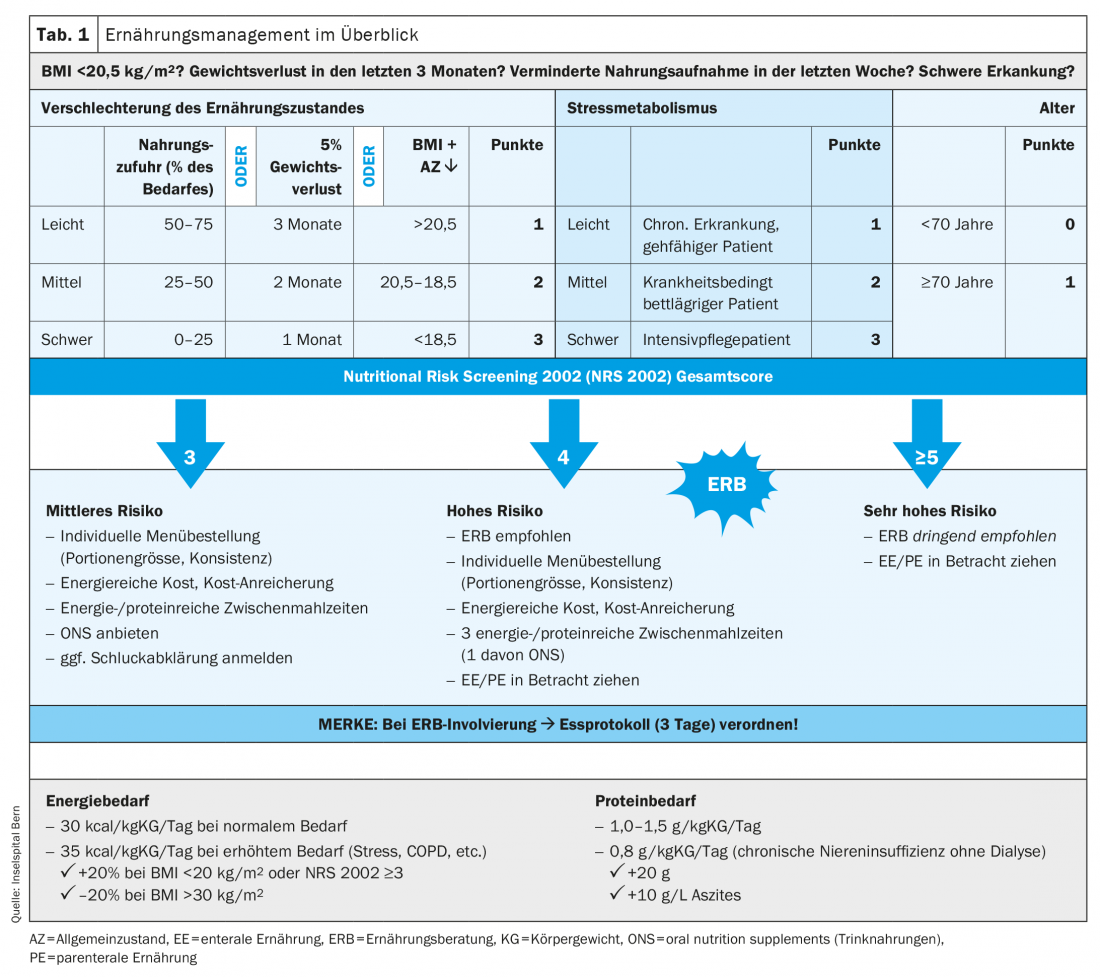
Cribado y evaluación en el ámbito ambulatorio: son necesarios procedimientos estandarizados para iniciar una terapia nutricional oportuna y adecuada. Debe realizarse un cribado sistemático del riesgo de ME, seguido de una evaluación nutricional exhaustiva, que conduzca al desarrollo de un plan nutricional personalizado. El cribado para determinar el riesgo de ME es el primer paso para identificar o, en el mejor de los casos, prevenir el deterioro del estado nutricional en una fase temprana. El cribado debe identificar de forma rápida y sensible a las personas que necesitan una evaluación nutricional.
El cribado debe realizarse con instrumentos validados. La ESPEN recomienda el cribado del riesgo nutricional 2002 (NRS 2002, Tab. 2). Puede realizarse en pocos minutos y es actualmente el instrumento de cribado mejor validado [9,10]. Fue desarrollado en 2002 por el grupo de Jens Kondrup y es uno de los más utilizados en los hospitales de todo el mundo. Consiste en un examen previo con 4 preguntas. Si se responde afirmativamente a una pregunta, deberá realizarse el cribado NRS 2002. Tiene en cuenta la evaluación del estado nutricional (0-3 puntos), la gravedad de la enfermedad (0-3 puntos) y la edad (1 punto si es ≥70años). Los puntos se suman a una puntuación total, en la que ≥3puntos indican riesgo de ME o ME manifiesta y se indica una evaluación nutricional.

Una evaluación nutricional es un procedimiento exhaustivo para la evaluación objetiva del estado nutricional. Incluye historial médico, exámenes físicos, medidas antropométricas (peso, altura, IMC), pruebas funcionales, calidad de vida, actividad física y valores de laboratorio. En la práctica, se puede realizar una evaluación simplificada basada en el peso, la altura, el IMC y los parámetros subjetivos que se correlacionan con el estado nutricional según la bibliografía, como el apetito, el bienestar general y el rendimiento. La forma más sencilla de registrar los parámetros subjetivos es con una escala analógica visual, similar al registro del dolor (escala 1-10).
Plan de nutrición: En línea con el desarrollo de la medicina personalizada, el plan de nutrición se adapta siempre a las necesidades individuales. Estas necesidades dependen en gran medida del estado nutricional evaluado en la valoración, siendo determinantes la enfermedad subyacente, el historial de peso, el apetito y la ingesta actual de alimentos. Problemas como el trastorno de la masticación, la odinofagia, la disfagia, la xerostomía, la disgeusia, la mucositis/soor, las náuseas/emesis, el estreñimiento/diarrea o el dolor también desempeñan un papel importante en el plan de nutrición. Deben tenerse en cuenta otros aspectos como los hábitos alimentarios, las preferencias/avatares, la situación psicosocial y la actividad física. Llevar un registro de comidas durante 3-5 días es muy útil para registrar de forma semicuantitativa la cantidad de comida consumida y conocer en detalle los hábitos alimentarios (en el caso de los pacientes hospitalizados, también puede utilizarse el modelo de tabla de platos). Antes de la terapia nutricional, debe optimizarse la terapia farmacológica, por ejemplo, antieméticos fijos, medidas laxantes, enjuague bucal, sustituto de la saliva, bloqueador de ácidos, etc.
Necesidades de energía, proteínas y líquidos: La determinación de las necesidades energéticas es un punto central de la evaluación nutricional. El consumo total de energía se compone del consumo de energía en reposo, la termogénesis inducida por los alimentos y la energía consumida durante la actividad física. Las necesidades energéticas totales pueden calcularse mediante una fórmula específica para la edad, el sexo y el peso que también tenga en cuenta los factores de actividad y estrés (por ejemplo, la fórmula de Harris-Benedict [11]). En la vida cotidiana práctica, puede estimarse aproximadamente mediante una fórmula simplificada basada en el peso, de la siguiente manera: 30-35 kcal/kg/día; más 20% para un NRS 2002 ≥3o un IMC <20 kg/m2; menos 20% para un IMC >30 kg/m2 [12]. Una dieta completa equilibrada para pacientes desnutridos debe cubrir el 40-60% de las necesidades energéticas con hidratos de carbono, el 10-20% con proteínas y el 30-40% con grasas.
Las necesidades proteínicas de los individuos sanos suelen ser de 0,8 g/kg/día. En la insuficiencia renal crónica, la ingesta de proteínas debe reducirse a 0,6 g/kg/día a menos que se realice diálisis. En pacientes ancianos (>65 años) con insuficiencia renal crónica, la ingesta de proteínas es de 0,8 g/kg/día. En caso de diálisis, la necesidad de proteínas es la misma que en el caso normal y existe una necesidad adicional de aproximadamente 20 g de proteínas después de la diálisis (pérdida dialítica). Los pacientes pierden unos 10 g de proteínas por litro de ascitis durante la paracentesis [4]. Para los pacientes desnutridos con enfermedades agudas o crónicas, las recomendaciones para la ingesta de proteínas son de 1,0-1,5 g/kg/día [13]. No existen recomendaciones específicas para los pacientes polimórbidos con insuficiencia renal crónica. Nuestra experiencia clínica demuestra que esta población requiere aproximadamente 1 g/kg/día [8]. Debe definirse un objetivo individual para cada paciente, ya que otros factores como el hipermetabolismo pueden alterar las necesidades proteínicas (por ejemplo, factores de estrés adicionales como la EPOC subyacente o la enfermedad tumoral).
En general, debe asegurarse una ingesta de líquidos suficiente y adecuada. La regulación de fluidos debe (i) compensar la pérdida imperceptible (500-1000 ml), (ii) proporcionar suficiente agua y electrolitos, (iii) mantener el estado normal de los compartimentos de fluidos corporales; y (iv) Proporcionar suficiente agua para permitir que el riñón excrete los productos de desecho (500-1500 ml). Las necesidades medias son de 30-35 ml de agua/kg/día, 1 mmol de sodio/kg/día y 1 mmol de potasio/kg/día. La directriz para la ingesta total de agua es de >2 litros al día (aproximadamente 1,1 ml de agua por kcal), de los cuales unos 1,4 litros deben consumirse en forma de bebidas. En caso de indicaciones especiales, son posibles cantidades de bebida que se desvíen de este valor orientativo y las determina el médico [14]. Las causas de la deficiencia de líquidos o deshidratación son múltiples y suelen basarse en una ingesta de líquidos demasiado escasa combinada con una pérdida de líquidos excesiva. Entre las etiologías más comunes se encuentran las enfermedades con diarrea, vómitos o fiebre (por cada grado por encima de 37 °C, el cuerpo necesita unos 300 ml adicionales de líquido al día), la ingesta de diuréticos o laxantes, la disfagia, la disminución de la sensación de sed, las temperaturas exteriores muy cálidas y el trabajo o el deporte físicamente extenuantes (necesidad adicional de 0,5-1,0 litros de agua por hora de actividad intensa). Cualquier prescripción de fluidos debe cubrir no sólo las necesidades diarias de mantenimiento sino también las pérdidas anormales. En caso de pérdidas por el tracto gastrointestinal, por ejemplo debido a una fístula o a una aspiración nasogástrica, la prescripción de líquidos debe incluir las necesidades diarias de mantenimiento más una reposición equivalente de agua y electrolitos.
Necesidades de micronutrientes: En los pacientes polimórbidos desnutridos, la necesidad de micronutrientes puede aumentar debido a la reducción de la ingesta de alimentos o a la enfermedad. Los micronutrientes deben suplementarse y/o sustituirse según la dosis diaria recomendada. Se considera que se cumplen las necesidades diarias de micronutrientes si la alimentación por sonda enteral es de al menos 1500 mL al día. Las soluciones nutritivas parenterales no contienen vitaminas ni oligoelementos y deben suplementarse adicionalmente [4].
Los cinco pasos de la terapia nutricional (Fig. 4) : El primer paso es informar a los pacientes sobre la nutrición rica en energía y proteínas, así como sobre los ritmos de las comidas (comidas frecuentes a lo largo del día), abordar cualquier problema existente que impida una ingesta adecuada de alimentos y evaluar las medidas de optimización. La nutrición oral con energía natural y alimentos ricos en proteínas debe ser la primera opción de terapia nutricional. Incluye adaptaciones de la textura de los alimentos (temperatura, sabor, consistencia, color), preferencias individuales, elección de alimentos con poco olor, tamaño adaptado de las raciones, así como una preparación suave de las comidas y el uso de ayudas (cuchara, taza, tetina, etc.). Además, las comidas pueden enriquecerse con alimentos naturales como aceite vegetal de alta calidad, mantequilla, nata, requesón, queso rallado, huevo o con productos especiales como proteínas o carbohidratos en polvo (maltodrextrina). En el programa diario pueden incluirse tentempiés adicionales de alta densidad energética (por ejemplo, batidos caseros, canapés, cremas).
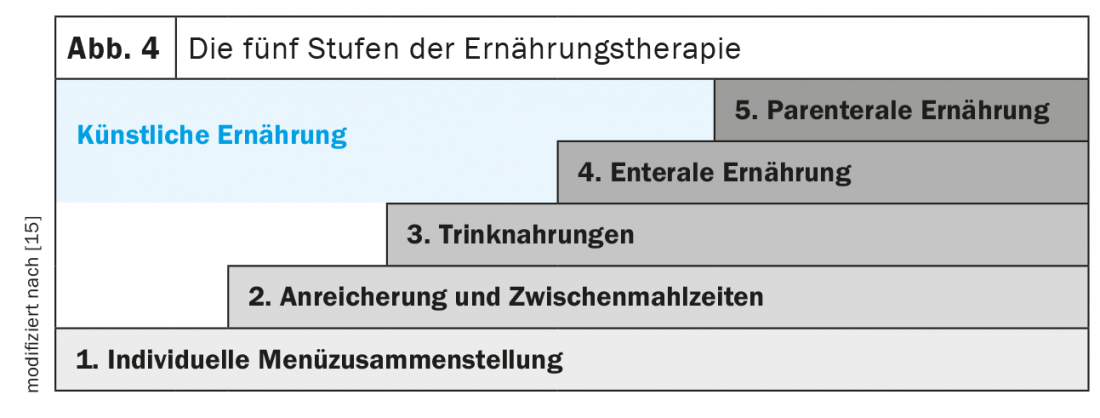
La siguiente etapa es la administración de alimentos comerciales totalmente equilibrados para sorber, que pueden servirse de forma atractiva y creativa. Ya en 1990, el estudio de Delmi et al. demostraron que la administración vespertina de un alimento bebible totalmente equilibrado (20 g de proteínas, 254 kcal) aumentaba la ingesta de energía en un 23% y la de proteínas en un 62% en pacientes geriátricos con fractura de cuello femoral. Esta intervención redujo significativamente las tasas de complicaciones, la duración de la estancia en hospitales y unidades de rehabilitación y la mortalidad [16]. Otros estudios demostraron que la administración complementaria de sorbos de pienso como tentempié no reduce el apetito, pero provoca un aumento significativo de la ingesta total de energía y proteínas. Varios estudios y metaanálisis han demostrado que la alimentación sip puede preservar la masa muscular y mejorar la calidad de vida, además de reducir significativamente las tasas de complicaciones, mortalidad y rehospitalización [7,8,17–21]. En general, varios estudios, que se basan principalmente en análisis retrospectivos de costes, indican que el uso de alimentación sip en el ámbito ambulatorio conlleva un beneficio global en términos de costes. Esto se asocia a menudo con resultados clínicamente relevantes, lo que indica una relación coste-eficacia [22].
Si la nutrición oral es insuficiente (<75% de las necesidades de energía y proteínas) o no es posible, debe considerarse la nutrición enteral y, si es necesario, la parenteral. La nutrición enteral es preferible en pacientes con un tracto gastrointestinal parcialmente funcional debido al menor riesgo de complicaciones infecciosas y no infecciosas. Ambas dietas artificiales e invasivas deben ser complementarias y no competitivas. Si no hay necesidades especiales, se recomienda empezar con una alimentación estándar por sonda o una solución nutritiva. En caso necesario, existe una amplia gama de productos más específicos para ambas dietas.
La ingesta de energía y proteínas debe evaluarse unas 2-3 veces por semana en el caso de los pacientes con enfermedades agudas, en función de los recursos de personal disponibles, y cada dos o cuatro semanas en el caso de los pacientes con enfermedades crónicas en la consulta del médico de cabecera como parte de una reevaluación. En función de la evolución, deben definirse otros objetivos e intervenciones nutricionales y, si es necesario, deben tomarse otras medidas terapéuticas. El contacto regular médico-paciente y los contactos con el asesor nutricional o las enfermeras de práctica avanzada ofrecen una buena oportunidad para revisar las recomendaciones terapéuticas y mejorar su aplicación.
Nutrición para estados de enfermedad específicos: En pacientes con insuficiencia renal, a menudo es necesario restringir la ingesta de potasio y fosfato. Los pacientes con insuficiencia cardíaca pueden beneficiarse de una restricción de sodio y agua o de un suplemento regular de tiamina y hierro en determinados casos. Existen escasas pruebas sobre el uso de suplementos nutricionales orales específicos o soluciones nutricionales enterales en pacientes hospitalizados polimórbidos. La arginina, la glutamina y el beta-hidroxi-beta-metilbutirato (HMB) pueden utilizarse en pacientes con úlceras por presión. Una mezcla de fibras solubles e insolubles puede utilizarse en pacientes crónicos alimentados con nutrición enteral y que sufren diarrea o estreñimiento, las complicaciones más comunes de la nutrición enteral. Debe prestarse especial atención al estado de hidratación, ya que la deshidratación puede provocar estreñimiento [4].
Momento de la terapia nutricional: Se recomienda el inicio precoz de la terapia nutricional (en el hospital en las 48 horas siguientes al ingreso) para prevenir el deterioro del estado nutricional y funcional y la sarcopenia. Aunque la duración óptima de la terapia nutricional aún no está clara, las pruebas actuales recomiendan el tratamiento más allá del alta hospitalaria [13].
Seguimiento de la terapia nutricional: Los equipos de nutrición clínica experimentados (en el ámbito hospitalario) y los asesores en nutrición o las enfermeras de práctica avanzada (en el ámbito ambulatorio) deben revisar a intervalos regulares la indicación, la vía de administración, los riesgos, los beneficios y los objetivos de la terapia nutricional. La duración de este intervalo depende del paciente y de los parámetros que deban controlarse (por ejemplo, parámetros nutricionales, antropométricos, bioquímicos, estado clínico) y puede prolongarse si el estado del paciente mejora con la terapia nutricional. Por ejemplo, se recomienda controlar la ingesta de nutrientes a través de la nutrición oral, enteral o parenteral en el ámbito hospitalario o al iniciar la terapia artificial, inicialmente a diario y dos veces por semana cuando el estado sea estable (por ejemplo, cuando exista un alto riesgo de desarrollar el síndrome de realimentación). Del mismo modo, los parámetros de laboratorio (por ejemplo, potasio, magnesio, fosfato, sodio, urea, creatinina) deben controlarse diariamente al principio, y más tarde 1-2 veces por semana. Además de los parámetros utilizados para controlar la respuesta a la terapia nutricional, deben recogerse regularmente índices funcionales (por ejemplo, la fuerza de cierre del puño) para evaluar otros resultados clínicos (por ejemplo, la supervivencia, la calidad de vida) [4]. Los intervalos entre las visitas de seguimiento en el sector ambulatorio son significativamente más largos que en el sector hospitalario.
Sensibilización sobre la prevención, la identificación y el tratamiento de la malnutrición
La EM debería abordarse con más frecuencia en la educación y formación del personal médico, tanto en los hospitales como en el sector ambulatorio. Es necesario aumentar la concienciación sobre la EM y considerar el tratamiento nutricional como parte del tratamiento médico multimodal. La EM sigue sin identificarse con demasiada frecuencia, está infradiagnosticada y, en consecuencia, no se trata.
Se necesitan protocolos y responsabilidades claramente definidos para abordar esta cuestión tanto en el ámbito hospitalario (en el momento del ingreso) como en el ambulatorio (en las consultas iniciales o de seguimiento). Esto comienza con la introducción de un cribado nutricional sistemático, seguido de una evaluación nutricional rápida y sencilla para los pacientes de riesgo. Un estudio reciente demostró que alrededor del 80% de los hospitales y residencias de ancianos de Suiza no han implantado un proceso sistemático de detección del riesgo de ME y que sólo el 25% de los hospitales examinan a los pacientes si sospechan que existe algún problema. Además, el 56% de los centros controla la ingesta de alimentos y el 50% supervisa y documenta el estado nutricional de sus pacientes [23].
Dado que la etiología de la EM suele ser multifactorial (desde la depresión a la pérdida de apetito, pasando por la incapacidad para alimentarse), debe garantizarse una comunicación y cooperación óptimas entre el equipo de tratamiento hospitalario, el equipo/red de tratamiento ambulatorio (médico de cabecera, Spitex, atención domiciliaria, asesoramiento nutricional, etc.) y el paciente. Esto permite abordar los posibles problemas de forma eficiente y eficaz.
El ME también es un problema común en el ámbito ambulatorio. El papel de los médicos de cabecera y las enfermeras de práctica avanzada, los especialistas de la práctica privada, los nutricionistas y las enfermeras es esencial para detectar precozmente los signos de la EM (cribado/precribado NRS 2002) y tratarlos adecuadamente. La terapia nutricional suele iniciarse durante la hospitalización y continuarse en el ámbito ambulatorio, revisándose periódicamente. Basándose en muchos años de experiencia clínica y en los resultados del estudio EFFORT, se ha planificado ahora el estudio de seguimiento “Effect of Nutritional Therapy on Frailty, Functional Outcomes and Recovery of Undernourished Medical Patients at Discharge Trial” (EFFORT II) en el ámbito ambulatorio – un suizo iniciada por el investigador, ensayo controlado aleatorio multicéntrico no comercial, que comenzará en el segundo semestre de 2021. El objetivo general de este estudio es demostrar el beneficio sostenido de la terapia nutricional domiciliaria individualizada en términos de mortalidad, complicaciones graves, rehospitalizaciones no electivas y funcionalidad según un algoritmo de aplicación sobre la nutrición habitual en pacientes polimórbidos desnutridos.
Conclusión
Una terapia nutricional adecuada e individualizada ha demostrado ser una opción terapéutica muy eficaz en la prevención y terapia de la EM. Reduce significativamente las tasas de morbilidad y mortalidad. También mejora significativamente la calidad de vida y la funcionalidad física. En vista de la complejidad de la EM y para poder lograr un éxito terapéutico a largo plazo de las intervenciones nutricionales, deberían integrarse medidas adicionales como la actividad física y el apoyo psicológico regular en el sentido de un enfoque terapéutico multimodal. Durante los contactos regulares con los pacientes, se debe preguntar sobre los problemas nutricionales y recoger datos antropométricos sencillos. Es importante incorporar los nuevos conocimientos presentados en esta revisión a la práctica clínica para garantizar que los pacientes reciban una atención óptima, de alta calidad y segura.
Mensajes para llevarse a casa
- La desnutrición es frecuente y está asociada a una mayor morbilidad y mortalidad.
- Es crucial identificar precozmente a los pacientes desnutridos con una sencilla herramienta de cribado (NRS 2002).
- La terapia nutricional debe planificarse, aplicarse, controlarse y ajustarse periódicamente.
- Las intervenciones nutricionales específicas y adecuadas son eficaces y reducen las tasas de complicaciones y mortalidad.
- Una gestión nutricional eficaz está orientada a los objetivos y garantiza una alta calidad del tratamiento.
Literatura:
- de van der Schueren MAE, Soeters PB, Reijven PLM, et al: Diagnóstico de la malnutrición – Detección y evaluación. En: Sobotka L, Allison SP, Forbes A, Meier RF, Schneider SM, Soeters PB, et al: Conceptos básicos en nutrición clínica. 5 ed. Praga: Galén 2019; 18-27.
- Schindlegger W: Causas de la anorexia en la vejez. Revista de Medicina Nutricional (Número para Suiza) 2001; 3(3): 20-23.
- Guigoz Y: La revisión bibliográfica de la minievaluación nutricional (MNA) – ¿Qué nos dice? The journal of nutrition, health & aging 2006; 10(6): 466-485; discusión 85-87.
- Reber E, Gomes F, Bally L, et al: Tratamiento nutricional de los pacientes médicos ingresados. Revista de medicina clínica 2019; 8(8).
- Gomes F, Baumgartner A, Bounoure L, et al: Association of Nutritional Support With Clinical Outcomes Among Medical Inpatients Who Are Malnourished or at Nutritional Risk: An Updated Systematic Review and Meta-analysis. Red JAMA abierta 2019; 2(11): e1915138.
- Estruch R, Ros E, Salas-Salvado J, et al: Prevención primaria de las enfermedades cardiovasculares con una dieta mediterránea suplementada con aceite de oliva virgen extra o frutos secos. The New England journal of medicine 2018; 378(25): e34.
- Deutz NE, Matheson EM, Matarese LE, et al: Readmisión y mortalidad en adultos desnutridos, mayores y hospitalizados tratados con un suplemento nutricional oral especializado: Un ensayo clínico aleatorizado. Nutrición clínica 2016; 35(1): 18-26.
- Schuetz P, Fehr R, Baechli V, et al: Apoyo nutricional individualizado en pacientes hospitalizados con riesgo nutricional: un ensayo clínico aleatorizado. Lancet 2019; 393(1088): 2312-2321.
- Kondrup J, Allison SP, Elia M, et al: Directrices ESPEN para el cribado nutricional 2002. Nutrición clínica 2003; 22(4): 415-421.
- Kondrup J, Rasmussen HH, Hamberg O, Stanga Z: Cribado del riesgo nutricional (NRS 2002): un nuevo método basado en un análisis de ensayos clínicos controlados. Nutrición clínica 2003; 22(3): 321-336.
- Harris JA, Benedict FG: Un estudio biométrico del metabolismo basal humano. Actas de la Academia Nacional de Ciencias de los Estados Unidos de América 1918; 4(12): 370-373.
- Reber E, Strahm R, Bally L, et al: Eficacia y eficiencia de los equipos de apoyo nutricional. Revista de medicina clínica 2019; 8(9).
- Gomes F, Schuetz P, Bounoure L, et al: Directrices ESPEN sobre el soporte nutricional para pacientes polimórbidos de medicina interna. Nutrición clínica 2018; 37(1): 336-353.
- Padhi S, Bullock I, Li L, Stroud M: Fluidoterapia intravenosa para adultos hospitalizados: resumen de las orientaciones del NICE. BMJ 2013; 347: f7073.
- Aubry E, Mareschal J, Gschweitl M, et al: Datos sobre la gestión de la nutrición clínica – una encuesta en línea. Medicina Nutricional Actual 2018; 42(06): 452-460.
- Delmi M, Rapin CH, Bengoa JM, et al: Suplementación dietética en pacientes ancianos con fractura de cuello de fémur. Lancet 1990; 335(8696): 1013-1016.
- Norman K, Pirlich M, Smoliner C, et al: Rentabilidad de una intervención de 3 meses con suplementos nutricionales orales en la malnutrición relacionada con la enfermedad: un estudio piloto aleatorizado y controlado. Revista europea de nutrición clínica 2011; 65(6): 735-742.
- Stratton RJ, Elia M: Una revisión de las revisiones: Una nueva mirada a las pruebas de los suplementos nutricionales orales en la práctica clínica. Nutrición clínica 2007; 2(1): 5-23.
- Instituto Nacional para la Excelencia Sanitaria y Asistencial. Apoyo nutricional para adultos: apoyo nutricional oral, alimentación enteral por sonda y nutrición parenteral (CG32)2006; última actualización 2017.
- Chew STH, Tan NC, Cheong M, et al: Impacto del suplemento nutricional oral especializado en los resultados clínicos, nutricionales y funcionales: Un ensayo aleatorizado y controlado con placebo en adultos mayores residentes en la comunidad con riesgo de desnutrición. Nutrición clínica 2020.
- Milne AC, Avenell A, Potter J: Metaanálisis: suplementación proteica y energética en personas mayores. Anales de medicina interna 2006; 144(1): 37-48.
- Elia M, Normand C, Laviano A, Norman K: Una revisión sistemática del coste y la rentabilidad del uso de suplementos nutricionales orales estándar en entornos comunitarios y de atención domiciliaria. Nutrición clínica 2016; 35(1): 125-137.
PRÁCTICA GP 2021; 16(4): 11-17











