Em doentes com asma inadequadamente controlada sob terapêutica inalatória máxima, deve questionar-se criticamente se o diagnóstico de asma está realmente presente e se todas as medidas de tratamento estão a ser adequadamente implementadas. Se assim for, é importante que se concentre nos medicamentos biológicos disponíveis para o tratamento da asma grave. A determinação de biomarcadores pode ajudar a selecionar a classe de substância mais adequada em cada caso.
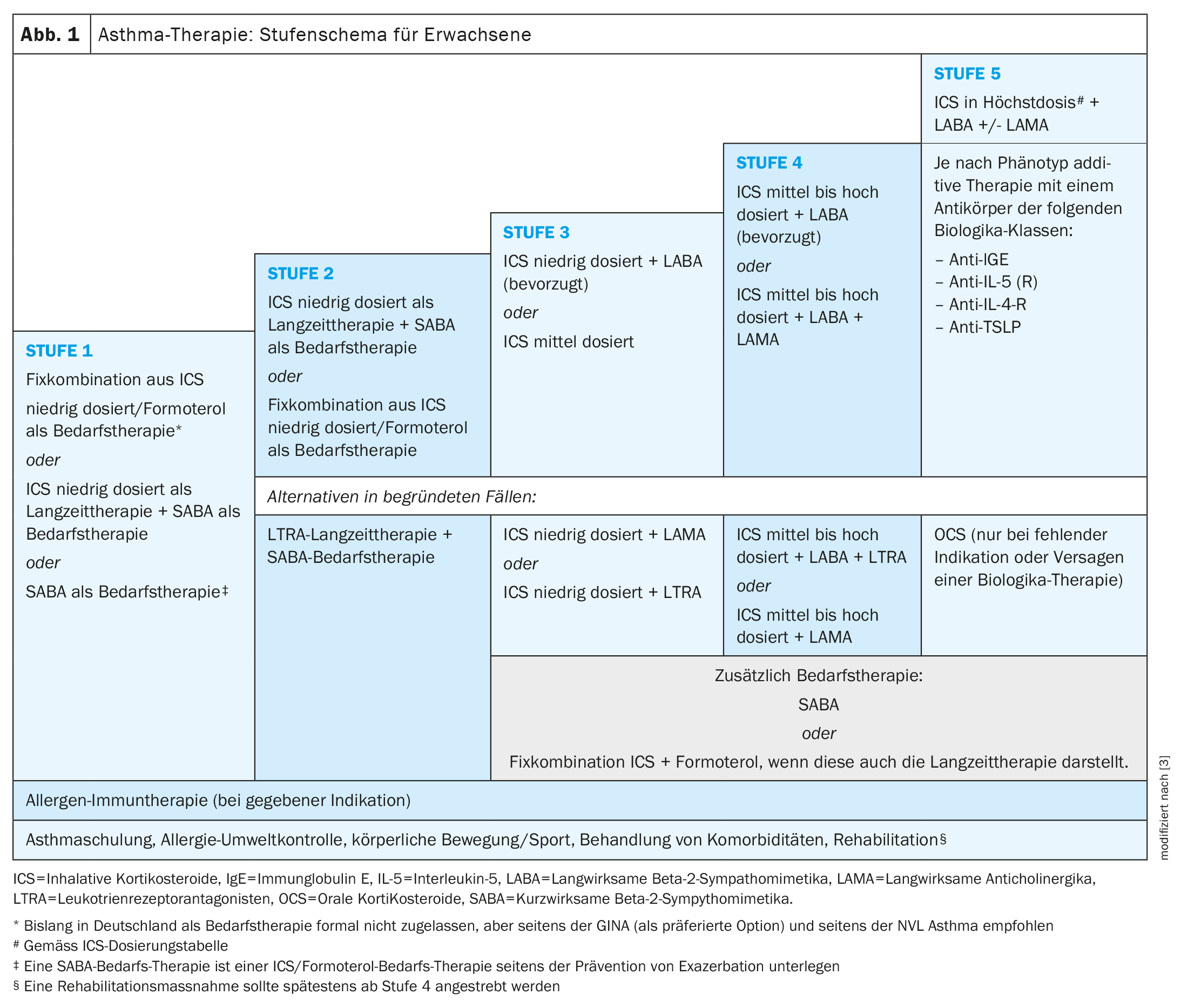
A asma ocorre frequentemente na infância e na adolescência, mas também se pode manifestar pela primeira vez na idade adulta [1]. A asma “de início na idade adulta” tende a ser mais grave e a ter taxas de exacerbação mais elevadas, informou o Prof. Christophe von Garnier, médico chefe do Departamento de Pneumologia do Hospital Universitário de Lausanne (CHUV) [2–4]. “A asma de início na idade adulta está menos frequentemente associada a alergias, mas mais frequentemente a rinossinusite crónica com pólipos nasais (RSCwNP) e outras comorbilidades. “A asma de início precoce corresponde geralmente à asma alérgica clássica. São utilizados medicamentos a longo prazo e a pedido para controlar os sintomas da asma, de acordo com o esquema passo-a-passo (Fig. 1). De acordo com a nova definição da GINA**, a asma é considerada grave se se revelar refractária à terapêutica tripla inalatória máxima (ICS em dose máxima e LABA mais possivelmente LAMA) [5]. Se, por exemplo, não se conseguir um controlo suficiente da doença num período de um mês com a terapêutica por inalação máxima, devem ser efectuadas primeiro várias investigações:
- É realmente asma ou é antes DPOC, por exemplo?
- O doente aplica as medidas de tratamento propostas?
- Está a utilizar a técnica de inalação correcta?
- Existem factores desencadeantes da asma que possam ser evitados (por exemplo, alergénios)?
- Existem comorbilidades não tratadas?
Se se concluir que a asma é realmente grave, o passo seguinte será testar o tratamento com produtos biológicos específicos do fenótipo como opção terapêutica complementar [2,3]. O objetivo a longo prazo é alcançar e manter a remissão da asma, ou seja, uma asma bem controlada a longo prazo.
** Directrizes da Iniciativa Global para a Asma (GINA) 2022
Eosinófilos no sangue e FeNO como biomarcadores
Os processos inflamatórios subjacentes à asma grave são complexos, heterogéneos e dinâmicos [6]. A diátese atópica é o fator predisponente mais forte para o desenvolvimento da asma identificado até à data. No entanto, em 30-50% dos adultos com asma, as alergias a alergénios ambientais não são detectáveis, quer pela história, quer por testes cutâneos ou determinação de IgE específica no soro, razão pela qual esta forma é também referida como asma não alérgica ou intrínseca [3]. A asma alérgica e não alérgica são resumidas na literatura sob o termo genérico de asma “tipo 2” ou “tipo 2-alta” [7]. Isto baseia-se na constatação de que certas citocinas podem ser libertadas não só por células T auxiliares específicas do alergénio (células Th2) do sistema imunitário adaptativo, mas também por células ILC2 não específicas do alergénio do sistema imunitário inato, e conduzir a padrões inflamatórios semelhantes.
Os biomarcadores do tipo 2 incluem os eosinófilos no sangue e o FeNO [3,8,9]. Para poder delimitar o fenótipo, as recomendações da GINA aconselham a medição destes dois biomarcadores pelo menos três vezes, uma vez que estão sujeitos a fortes flutuações individuais. Por exemplo, o número de eosinófilos no sangue é influenciado pela hora do último contacto com o alergénio e pela época do ano, e os níveis de FeNO são influenciados por infecções ou pela exposição a poluentes [3,10]. Além disso, ambos os biomarcadores são significativamente influenciados pelas terapêuticas com CI e CO [3,11,12].
A eosinofilia elevada provoca danos no tecido pulmonar, hiperresponsividade e remodelação das vias respiratórias devido à ativação das células eosinofílicas [13]. O diagnóstico de asma eosinofílica grave requer pelo menos duas detecções de mais de 300 eosinófilos/µl no sangue fora das exacerbações e sem medicação com corticosteróides sistémicos.
Biológicos como terapêutica de manutenção complementar
As substâncias activas que têm como alvo as interleucinas (anti-IL-5-(R), anti-IL-4-R) ou IgE visam a via inflamatória do tipo 2. A eosinofilia sanguínea (≥300 células/μl) é considerada um fator de previsão da resposta a anticorpos monoclonais contra a IL-5 (mepolizumab, reslizumab) ou contra a IL-5-R (benralizumab) [20]. A eosinofilia sanguínea (≥300 células/μl) ou uma concentração de FeNO >25 ppb são também factores de previsão de uma resposta ao tratamento com o anticorpo anti-IL4R dupilumab. Os doentes com asma alérgica grave e níveis elevados de IgE, por outro lado, têm maior probabilidade de responder ao omalizumab. Se o valor de referência da IgE for inferior a 76 U.I./ml, é menos provável que o anticorpo anti-IgE tenha um benefício clínico [19]. O anticorpo monoclonal tezepelumab, que será autorizado na Suíça em 2022, tem um modo de ação diferente do das substâncias acima referidas. O alvo deste produto biológico é a TSLP (linfopoietina do estroma tímico). Ao ligar-se ao TSLP, o tezepelumab impede a sua interação com o recetor heterodimérico do TSLP. A TSLP é uma citocina da família das alarminas que é libertada principalmente pelas células epiteliais em resposta a vários estímulos (por exemplo, vírus, alergénios e poluentes), está envolvida na cascata inflamatória na asma e desempenha um papel na iniciação e persistência da inflamação asmática das vias aéreas [15]. Na asma, tanto os estímulos alérgicos como os não alérgicos induzem a produção de TSLP. O bloqueio do TSLP com tezepelumab afecta um amplo espetro de biomarcadores e citocinas associados à inflamação (por exemplo, eosinófilos no sangue, IgE, FeNO, IL-5 e IL-13) [15–17]. Por conseguinte, a TSLP desempenha um papel patogénico importante em vários subtipos de asma [16,17]. Um artigo de revisão publicado em 2022 mostrou que o tezepelumab é uma opção de tratamento adequada para a asma grave não controlada e <1500 eosinófilos/μl, independentemente do FeNO e do estado de alergia [18]. Além disso, o tezepelumab demonstrou reduzir a taxa de exacerbação em doentes com asma grave não controlada, independentemente da contagem de eosinófilos na linha de base.
Congresso: Atualização sobre Alergia e Imunologia
Literatura:
- Akar-Ghibril N, et al: Endótipos alérgicos e fenótipos da asma. J Allergy Clin Immunol Pract 2020; 8(2): 429-440.
- “Como reconhecer e tratar a asma grave (Th2)”, Prof. Dr. Christophe von Garnier, Allergy & Immunology Update, Grindelwald, 27.01.2024.
- Lommatzsch M, et al: S2k guideline for the specialist diagnosis and treatment of asthma 2023, Sociedade Alemã de Pneumologia e Medicina Respiratória e.V. (ed.), https://register.awmf.org,(último acesso em 07.03.2024)
- Baan EJ, et al: Caracterização da asma por idade de início: um estudo de coorte com várias bases de dados. J Allergy Clin Immunol Pract 2022; 10: 1825-1834.e1828.
- Iniciativa Global para a Asma (GINA), 2022, www.ginasthma.com,(último acesso em 07/03/2024)
- Busse WW: Biological treatments for severe asthma: A major advance in asthma care. Allergol Int 2019; 68(2): 158-166.
- Hinks TSC, Levine SJ, Brusselle GG: Opções de tratamento na asma baixa tipo 2. Eur Respir J 2021; 57(1).
- Hammad H, Lambrecht BN: A imunologia básica da asma. Cell 2021; 184: 1469-1485.
- Lommatzsch M: Modulação imunitária na asma: conceitos actuais e estratégias futuras. Respiração 2020; 99: 566-576.
- Chipps BE, et al: Uma análise abrangente da estabilidade dos níveis de eosinófilos no sangue. Ann Am Thorac Soc 2021; 18: 1978-1987.
- Lommatzsch M, et al: Impacto de um aumento da dose de corticosteroide inalado nos eosinófilos sanguíneos na asma. Thorax 2019; 74: 417-418.
- Jackson DJ, et al: Caracterização dos doentes com asma grave no Registo de Asma Grave do Reino Unido na era biológica. Thorax 2021; 76: 220-227.
- Patterson MF, Borish L, Kennedy JL: O passado, o presente e o futuro dos anticorpos monoclonais contra a IL-5 e a asma eosinofílica: uma revisão. J Asthma Allergy 2015; 8: 125-134.
- Berry M, et al: Pathological features and inhaled corticosteroid response of eosinophilic and non-eosinophilic asthma (Características patológicas e resposta a corticosteróides inalados na asma eosinofílica e não eosinofílica). Thorax 2007; 62: 1043-1049.
- Compêndio Suíço de Drogas,
https://compendium.ch,(último acesso em 07/03/2024) - Menzies-Gow A, Wechsler ME, Brightling CE: Necessidades não satisfeitas na asma grave não controlada: pode a terapêutica anti-TSLP com tezepelumab constituir uma nova e valiosa opção de tratamento? Respiratory research 2020; 21(1): 268.
- Gauvreau GM, et al: Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Parecer de peritos sobre alvos terapêuticos 2020; 24(8): 777-792.
- Brusselle GG, Koppelman GH: Terapias Biológicas para a Asma Grave. The New England journal of medicine 2022; 386(2): 157-171.
- Omalizumab, https://ec.europa.eu/health/documents/community-register/2022/20221014157073/anx_157073_de.pdf,(último acesso em 07/03/2024)
- Mepolizumab, reslizumab e benralizumab, www.leitlinien.de/themen/asthma/4-auflage/kapitel-4,(último acesso em 07/03/2024).
HAUSARZT PRAXIS 2024; 19(3): 26-28 (publicado em 20.3.24, antes da impressão)