La tromboembolia venosa (TEV) es la tercera enfermedad cardiovascular más frecuente en Europa Central. Se manifiestan como trombosis venosa profunda en unos dos tercios de los casos y con síntomas de embolia pulmonar en aproximadamente un tercio. Durante la edad reproductiva, las mujeres experimentan episodios de TEV con mayor frecuencia que los hombres de la misma edad.
La tromboembolia venosa (TEV) es la tercera enfermedad cardiovascular más frecuente en Europa Central. Se manifiestan como trombosis venosa profunda en unos dos tercios de los casos y con síntomas de embolia pulmonar en aproximadamente un tercio. Durante la edad reproductiva, las mujeres experimentan episodios de TEV con mayor frecuencia que los hombres de la misma edad. Esto se atribuye principalmente a factores de riesgo específicos de la mujer, como el uso de anticonceptivos hormonales y los embarazos. A pesar de este aumento relativo del riesgo, el riesgo global de TEV sigue siendo bajo, en torno a 2-5 por cada 10.000 mujeres al año [1].
Hormonas y hemostasia
Los estrógenos influyen en la expresión genética hepática y modifican el equilibrio entre los factores coagulantes y anticoagulantes hacia una mayor coagulabilidad. El nivel de la dosis de estrógeno y el tipo de progestágeno en los preparados combinados determinan el riesgo de complicaciones trombóticas. Pueden detectarse actividades aumentadas de los factores trombogénicos (fibrinógeno, protrombina, factor VII, factor VIII, factor X) y actividades reducidas de los inhibidores fisiológicos de la coagulación (antitrombina, proteína S, inhibidor de la vía del factor tisular [TFPI]) cuando se toman preparados hormonales [2,3]. Esto provoca una resistencia a la proteína C activada (la llamada resistencia adquirida a la APC). El grado de esta resistencia a los APC se correlaciona con el riesgo de TEV [4].
Anticonceptivos hormonales combinados
Los anticonceptivos hormonales combinados (AHC) representan la mayor proporción de métodos anticonceptivos utilizados. Pocos años después de su introducción en el mercado en 1960, ya se sabía que las cardiopatías coronarias aumentan el riesgo de trombosis venosa y, en menor medida, de trombosis arterial [5]. La composición de la cardiopatía isquémica ha cambiado en los últimos 60 años, pero los componentes básicos no han cambiado. Los CHD modernos contienen una combinación de un estrógeno (normalmente etinilestradiol en una dosis de 20 -35 µg) y un progestágeno producido sintéticamente. La composición determina la magnitud del aumento del riesgo de episodios tromboembólicos (tab. 1) . Entre los CHD, los preparados que contienen una dosis baja de estrógenos y levonorgestrel como progestágeno presentan el menor riesgo de TEV [6,7]. Con otros componentes progestágenos, el riesgo de TEV es a veces significativamente mayor. Se ha descrito un mayor riesgo de trombosis no sólo en los CHD de aplicación oral, sino también en los preparados combinados de aplicación transdérmica y transvaginal [8].

El riesgo de tromboembolismo es mayor en los primeros meses de uso y disminuye significativamente durante el primer año. Sin embargo, incluso con un uso prolongado, las mujeres que lo utilizan siguen teniendo un riesgo de TEV aproximadamente 2 veces mayor que las mujeres que no utilizan anticonceptivos hormonales [9]. Si se interrumpe la anticoncepción hormonal durante varias semanas, existe un riesgo temporalmente mayor de TEV con la reanudación que con el uso continuado. Por lo tanto, no parece razonable pausar el CHD perioperatoriamente para reducir el riesgo de TEV. Por lo tanto, si el riesgo de TEV es elevado, debe administrarse profilaxis del TEV con una heparina de bajo peso molecular u otra sustancia aprobada para la indicación [1].
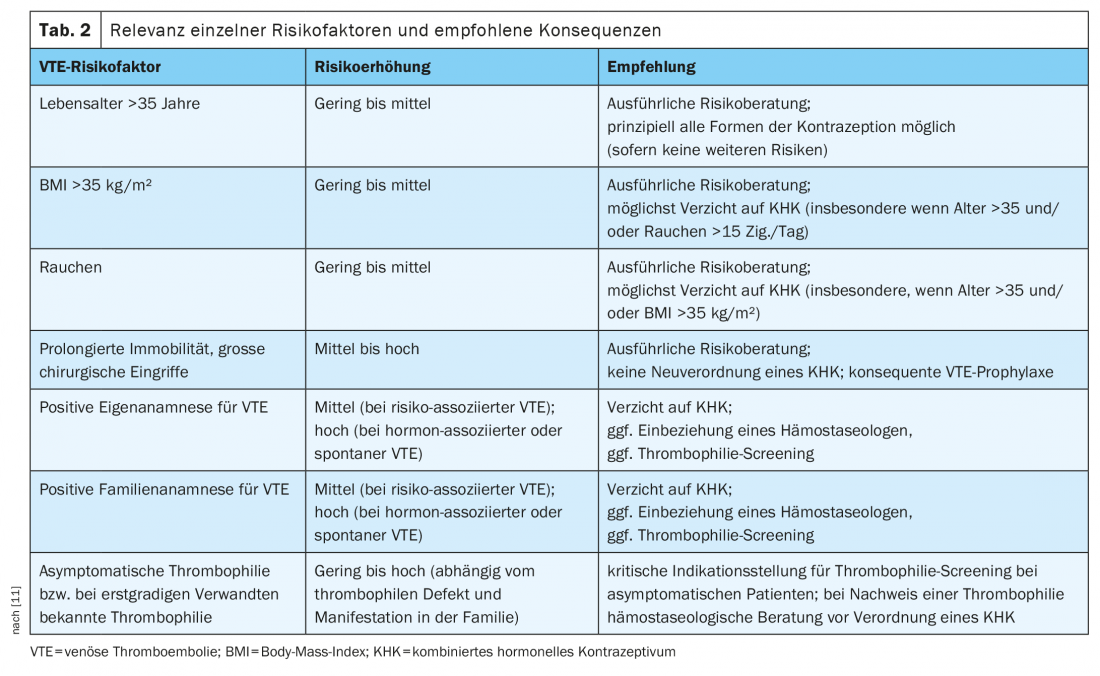
En presencia de factores de riesgo adicionales (por ejemplo, trombofilia hereditaria, antecedentes familiares positivos, edad avanzada, obesidad, tabaquismo), el riesgo de TEV aumenta aún más [10]. El riesgo individual de TEV debe evaluarse cada vez que se prescriba un nuevo CHD mediante una cuidadosa historia clínica. La directriz S3 de la AWMF sobre anticoncepción hormonal, recientemente actualizada, recomienda que se incluyan en la evaluación del riesgo factores como la edad, el índice de masa corporal, el hábito de fumar, los problemas de movilidad, una cirugía mayor próxima, información sobre los antecedentes propios y familiares de episodios de TEV y cualquier trombofilia conocida [11]. En la tabla 2 se ofrece una visión general de los factores de riesgo y las consecuencias recomendadas.
Trombofilia hereditaria y anticoncepción hormonal
La cuestión de si unos antecedentes familiares positivos constituyen por sí solos una contraindicación para la anticoncepción hormonal es objeto de controversia. Algunos estudios han demostrado que la trombofilia hereditaria junto con el uso de un CHD aumenta significativamente el riesgo relativo de TEV [12,13]. Hoy en día hay acuerdo en que el cribado general de la trombofilia antes de la primera prescripción de una cardiopatía isquémica no es útil. Se puede detectar al menos una trombofilia hereditaria en el 3-9% de la población centroeuropea (Tab. 3) . Las más comunes son la heterocigosidad para una mutación del factor V Leiden (aprox. 2-7%) o una mutación de la protrombina G20210A (aprox. 1-2%). A pesar de la elevada prevalencia de estas mutaciones, el riesgo absoluto de TEV en los afectados es bajo, a menos que se añadan otros factores de riesgo.

Un reciente trabajo francés que incluía a 2214 parientes de 651 familias con trombofilia hereditaria conocida y manifestaciones de TEV calculó un riesgo absoluto anual de TEV del 0,36% (HR 1,91; IC 95% 1,30-2,80) para los individuos con trombofilia leve pero sin eventos previos de TEV propios, y del 0,64% (HR 3,78; IC 95% 2,50-5,73) para los individuos con trombofilia grave. [14]. Sin embargo, el riesgo de TEV aumenta significativamente cuando se toma un CHD.
Otro grupo de investigación calculó un riesgo relativo de TEV hasta 45 veces mayor en mujeres con una mutación del factor V Leiden [15]. Por lo tanto, a las mujeres con trombofilia y antecedentes familiares positivos no se les debe prescribir CHD si es posible, especialmente si la paciente índice ha tenido un episodio de TEV a una edad temprana sin otros factores de riesgo o asociados a las hormonas. Si la prescripción de un CHD es inevitable debido a circunstancias concomitantes o comorbilidades, debe considerarse una evaluación hemostaseológica y la prescripción de un CHD con levonorgestrel como componente progestágeno. Debe evitarse en casos de trombofilia grave conocida; en estos casos, debe preferirse un método anticonceptivo sin estrógenos.
Monopreparados de progestágeno
Según los conocimientos actuales, los anticonceptivos con un componente de progestágeno solo (es decir, los preparados orales con desogestrel o levonorgestrel o los dispositivos intrauterinos que contienen levonorgestrel) no aumentan significativamente el riesgo de TEV. Por tanto, pueden utilizarse en mujeres con mayor riesgo de TEV o con antecedentes de TEV [1,16]. Sin embargo, esto no se aplica al acetato de medroxiprogesterona de depósito (DMPA; la llamada inyección de 3 meses), para el que se ha descrito un riesgo aproximadamente 3 veces mayor de TEV [17]. Por lo tanto, debe evitarse la administración de AMPD en mujeres con mayor riesgo de TEV.
Anticoncepción bajo anticoagulación
A menudo, las mujeres con TEV asociado a hormonas dejan de tomar el anticonceptivo inmediatamente después de que se confirme el diagnóstico. Esto es -problemático en la medida en que la interrupción conduce a hemorragias abortivas, que pueden ser más graves bajo dosis más altas de anticoagulantes en la fase inicial (apixaban, rivaroxaban) o anticoagulación solapada (NMH más antagonista de la vitamina K [VKA]) que en la fase de terapia de mantenimiento. Además, aumenta el riesgo de un embarazo no deseado. La actual directriz S3 de la AWMF pide una anticoncepción segura para todas las mujeres en tratamiento con anticoagulantes orales [11], ya que tanto los anticoagulantes orales directos (DOAK) como los AVK son compatibles con la placenta y, por tanto, potencialmente embriotóxicos. Según la evaluación actual, el efecto protrombogénico de la CHD se compensa con una anticoagulación totalmente terapéutica, por lo que la anticoncepción continuada con una CHD bajo protección anticoagulante se considera segura.
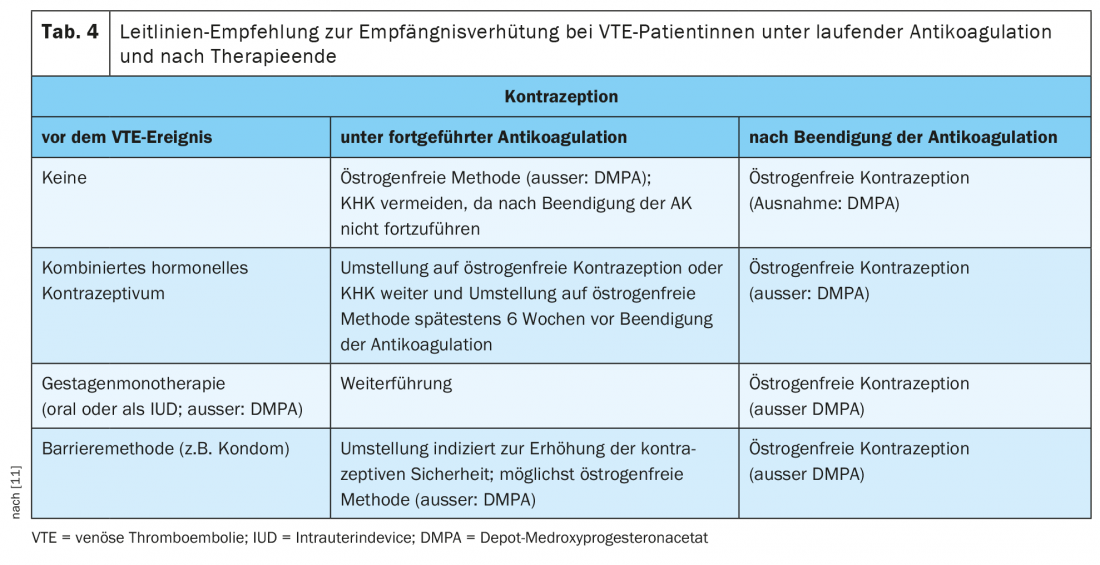
En un análisis post hoc de subgrupos de los ensayos EINSTEIN-DVT y EINSTEIN-PE en el que se comparó el riesgo de recurrencia en mujeres antes de los 60 años con y sin terapia hormonal continuada, no hubo pruebas de un aumento de la tasa de recurrencia de TEV con la terapia hormonal continuada (3,7% frente a 4,7%; HR 0,56; IC del 95%: 0,23-1,39) [18]. Para minimizar el riesgo de TEV bajo anticoagulación, la directriz S3 de la AWMF recomienda un monopreparado de progestágeno (oral o como dispositivo intrauterino) o un DIU de cobre como método de primera elección (los llamados métodos sin estrógenos). (Tab. 4). Si la paciente, junto con su médico, decide continuar con la anticoncepción con un CHD, se recomienda cambiar a un preparado con levonorgestrel como componente progestágeno [11].
ETV asociada a hormonas y riesgo de recurrencia
Según las evaluaciones de riesgo actuales, las cardiopatías coronarias se consideran factores de riesgo débiles y transitorios [19]. Dado que el uso continuado de CHD tras la interrupción de la anticoagulación se acompaña de un riesgo presumiblemente alto de recurrencia, debe interrumpirse el uso de CHD o cambiarse a un anticonceptivo sin estrógenos al menos 6 semanas antes de la interrupción prevista de la anticoagulación.
En principio, las mujeres tienen un menor riesgo de recurrencia tras un primer episodio de TEV que los hombres de la misma edad. En el plazo de un año, el 5,3% y en el plazo de 5 años el 11,1% de todas las mujeres sufren una recidiva. El riesgo de recurrencia es menor tras una ETV asociada a hormonas que tras una ETV espontánea (HR 0,5; IC 95% 0,3-0,8) [20]. Los estudios de cohortes informan de un riesgo absoluto anual del 1,1-2,5% [21–23]. Esto se compara con un riesgo medio de hemorragia bajo anticoagulación totalmente terapéutica de alrededor del 1-3% anual [24]. Algunos estudios informan incluso de un mayor riesgo de hemorragias graves y clínicamente relevantes en las mujeres en comparación con los hombres [10].
Por lo tanto, teniendo en cuenta los beneficios y los riesgos, la anticoagulación tras una ETV asociada a una cardiopatía coronaria y en ausencia de factores de riesgo persistentes suele limitarse a 3 – 6 meses. Si se ha continuado con la anticoncepción con una CHD, debe procurarse cambiarla por un método anticonceptivo sin estrógenos al menos 6 semanas antes del cese previsto de la anticoagulación.
Técnicas de reproducción asistida y riesgo de TEV
La proporción de embarazos resultantes de técnicas de reproducción asistida (TRA) ha aumentado en los últimos años. La terapia hormonal necesaria para ello aumenta el riesgo de TEV. Por ejemplo, las mujeres que se han quedado embarazadas tras una fecundación in vitro (FIV) tienen un riesgo aproximadamente 2 veces mayor que las mujeres que se han quedado embarazadas espontáneamente [25,26]. En un análisis sueco basado en la población de 140.458 registros de 1990 a 2008, el riesgo absoluto de TEV para las mujeres embarazadas tras un tratamiento de FIV fue del 0,42% en comparación con el 0,25% para las mujeres con un embarazo de inicio espontáneo (HR 1,77; 95% CI 1,41-2,23). El riesgo de TEV se mantuvo más elevado durante todo el curso del embarazo, pero fue mayor en el primer trimestre (HR 4,22; IC 95% 2,46 -7,26) [25]. Es especialmente elevado (1- 4%) en el caso de las mujeres que desarrollan un síndrome de hiperestimulación ovárica (SHO) grave en el curso [27,28].
Terapia hormonal sustitutiva y riesgo de TEV
La terapia hormonal sustitutiva (THS) se utiliza para tratar los síntomas de la menopausia y las enfermedades causadas por la carencia de estrógenos. La THS no pretende mantener los niveles hormonales previos, sino eliminar síntomas como los sofocos, los trastornos del sueño, el estado de ánimo depresivo o las molestias urogenitales debidas a la atrofia de la mucosa con la dosis eficaz más baja. Dado que la monoterapia con estrógenos se asocia a un mayor riesgo de carcinoma endometrial, suelen utilizarse preparados combinados.
Tanto los monopreparados de estrógenos como los preparados combinados de estrógenos y progestágenos se asocian a un riesgo aproximadamente 2-3 veces mayor de TEV [29]. En el caso de las mujeres con TEV previa, se ha descrito incluso un aumento del riesgo de aproximadamente 4 veces [30,31]. Al igual que ocurre con los anticonceptivos hormonales, el riesgo de TEV aumenta con la dosis de estrógenos y en función del componente progestágeno (fig. 1). El riesgo es mayor en el primer año de uso y sigue siendo elevado mientras dure el uso. Aumenta con la edad y la obesidad. A diferencia de la cardiopatía coronaria, el riesgo no parece aumentar con la aplicación transdérmica [32,33].

Conclusión para la práctica
Conociendo el mayor riesgo de episodios tromboembólicos, al prescribir un CHD debe preferirse una formulación con el menor riesgo conocido de trombosis. Además, toda mujer que utilice un CHD debe ser informada sobre el mayor riesgo de tromboembolismo. Lo mismo se aplica a las mujeres que utilizan métodos de inseminación artificial o que van a someterse a la THS durante la menopausia. Antes de prescribirlo, deben investigarse los factores de riesgo individuales adicionales, como los episodios de trombosis venosa y arterial en los antecedentes propios o familiares del paciente, una trombofilia conocida, el tabaquismo o la obesidad. También debe informarse a la mujer sobre los signos que indican trombosis o embolia pulmonar, para que pueda buscar ayuda médica inmediatamente si presenta síntomas.
Mensajes para llevarse a casa
- La terapia con preparados combinados de estrógeno y progestágeno aumenta el riesgo de tromboembolismo, por lo que la magnitud del aumento del riesgo depende tanto de la dosis de estrógeno como del componente de progestágeno.
- El riesgo de TEV es mayor en el primer año de uso, pero sigue siendo elevado a partir de entonces en comparación con las mujeres que no toman CHD.
- Según los conocimientos actuales, los monopreparados de progestágeno (oral o DIU) no aumentan el riesgo de trombosis.
- Las directrices actuales recomiendan una anticoncepción segura en los casos de TEV probada; es posible seguir utilizándola siempre que la paciente siga una anticoagulación totalmente terapéutica.
- Tras un episodio de TEV asociado a hormonas, el riesgo de recurrencia es bajo si se interrumpió la terapia con un fármaco combinado antes de suspender la anticoagulación.
Literatura:
- Rott H: Píldoras anticonceptivas y riesgos trombóticos: Diferencias de los métodos anticonceptivos con y sin estrógenos. Hamostaseología 2019; 39(1): 42-48; doi: 10.1055/s-0039-1677806.
- Tchaikovski SN, Rosing J: Mecanismos del tromboembolismo venoso inducido por estrógenos. Investigación sobre trombosis 2010; 126(1): 5-11; doi: 10.1016/j.thromres.2010.01.045.
- Oger E, Alhenc-Gelas M, Lacut K, et al: Efectos diferenciales de los regímenes de estrógeno/progesterona oral y transdérmica sobre la sensibilidad a la proteína C activada entre las mujeres posmenopáusicas: un ensayo aleatorizado. Arterioscler Thromb Vasc Biol 2003; 23(9): 1671-1676; doi: 10.1161/01.ATV.0000087141.05044.1F.
- Tans G, van Hylckama Vlieg A, Thomassen MCLGD, et al: La resistencia a la proteína C activada determinada con una prueba basada en la generación de trombina predice la trombosis venosa en hombres y mujeres. Br J Haematol 2003; 122(3): 465-470; doi: 10.1046/j.1365-2141.2003.04443.x.
- Tyler ET: Anticoncepción oral y trombosis venosa. JAMA 1963; 185(2): 131; doi: 10.1001/jama.1963.03060020091034.
- Dragoman MV, Tepper NK, Fu R, et al: Revisión sistemática y metaanálisis del riesgo de trombosis venosa entre las usuarias de anticonceptivos orales combinados. Int J Gynaecol Obstet 2018; 141(3): 287-294; doi: 10.1002/ijgo.12455.
- Bastos M de, Stegeman BH, Rosendaal FR, et al: Anticonceptivos orales combinados: trombosis venosa. Cochrane Database Syst Rev 2014; (3): CD010813; doi: 10.1002/14651858.CD010813.pub2.
- Lidegaard O, Nielsen LH, Skovlund CW, et al: Trombosis venosa en usuarias de anticonceptivos hormonales no orales: estudio de seguimiento, Dinamarca 2001-10. BMJ 2012; 344: e2990; doi: 10.1136/bmj.e2990.
- Lidegaard Ø, Nielsen LH, Skovlund CW, et al: Riesgo de tromboembolismo venoso por el uso de anticonceptivos orales que contienen diferentes dosis de progestágenos y estrógenos: estudio de cohortes danés, 2001-9. BMJ 2011; 343: d6423; doi: 10.1136/bmj.d6423.
- Bistervels IM, Scheres LJJ, Hamulyák EN, et al: Sex matters: Practice 5P’s when treating young women with venous thromboembolism. J Thromb Haemost 2019; 17(9): 1417-1429; doi: 10.1111/jth.14549.
- Directriz AWMF S3. Anticoncepción hormonal. Registro AWMF número 015/015.
- van Vlijmen EFW, Wiewel-Verschueren S, Monster TBM, et al: Anticonceptivos orales combinados, trombofilia y riesgo de tromboembolia venosa: revisión sistemática y metaanálisis. J Thromb Haemost 2016; 14(7): 1393-1403; doi: 10.1111/jth.13349.
- Wu O, Robertson L, Langhorne P, et al: Anticonceptivos orales, terapia hormonal sustitutiva, trombofilias y riesgo de tromboembolia venosa: una revisión sistemática. El estudio Trombosis: riesgo y evaluación económica del cribado de la trombofilia (TREATS). Thromb Haemost 2005; 94(1): 17-25; doi: 10.1160/TH04-11-0759.
- Suchon P, Resseguier N, Ibrahim M, et al: Los factores de riesgo comunes se suman a la trombofilia hereditaria para predecir el riesgo de tromboembolia venosa en las familias. TH Open 2019; 3(1): e28-e35; doi: 10.1055/s-0039-1677807.
- Hugon-Rodin J, Horellou MH, Conard, J et al: Tipo de anticonceptivos combinados, mutación del factor V Leiden y riesgo de tromboembolia venosa. Thromb Haemost 2018; 118(5): 922-928; doi: 10.1055/s-0038-1641152.
- Klok FA, Barco S: Gestión óptima de los anticonceptivos hormonales tras un episodio de tromboembolia venosa. Investigación sobre trombosis 2019; 181: S1-S5; doi: 10.1016/S0049-3848(19)30357-3.
- van Hylckama Vlieg A, Helmerhorst FM, Rosendaal FR: El riesgo de trombosis venosa profunda asociado a los anticonceptivos inyectables de acetato de medroxiprogesterona de depósito o a un dispositivo intrauterino de levonorgestrel. Arterioscler Thromb Vasc Biol 2010; 30(11): 2297-2300; doi: 10.1161/ATVBAHA.110.211482.
- Martinelli I, Lensing AWA, Middeldorp S, et al: Tromboembolismo venoso recurrente y hemorragia uterina anormal con el uso de anticoagulantes y terapia hormonal. Sangre 2016; 127(11): 1417-1425; doi: 10.1182/blood-2015-08-665927.
- Kearon C, Ageno W, Cannegieter SC, et al: Categorización de los pacientes como pacientes con tromboembolia venosa provocada o no provocada: orientación del CSE de la ISTH. J Thromb Haemost 2016; 14(7): 1480-1483; doi: 10.1111/jth.13336.
- Douketis J, Tosetto A, Marcucci M, et al. Riesgo de recurrencia tras una tromboembolia venosa en hombres y mujeres: metaanálisis a nivel de paciente. BMJ 2011; 342: d813; doi: 10.1136/bmj.d813.
- Christiansen SC, Lijfering WM, Helmerhorst FM, et al: Diferencia de sexo en el riesgo de trombosis venosa recurrente y el perfil de riesgo de un segundo evento. J Thromb Haemost 2010; 8(10): 2159-2168; doi: 10.1111/j.1538-7836.2010.03994.x.
- Vaillant-Roussel H, Ouchchane L, Dauphin C, et al: Factores de riesgo de recurrencia del tromboembolismo venoso asociados al uso de anticonceptivos orales. Anticoncepción 2011; 84(5): e23-30; doi: 10.1016/j.contraception.2011.06.008.
- Eischer L, Eichinger S, Kyrle PA: El riesgo de recurrencia en mujeres con tromboembolia venosa mientras usan estrógenos: un estudio prospectivo de cohortes. J Thromb Haemost 2014; 12(5): 635-640; doi: 10.1111/jth.12528.
- van Es N, Coppens M, Schulman S, et al: Anticoagulantes orales directos comparados con antagonistas de la vitamina K para el tromboembolismo venoso agudo: pruebas de ensayos de fase 3. Sangre 2014; 124(12): 1968-1975; doi: 10.1182/blood-2014-04-571232.
- Henriksson P, Westerlund E, Wallén H, et al: Incidencia de tromboembolismo pulmonar y venoso en embarazos tras fecundación in vitro: estudio transversal. BMJ 2013; 346: e8632; doi: 10.1136/bmj.e8632.
- Rova K, Passmark H, Lindqvist PG: Tromboembolismo venoso en relación con la fecundación in vitro: un enfoque para determinar la incidencia y el aumento del riesgo en los ciclos con éxito. Fertil Steril 2012; 97(1): 95-100; doi: 10.1016/j.fertnstert.2011.10.038.
- Sennström M, Rova K, Hellgren M, et al: Tromboembolismo y fecundación in vitro: una revisión sistemática. Acta Obstet Gynecol Scand 2017; 96(9): 1045-1052; doi: 10.1111/aogs.13147.
- Bates SM, Greer IA, Middeldorp S, et al: VTE, thrombophilia, antithrombotic therapy, and pregnancy: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141(2 Suppl): e691S-e736S; doi: 10.1378/chest.11-2300.
- Canonico M, Plu-Bureau G, Lowe GDO, et al: Terapia hormonal sustitutiva y riesgo de tromboembolia venosa en mujeres posmenopáusicas: revisión sistemática y metaanálisis. BMJ 2008; 336(7655): 1227-1231; doi: 10.1136/bmj.39555.441944.BE.
- Cushman M, Kuller LH, Prentice R, et al: Estrógeno más progestina y riesgo de trombosis venosa. JAMA 2004; 292(13): 1573-1580; doi: 10.1001/jama.292.13.1573.
- Høibraaten E, Qvigstad E, Arnesen H, et al: Mayor riesgo de tromboembolismo venoso recurrente durante la terapia hormonal sustitutiva – resultados del ensayo aleatorizado, doble ciego y controlado con placebo sobre el estrógeno en el tromboembolismo venoso (EVTET). Thromb Haemost 2000; 84(6): 961-967.
- Roach REJ, Lijfering WM, Helmerhorst FM, et al: El riesgo de trombosis venosa en mujeres mayores de 50 años que utilizan anticonceptivos orales o terapia hormonal posmenopáusica. J Thromb Haemost 2013; 11(1): 124-131; doi: 10.1111/jth.12060.
- Renoux C, Dell’Aniello S, Suissa S: Terapia hormonal sustitutiva y riesgo de tromboembolia venosa: un estudio basado en la población. J Thromb Haemost 2010; 8(5): 979-986; doi: 10.1111/j.1538-7836.2010.03839.x.
- Mannucci PM, Franchini M: Variantes genéticas trombofílicas clásicas. Thromb Haemost 2015; 114(5): 885-889; doi: 10.1160/TH15-02-0141.
- Linnemann B, Hart C: Diagnóstico de laboratorio en la trombofilia. Hamostaseología 2019; 39(1): 49-61; doi: 10.1055/s-0039-1677840.
- www.bfarm.de/DE/Arzneimittel/Pharmakovigilanz/KOK/_node.html; recuperado el: 7.12.2020.
PRÁCTICA GP 2021; 16(1): 8-13