Los nuevos datos de fase III de los ensayos DISCOVER-1 y DISCOVER-2 muestran una mejoría de los síntomas articulares y cutáneos de la artritis psoriásica en la semana 52. Actualmente se está estudiando una ampliación de la indicación del guselkumab. Sería un nuevo avance en las opciones de tratamiento de esta angustiosa enfermedad autoinmune.
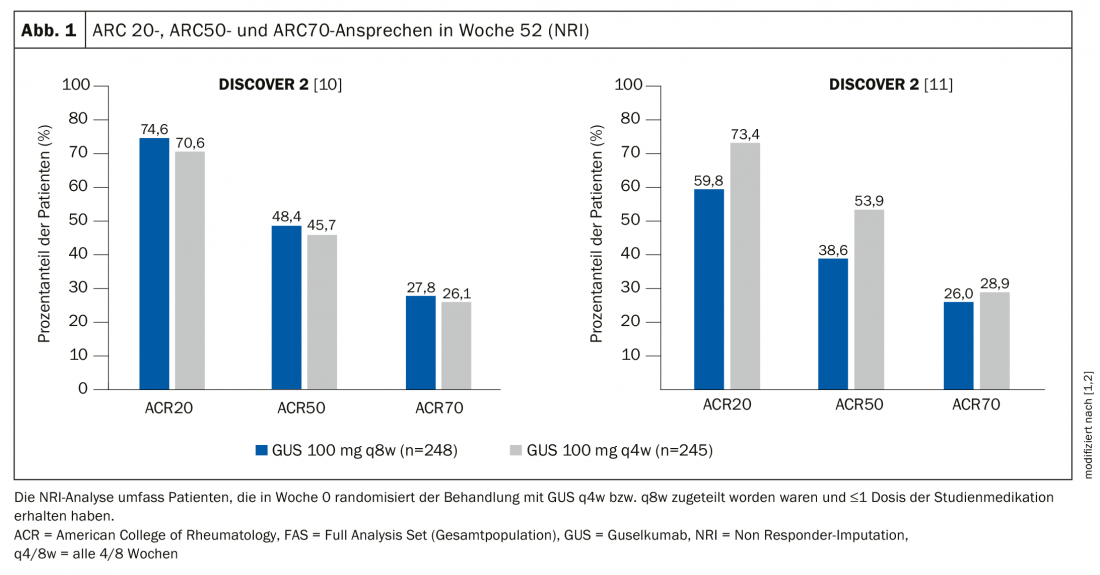
Los datos de los dos estudios del programa DISCOVER constituyeron la base de la solicitud de autorización de comercialización presentada para Tremfya® para el tratamiento de pacientes adultos con APs activa. Alrededor del 75% de los pacientes tratados con Tremfya® lograron una respuesta ACR-20 en los estudios DISCOVER-1 y DISCOVER-2 [1,2]. Estos son los primeros resultados de fase III de un año de duración que investigan la inhibición específica de la IL23p19 en la artritis psoriásica activa. Los datos se presentaron en el E-Congress 2020 de la Liga Europea contra el Reumatismo (EULAR) y se publicaron en The Lancet [3–5]. En los dos ensayos clínicos de fase III, el guselkumab (Tremfya®) en pacientes adultos con artritis psoriásica (APs) activa mostró mejoras en varios criterios de valoración clínicos, como los síntomas articulares y cutáneos, la inflamación de los tejidos blandos, el funcionamiento físico y la reducción de la progresión radiográfica en la semana 52 [1,2]. El Tremfya® no está aprobado actualmente para el tratamiento de la APs y está siendo revisado por Swissmedic para este uso.
| Abreviaturas ACR = Criterio de respuesta ACR MDA = Actividad mínima de la enfermedad DAS-28 = Puntuación de la actividad de la enfermedad 28 VLDA = Muy baja actividad de la enfermedad HAQ-DI = Índice de Discapacidad del Cuestionario de Evaluación de la Salud SF-36 = Cuestionario de la Encuesta de Salud del Formulario Corto 36 PCS = Resumen del componente físico SCM = Resumen del componente mental |
DISCOVER-1 y DISCOVER-2 demuestran su eficacia y seguridad
Los pacientes incluidos en DISCOVER-1 no habían recibido biológicos o habían recibido anteriormente biológicos anti-TNF-α. DISCOVER-2 incluyó únicamente a pacientes sin tratamiento biológico. DISCOVER-2 también investigó la progresión radiológica del daño articular. En ambos ensayos, se aleatorizó a los pacientes durante un año en dos grupos verum, Tremfya® 100 mg cada 4 semanas (q4w) o cada 8 semanas (q8w), y grupos placebo con cruce en la semana 24 a Tremfya® q4w. Los resultados se presentaron en forma de póster en el e-congreso EULAR de este año [1,2]. Los ensayos DISCOVER también mostraron mejoras en varios criterios de valoración secundarios en la semana 52 en comparación con la semana 24, incluida la respuesta ACR70, la resolución de la inflamación de los tejidos blandos (entesitis y dactilitis) [7], la puntuación de la actividad de la enfermedad (DAS-28), la proteína C reactiva (PCR) [4], la actividad mínima de la enfermedad (MDA) [8], la actividad muy baja de la enfermedad (VLDA) [9], la mejora del funcionamiento físico (HAQ-DI) [7], la mejora global de la salud (SF-36*, PCS**, MCS†).
En ambos estudios, el Tremfya® fue bien tolerado hasta el final del estudio, y los acontecimientos adversos observados fueron en general coherentes con los estudios previos del Tremfya® y la información de prescripción actual [6]. Se produjeron efectos adversos graves e infecciones graves en el 4% y el 1% de los pacientes tratados con Tremfya® tanto en DISCOVER-1 como en DISCOVER-2. No se notificaron muertes en pacientes tratados con Tremfya® y ningún paciente tratado con Tremfya presentó enfermedad inflamatoria intestinal, infecciones oportunistas, tuberculosis activa o reacciones anafilácticas o similares a la enfermedad del suero [1,2].
Fuente: Janssen
*/** SF-36 es un cuestionario para pacientes que mide la salud funcional y el bienestar basándose en los informes de los pacientes. Como parte del SF-36, la subescala PCS se compone de cuatro escalas que evalúan la función física, las limitaciones causadas por problemas físicos, los síntomas de dolor somático y la salud general.
† El MCS se compone de cuatro escalas que evalúan la vitalidad, el impacto emocional, el funcionamiento social y la salud mental.
Literatura:
- Ritchlin C, et al: Guselkumab, an IL-23 Inhibitor That Specifically Binds to the IL23p19-Subunit, for Active Psoriatic Arthritis: One Year Results of a Phase 3, Randomized, Double-blind, Placebo-controlled Study of Patients who were Biologic-Naïve or TNFα Inhibitor-Experienced. SAT0397. Presentado en el E-Congress EULAR 2020 del 3 al 6 de junio.
- McInnes I, et al: Eficacia y seguridad de Guselkumab, un anticuerpo monoclonal específico de la subunidad p19 de la interleucina-23, hasta la semana 52 de un estudio de fase 3, aleatorizado, doble ciego y controlado con placebo realizado en pacientes sin tratamiento biológico con artritis psoriásica activa. SAT0402. Presentado en el E-Congress EULAR 2020 del 3 al 6 de junio.
- Business Wire. Janssen pretende ampliar el uso de TREMFYA, www.businesswire.com/news/home/20191022006172/en/Janssen-Seeks-Expand-TREMFYAC2AEE296%BC-guselkumab-Treatment-Adults® (guselkumab) en el tratamiento de adultos con artritis psoriásica activa. última convocatoria 28.07.2020.
- Deodhar A, et al: Guselkumab in Patients with Active Psoriatic Arthritis who were Biologic-naive or had Previously Received TNFα Inhibitor Treatment (DISCOVER-1): a Double-blind, Randomised, Placebo-controlled Phase 3 Trial. The Lancet 2020; 395: 1115-1125.
- Mease PJ, et al: Guselkumab en pacientes sin tratamiento biológico con artritis psoriásica activa (DISCOVER-2): Un ensayo de fase 3 doble ciego, aleatorizado y controlado con placebo. The Lancet 2020; 395: 1126-1136.
- Información técnica de TREMFYA®, a partir de 09/2019 disponible en www.swissmedicinfo.ch
- Clinicaltrials.gov: Estudio de evaluación de la eficacia y seguridad de guselkumab administrado por vía subcutánea en participantes con artritis psoriásica activa, incluidos los tratados previamente con agente(s) biológico(s) antifactor de necrosis tumoral (TNF) alfa (DISCOVER-1). Identificador: NCT03162796. https://clinicaltrials.gov/ct2/show/NCT03162796, último acceso el 28.07.2020.
- Gossec L, et al: Actividad mínima de la enfermedad como objetivo de tratamiento en la artritis psoriásica: una revisión de la literatura. J Rheumatol 2018; 45: 6-13.
- Coates L, et al: Resumen 2548. Presentado en la Reunión Anual ACR/ARHP 2017. Disponible en: https://acrabstracts.org/abstract, último acceso el 28.07.2020.
- McInnes, et al.: Presentado en el EULAR E-Congress, junio de 2020. Póster 0402.
- Ritchlin, et al: Presentado en el EULAR E-Congress, junio de 2020, póster 0397.
PRÁCTICA GP 2020, 15(8): 36-37
PRÁCTICA DERMATOLÓGICA 2020; 30(4): 28-29