En el transcurso de las últimas décadas, la gama de parámetros para el esclarecimiento de las enfermedades neurológicas ha aumentado de forma desproporcionada en comparación con otras áreas de la inmunología. Muchas enfermedades cuya patogenia se desconocía o que habían sido etiquetadas como psiquiátricas son en realidad autoinmunes.
En el transcurso de las últimas décadas, la gama de parámetros para el esclarecimiento de las enfermedades neurológicas ha aumentado de forma desproporcionada en comparación con otras áreas de la inmunología. Muchas enfermedades cuya patogenia se desconocía o que habían sido etiquetadas como psiquiátricas son en realidad autoinmunes. Estos autoanticuerpos se dividen en dos grupos que difieren en términos de patogenia, clínica, asociación tumoral, terapia, pronóstico y diagnóstico [1]. Los anticuerpos uno reconocen antígenos intracelulares, están asociados a síndromes paraneoplásicos y por ello también se denominan anticuerpos onconeuronales. Los otros se dirigen contra dominios extracelulares de receptores o canales. Provocan encefalitis autoinmunes, responden mejor a la inmunoterapia y muestran un mejor pronóstico con una terapia precoz, por lo que es importante un diagnóstico correcto. Los anticuerpos contra la GAD (glutamato descarboxilasa) ocupan una posición intermedia. El antígeno se asienta presinápticamente de forma intracelular en las vesículas sinápticas, pero se libera en la hendidura sináptica durante la transmisión de la señal [2].
Anticuerpos contra antígenos intracelulares
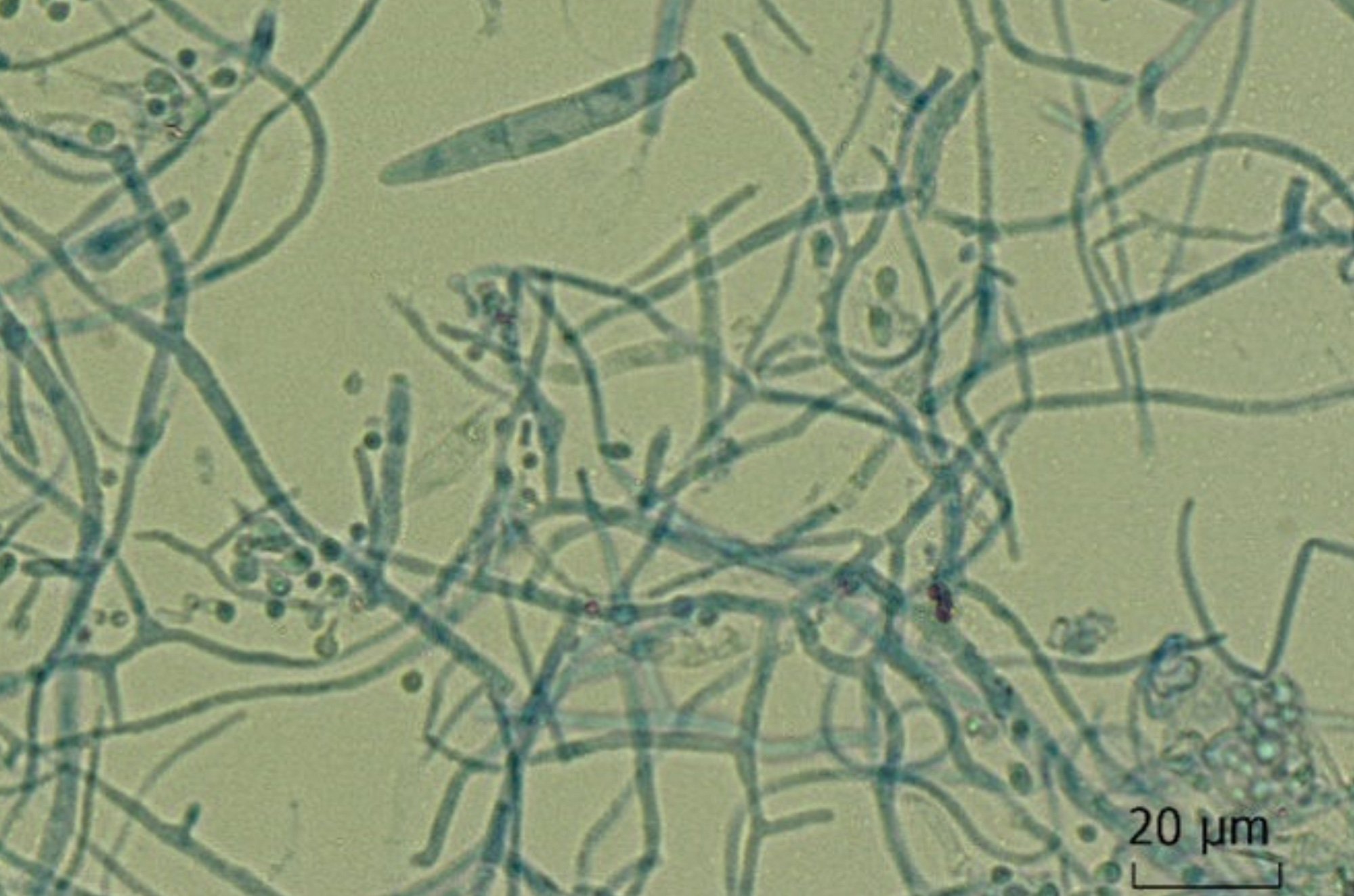
En el contexto de los tumores, pueden aparecer síntomas neurológicos no desencadenados por el propio tumor o la terapia. Si un tumor, por ejemplo un carcinoma bronquial microcítico, que se origina en el neuroectodermo, expresa proteínas neuronales ectópicas [3], el sistema inmunitario activa células T citotóxicas como defensa, lo que puede dañar secundariamente las estructuras neurológicas. En dos tercios de los pacientes, el tumor aún no se conoce cuando aparecen los síntomas neurológicos. Pueden detectarse anticuerpos paraneoplásicos en la sangre, que no son patógenos en sí mismos pero son importantes para el diagnóstico [4]. Por regla general, estos anticuerpos se determinan mediante inmunoblot. El suero es suficiente, las pruebas de LCR no aportan información adicional. Es esencial que el laboratorio vuelva a analizar cada resultado positivo mediante inmunofluorescencia indirecta en tejido cerebral (Fig. 1) [5].
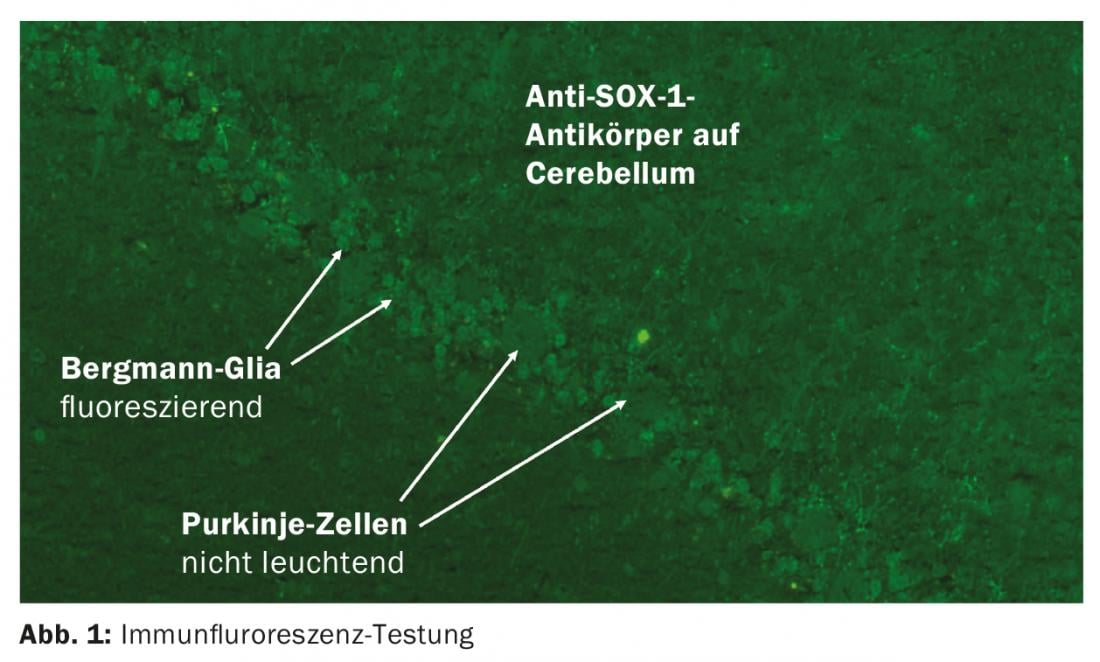
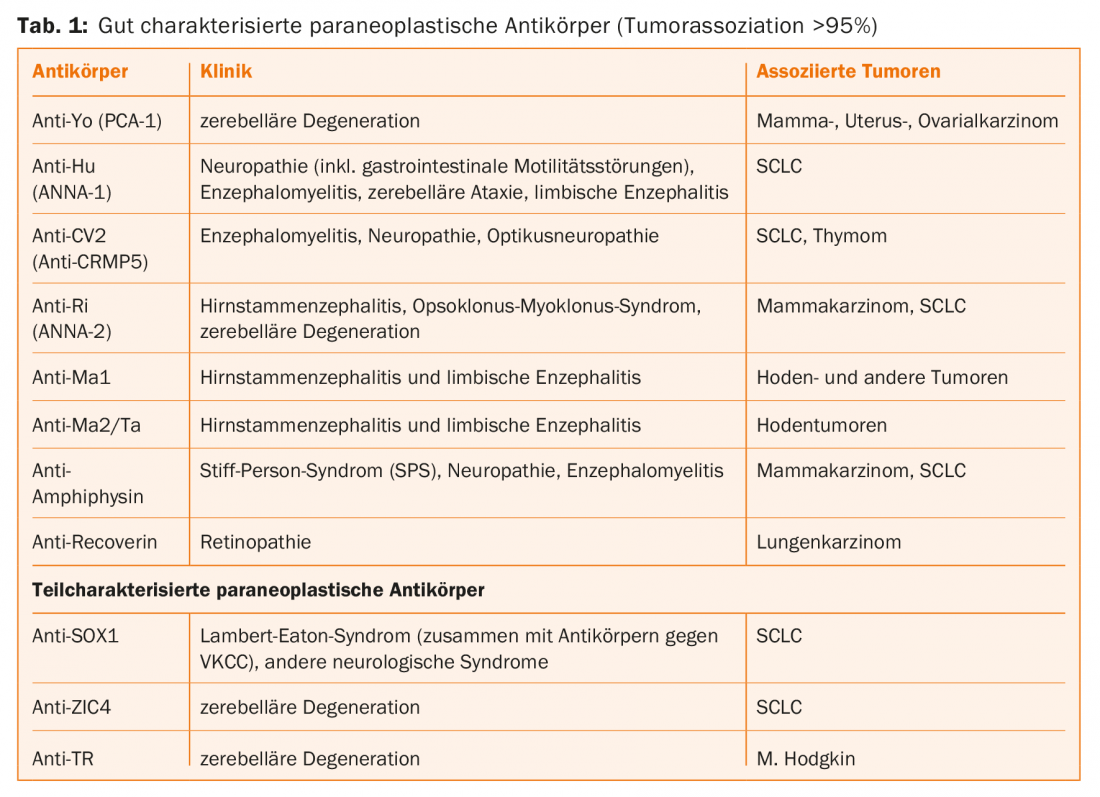
Entre los anticuerpos paraneoplásicos, hay algunos bien caracterizados que se sabe que tienen una malignidad detrás en >95% de los casos. Especialmente en niños, también hay casos sin tumor, por lo que en este grupo de edad se deben buscar estos anticuerpos si hay síntomas correspondientes [6]. En el caso de los anticuerpos paraneoplásicos parcialmente caracterizados, el valor predictivo con respecto a los tumores no está claro debido a la todavía insuficiente base de datos [5]. Los anti-Tr y anti-Sox-1 parecen ser especialmente relevantes como indicación de malignidad. Sin embargo, los anticuerpos paraneoplásicos no pueden detectarse en todos los pacientes, por lo que la detección de anticuerpos no es obligatoria para el diagnóstico. La búsqueda de tumores puede ser más selectiva si se tiene en cuenta el síndrome clínico, los anticuerpos y la información sobre la edad, el sexo y los antecedentes nicotínicos.
La tabla 1 enumera los anticuerpos que se determinan de forma rutinaria. Se enumeran las manifestaciones neurológicas más comunes y las neoplasias malignas asociadas.
Anticuerpos contra antígenos de superficie
Los anticuerpos contra canales y receptores reconocen epítopos complejos en contraste con los epítopos lineales de los anticuerpos intracelulares. Los anticuerpos desencadenan directamente los síntomas de la enfermedad, ya que provocan cambios electrofisiológicos, alteraciones de la transmisión sináptica y de la plasticidad neuronal. Los posibles mecanismos de acción son la reticulación y la internalización de las proteínas. Los pacientes suelen responder bien a la inmunoterapia porque cuando se elimina el anticuerpo, las proteínas pueden retomar su posición en la membrana y realizar su función. El curso suele ser monofásico, pero las recidivas son posibles. Estos anticuerpos tienen muchas menos probabilidades de ser paraneoplásicos. La detección de estos anticuerpos se realiza mediante inmunofluorescencia indirecta en células transfectadas (Fig. 2), para la detección de anticuerpos contra VGCC (canales de calcio activados por voltaje) también mediante RIA (radioinmunoensayo). Los inmunoblots no son adecuados porque desnaturalizan las proteínas, lo que significa que ya no son reconocidas por los anticuerpos. Los cambios inflamatorios en el LCR y la IRM pueden estar ausentes, por lo que el diagnóstico de estas afecciones puede resultar difícil. En la tabla 2 encontrará un resumen de los anticuerpos más importantes.
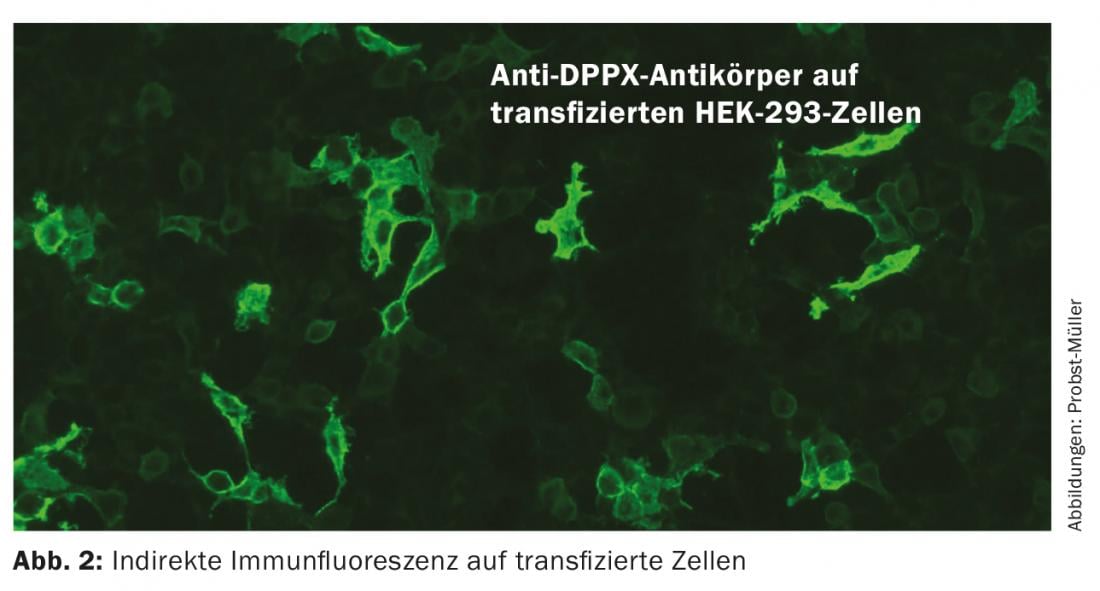
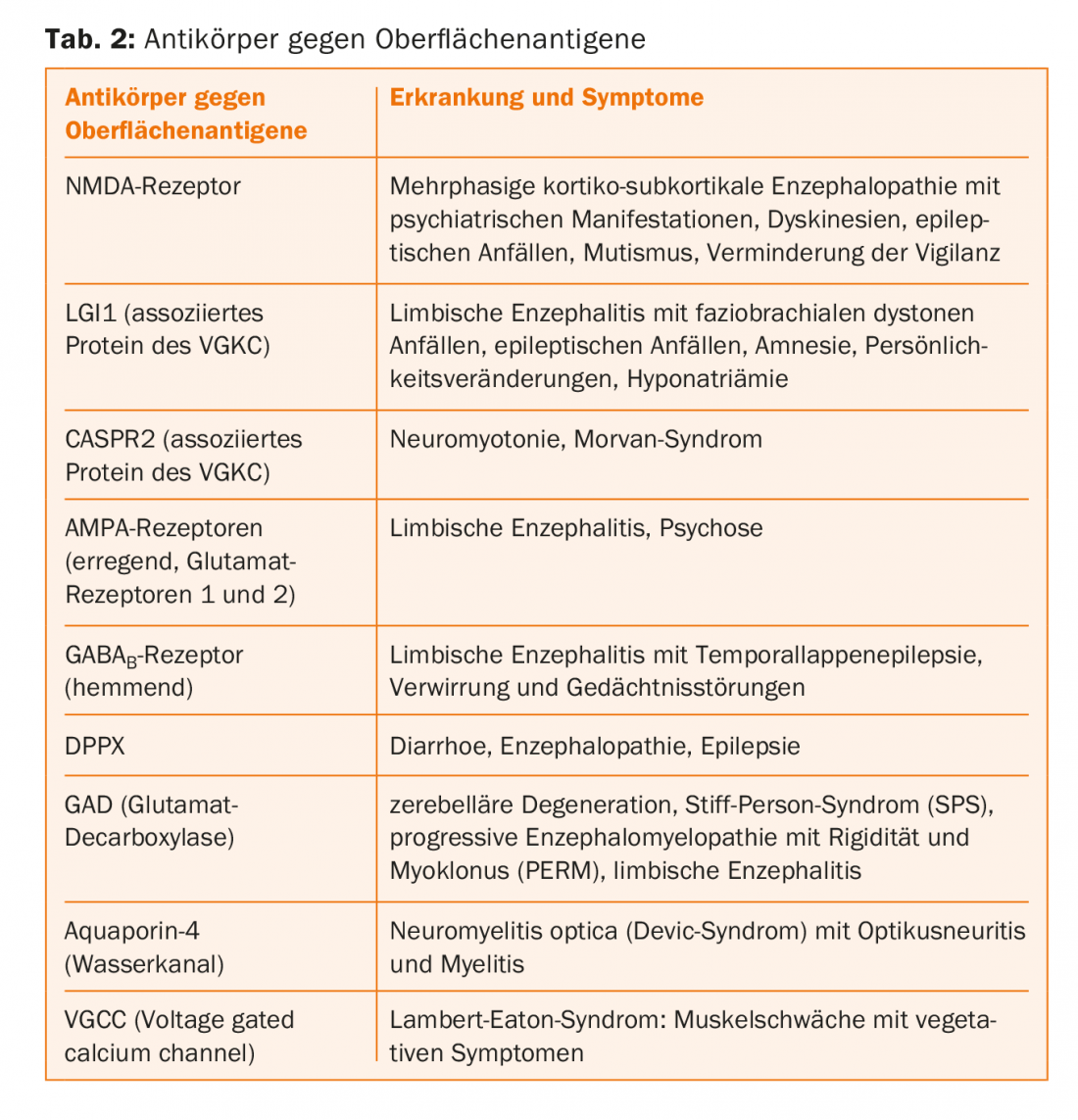
Encefalitis límbica (LE): Los síntomas típicos de la LE son la pérdida de memoria, las anomalías psiquiátricas y los ataques epilépticos. En ausencia de esta última, la afección se consideraba a menudo psiquiátrica en el pasado. El LCR muestra a menudo, pero por desgracia no siempre, cambios inflamatorios: pleocitosis linfocítica, elevación de proteínas, leve alteración de la barrera y posiblemente bandas oligoclonales. Pueden presentarse anomalías mediotemporales en el electroencefalograma e inflamación del hipocampo en la resonancia magnética. Además, los pacientes deben someterse a pruebas de detección de anticuerpos asociados al LE. Lo ideal sería analizar el suero y, si es posible, el líquido cefalorraquídeo. Se ha descrito una gran variedad de anticuerpos en LE (Tab. 2). Otros mamíferos también pueden enfermar. La convulsión que provocó el ahogamiento del oso polar Knut fue desencadenada por anticuerpos del receptor NMDA.
Encefalitis AK por receptores NMDA: Los receptores NMDA son canales iónicos activados por el glutamato. Existen muchos receptores de glutamato diferentes en el sistema nervioso. Son importantes para los impulsos nerviosos excitatorios. El nombre de receptor NMDA proviene del hecho de que este canal es activado por la molécula sintética NMDA. La encefalitis desencadenada por anticuerpos contra el receptor NMDA [7,8] se describió originalmente en mujeres jóvenes o niñas con teratoma de ovario, pero también se ven afectados otros grupos de edad y hombres. En estos pacientes no hay teratomas. Al principio de la enfermedad, los trastornos psiquiátricos ocupan un primer plano, seguidos de las pérdidas cognitivas y los ataques epilépticos. Las alteraciones de la conciencia y la desregulación autonómica pueden conducir al ingreso en la unidad de cuidados intensivos. En la mayoría de los casos, la detección de anticuerpos a partir del suero es suficiente. En raras ocasiones, sólo el LCR es positivo, por lo que en casos de fuerte sospecha, debe examinarse también el LCR.
Encefalitis causada por anticuerpos contra LGI1 y CASPR2: Los canales de potasio activados por voltaje (VGKC) existen en todo el cerebro. Sirven para restablecer el potencial de membrana durante la hiperpolarización. Mediante RIA, se pueden encontrar anticuerpos contra las VGKC en pacientes con neuromiotonía y encefalitis límbica. Hoy sabemos que los anticuerpos no se dirigen directamente contra la VGKC, sino contra dos proteínas asociadas, contra la LGI1 y la CASPR2 [9]. Los pacientes con estos anticuerpos son predominantemente varones. Sufren principalmente encefalitis límbica con síntomas extralímbicos como neuromiotonía con espasmos musculares dolorosos, trastornos del movimiento, trastornos del sueño e hiponatremia sérica. Dependiendo del anticuerpo, estos síntomas aparecen con una frecuencia variable. Las crisis distónicas faciobraquiales sólo se producen en pacientes LGI1 positivos. Se trata de convulsiones unilaterales con muecas y distonía del brazo ipsilateral que duran menos de tres segundos pero que pueden producirse hasta cientos de veces al día. Estas convulsiones se desencadenan por movimientos, emociones y ruidos fuertes. Dado que estas convulsiones se producen antes de que se desarrolle la encefalitis límbica con déficit cognitivo, permiten un diagnóstico y una terapia precoces. La disautonomía es peligrosa y puede provocar, entre otras cosas, bradicardia y muerte súbita cardiaca. Esto afecta principalmente a los pacientes CASPR2-positivos.
Los pacientes doblemente negativos son aquellos que tienen anticuerpos contra el VGKC pero son negativos para los anticuerpos contra el LGI1 y el CASPR2. Estudios recientes demuestran que estos anticuerpos se unen a partes intracelulares del VGKC o a la dendrotoxina del veneno de serpiente utilizada en la RIA, y no son patógenos. Se encuentran en personas sanas o en pacientes con enfermedades no autoinmunes como la enfermedad de Alzheimer o la enfermedad de Parkinson. Además, son detectables en trabajadores sanos de mataderos expuestos a aerosoles procedentes de cerebros de animales. Estos datos demuestran que probablemente baste con determinar únicamente los anticuerpos contra LGI1 y CASPR2, pero no los anticuerpos contra el complejo VGKC.
Anti-GAD
La enzima glutamato descarboxilasa (GAD) convierte en un solo paso el glutamato, el neurotransmisor activador más importante, en ácido γ-aminobutírico (GABA), el neurotransmisor inhibidor más importante. La enzima se encuentra en el sistema nervioso y en el páncreas. Aunque el TAG es una molécula intracelular, se libera cuando se descargan las vesículas sinápticas del cerebro y puede ser reconocido por los autoanticuerpos. Los autoanticuerpos contra el TAG se dan, por un lado, en la diabetes mellitus tipo I y, por otro, en las enfermedades neurológicas [10]. En la diabetes mellitus, los títulos son bajos. En las enfermedades neurológicas, los títulos son muy elevados. Las enfermedades asociadas son la ataxia cerebelosa, la encefalitis límbica y el síndrome de la persona rígida (SPS). El SPS es una enfermedad rara que puede ser espontánea o paraneoplásica. Una característica típica es un aumento del tono muscular que se incrementa con los años. Se producen calambres espontáneos o desencadenados. Dado que estos espasmos también se desencadenan por las emociones, los sonidos, el tacto, etc., la afección suele descartarse inicialmente como psiquiátrica. En el electromiograma se encuentra una actividad permanente, incluso cuando el paciente intenta relajarse. Si se detectan anticuerpos contra el TAG, el SPS no suele ser paraneoplásico. La detección de anticuerpos contra la anfifisina (Tab. 1 ) afecta a mujeres con carcinoma de mama.
Outlook
Los anticuerpos presentados aquí son sólo los más importantes. Sin duda, en los próximos años se añadirán más anticuerpos. Es importante recordar esto en los pacientes con síntomas neurológicos poco claros para que el diagnóstico se haga precozmente y se pueda ofrecer al paciente la mejor terapia posible.
Mensajes para llevarse a casa
- En los últimos años se ha descrito un gran número de anticuerpos relevantes para el diagnóstico y el pronóstico que desencadenan enfermedades inmunomediadas del sistema nervioso central y periférico.
- Los antígenos diana de los anticuerpos se clasifican según su localización en membranosos e intracelulares.
- Los anticuerpos contra antígenos intracelulares como Hu, Ri, Yo, CV2, SOX-1 también se denominan onconeuronales, ya que suelen aparecer en el contexto de neoplasias malignas. Debe buscarse un tumor. La inmunoterapia sólo es muy prometedora hasta cierto punto.
- Los anticuerpos contra antígenos de membrana como receptores y canales, por ejemplo los receptores NMDA o los canales de potasio, desencadenan directamente los síntomas y provocan encefalitis autoinmunes. Los pacientes suelen responder bien a la inmunoterapia.
Literatura:
- Rachel L, et al: Pruebas de autoanticuerpos en las encefalopatías. Neurología práctica 2012; 12: 4-13.
- Bost C, et al: Encefalitis autoinmune en instituciones psiquiátricas: perspectivas actuales. Enfermedades neuropsiquiátricas y tratamiento 2016; 12: 2775-2787
- Onganer PU, et al: Características neuronales del cáncer de pulmón microcítico. British Journal of Cancer; 93: 1197-1201.
- Dalmau JO, et al: Síndromes paraneoplásicos. Arch Neurol 1999; 56: 405-408.
- www.dgn.org/leitlinien/2383-ll-79-2012-paraneoplastische-neurologische-syndrome
- Honnorat J, et al: Encefalopatía límbica autoinmune y anticuerpos anti-Hu en niños sin cáncer. Neurología 2013; 80(24): 2226-2232.
- Gresa-Arribas N, et al: Títulos de anticuerpos en el momento del diagnóstico y durante el seguimiento de la encefalitis por receptores anti-NMDA: un estudio retrospectivo. Lancet Neurol 2014; 13(2): 167-177.
- Dalmau J, et al: Encefalitis por receptores anti-NMDA: serie de casos y análisis de los efectos de los anticuerpos. Lancet Neurol 2008; 7(12): 1091-1098.
- Binks NM, et al: LGI1, CASPR2 y anticuerpos relacionados: una evolución molecular de los fenotipos. J Neurol Neurosurg Psychiatry 2017; 0: 1-9.
- Saiz A, et al.: Espectro de síndromes neurológicos asociados a anticuerpos antiácido glutámico descarboxilasa: claves diagnósticas de esta asociación. Cerebro 2008; 131: 2553-2563.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2018; 16(2): 4-8.