La depleción de células B y los resultados del estudio ORATORIO publicados recientemente en el New England Journal of Medicine también estuvieron en boca de todos en el ACTRIMS Forum 2017. Entre otras cosas, porque el proceso de aprobación en EE.UU. está actualmente en pleno apogeo. Ahora se trata de clasificar los datos y examinar su relevancia clínica. En el congreso se retomaron algunas conclusiones interesantes al respecto. ¿Dónde encajará el nuevo anticuerpo -y, por tanto, la primera terapia dirigida a las células B para la EM- en el espectro terapéutico?
Incluso en las pasadas conferencias ECTRIMS, fue difícil evitar el tema del agotamiento de las células B en la EM, tan prominentemente se discutió. Mientras tanto, se ha publicado en NEJM [1] ORATORIO, un ensayo de fase III que prueba el anticuerpo ocrelizumab en la esclerosis múltiple (EM) primaria progresiva. En este estudio, el anticuerpo, que se dirige de forma selectiva y específica a los linfocitos B CD20 positivos, mostró una reducción significativa del riesgo del 24% (32,9% frente a 39,3%) en el criterio de valoración primario definido como la progresión de la discapacidad durante un periodo de doce semanas (es decir, aumento en la Escala Expandida del Estado de Discapacidad, EDSS) en un total de 732 pacientes aleatorizados en comparación con placebo. 39,3%) en criterios de valoración secundarios como la progresión en un periodo de 24 semanas, una reducción significativa del riesgo del 25% (29,6% frente a 35,7%), un deterioro menos grave en la marcha cronometrada de 25 pies (T25-FW) del 38,9% a las 120 semanas (frente al 55,1% con placebo) y una disminución menor del volumen cerebral.
La tolerancia se evaluó como provisionalmente buena, al igual que en los estudios paralelos con curso remitente-recurrente. Con el anticuerpo administrado por vía intravenosa se produjeron más reacciones asociadas a la infusión, infecciones del tracto respiratorio superior y herpes oral, pero no hubo diferencias clínicamente significativas en las tasas de acontecimientos adversos graves e infecciones. Se encontraron tumores en el 2,3% (ocrelizumab) y el 0,8% (placebo) de los participantes.
Clasificación de los resultados
También se acordó en el Foro ACTRIMS 2017 que los resultados son de gran relevancia para los pacientes con EM primaria progresiva, ya que el anticuerpo CD20 es la primera sustancia que fue capaz de frenar esta forma de EM en un ensayo de fase III. La EM primaria progresiva se caracteriza por una acumulación constante de discapacidad desde el inicio de la enfermedad (con/sin mesetas temporales en la progresión). Por tanto, ralentizar la progresión de la discapacidad es un objetivo terapéutico importante en este caso, que apenas se ha logrado en los ensayos clínicos hasta la fecha [2–4]. Esto debería cambiar ahora con el ocrelizumab. Además, el compuesto se está investigando en otros dos ensayos de fase III en EM remitente-recidivante (OPERA) [5], en los que se consiguió un efecto significativamente más favorable que con el tratamiento con dosis altas de interferón. Ahora se trata de esperar a los datos a largo plazo, que serán relevantes tanto en términos de eficacia como de seguridad.
Lo realmente nuevo del ocrelizumab es el enfoque terapéutico. En lugar de dirigirse a las células T responsables de atacar las vainas de mielina de los nervios del sistema nervioso central, como hacen la mayoría de los fármacos para la EM, el anticuerpo se une a las proteínas de superficie CD20 expresadas en determinadas células B (más concretamente, células B precursoras hasta el estadio de plasmoblasto, pero ni células B troncales/pro-B ni células plasmáticas, preservando así importantes funciones del sistema inmunitario).
El papel de las células B ha sido subestimado durante mucho tiempo en la investigación. Sin embargo, las células B que migran al SNC tienen el potencial de influir fundamentalmente en la fisiopatología de la EM a través de varios mecanismos. Sus funciones incluyen la producción de citoquinas y autoanticuerpos, así como la presentación/coestimulación de antígenos, todo lo cual podría contribuir directa o indirectamente al daño de la vaina de mielina o del axón y, por tanto, a la discapacidad de los pacientes con EM.
El impulso para desarrollar el ocrelizumab vino precedido por el descubrimiento de que el rituximab, que también destruye selectivamente las células B, puede lograr resultados sorprendentes en la EM. Incluso en el caso de la forma primaria progresiva, que apenas se ha tratado eficazmente hasta ahora, se consigue ralentizar la progresión, al menos en los pacientes más jóvenes y en los que presentan lesiones enriquecidas con gadolinio [3]. El desarrollo de un anticuerpo anti-CD20 más nuevo, esta vez totalmente humanizado (el rituximab es un anticuerpo quimérico ratón/humano), promete una mejor tolerabilidad. La decisión de no seguir invirtiendo en el “viejo representante” rituximab, sino de impulsar el ocrelizumab en su lugar, también puede estar relacionada, por supuesto, con la expiración de la protección de la patente del rituximab.
En consonancia con los resultados del rituximab, los participantes en el estudio ORATORIO eran más jóvenes o mayores. padecen EM desde hace menos de 10 ó 15 años (según el grado de discapacidad). Por tanto, la población estaba “enriquecida”, como se diría en inglés, lo que puede haber favorecido aún más los resultados positivos. Queda por ver si esta selección se refleja en el texto de admisión. Lo que es seguro es que el ocrelizumab es un agente potente, lo que resulta más evidente en su actividad antiinflamatoria.
NEP – un criterio de valoración clínicamente relevante
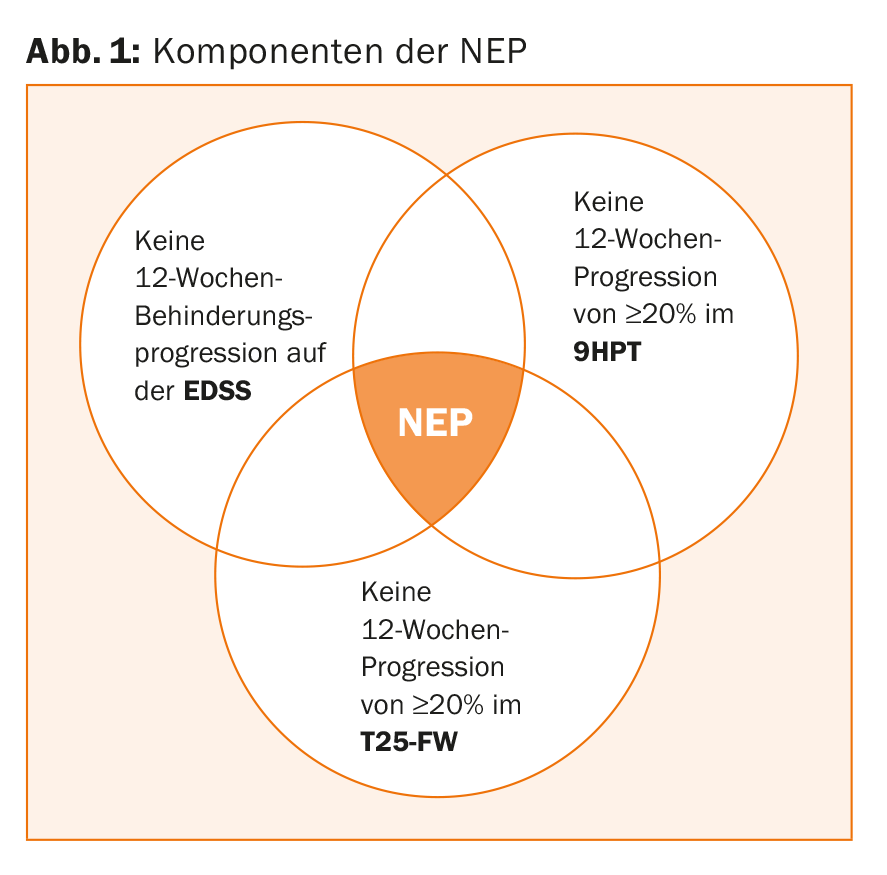
Ahora, en un nuevo análisis del estudio ORATORIO presentado en el Foro ACTRIMS 2017, los investigadores se preguntaron hasta qué punto la progresión de la discapacidad se refleja en la denominada “ausencia de evidencia de progresión” (NEP). La NEP es un criterio de valoración compuesto clínicamente relevante que, además de la EDSS, también incluye otras medidas importantes de discapacidad, a saber, la denominada prueba de la clavija de nueve agujeros (9HPT) y la T25-FW. Éstas proporcionan información sobre si la enfermedad se ha estabilizado realmente desde el punto de vista clínico. El 9HPT prueba cuánto tiempo tarda el paciente en colocar nueve alfileres en los orificios designados y volver a retirarlos. Esta prueba ofrece una buena sensibilidad para evaluar la destreza manual en personas con EM. En el T25-FW, se pide al paciente que camine 25 pies de la forma más rápida y segura posible. El tiempo se detiene en el proceso. Concretamente, el punto final NEP requerido (Fig. 1):
- Sin progresión de la discapacidad en la EDSS
- Sin progresión de ≥20% en las extremidades superiores (9HPT)
- Sin progresión de ≥20% en curso (T25-FW).
Para el análisis exploratorio, los investigadores pudieron evaluar los datos de 691 del total de 732 pacientes, en el periodo comprendido entre el inicio y las 120 semanas. El resultado fue un aumento relativo de la probabilidad de no experimentar progresión de la discapacidad en ninguna de las tres pruebas del 47% con ocrelizumab (RR 1,47; IC 95%: 1,17-1,84; p=0,0006). En concreto, el 42,7% del grupo de ocrelizumab pero sólo el 29,1% del grupo de placebo lograron la NEP. Incluso cuando se diseccionó el criterio de valoración compuesto, los beneficios del anticuerpo anti-CD20 siguieron siendo sorprendentes (Tabla 1).

El beneficio del ocrelizumab en la NEP complementa de forma consistente los resultados de los criterios de valoración primarios y secundarios de ORATORIO. El cuadro general es de ralentización de la discapacidad tanto en las extremidades superiores como en las inferiores. Para los pacientes con EM primaria progresiva, se trata de una buena noticia (largamente esperada). Los resultados en la EM remitente-recurrente de los ensayos OPERA también son prometedores. Queda por ver cuál será el texto final de la autorización. La FDA tomará su decisión a finales de marzo, es decir, en estos días. Mientras tanto, el fármaco seguirá siendo sin duda un tema de conversación en los congresos sobre la EM.
Fuente: Foro del Comité de las Américas para el Tratamiento y la Investigación de la Esclerosis Múltiple (ACTRIMS), 23-25 de febrero de 2017, Orlando
Literatura:
- Montalban X, et al: Ocrelizumab frente a placebo en la esclerosis múltiple primaria progresiva. N Engl J Med 2017; 376: 209-220.
- Wolinsky JS, et al: Glatiramer acetate in primary progressive multiple sclerosis: results of a multinational, multicenter, double-blind, placebo-controlled trial. Ann Neurol 2007; 61: 14-24.
- Hawker K, et al: Rituximab en pacientes con esclerosis múltiple primaria progresiva: resultados de un ensayo multicéntrico aleatorizado doble ciego controlado con placebo. Ann Neurol 2009; 66: 460-471.
- Lublin F, et al: Fingolimod oral en la esclerosis múltiple primaria progresiva (INFORMS): un ensayo de fase 3, aleatorizado, doble ciego y controlado con placebo. Lancet 2016; 387: 1075-1084.
- Hauser SL, et al: Ocrelizumab frente a interferón beta-1a en la esclerosis múltiple recidivante. N Engl J Med 2017; 376: 221-234.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2017; 15(2): 33-36