La enfermedad arterial periférica (EAP) es la manifestación de una enfermedad que a menudo es juzgada erróneamente en su importancia por los pacientes, pero también por los médicos. Aunque la prevalencia global se sitúa entre el 3 y el 10%, ya ronda el 20% en los pacientes >70 años [1]. Inicialmente, sólo es ligeramente sintomático, pero el dolor que se produce durante el esfuerzo conduce gradualmente a una restricción de la actividad física, lo que se traduce en una reducción de la calidad de vida [2]. El pronóstico de los pacientes afectados está significativamente limitado por la manifestación de la enfermedad en otros órganos. La rehabilitación multimodal es el único concepto terapéutico que va más allá del tratamiento de los síntomas locales y mejora el pronóstico de los pacientes a largo plazo.
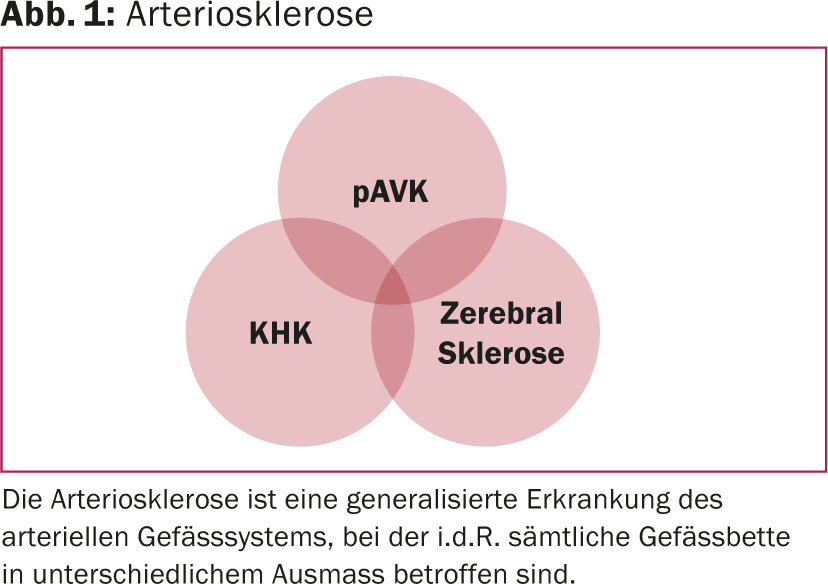
La enfermedad arterial periférica (EAP) es la manifestación de una enfermedad vascular sistémica que puede afectar por igual a todas las zonas de los vasos arteriales. Además de las arterias de las piernas, suelen verse afectadas las arterias renales, las arterias coronarias y las arterias que irrigan el cerebro. Aunque los síntomas de la PAOD puedan reducirse localmente con diversas estrategias de tratamiento, la enfermedad sistémica permanece – y progresa. En última instancia, el pronóstico de los pacientes afectados viene determinado de forma decisiva por la manifestación de la enfermedad en otros órganos: concretamente en las coronarias o en las arterias que suministran sangre al cerebro. El riesgo de complicaciones cardiovasculares es mayor en los pacientes con PAOD que tras un infarto de miocardio (Fig. 1).
Por ello, cuando se trata a pacientes con PAOD, es especialmente importante frenar la progresión de la enfermedad subyacente además de los síntomas manifiestos. En consecuencia, el concepto de tratamiento comprende dos enfoques (Fig. 2):
- Tratamiento local de la PAOD con el objetivo de aliviar los síntomas o ampliar la distancia de marcha.
- El tratamiento de la enfermedad subyacente con el objetivo de mejorar la mortalidad reduciendo las complicaciones cardiovasculares. El tratamiento de los factores de riesgo vascular es especialmente importante.

Directrices
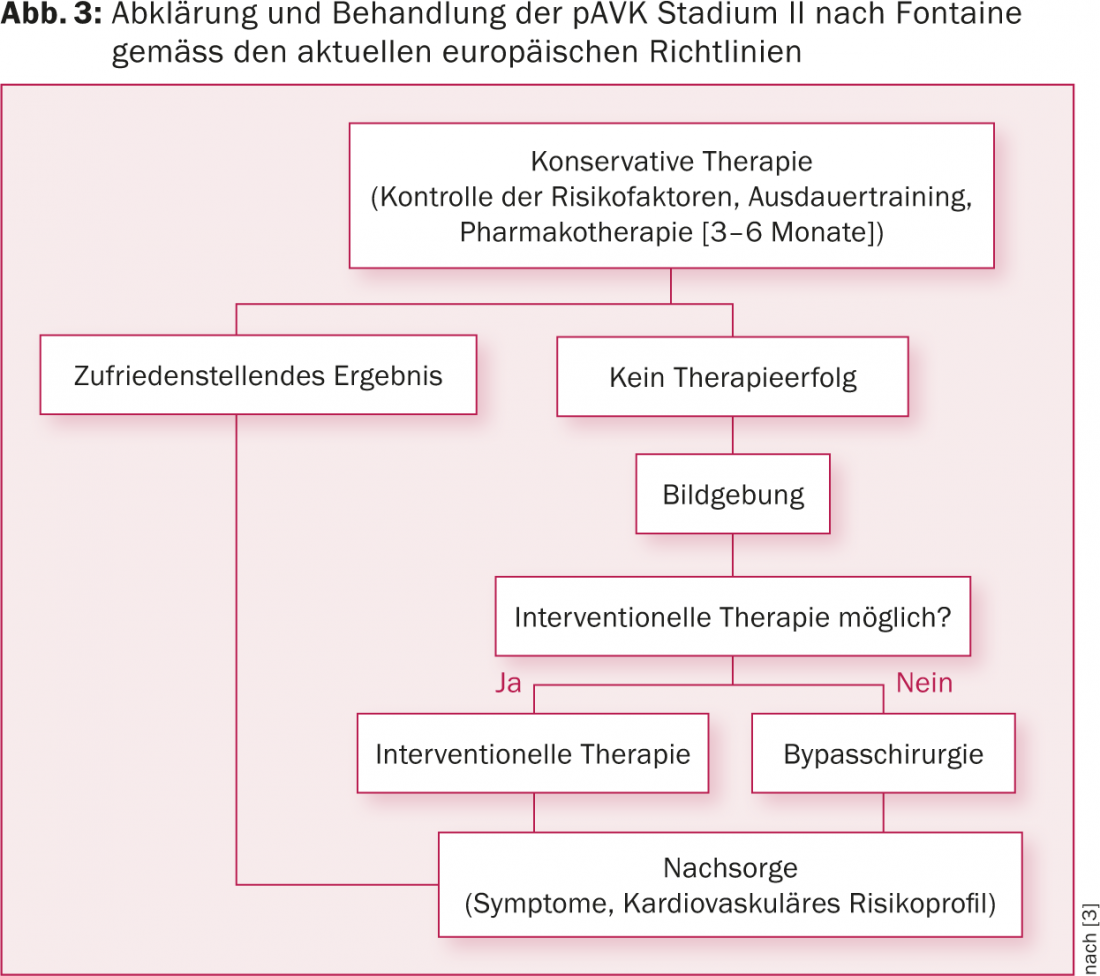
Según las directrices actuales, se recomienda un enfoque multimodal para los pacientes con PAOD [3]. Esto incluye optimizar los factores de riesgo vascular además de la terapia farmacológica. En la FAVK asintomática (estadio I según Fontaine) o la claudicación intermitente (estadio II según Fontaine), puede adoptarse un enfoque conservador durante tres a seis meses. A diferencia de la formación independiente, la formación supervisada recibe una recomendación de AI [3]. Sólo si esto no mejora los síntomas se recomienda un procedimiento intervencionista o quirúrgico (Fig. 3).
Opciones terapéuticas
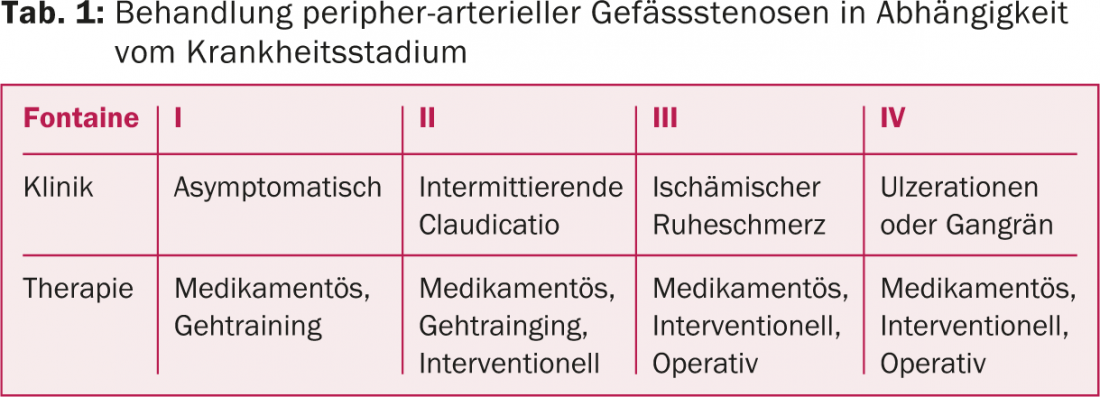
Para tratar las estenosis periféricas, están indicados el entrenamiento de la marcha y las terapias intervencionistas o quirúrgicas en función del estadio de la enfermedad (tabla 1).
En muchos casos, la EAP en estadio I y II de Fontaine puede tratarse de forma conservadora. A partir de la fase II, se utilizan procedimientos intervencionistas adicionales. A partir de los estadios III y IV, un enfoque intervencionista o quirúrgico suele ser el tratamiento de elección.
A continuación, se analizarán las opciones de tratamiento conservador para los pacientes con PAOD.
Tratamiento farmacológico
La inhibición de la agregación plaquetaria para mejorar la reología y la terapia con estatinas son estándar en pacientes con PAOD. Las estatinas tienen propiedades pleomórficas más allá de su efecto reductor del colesterol, que tienen un impacto positivo en la progresión de la PAOD. Además de una reducción significativa de los accidentes cerebrovasculares, las estatinas también provocaron un aumento de la distancia recorrida a pie en comparación con el placebo [4].
Entrenamiento de marcha
Las posibilidades terapéuticas del entrenamiento (de la marcha), que puede llevarse a cabo hasta la fase II, sólo son conocidas por unos pocos. Varios estudios han demostrado que un programa de ejercicio estructurado en pacientes con PAOD en estadios I y II es equivalente a la terapia intervencionista en cuanto al aumento de la distancia recorrida sin dolor y absoluta [5]. Además, los pacientes con un enfoque terapéutico basado en el ejercicio para tratar la PAOD requieren menos procedimientos invasivos en general [5], es una terapia rentable [6] (Fig. 4).
El entrenamiento provoca una mejora de la función endotelial y de la capilarización, así como un mejor agotamiento del O2 en la periferia [7]. No se ha podido demostrar en los estudios un aumento de la colateralización. La mejora de la perfusión conduce además a una economización de las secuencias de movimiento y a una remodelación de la musculatura, lo que se traduce en una mejora adicional del rendimiento. Es interesante que pueda demostrarse una mejora de la distancia recorrida sin dolor con diferentes formas de entrenamiento [8]. Además del entrenamiento de carrera, también se pudieron demostrar efectos positivos para el entrenamiento ergométrico o de fuerza, y el entrenamiento de la parte superior del brazo también fue eficaz [9]. Los pacientes que sólo pueden participar de forma limitada en el entrenamiento de la marcha pueden así utilizar formas alternativas de entrenamiento para mejorar su estado y ampliar su distancia de marcha. Este tipo de entrenamiento alternativo también puede considerarse en el estadio III según Fontaine, mientras que el entrenamiento basado en el movimiento está contraindicado en el estadio IV. Cabe esperar efectos positivos del entrenamiento especialmente en pacientes con lesiones proximales en los que aún pueden medirse buenas presiones de cierre del tobillo (óptimo >80 mmHg). Un largo historial médico o una enfermedad concomitante limitante, ambos factores que restringen el entrenamiento físico, tienen un efecto desfavorable en el éxito del entrenamiento.

Mejora del perfil de riesgo cardiovascular
La mejora del pronóstico de los pacientes con PAOD sólo se consigue mejorando el perfil de riesgo cardiovascular [7]. El factor de riesgo más importante, pero también el más difícil de controlar, es el tabaquismo. El consumo de cigarrillos provoca una progresión más rápida de la PAOD, un aumento de las amputaciones y un incremento significativo de la mortalidad cardiovascular [10]. La hipertensión, la hipercolesterolemia, la obesidad y la diabetes son otros factores de riesgo con impacto en el pronóstico [11]. Un ajuste óptimo de la presión arterial puede reducir los eventos cardiovasculares. En general, se persiguen valores de tensión arterial <140/90 mmHg – se ha levantado la contraindicación para los betabloqueantes que existía a partir de la fase III. En los diabéticos, debe alcanzarse siempre una HbA1c inferior a 6,5 y aspirarse a valores de tensión arterial inferiores a 130/85 mmHg para [12]. Bajo tratamiento con estatinas, el valor objetivo para el colesterol LDL es <1,8 mmol/l.
Terapia integral a través de la rehabilitación PAVK – ¿El mejor tratamiento médico?
Un programa de rehabilitación ambulatoria específico para la PAOD (Tabla 2 ) es actualmente la única opción para el tratamiento integral de los pacientes. Los costes de este programa de rehabilitación ambulatoria de doce semanas están cubiertos por los fondos del seguro de enfermedad. La combinación de un entrenamiento supervisado y guiado por profesionales junto con la modificación de los factores de riesgo y la optimización del tratamiento farmacológico mediante un estrecho seguimiento por parte de los médicos y los servicios asociados permite una mejora de los síntomas y del pronóstico [13]. La continuidad de los cuidados ofrece a los pacientes apoyo para realizar los cambios de comportamiento necesarios.
En general, se puede conseguir un aumento de la distancia recorrida andando del 50-200% mediante el entrenamiento. Para lograr un éxito óptimo (es decir, una mejora en la distancia caminada), debe realizarse un entrenamiento adecuado al menos tres veces por semana durante 30 minutos durante un periodo de al menos tres meses [14]. El entrenamiento supervisado es superior al entrenamiento independiente [15,16].
Como parte de un programa de rehabilitación, se motiva a los pacientes para que realicen una actividad física regular y, en particular, para que aprendan a caminar de forma adecuada y eficaz. El programa de formación suele incluir diferentes formas de entrenamiento para dirigirse al mayor número posible de pacientes y motivarles para que integren la actividad física en su vida diaria. Así, el entrenamiento de carrera a pie se lleva a cabo en alternancia con otras formas de entrenamiento. Se pide a los pacientes que corran a una intensidad predeterminada hasta la aparición del dolor, tras lo cual se toma un descanso hasta que el dolor se haya recuperado. El concepto de entrenamiento en el rango del dolor se abandonó debido al menor cumplimiento por parte del paciente. Además, no se pudo demostrar con certeza el beneficio adicional de dicho entrenamiento “en la zona de isquemia”.
Para tratar los factores de riesgo secundarios de la mejor manera posible, se evalúan de forma estándar los antecedentes de tabaquismo y la voluntad de dejar de fumar mediante un asesoramiento especializado para dejar de fumar. Si existe el deseo de dejar de fumar, se lleva a cabo una terapia conductual con el apoyo de medicación si es necesario. La disponibilidad de estos servicios en los programas de rehabilitación facilita el acceso de los pacientes; la estrecha supervisión durante el programa de rehabilitación aumenta las posibilidades de éxito. Las charlas de acompañamiento y el asesoramiento nutricional exhaustivo apoyan un cambio de comportamiento autorresponsable, que a largo plazo consigue una mejora del perfil de riesgo y del pronóstico. Con el apoyo de un psicólogo, a menudo es más posible modificar los factores psicosociales que afectan al cumplimiento y al éxito de la terapia a largo plazo.

Resumen
Los programas de rehabilitación estructurados para pacientes con PAOD aplican el concepto de terapia multimodal recomendado en las directrices. Los pacientes aprenden un entrenamiento estructurado y eficaz y mejoran su perfil de riesgo cardiovascular, lo que explica los resultados positivos a largo plazo con una tasa de intervención global más baja. La rehabilitación multimodal es el único concepto terapéutico que va más allá del tratamiento de los síntomas locales a largo plazo y, por tanto, también mejora el pronóstico de los pacientes. Los costes del programa están cubiertos por las compañías de seguros de enfermedad de acuerdo con la Ordenanza de Prestaciones Sanitarias de Suiza.
Literatura:
- Selvin E, Erlinger TP: Prevalencia y factores de riesgo de la enfermedad arterial periférica en Estados Unidos: resultados de la Encuesta Nacional de Examen de Salud y Nutrición, 1999-2000. Circulation 2004; 110(6): 738-743. Epub 2004/07/21.
- Spronk S, et al: Impacto de la claudicación y su tratamiento en la calidad de vida. Seminarios de cirugía vascular 2007; 20(1): 3-9. Epub 2007/03/28.
- Tendera M, et al.: ESC Guidelines on the diagnosis and treatment of peripheral artery diseases: Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries: the Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology (ESC). Revista europea del corazón 2011; 32(22): 2851-2906. Epub 30/08/2011.
- Mohler ER, Hiatt WR, Creager MA: La reducción del colesterol con atorvastatina mejora la distancia caminada en pacientes con enfermedad arterial periférica. Circulation 2003; 108(12): 1481-1486. Epub 2003/09/04.
- Fakhry F, et al: Eficacia clínica a largo plazo de la terapia de ejercicio supervisada frente a la revascularización endovascular para la claudicación intermitente a partir de un ensayo clínico aleatorizado. The British journal of surgery 2013; 100(9): 1164-1171. Epub 2013/07/12.
- Spronk S, et al.: Rentabilidad de las nuevas estrategias de rehabilitación cardiaca y vascular para pacientes con enfermedad arterial coronaria. PloS one 2008; 3(12): e3883. Epub 2008/12/10.
- Hamburg NM, Balady GJ: Rehabilitación mediante ejercicio en la arteriopatía periférica: impacto funcional y mecanismos de los beneficios. Circulation 2011; 123(1): 87-97. Epub 2011/01/05.
- Lauret GJ, et al: Modos de entrenamiento con ejercicio para la claudicación intermitente. Cochrane Database Syst Rev 2014; 7: CD009638. Epub 2014/07/06.
- Parmenter BJ, et al: Revisión sistemática de ensayos controlados aleatorizados: prescripción de caminar frente a ejercicios alternativos como tratamiento de la claudicación intermitente. Aterosclerosis 2011; 218(1): 1-12. Epub 2011/05/24.
- Lu L, Mackay DF, Pell JP: Metaanálisis de la asociación entre el consumo de cigarrillos y la enfermedad arterial periférica. Corazón 2013. Epub 2013/08/08.
- Kjeldsen SE, Aksnes TA, Ruilope LM: Implicaciones clínicas de las directrices sobre hipertensión de la ESH/ESC de 2013: objetivos, elección del tratamiento y control de la presión arterial. Medicamentos en I+D 2014; 14(2): 31-43. Epub 2014/05/21.
- Adam DJ, Bradbury AW: Documento TASC II sobre el tratamiento de la enfermedad arterial periférica. Revista europea de cirugía vascular y endovascular : la revista oficial de la Sociedad Europea de Cirugía Vascular 2007; 33(1): 1-2. Epub 2006/12/13.
- Norgren L, et al: Consenso intersocietario para el tratamiento de la enfermedad arterial periférica (TASC II). European journal of vascular and endovascular surgery: the official journal of the European Society for Vascular Surgery 2007; 33 Suppl 1: S1-75. Epub 2006/12/05.
- Gardner AW, Poehlman ET: Programas de rehabilitación con ejercicios para el tratamiento del dolor por claudicación. Un metaanálisis. JAMA : la revista de la Asociación Médica Americana 1995; 274(12): 975-980. Epub 1995/09/27.
- Bendermacher BL, et al: Terapia de ejercicios supervisada frente a terapia de ejercicios no supervisada para la claudicación intermitente. Cochrane Database Syst Rev 2006(2): CD005263. Epub 2006/04/21.
- Fakhry F, et al: Terapia de marcha supervisada en pacientes con claudicación intermitente. Revista de cirugía vascular 2012; 56(4): 1132-1142. Epub 2012/10/03.
CARDIOVASC 2014; 13(6): 30-33