La EPOC se considera una enfermedad prevenible y tratable, pero esto sólo es cierto en parte. El tabaquismo es el factor de riesgo más comúnmente identificado y prevenible en este país, pero en muchas cohortes de pacientes, incluida Suiza, un tercio o incluso más son no fumadores [1]. Los factores laborales y medioambientales pueden influir. El diagnóstico de EPOC se basa en la obstrucción de las vías respiratorias, definida como una relación (tras la broncodilatación con medicación) de FEV1/FVC inferior a 0,7 [2]. Aunque este punto de corte se ha cuestionado y en su lugar se han propagado los límites inferiores en función de la edad (LLN, “lower limits of normal”), sigue siendo válido. El siguiente artículo ofrece una visión actualizada del diagnóstico y el tratamiento de la EPOC.
Se cree que 330 millones de personas en todo el mundo están afectadas por la EPOC y sólo una cuarta parte de ellas son diagnosticadas. Para 2020, los epidemiólogos esperan que la EPOC sea la tercera enfermedad mortal más común en los países occidentales [3]. También se puede encontrar una estrategia global para el diagnóstico, el tratamiento y la prevención de la EPOC en el Resumen Ejecutivo de la GOLD [4].
Diagnóstico y evaluación
Historia, clínica y práctica de la espirometría: Los síntomas típicos son la disnea, la tos crónica y la producción de esputo. A menudo se recomienda realizar una espirometría en el consultorio en pacientes mayores de 40 años con mayor riesgo, con o sin síntomas [5]. Esto es sencillo y permite diagnosticar la EPOC y clasificarla en los niveles de gravedad I-IV (leve, moderada, grave y muy grave), tal y como recomendó el Comité de la Iniciativa Global para la Enfermedad Pulmonar Obstructiva Crónica (GOLD) en el primer Informe de Consenso de 2001. Hasta el momento, no existe ninguna base para un cribado general.
La estrategia actual de la GOLD: En los años siguientes, se hizo evidente que la obstrucción de las vías respiratorias sólo se correlacionaba de forma condicional con diversos problemas de salud y consecuencias para los pacientes, y que era necesario un concepto más amplio para captar los diferentes fenotipos [6].
Aunque una orientación completamente nueva de un sistema de clasificación que sólo ha sido válido durante unos pocos años no es fácil de comunicar, la categorización en cuatro grupos de riesgo (A, B, C, D) también presenta claras ventajas: La clasificación sigue basándose en la gravedad de la obstrucción, pero ahora también se tienen en cuenta la gravedad de los síntomas y la frecuencia de las exacerbaciones. Así, la mortalidad más baja se encuentra en la categoría A, la más alta en la categoría D, y una tasa comparable en las categorías B y C. Lo mismo ocurre con la frecuencia de las hospitalizaciones, pero las exacerbaciones aumentan continuamente de A a D. Las comorbilidades son (como era de esperar) más frecuentes en las categorías B y D, más sintomáticas. Ni siquiera esta clasificación actual será perfecta, ya que los pacientes con EPOC se manifiestan de forma demasiado heterogénea, por ejemplo con o sin enfisema concomitante, con diferentes patrones de inflamación, alteraciones en el intercambio gaseoso, hallazgos adicionales detectables radiológicamente y mucho más [2].
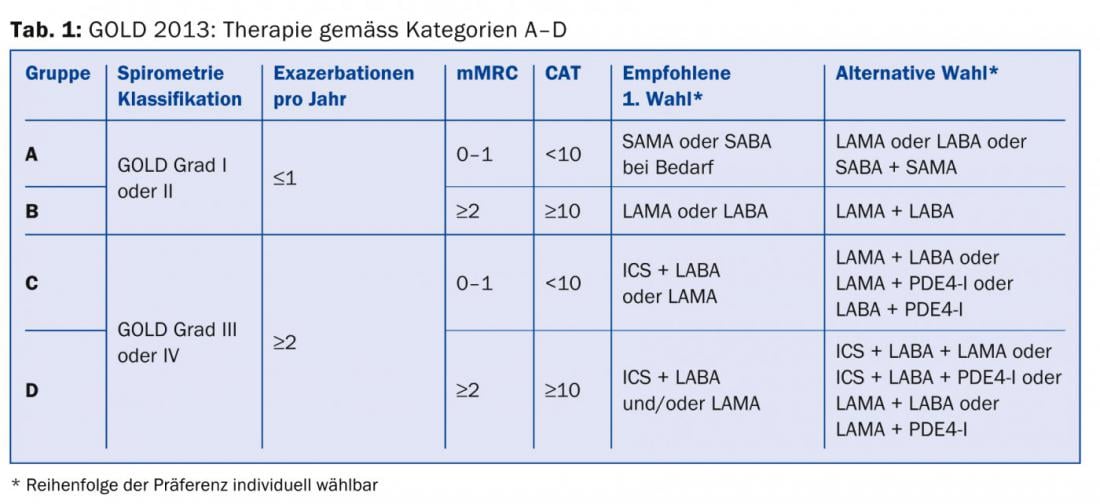
Aunque las directrices suizas publicadas recientemente no han adoptado esta nueva clasificación [7], al menos como neumólogo uno no podrá evitarla aquí.

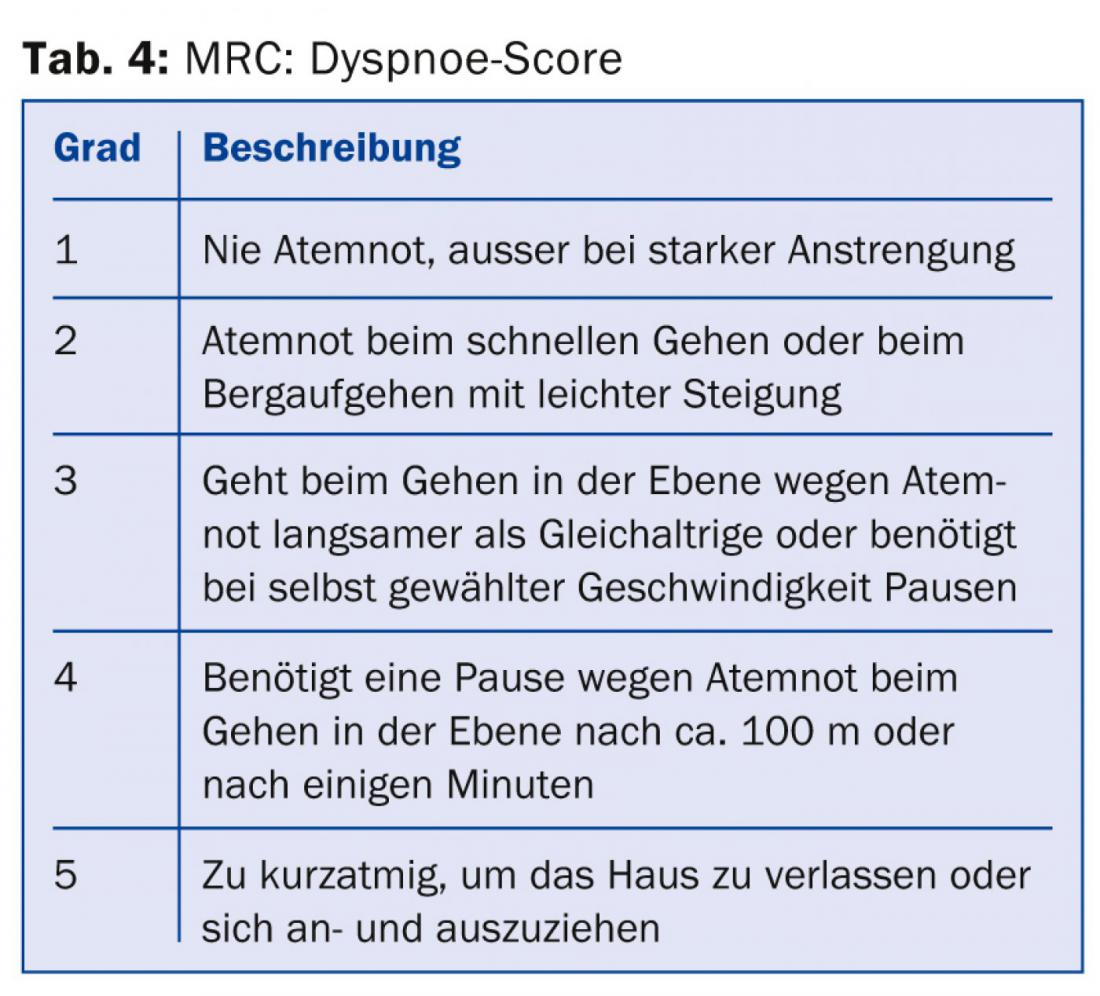
Todos los médicos que tratan a pacientes con EPOC deben ser conscientes al menos de que, además de la gravedad de la obstrucción de las vías respiratorias, la gravedad de los síntomas y la frecuencia de las exacerbaciones [8] deben incluirse en la estratificación del riesgo y el plan de tratamiento. La información necesaria para la categorización y la recomendación terapéutica (tab. 1) puede obtenerse de la función pulmonar (tab. 2), la puntuación CAT (tab. 3), la puntuación de disnea (tab. 4) y el historial de exacerbaciones.
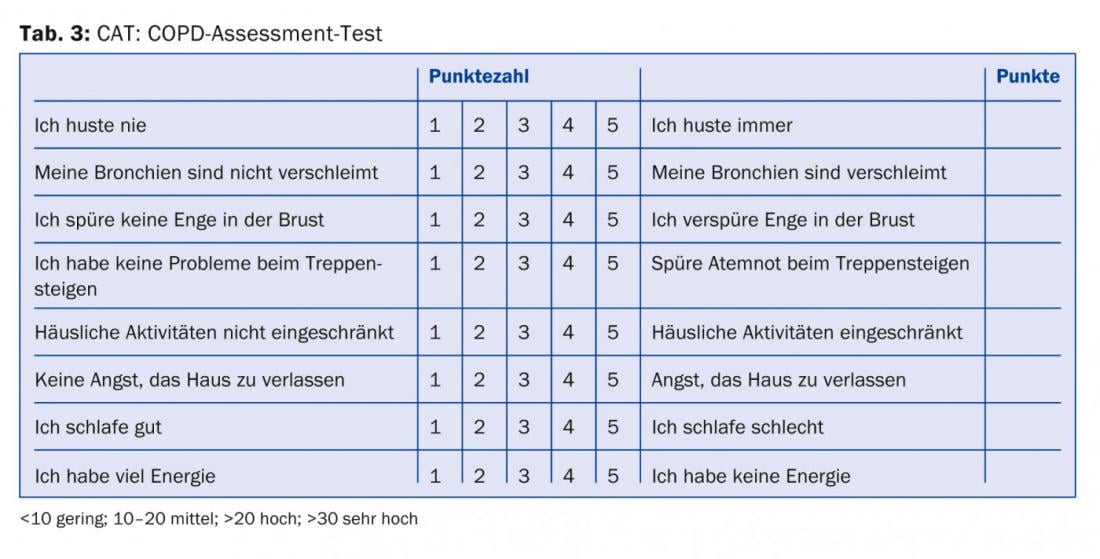
La experiencia demuestra que a menudo los pacientes no son tratados según las directrices [9]. Esto puede tener razones individuales y, a menudo, las recomendaciones se publican antes de que se haya demostrado su superioridad sobre una práctica anterior. Sin embargo, cabe esperar un ahorro de costes y quizá también la evitación de efectos secundarios con un tratamiento que se ajuste a las directrices. Los tratamientos polipragmáticos y un uso “sin concepto” de todos los medicamentos posibles, a veces con varias sustancias de los mismos grupos de principios activos, reflejan por un lado sólo un efecto limitado y la persistencia de los síntomas a pesar del tratamiento, pero por otro también una gestión del paciente por parte del médico insuficientemente determinada.
Opciones terapéuticas
La mayoría de las opciones de tratamiento no prolongan la vida y tienen poco o ningún efecto sobre la progresión de la enfermedad. No obstante, el interés de las empresas farmacéuticas por esta enfermedad es elevado, probablemente también debido al inmenso número de pacientes y a la gran cantidad de casos aún sin diagnosticar. En la actualidad se están lanzando o están a punto de lanzarse varios fármacos y combinaciones nuevos. Sin embargo, no cabe esperar de inmediato un cambio fundamental en la gravedad y el pronóstico de la EPOC, sino más bien diferencias graduales en el inicio de la acción, en la potencia del efecto, así como la mejora en criterios de valoración adicionales como el rendimiento de resistencia o el “FEV1 valle” (capacidad del primer segundo al final del intervalo de dosificación). Pero la facilidad de uso de los dispositivos de inhalación también se mejora constantemente. Por su parte, los defensores de las sustancias que llevan más tiempo en el mercado destacan los datos con un gran número de casos sobre la seguridad del tratamiento y el beneficio clínico demostrado.
Terapias farmacológicas
Broncodilatadores y esteroides inhalables: Los broncodilatadores de acción prolongada (betaagonistas de acción prolongada [LABA] y agonistas antimuscarínicos de acción prolongada [LAMA]) son el pilar del tratamiento farmacológico. Aunque esto sólo mejora ligeramente la capacidad de primer segundo, la disminución de la hiperinsuflación y los efectos antiinflamatorios e inmunomoduladores conducen sin embargo a una disminución de la disnea, la mejora de los síntomas, la prevención de las exacerbaciones, la mejora de la calidad de vida y la reducción de la necesidad de medicación de “rescate” [10,11]. Se recomienda el uso combinado de LABA/LAMA y esteroides tópicos inhalados (CSI) en pacientes con exacerbaciones frecuentes y/o con una gravedad de obstrucción bronquial GOLD III o superior. En la práctica, los CSI se prescriben con demasiada frecuencia [12]. La evitación de exacerbaciones se ve contrarrestada por un aumento previamente subestimado de la neumonía debido al uso de CSI [13].
Otras terapias antiinflamatorias: La N-acetilcisteína, comúnmente prescrita, no tiene probablemente ningún efecto terapéutico ni pronóstico en la terapia de la EPOC. Una nueva sustancia eficaz es el inhibidor de la fosfodiesterasa-4 roflumilast. Con esta sustancia pueden evitarse las exacerbaciones principalmente en pacientes con un “fenotipo bronquítico” [14]. Sin embargo, aparentemente sólo pueden prevenirse de forma significativa las exacerbaciones moderadamente graves; aún no se han demostrado ventajas con respecto a la calidad de vida y la mortalidad.

Otras opciones de tratamiento
Rehabilitación: Los pacientes con EPOC suelen beneficiarse del entrenamiento físico. Las ofertas de programas para la terapia de formación médica (MTT) pueden consultarse en www.pneumo.ch. La MTT realizada en régimen ambulatorio o de hospitalización mejora significativamente la disnea, la resistencia, la calidad de vida y reduce las hospitalizaciones por exacerbaciones [15].
Oxígeno: El oxígeno puede utilizarse con fines pronósticos, ya sea por razones paliativas o en casos de hipoxemia e hipertensión pulmonar. Los pacientes móviles son los que más se benefician del oxígeno líquido ambulatorio. Los pacientes potencialmente aptos para el tratamiento con oxígeno a largo plazo deben ser identificados por los médicos de cabecera y remitidos a los neumólogos para su titulación, prescripción y seguimiento [16].
Cirugía: La reducción quirúrgica del volumen pulmonar (RVP) se considera para pacientes con angustia significativa y limitaciones a bajo esfuerzo, hiperinsuflación grave y enfisema predominantemente heterogéneo. Con una selección correcta, puede incluso esperarse una ventaja de supervivencia [17]. El procedimiento puede llevarse a cabo con un riesgo aceptable, pero sigue siendo necesaria una abstinencia controlada del tabaco. El trasplante de pulmón sigue siendo el último recurso.
RVL endoscópica: La reducción del volumen pulmonar también puede lograrse con procedimientos parcialmente endoscópicos, relativamente sencillos y poco estresantes (uso de válvulas o espirales). La selección de pacientes es crucial en este caso; sólo unos pocos centros tienen experiencia suficiente y resultados controlados hasta el momento [18].
Estrategias de afrontamiento (“gestión de la enfermedad”): La formación específica para una enfermedad suele tener lugar en el contexto de la MTT. Los médicos de cabecera tienen el reto de formar a los pacientes para reconocer una exacerbación, desarrollar un plan de emergencia y ayudar a romper la espiral descendente de enfermedad, ansiedad, aislamiento y depresión [19].
Vacunas: La vacunación contra la gripe reduce las tasas de exacerbación y, especialmente en los pacientes de más edad, la hospitalización y la mortalidad. Debería hacerse anualmente. Recientemente se han cuestionado las recomendaciones de vacunación antineumocócica polivalente. Actualmente no se recomiendan las vacunaciones de refuerzo con la vacuna 23-valente (PPV 23). El calendario de vacunación suizo prevé actualmente una dosis única de la vacuna antineumocócica 13-valente (PCV-13) para las personas con mayor riesgo de complicaciones por enfermedad neumocócica. Esta vacuna debe administrarse con un intervalo mínimo de cuatro semanas desde una vacunación antigripal. Actualmente, sin embargo, los costes de la vacunación neumocócica sólo están cubiertos para los niños de hasta cinco años.
Exacerbaciones agudas
Las exacerbaciones agudas, las complicaciones más frecuentes en la práctica, se definen por un aumento persistente de la disnea, la tos o la producción de esputo. El tratamiento incluye un aumento de los inhalantes, corticosteroides orales, que como mucho pueden utilizarse durante menos tiempo que antes (sólo durante cinco días) a una dosis de 50 mg equivalentes de prednisona [20], y antibióticos en caso de aumento de la purulencia del esputo.
Controversias
Las expectativas de que la farmacoterapia pudiera ralentizar el curso de la EPOC siguen sin cumplirse hasta ahora. No está claro si el uso precoz de inhalables puede detener la pérdida de función pulmonar, o si las terapias combinadas consistentes en LABA + LAMA + CSI benefician a los pacientes. Habrá que seguir cuestionando el uso del ICS. La relación riesgo-beneficio se ha considerado probablemente demasiado favorable hasta ahora. En el futuro, se dará más importancia al tratamiento de las comorbilidades y a una terapia lo más adaptada posible al fenotipo.
Prof. Dr. med. Robert Thurnheer
Literatura:
1. Ackermann-Liebrich U, et al: American journal of respiratory and critical care medicine 1997; 155: 122-129.
Iniciativa Global para la Enfermedad Pulmonar Obstructiva Crónica, actualizado en 2014.
Halbert RJ, et al: ERJ 2006; 28: 523-532.
4. Vestbo J, et al: American journal of respiratory and critical care medicine 2013; 187: 347-365.
Rothe T: Praxis 2012; 101: 1481-1487.
6. Vestbo J: Clinics in chest medicine 2014; 35: 1-6.
7 Russi EW, et al: Respiration 2013; 85: 160-174.
8. Aaron SD: American journal of respiratory and critical care medicine 2009; 179: 335-336.
9. Fritsch K, et al: Swiss medical weekly 2005; 135: 116-121.
10. Calverley PM, et al: NEJM 2007; 356: 775-789.
11 Tashkin DP, et al: NEJM 2008; 359: 1543-1554.
12. Jochmann A, et al: Swiss medical weekly 2012; 142: w13567.
13 Suissa S, et al: Lancet 2009; 374: 695-703.
15 Casaburi R, ZuWallack R: NEJM 2009; 360: 1329-1335.
16 Calverley PM: Thorax 2000; 55: 537-538.
17 Meyers BF, et al: Anales de cirugía torácica 2001; 71: 2081.
18 Herth FJ, et al: Respiration 2010; 79: 5-13.
19. Bourbeau J: Copd 2011; 8: 143-144.
20 Leuppi JD, et al: JAMA 2013; 309: 2223-2231.
CONCLUSIÓN PARA LA PRÁCTICA
- Aunque todavía no se ha logrado un gran avance en el tratamiento de la EPOC, una nueva comprensión de la enfermedad ha contribuido a una variedad de posibles intervenciones y a un cambio notable.
- A menudo no se trata a los pacientes de acuerdo con las directrices.
- Los dispositivos de inhalación son cada vez más fáciles de usar.
- Los pacientes con EPOC suelen beneficiarse del ejercicio físico.
- La farmacoterapia aún no ha conseguido ralentizar el curso de la EPOC.
PRÁCTICA GP 2014; 9(8): 18-21