El tratamiento agudo del ictus isquémico ha progresado enormemente en las dos últimas décadas. Los hitos de la investigación clínica son la trombólisis intravenosa (TIV) y la recanalización mecánica. La IVT se realiza tras descartar el infarto hemorrágico y otras contraindicaciones. El plazo se ha ampliado ahora a 4,5 horas. Varios estudios realizados en 2015 demostraron la superioridad de la recanalización mecánica sobre la terapia conservadora en pacientes con oclusiones proximales de vasos de la circulación anterior. Tanto en la IVT como en la recanalización mecánica, el gran reto es optimizar las estructuras y los procesos para realizar una reperfusión rápida en la práctica clínica diaria, incluso fuera de los estudios.
En las naciones industrializadas, el ictus es la causa más común de discapacidad física persistente adquirida. Los costes para el sistema sanitario derivados de las consecuencias de un ictus son considerables. Aunque sólo una pequeña proporción de los ictus se deben a una hemorragia intracerebral, la mayoría tienen una génesis isquémica (85-90%).
El tratamiento agudo del ictus isquémico ha progresado enormemente en las dos últimas décadas. En este contexto, los hitos de la investigación clínica incluyen, sobre todo, la demostración de la eficacia de la trombólisis intravenosa en 1995 [1] y la recanalización mecánica en 2015 [2]. El rápido restablecimiento de la perfusión en el territorio vascular afectado es el objetivo de ambas estrategias. La trombólisis intravenosa requiere relativamente poco esfuerzo técnico y de personal, mientras que el tratamiento intervencionista sólo puede llevarlo a cabo un equipo interdisciplinar bien entrenado y altamente especializado en un hospital del centro. Los impresionantes resultados de los estudios correspondientes justifican este esfuerzo en las oclusiones de vasos proximales.
Trombólisis intravenosa
La trombólisis intravenosa (TIV) con activador tisular del plasminógeno (tPA) forma parte integral del tratamiento agudo del ictus isquémico desde hace 20 años. La eficacia de esta terapia se confirmó posteriormente una y otra vez [3–5]. El tratamiento se administra por vía i.v. durante una hora a una dosis de 0,9 mg/kg de peso corporal (dosis máxima de 90 mg) tras descartar un infarto hemorrágico (por ejemplo, mediante un TAC craneal nativo) y otras contraindicaciones, con un 10% de la dosis administrada en bolo al inicio. El plazo original de iniciar la terapia hasta un máximo de tres horas después del inicio de los síntomas se ha ampliado ahora a 4,5 horas [4]. Sin embargo, a pesar de la ampliación de la ventana temporal, no debe olvidarse que el éxito de la terapia depende claramente del tiempo, y bajo ninguna circunstancia debe producirse un retraso en la terapia [5]. Cuanto más tiempo pase desde el inicio de los síntomas hasta la terapia, menos se beneficiará el paciente y mayor será el riesgo de complicaciones graves.
Recomendaciones del DGN sobre IVT
Basándose en la situación actual del estudio, se complementaron las directrices de la Sociedad Alemana de Neurología (DGN) con recomendaciones [6]. Éstas se refieren, por un lado, a la utilización de la TIV fuera de los criterios de aprobación establecidos y, por otro, a la trombectomía mecánica. A continuación se expondrán brevemente las recomendaciones más importantes. La novedad es que las recomendaciones para la IVT ya no especifican un límite superior de edad. En pacientes tratados con anticoagulación oral, puede considerarse el tratamiento fuera de los criterios de aprobación en determinadas condiciones si el riesgo de hemorragia es aceptable:
- en tratamiento con antagonistas de la vitamina K con un valor INR de hasta 1,7;
- bajo nuevos anticoagulantes orales si el tiempo de trombina diluido o el nivel de factor Xa son normales o el paciente no ha tomado la medicación en las últimas 48 horas con una función renal normal.
Iniciar la terapia hasta seis horas después del inicio de los síntomas no parece conllevar un aumento significativo de la tasa de complicaciones y, por lo tanto, puede considerarse en casos individuales (por ejemplo, imágenes de desajuste, imágenes colaterales). La terapia de lisis también puede realizarse en presencia de los denominados signos tempranos de infarto en la ventana temporal de 4,5 horas.
En resumen, la TIV tiene pocas complicaciones en manos de un neurólogo familiarizado con la terapia, en combinación con los cuidados agudos del paciente en una unidad de ictus y respetando las contraindicaciones absolutas.
Terapia endovascular
A pesar del éxito indiscutible de la TIV, la tasa relativamente baja de recanalización vascular, especialmente en las oclusiones proximales, ha impulsado la búsqueda de métodos alternativos [3,7]. Siguiendo los procedimientos de terapia endovascular establecidos en cardiología, se han realizado diversos intentos para lograr una mayor tasa de recanalización y, por tanto, un mejor resultado clínico mediante el acceso directo al trombo. Hubo algunos contratiempos en el proceso, pero en general condujeron a una clara mejora de la técnica aplicada inicialmente. Entre otras cosas, la lisis local intraarterial con uroquinasa, que se investigó sistemáticamente por primera vez en el estudio PROACT, no recibió la aprobación en EE.UU. debido a un beneficio clínico insuficiente [8]. Este proceso se abandonó posteriormente en favor de procesos puramente mecánicos. La colocación permanente de un stent sobre la zona de oclusión del vaso aumentó la tasa de recanalización, pero provocó un aumento de las complicaciones hemorrágicas, debido principalmente a la doble inhibición de la agregación plaquetaria necesaria tras la intervención [9]. Por ello, las endoprótesis intracraneales sólo se utilizan en casos excepcionales en la práctica clínica.
En 2013 se publicaron tres ensayos clínicos que investigaron procedimientos de recanalización de oclusiones vasculares cerebrales proximales en los que el trombo se extraía mecánicamente (Interventional Management of Stroke III [10], MR RESCUE [11], SYNTHESIS Expansion [12]). Estos estudios tampoco lograron demostrar la superioridad de la terapia endovascular sobre la terapia farmacológica sola. Se pueden identificar tres puntos débiles del fracaso de estos estudios, que no sólo se evitaron en estudios posteriores (exitosos), sino de los que también se pueden derivar implicaciones para la acción clínica diaria:
- En primer lugar, a veces se producían retrasos drásticos hasta la apertura real del vaso, lo que probablemente se debía principalmente a que los procesos desde la llegada del paciente hasta la intervención no funcionaban con la suficiente eficacia.
- En segundo lugar, hubo una selección inadecuada de pacientes, principalmente debido a un diagnóstico por imagen inadecuado. En particular, no se identificó con prontitud a los pacientes elegibles con una oclusión del tronco principal ni se excluyó del estudio a los pacientes con un núcleo infartado extenso.
- En tercer lugar, el éxito de la recanalización fue relativamente bajo incluso en pacientes aptos debido al uso de procedimientos de trombectomía más antiguos. En particular, las endoprótesis retráctiles, tan exitosas posteriormente, sólo se utilizaron de forma esporádica.
Los puntos débiles mencionados se abordaron en los estudios posteriores y condujeron a unos resultados impresionantes en los estudios finalmente publicados en 2015 (Fig. 1 y 2) . MR-CLEAN fue el primer ensayo controlado aleatorizado que demostró claramente un beneficio de la trombectomía mecánica [2]. Como consecuencia directa, se llevaron a cabo análisis provisionales en otros estudios en curso (ESCAPE [13], EXTEND-IA [14], REVASCAT [15], SWIFT PRIME [16]), que condujeron a la finalización del estudio en todos los centros, dado que la recanalización mecánica ya era claramente superior a la terapia conservadora en ese momento.
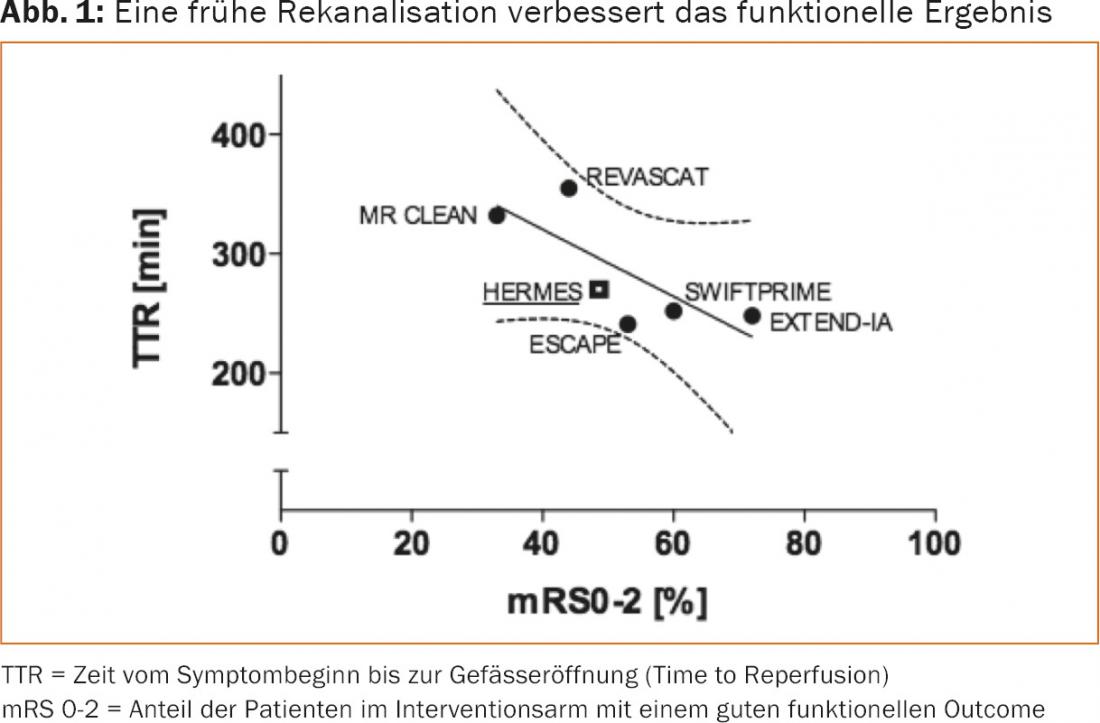
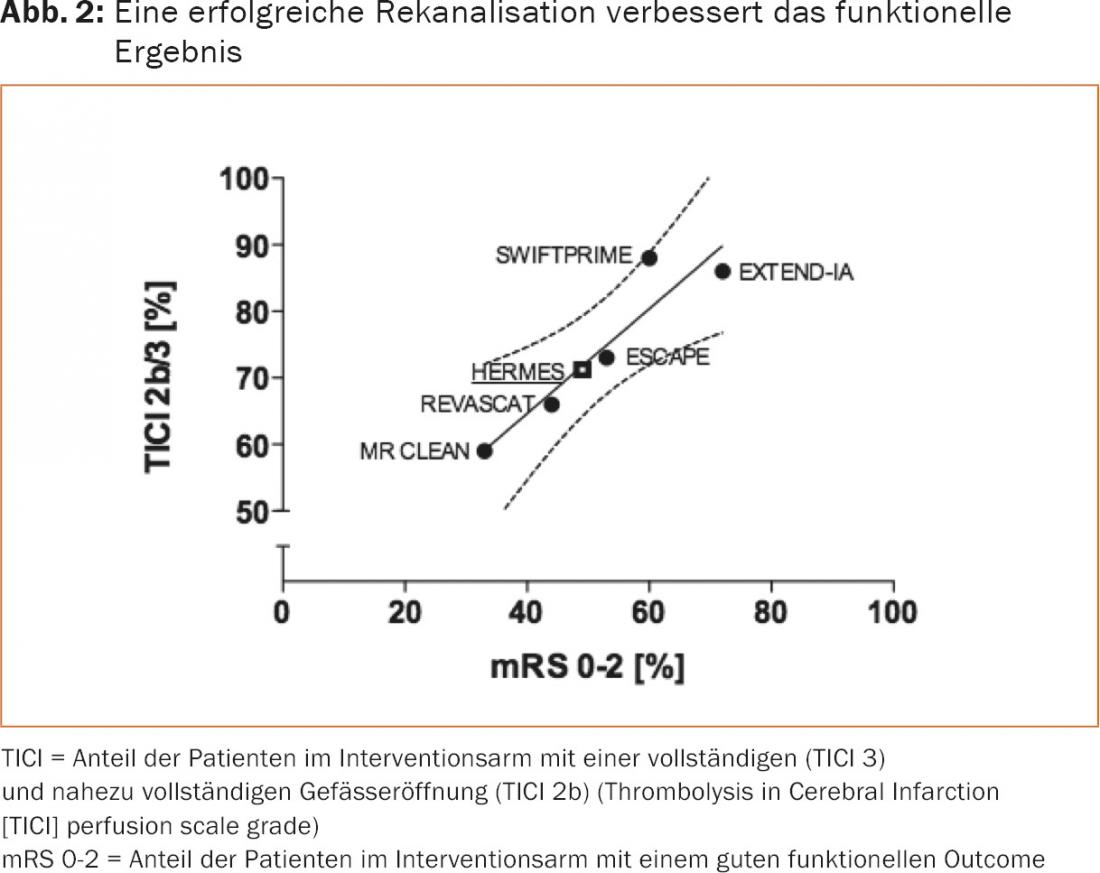
Aparte de algunas diferencias en el diseño de los estudios, que no pueden discutirse en detalle aquí, los estudios muestran similitudes relevantes en puntos esenciales: Se seleccionó específicamente a los pacientes con oclusión proximal del vaso (carótida T y M1) y déficit clínico grave, se optimizaron los procedimientos hospitalarios para una recanalización rápida (mediana del tiempo transcurrido hasta la punción inguinal: 210-270 minutos) y se utilizaron principalmente recuperadores de endoprótesis (81-100%). En parte, también se excluyó a los pacientes con infartos grandes demarcados precozmente. Estos factores dieron lugar a una mejora significativa de los resultados clínicos y a una reducción de la mortalidad a los 90 días en comparación con los grupos de control, debido a las elevadas tasas de recanalización (TICI2b/3: 59-88%) con escasas complicaciones (hemorragia intracraneal sintomática: 0-8% ) (tabla 1).
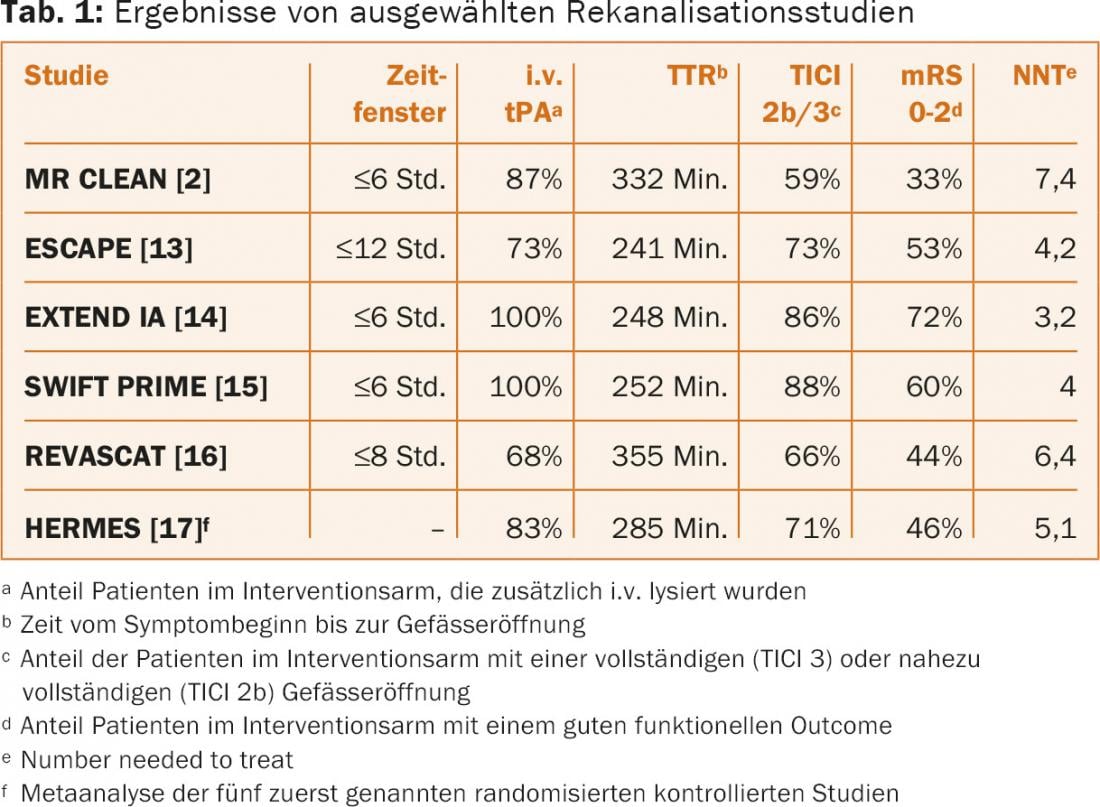
Los resultados de los estudios mencionados se examinaron recientemente en un metaanálisis conjunto [17]. Esto demostró que la trombectomía mecánica tiene un claro beneficio en casi todos los pacientes con oclusiones vasculares proximales de la circulación anterior, independientemente de otros factores (como la edad).
Recomendaciones de la DGN para la recanalización mecánica
Como consecuencia de los estudios mencionados, las directrices de la DGN para el tratamiento del ictus isquémico también se han completado ahora con recomendaciones, que se resumen brevemente a continuación.
Imagen vascular: La imagen vascular (TC-A o RM-A) debe realizarse inmediatamente para permitir una selección rápida y significativa de los pacientes apropiados.
Ventana temporal: Se recomienda la recanalización mecánica para las oclusiones proximales de vasos de la circulación anterior hasta seis horas después del inicio de los síntomas. En casos individuales puede considerarse una ampliación de la ventana temporal más allá de las seis horas (por ejemplo, con la ayuda de imágenes de desajuste o imágenes colaterales).
IVT: En ausencia de contraindicaciones, la IVT debe aplicarse siempre en un plazo de 4,5 horas; si esto no es posible, la recanalización mecánica sola es el tratamiento de primera elección. En la medida de lo posible, ambos procedimientos terapéuticos deben complementarse y ninguno de ellos debe provocar un retraso del otro. En particular, no espere a que la IVT tenga éxito y retrase los preparativos para la recanalización mecánica.
Límite de edad: No existe un límite superior de edad general.
Duración de los procedimientos clínicos: En lo que respecta a los procedimientos clínicos, se exige que el tiempo transcurrido desde la llegada hasta la punción inguinal (“puerta a punción inguinal”) no supere los 90 minutos y que el tiempo transcurrido entre la punción inguinal y la apertura del vaso no supere los 30 minutos.
Tendiendo puentes: Los pacientes remitidos a hospitales sin posibilidad de recanalización mecánica deben someterse a una IVT una vez descartadas las contraindicaciones, y deben ser trasladados inmediatamente a un hospital del centro para una recanalización mecánica (“puente”) mientras continúa la terapia.
Resultados: Como resultado de la recanalización mecánica, debe conseguirse una apertura completa o casi completa del vaso en más del 75% de los pacientes (Thrombolysis in Cerebral Infarction [TICI]-escala de perfusión de grado 3 o 2b).
Garantía de calidad: Los centros que ofrecen recanalización mecánica deben participar en programas de garantía de calidad y certificación.
En resumen, la recanalización mecánica abre nuevas perspectivas especialmente para los pacientes con oclusiones proximales de vasos en la circulación anterior. Un reto importante sigue siendo la implantación de estructuras y procesos para realizar una reperfusión rápida fuera de los ensayos en la práctica clínica diaria. Por encima de todo, es importante mantener lo más bajas posible las pérdidas por fricción derivadas de la cooperación de tres o más disciplinas (incluidas la medicina de urgencias, la neurología, la neurorradiología y la anestesia), porque en la atención al ictus isquémico agudo se sigue aplicando la única regla de oro: el tiempo es cerebro.
Literatura:
- Activador tisular del plasminógeno para el ictus isquémico agudo. El Grupo de Estudio de Accidentes Cerebrovasculares rt-PA del Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares. N Engl J Med 1995; 333(24): 1581-1587.
- Berkhemer OA, et al: Un ensayo aleatorizado de tratamiento intraarterial para el ictus isquémico agudo. N Engl J Med 2015; 372(1): 11-20.
- Rha JH, Saver JL: El impacto de la recanalización en el resultado del ictus isquémico: un metaanálisis. Ictus 2007; 38(3): 967-973.
- Hacke W, et al: Trombolisis con alteplasa entre 3 y 4,5 horas después de un ictus isquémico agudo. N Engl J Med 2008; 359(13): 1317-1329.
- Emberson J, et al: Efecto del retraso del tratamiento, la edad y la gravedad del ictus en los efectos de la trombólisis intravenosa con alteplasa para el ictus isquémico agudo: un metaanálisis de los datos de pacientes individuales de ensayos aleatorizados. Lancet 2014; 384(9958): 1929-1935.
- Ringleb PA, et al: Terapia del ictus isquémico agudo – suplemento 2015; Terapia recanalizadora. www.dgn.org/images/red_leitlinien/LL_2015/PDFs_Download/030140_LL_akuter-ischaemischer-schlaganfall_final.pdf, 2015.
- Lee KY, et al: Recanalización precoz tras la administración intravenosa de activador tisular del plasminógeno recombinante evaluada mediante angiografía pre y postrombolítica en pacientes con ictus isquémico agudo. Ictus 2007; 38(1): 192-193.
- Furlan A, et al: Prouroquinasa intraarterial para el ictus isquémico agudo. El estudio PROACT II: un ensayo controlado aleatorizado. Prolyse en el tromboembolismo cerebral agudo. JAMA 1999; 282(21): 2003-2011.
- Chimowitz MI, et al: Colocación de endoprótesis versus tratamiento médico agresivo para la estenosis arterial intracraneal. N Engl J Med 2011; 365(11): 993-1003.
- Broderick JP, et al: Terapia endovascular tras t-PA intravenoso frente a t-PA solo para el ictus. N Engl J Med 2013; 368(10): 893-903.
- Kidwell CS, et al: Un ensayo de selección de imágenes y tratamiento endovascular para el ictus isquémico. N Engl J Med 2013; 368(10): 914-923.
- Ciccone A, et al: Tratamiento endovascular del ictus isquémico agudo. N Engl J Med 2013; 368(10): 904-913.
- Goyal M, et al: Evaluación aleatorizada del tratamiento endovascular rápido del ictus isquémico. N Engl J Med 2015; 372(11): 1019-1030.
- Campbell BC, et al: Terapia endovascular para el ictus isquémico con selección de imágenes de perfusión. N Engl J Med 2015; 372(11): 1009-1018.
- Jovin TG, et al: Trombectomía en las 8 horas siguientes al inicio de los síntomas en el ictus isquémico. N Engl J Med 2015; 372(24): 2296-2306.
- Saver JL, et al: Trombectomía con stent-retriever tras t-PA intravenoso frente a t-PA solo en ictus. N Engl J Med 2015; 372(24): 2285-2295.
- Goyal M, et al: Trombectomía endovascular tras un ictus isquémico de gran vaso: un metaanálisis de los datos de pacientes individuales de cinco ensayos aleatorizados. Lancet 2016: 387(10029): 1723-1731.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2016; 14(4): 17-20.
PRÁCTICA GP 2016; 11(10): 20-23











