Con la ICP, la mortalidad por síndrome coronario agudo se ha reducido significativamente. Una visión general de los avances técnicos actuales (stents), las pautas de tratamiento más importantes y las terapias concomitantes. Incluye una visión general de las opciones de tratamiento intervencionista frente a las quirúrgicas.
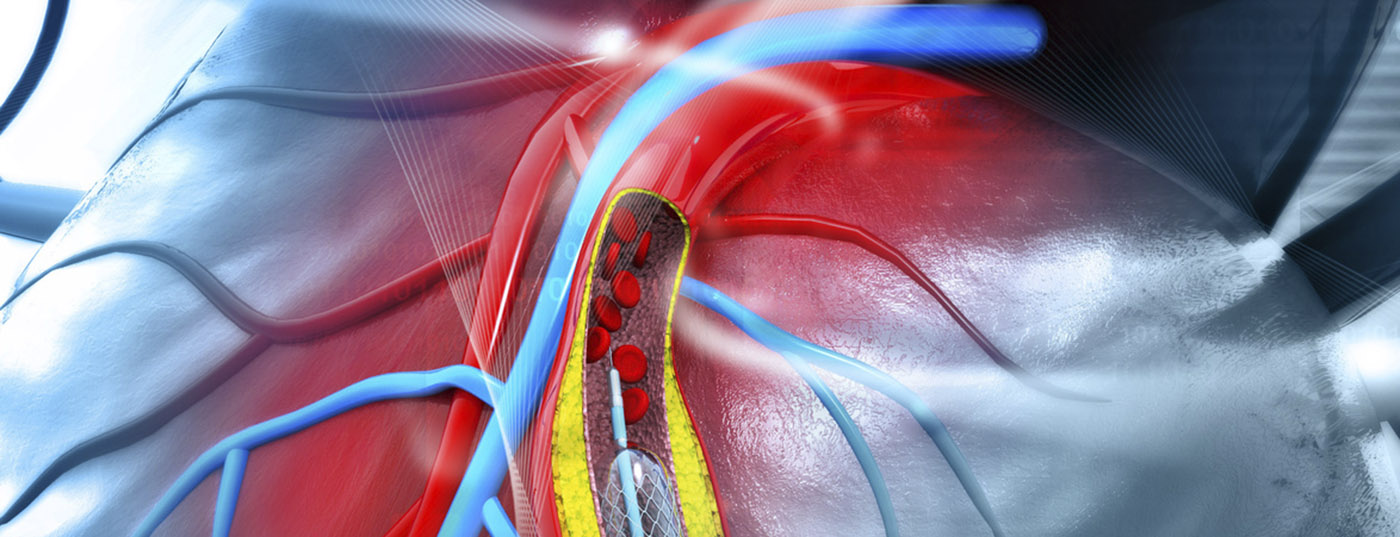
La angioplastia transluminal percutánea coronaria con balón (ACTP) fue introducida en la práctica clínica hace 40 años por Andreas Grüntzig y fue la piedra angular del rápido desarrollo de la cardiología intervencionista. Desde entonces, esta disciplina no ha dejado de ampliar el abanico de indicaciones debido a los numerosos avances tecnológicos y farmacológicos. En concreto, la introducción de los stents y su posterior desarrollo, desde los stents metálicos sin recubrimiento (BMS) a los stents liberadores de fármacos (DES) de primera generación hasta los DES de la generación más reciente, llevó a la intervención coronaria percutánea (ICP) a convencer con excelentes resultados tanto en el síndrome coronario agudo (SCA) como en la enfermedad arterial coronaria (EAC) estable. El tratamiento farmacológico complementario es esencial no sólo para prevenir la rara trombosis del stent, sino también para influir favorablemente en la aterosclerosis subyacente.
Beneficios de la ICP en el síndrome coronario agudo y la enfermedad coronaria estable
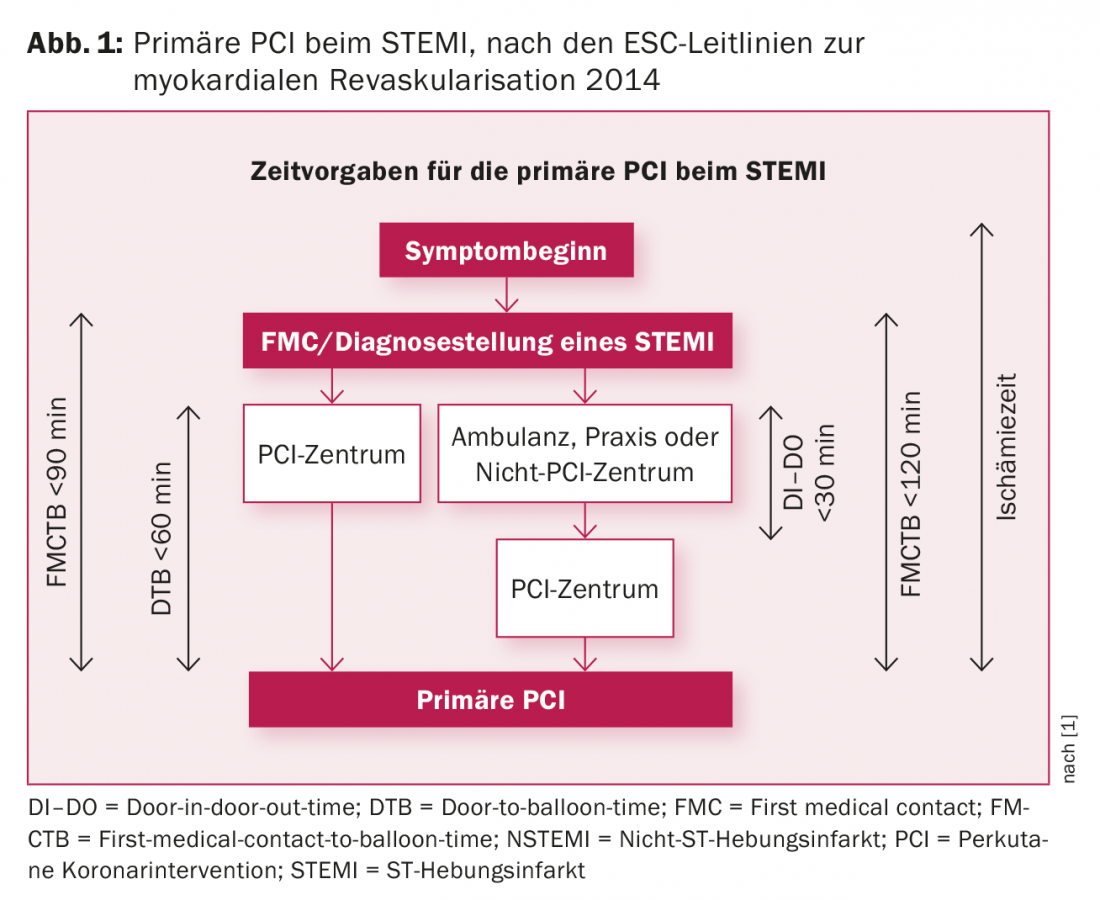
La intervención coronaria percutánea es la piedra angular en el tratamiento del síndrome coronario agudo con importancia pronóstica. Gracias a la rápida disponibilidad de la ICP de urgencia en toda Suiza, prácticamente todos los infartos de miocardio con elevación del ST (IAMCEST) pueden revascularizarse en los 60-90 minutos recomendados (Fig. 1) [1]. En comparación con la trombólisis, la ICP primaria reduce el tamaño del infarto, la tasa de reinfarto y reoclusión y la hemorragia intracraneal, y mejora la supervivencia. Con un tiempo puerta-balón (ingreso en un hospital con capacidad de ICP hasta la reapertura del vaso) inferior a 60 minutos, la mortalidad media de un IAMCEST es hoy del 3%, mientras que en la era de la trombólisis la mortalidad era el doble. En el shock cardiogénico debido a un infarto agudo de miocardio, la revascularización inmediata mejora la supervivencia en comparación con los cuidados intensivos solos del 37% al 50% durante los seis primeros meses.
Para los pacientes con enfermedad arterial coronaria estable que sufren angina a pesar de la terapia antiisquémica, la revascularización miocárdica está indicada como terapia sintomática, y existen pruebas de que con los DES de nueva generación, la ICP también puede mejorar el pronóstico [2].
Tipo de endoprótesis
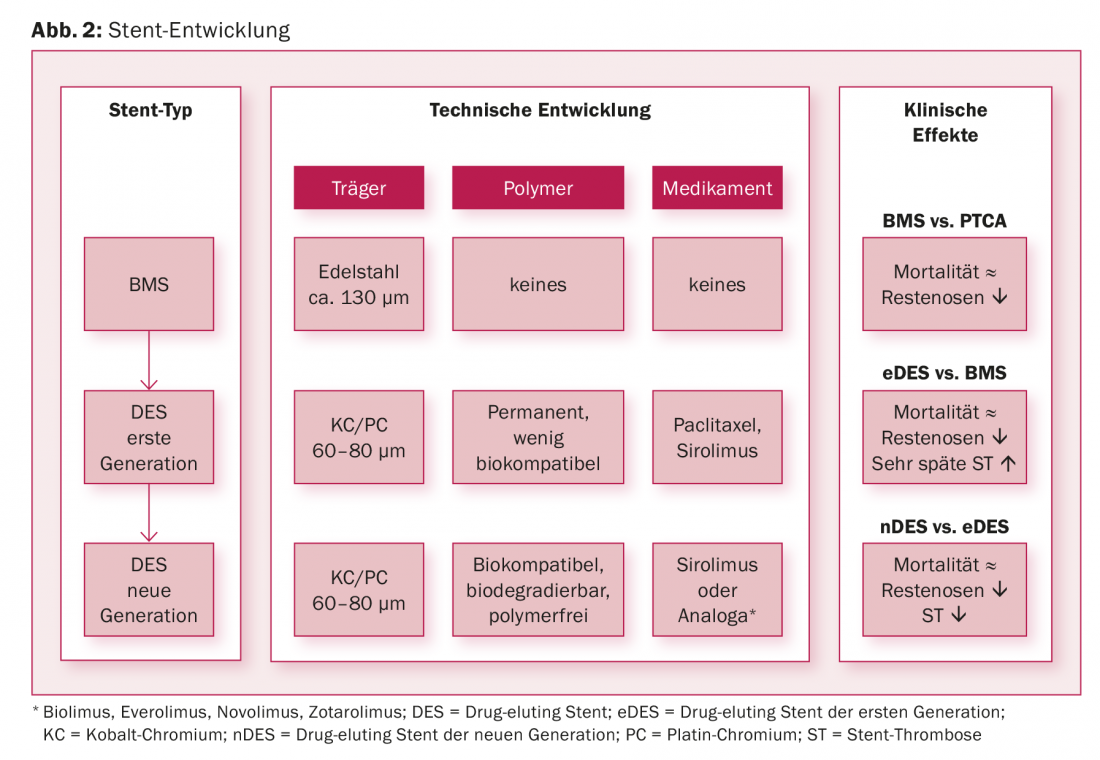
Las limitaciones importantes de la angioplastia con balón eran la aparición de disecciones, la oclusión inminente del vaso y la reestenosis. El desarrollo del BMS ha permitido tratar eficazmente las oclusiones vasculares agudas cubriendo la membrana de disección, lo que ha eliminado la necesidad de una cirugía de bypass de urgencia. Aunque los BMS también influyeron favorablemente en la tasa de reestenosis, ya que las rejillas metálicas impiden el retroceso elástico de los vasos dilatados. Sin embargo, la reestenosis (reestenosis instintiva) siguió siendo frecuente con el BMS. Esto condujo al desarrollo de stents liberadores de fármacos que contienen un fármaco antiproliferativo soportado por polímeros en dosis muy pequeñas además del andamiaje metálico. Éste se libera en la pared arterial entre unas semanas y meses después de la implantación del stent, suprimiendo eficazmente la hiperplasia neointimal. De hecho, la tasa de reestenosis pudo reducirse con los DES de primera generación y, por tanto, también la necesidad de nuevas revascularizaciones en más de la mitad, pero esto se produjo al precio de un mayor riesgo de trombosis del stent mucho más tarde (>1 año después de la implantación). En el desarrollo posterior del DES intervinieron tanto el andamio como el polímero y el fármaco. En primer lugar, los DES de nueva generación tienen andamios de cobalto o platino-cromo más finos, lo que los hace menos trombogénicos y los endoteliza más rápidamente. Además, se componen de polímeros más finos, biocompatibles o biodegradables, o incluso prescinden de los polímeros. Además, podría reducirse la cantidad necesaria de sirolimus inmunosupresor o de sus análogos más potentes (Fig. 2). Así, con los DES de nueva generación, las tasas de trombosis del stent siguen siendo del 0,5-1%, las de reestenosis del <5% y la mortalidad por síndrome coronario agudo podría reducirse al 2-3% a largo plazo [3,4]. Así pues, los stents liberadores de fármacos de nueva generación representan el patrón oro en la intervención coronaria percutánea y ocupan una indicación de clase IA en las directrices [1]. Los esfuerzos por mejorar aún más los SLF o nuevos enfoques como los andamios biorreabsorbibles tendrán dificultades para lograr nuevas mejoras clínicamente relevantes debido a los ya excelentes resultados de los nuevos SLF.
Andamios biorreabsorbibles
La idea básica de los andamios vasculares bioabsorbibles (BVS) es que, a diferencia de los stents metálicos que permanecen permanentemente como cuerpos extraños en las arterias coronarias, consisten en un andamio a base de polímeros o aleaciones de magnesio que el organismo absorbe por completo en un plazo de 6 a 36 meses, según el producto. 3-6 meses después de la implantación, pero sin embargo pueden sellar las lesiones gracias a sus propiedades mecánicas, evitar el retroceso elástico de los vasos y también pueden recubrirse con fármacos antiproliferativos para prevenir la hiperplasia neointimal. Sin embargo, a diferencia de las aleaciones metálicas utilizadas habitualmente para las endoprótesis, los materiales empleados tienen una fuerza radial y unos límites de expansión reducidos a pesar de que los struts son más gruesos, lo que dificulta la implantación. Aunque los estudios piloto mostraron resultados prometedores, fueron inferiores a los DES de nueva generación en cuanto a reestenosis y trombosis del stent en los primeros ensayos controlados aleatorizados. En la actualidad se están probando andamiajes con puntales más finos, otras propiedades de los materiales y el uso de técnicas de implantación especiales [5].
El abordaje: radial frente a femoral
Aunque el abordaje femoral es técnicamente más sencillo (arteria más grande y fácil de puncionar, mayor estabilidad del catéter debido a menos curvas desde el lugar de punción hasta las salidas coronarias), tiene un mayor riesgo de hemorragia en comparación con el abordaje por la arteria radial, que es más fácil de comprimir. El ensayo MATRIX, que aleatorizó el acceso radial frente al femoral en pacientes con síndrome coronario agudo, demostró que esta mayor tasa de complicaciones hemorrágicas relevantes con la punción femoral se asociaba a una mayor mortalidad (2,2% frente a 1,6%, p=0,045) [6]. Desde el punto de vista del paciente, el abordaje radial también tiene la ventaja de acortar el periodo de inmovilización tras la ICP.
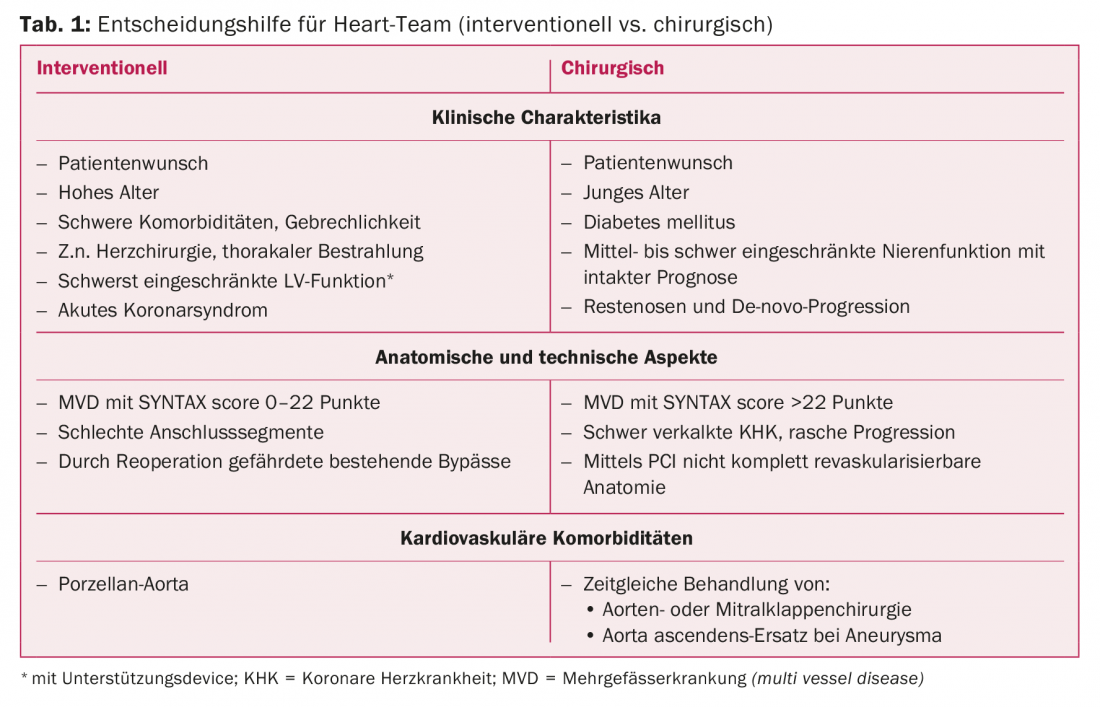
La enfermedad coronaria “compleja” y el tronco principal: intervencionismo frente a cirugía
Al igual que en la enfermedad coronaria de tres vasos con una elevada complejidad de la lesión o diabetes mellitus como comorbilidad, la cirugía de bypass aortocoronario (CAB) se ha considerado superior a la ICP (con DES de primera generación) para la estenosis del tronco principal. Los ensayos aleatorios más recientes (EXCEL [7]) y los metaanálisis que comparan el tratamiento de la estenosis del tronco principal con la ICP frente a la BCA mostraron resultados equivalentes a medio plazo en términos de muerte, infarto de miocardio e ictus. La ventaja de un menor riesgo periprocedimiento de infarto de miocardio con la ICP se pierde en el curso a largo plazo debido a una tasa ligeramente superior de infarto de miocardio espontáneo después de 30 días. Aunque la cirugía cardiaca ha realizado avances que han permitido reducir los accidentes cerebrovasculares periprocedimiento, sigue existiendo un riesgo ligeramente mayor tras la ACB en comparación con la ICP. Por el contrario, las revascularizaciones repetidas se producen con mayor frecuencia tras la ICP en comparación con la BCA. Hoy en día, en caso de enfermedad multivaso o estenosis del tronco principal, tiene lugar una discusión interdisciplinar en el equipo cardiológico, teniendo en cuenta las comorbilidades y la situación individual, para poder ofrecer al paciente la estrategia de tratamiento óptima (Tab. 1) [1]. Recientemente se han realizado grandes progresos en la reapertura de vasos ocluidos crónicamente (“oclusión total crónica”, OTC). En manos de cirujanos especializados, la OTC puede reabrirse ahora mediante abordajes anterógrados o retrógrados en un >90%.
Terapia de acompañamiento
Aunque la intervención coronaria percutánea para la enfermedad arterial coronaria (EAC) consigue muy buenos resultados, es un tratamiento focal para estenosis u oclusiones. Sin embargo, la aterosclerosis de las arterias coronarias subyacente a la cardiopatía coronaria requiere una terapia sistémica a largo plazo. Además de controlar los factores de riesgo cardiovascular, el tratamiento farmacológico antiagregante plaquetario y reductor del colesterol son especialmente importantes.
Terapia antiagregante
La elección del inhibidor de P2Y12 para la terapia antiagregante plaquetaria dual (TAPD) además del ácido acetilsalicílico (AAS) depende de la indicación y de la presencia de contraindicaciones. En el SCA, se ha demostrado la superioridad tanto del prasugrel como del ticagrelor sobre el clopidogrel en términos de complicaciones cardiovasculares (muerte cardiovascular, infarto de miocardio e ictus), pero no existe una comparación concluyente cara a cara entre el prasugrel y el ticagrelor. Sin embargo, dado que existen contraindicaciones para el prasugrel (en particular un ictus previo o un accidente isquémico transitorio), actualmente se utiliza con más frecuencia el ticagrelor. Tras un SCA, se recomienda un TAPD durante 12 meses (Fig. 3). Un DAPT prolongado (>12 meses) conlleva menos complicaciones isquémicas, pero se asocia a un mayor riesgo de hemorragia, por lo que no hay beneficio para la mortalidad [8].
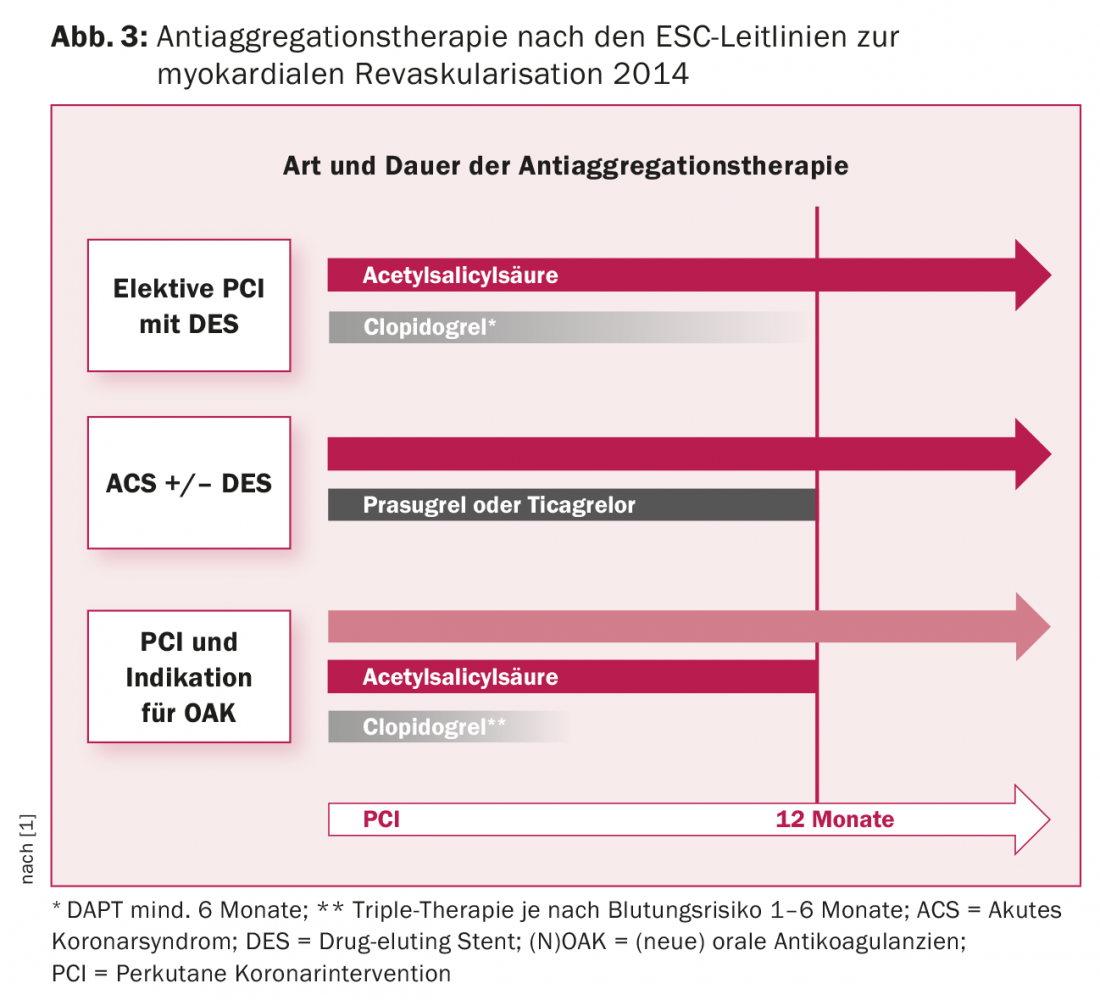
Para la ICP electiva, se recomienda el DAPT con clopidogrel durante una duración de 6-12 meses [1]. Sin embargo, con los nuevos SLF, también puede optarse por una duración más corta, de al menos 1-3 meses, debido al menor riesgo de trombosis del stent para los pacientes con mayor riesgo de hemorragia, anticoagulación oral concomitante (en el sentido de triple terapia) o necesidad de cirugía no cardiaca [9]. La puntuación PRECISE-DAPT es adecuada para calcular el perfil beneficio-riesgo individual y puede ser un apoyo útil para determinar la duración óptima del DAPT [10]. La triple terapia se asocia generalmente a un aumento de las tasas de hemorragia. Los regímenes de tratamiento menos intensivos con OAK y clopidogrel o rivaroxaban y clopidogrel sin aplicación de aspirina muestran menos hemorragias [11]. En pacientes que requieren anticoagulación a largo plazo, por ejemplo debido a fibrilación auricular o a una prótesis valvular cardiaca mecánica, 12 meses después de la ICP es suficiente continuar únicamente con anticoagulación oral sin AAS.
La terapia para reducir el colesterol
La hipercolesterolemia es, junto con el consumo de nicotina y la hipertensión arterial, el factor de riesgo cardiovascular más importante. El tratamiento con dosis altas de estatinas reduce el nivel de colesterol de lipoproteínas de baja densidad (LDL-C) hasta en un 40-50% (con rosuvastatina 20 mg/d y atorvastatina 40-80 mg/d). Además, consigue una estabilización (y a dosis muy altas también una regresión) de las placas ya existentes, así como una reducción de la actividad inflamatoria vascular a través de efectos pleiotrópicos y reduce las complicaciones cardiovasculares a largo plazo. Por lo tanto, las estatinas están indicadas como profilaxis secundaria en todos los pacientes con cardiopatía coronaria y como terapia intensificada tras un síndrome coronario agudo. Si no se alcanza el objetivo de C-LDL de <1,8 mmol/l (o una reducción de >50% respecto al valor inicial) con el tratamiento con estatinas, puede conseguirse una reducción adicional del C-LDL de aproximadamente un 10% añadiendo Ezetimiba. Los nuevos inhibidores de la proproteína convertasa subtilisina kexina tipo 9 (PCSK9) están disponibles desde 2016. Estos fármacos subcutáneos que se administran una vez cada dos semanas permiten una reducción potente del LDL-C superior a la de las estatinas y están aprobados en pacientes con dislipidemia familiar y como tratamiento complementario para pacientes con enfermedad cardiovascular aterosclerótica manifiesta en tratamiento con estatinas de tolerancia máxima. Aún no existen pruebas de una reducción de la mortalidad a largo plazo (en comparación con las tasas de infarto de miocardio e ictus) [12].
Mensajes para llevarse a casa
- La intervención coronaria percutánea es una de las intervenciones terapéuticas más frecuentes en medicina. La rápida y generalizada disponibilidad de la ICP primaria ha dado lugar a una impresionante reducción de la mortalidad por síndrome coronario agudo.
- Los stents liberadores de fármacos de nueva generación son el patrón oro actual.
- La ICP también se realiza cada vez más en pacientes con enfermedad del tronco principal y de tres vasos.
- El DAPT (AAS + inhibidor de P2Y12) se recomienda durante 6-12 meses tras una ICP o un síndrome coronario agudo.
- Si los pacientes con cardiopatía coronaria no consiguen una reducción suficiente del colesterol LDL con el tratamiento con estatinas o si éstas no se toleran, ya están disponibles los inhibidores de la PCSK9.
Literatura:
- Windecker S, et al.: 2014 ESC/EACTS Guidelines on myocardial revascularization: The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS) Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2014; 35(37): 2541-2619.
- Windecker S, et al: Revascularización frente a tratamiento médico en pacientes con enfermedad arterial coronaria estable: metaanálisis en red. BMJ 2014: 348: g3859.
- Räber L., et al.: Trombosis coronaria muy tardía de un stent liberador de everolimus de última generación en comparación con los stents liberadores de fármacos de primera generación: un estudio prospectivo de cohortes. Circulation 2012; 125(9): 1110-1121.
- Bønaa KH, et al: Stents liberadores de fármacos o metálicos sin recubrimiento para la enfermedad arterial coronaria. N Engl J Med 2016; 375(13): 1242-1252.
- Sotomi Y, et al: Andamio biorreabsorbible: la realidad emergente y las direcciones futuras. Circ Res 2017; 120(8): 1341-1352.
- Valgimigli M, et al: Acceso radial frente a femoral en pacientes con síndromes coronarios agudos sometidos a tratamiento invasivo: un ensayo multicéntrico aleatorizado. Lancet 2015; 385(9986): 2465-2476.
- Stone GW, et al: Stents liberadores de everolimus o cirugía de bypass para la enfermedad de la arteria coronaria principal izquierda. N Engl J Med 2016; 375(23): 2223-2235.
- Bonaca M, et al: Uso a largo plazo de ticagrelor en pacientes con infarto de miocardio previo. N Engl J Med 2015; 372(19): 1791-1800.
- Levine GN, et al: 2016 ACC/AHA Guideline Focused Update on Duration of Dual Antiplatelet Therapy in Patients With Coronary Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol 2016; 68(10): 1082-1115.
- Costa F, et al: Derivación y validación de la puntuación de predicción de complicaciones hemorrágicas en pacientes sometidos a implantación de stent y posterior tratamiento antiplaquetario dual (PRECISE-DAPT): un análisis conjunto de conjuntos de datos de pacientes individuales procedentes de ensayos clínicos. Lancet 2017; 389(10073): 1025-1034.
- Gibson CM, et al: Prevención de hemorragias en pacientes con fibrilación auricular sometidos a ICP. N Engl J Med 2016; 375(25): 2423-2434.
- Sabatine MS, et al: Evolocumab y resultados clínicos en pacientes con enfermedad cardiovascular. N Engl J Med 2017.
CARDIOVASC 2017; 16(3): 4-8