La fibrilación auricular es la arritmia sostenida más frecuente. La prevalencia en la población general es del 1,5-2% [1]. Con un riesgo cinco veces mayor de ictus y tres veces mayor de descompensación cardiaca, la FA es una causa común de hospitalización y se asocia a una mayor morbilidad y mortalidad [2]. ¿Cómo se realiza el diagnóstico y qué se puede conseguir con la anticoagulación y la ritmización? El siguiente artículo pretende aclarar estas cuestiones.
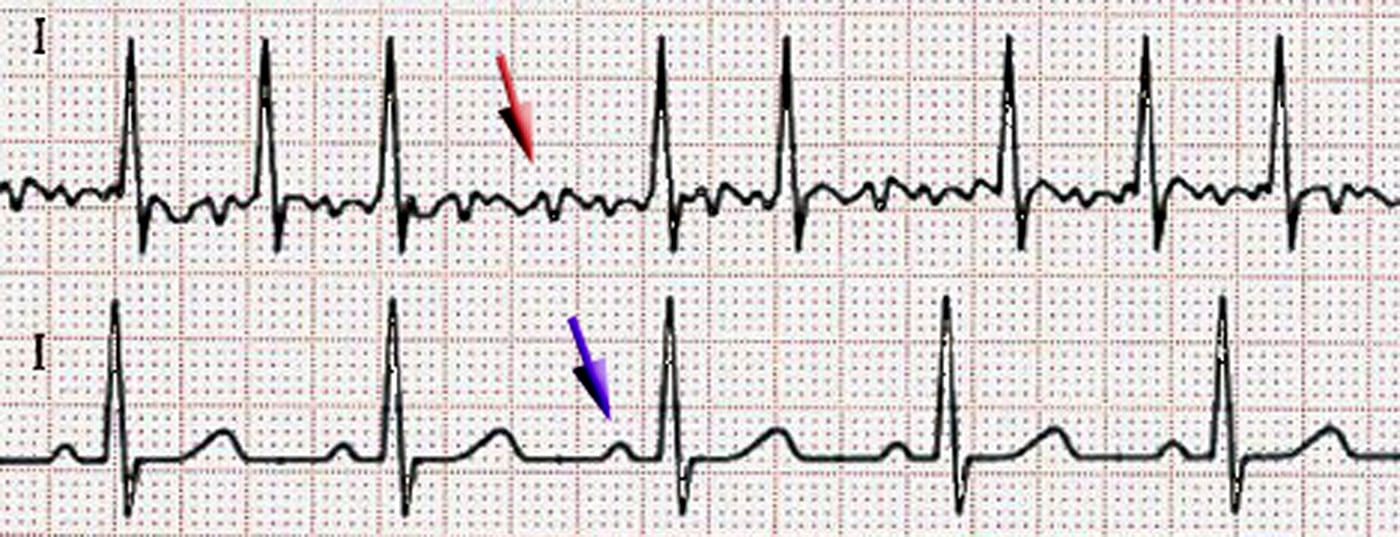
El diagnóstico de fibrilación auricular requiere la documentación de una arritmia absoluta sin ondas P de más de 30 segundos en una monitorización de ECG o en un ECG de 12 derivaciones [3], por lo que la documentación del ECG es obligatoria. Según la duración del episodio de fibrilación auricular, se habla de fibrilación auricular paroxística, persistente o permanente. El diagnóstico precoz ayuda a prevenir las complicaciones de la fibrilación auricular. Dado que la fibrilación auricular es más frecuente con la edad, se recomienda el cribado mediante palpación del pulso a todos los pacientes mayores de 65 años. Si se detecta un pulso irregular, debe realizarse un ECG en reposo para confirmar el diagnóstico o comprobar la frecuencia del pulso. para diferenciarla de otras arritmias (por ejemplo, extrasístole o aleteo auricular) [2].
Anticoagulación
La indicación de anticoagulación oral (ACO) en la FA se basa en la puntuación CHA2DS2 VASc (tabla 1), y todos los pacientes con ≥1 punto requieren ACO [3]. En pacientes con una puntuación CHA2DS2-VASc de 0 puntos o mujeres menores de 65 años sin otros factores de riesgo, el riesgo de embolia es tan bajo que debe evitarse la anticoagulación [2]. Actualmente ya no se recomiendan los inhibidores de la agregación plaquetaria para la profilaxis de las embolias. En la práctica clínica, en ocasiones se utilizan agentes antiplaquetarios en lugar de OAK en pacientes ancianos y frágiles con una mayor tendencia a caerse por temor a una hemorragia intracraneal. Sin embargo, estos pacientes también tienen un alto riesgo de sufrir un ictus isquémico, contra el que está mejor protegido un OAK [3,4]. Por ejemplo, en el estudio AVERROES, el apixaban demostró ser claramente superior al ácido acetilsalicílico en la profilaxis de los ictus isquémicos [5]. Además, hasta ahora no se ha demostrado ninguna diferencia significativa en la aparición de hemorragias intracraneales con los antiagregantes plaquetarios en comparación con los antagonistas de la vitamina K [6]. Así pues, los antiagregantes plaquetarios deben utilizarse para la profilaxis embólica sólo en pacientes que rechacen cualquier otra forma de ACO [2].
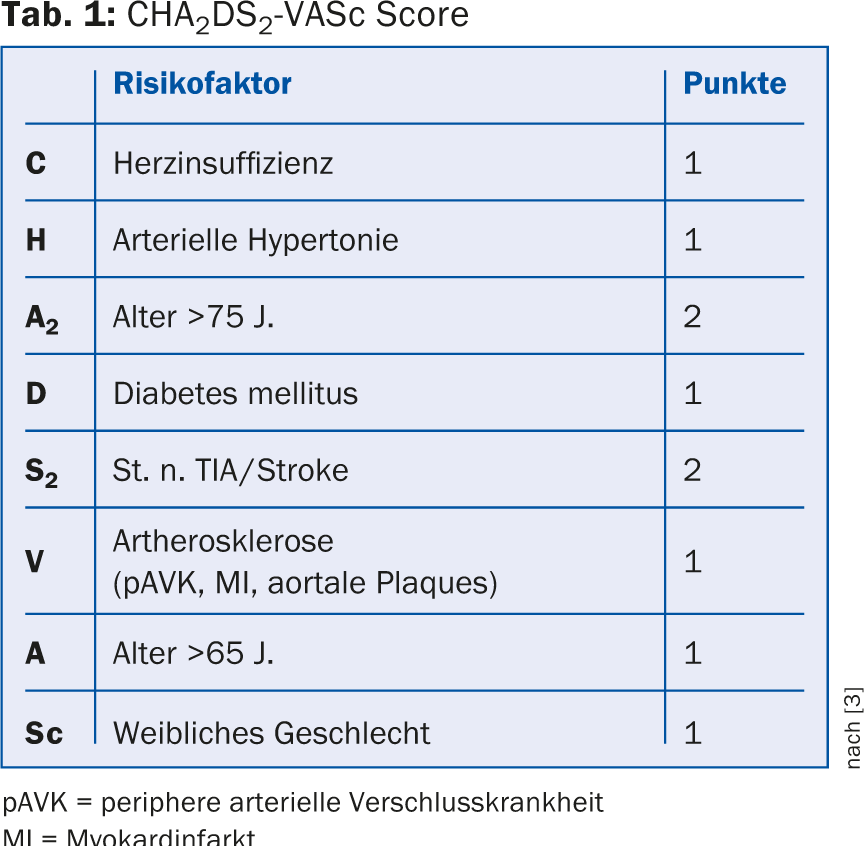
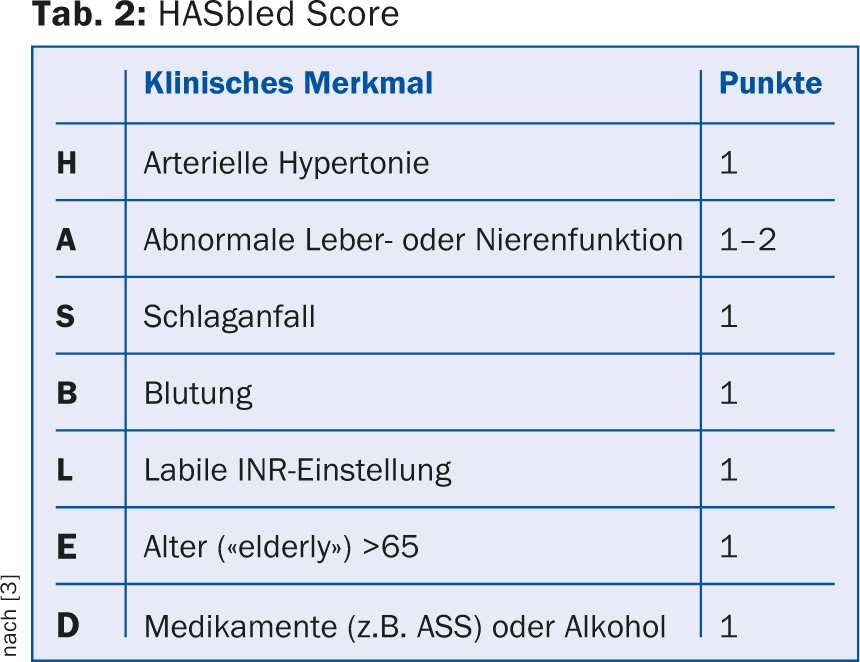
El riesgo individual de hemorragia puede calcularse utilizando varios sistemas de puntuación, por ejemplo la puntuación HASbled (Tab. 2). Sin embargo, una puntuación de hemorragia elevada no debe interpretarse automáticamente como una contraindicación para la OAK. Más bien, en el caso de un alto riesgo de hemorragia, todos los factores de riesgo tratables de hemorragia deben abordarse de forma coherente, por ejemplo, el ajuste de la hipertensión arterial, el cambio a nuevos anticoagulantes (NOAK) en el caso de valores INR inestables, la interrupción de la medicación conjunta con antiinflamatorios no esteroideos (AINE) e inhibidores de la agregación plaquetaria, a menos que sea absolutamente necesario.
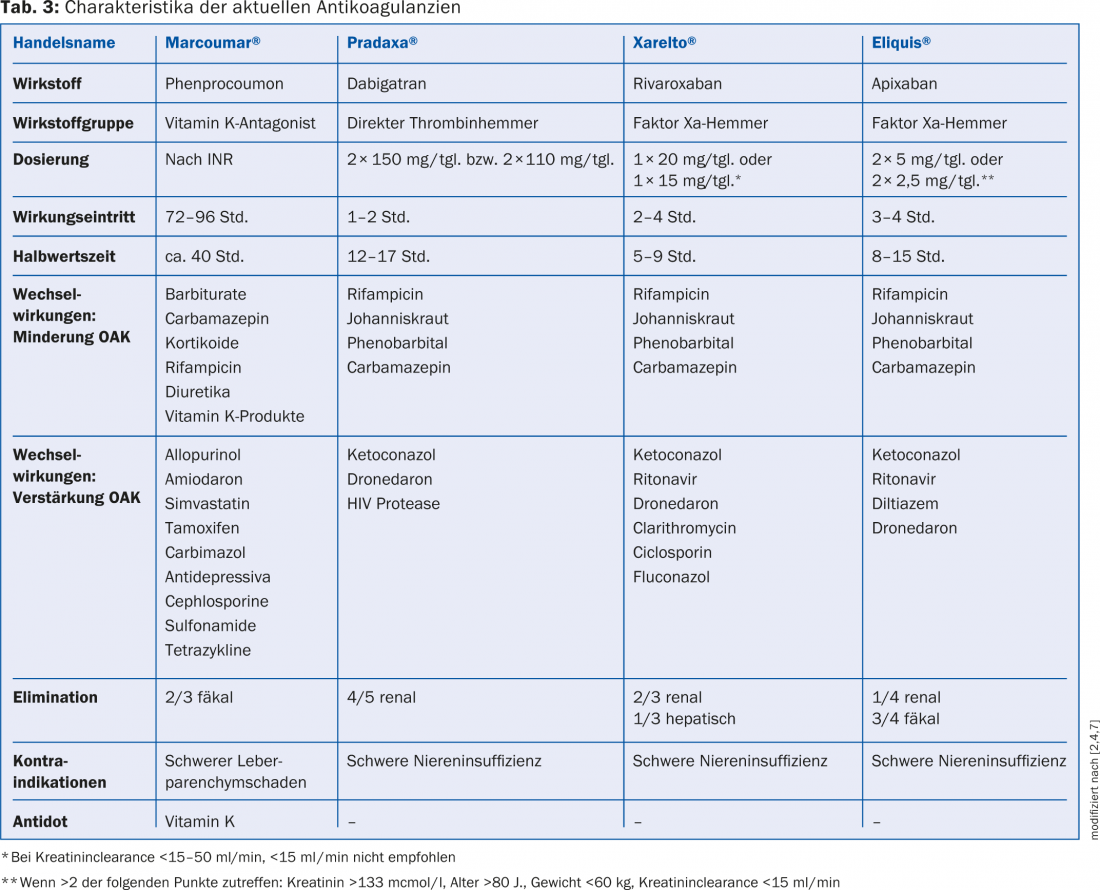
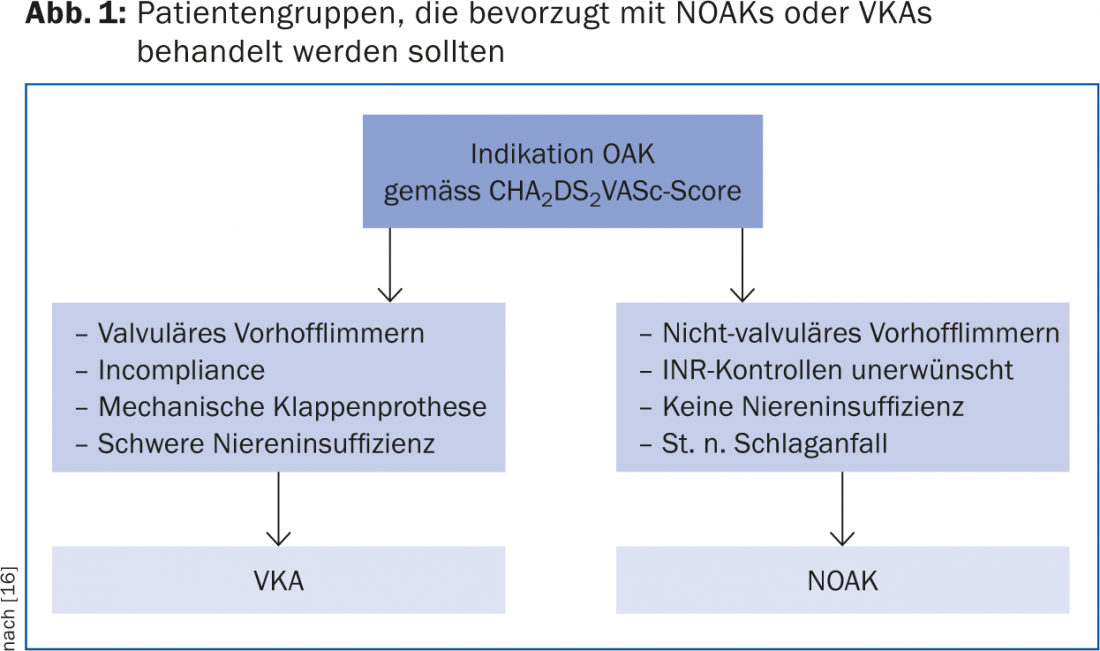
Antagonistas de la vitamina K (AVK) y NOAK: Los antagonistas de la vitamina K acenocumarol (Sintrom®) y fenprocumón (Marcoumar®) son los más utilizados en Suiza y son también la única opción anticoagulante hasta ahora para las prótesis valvulares mecánicas, la fibrilación auricular valvular y en pacientes con insuficiencia renal grave. Para la profilaxis embólica en la FA no valvular, los tres NOAK (rivaroxabán, dabigatrán y apixabán) no fueron inferiores a los AVK en los grandes ensayos clínicos de fase III y también presentaron un mejor perfil de seguridad. A partir de una puntuación CHA2DS2-VASc ≥2 puntos, los tres NOAK fueron incluso superiores a los AVK en cuanto a la profilaxis de los accidentes cerebrovasculares isquémicos y la incidencia de hemorragia intracraneal [2], razón por la cual se recomiendan actualmente como forma preferida de anticoagulación [7]. Las características de cada NOAK y las interacciones farmacológicas clave se enumeran en la Tabla 3. La figura 1 ofrece una visión general de las poblaciones de pacientes adecuadas para los NOAK o los AVK.
Oclusión de la orejuela auricular: Más del 90% de todos los trombos en pacientes con fibrilación auricular no valvular se originan en la orejuela auricular izquierda [8]. Existe la opción del cierre auricular tanto quirúrgico como intervencionista. Los estudios retrospectivos y observacionales han proporcionado resultados inconsistentes sobre el cierre quirúrgico del apéndice auricular [2]. Existen dos sistemas de cierre diferentes para el cierre intervencionista de la orejuela auricular, el dispositivo Watchman® y el Amplatzer Cardiac Plug®, que se colocan por vía transeptal desde la aurícula derecha hasta la orejuela auricular izquierda. Actualmente se están realizando ensayos prospectivos aleatorizados (PROTECT AF, PREVAIL). Dados los datos actuales, el cierre del apéndice auricular sólo debe evaluarse en casos de mayor riesgo tromboembólico y una contraindicación concomitante a la OAK [2].
¿Ritmización o control de frecuencia?
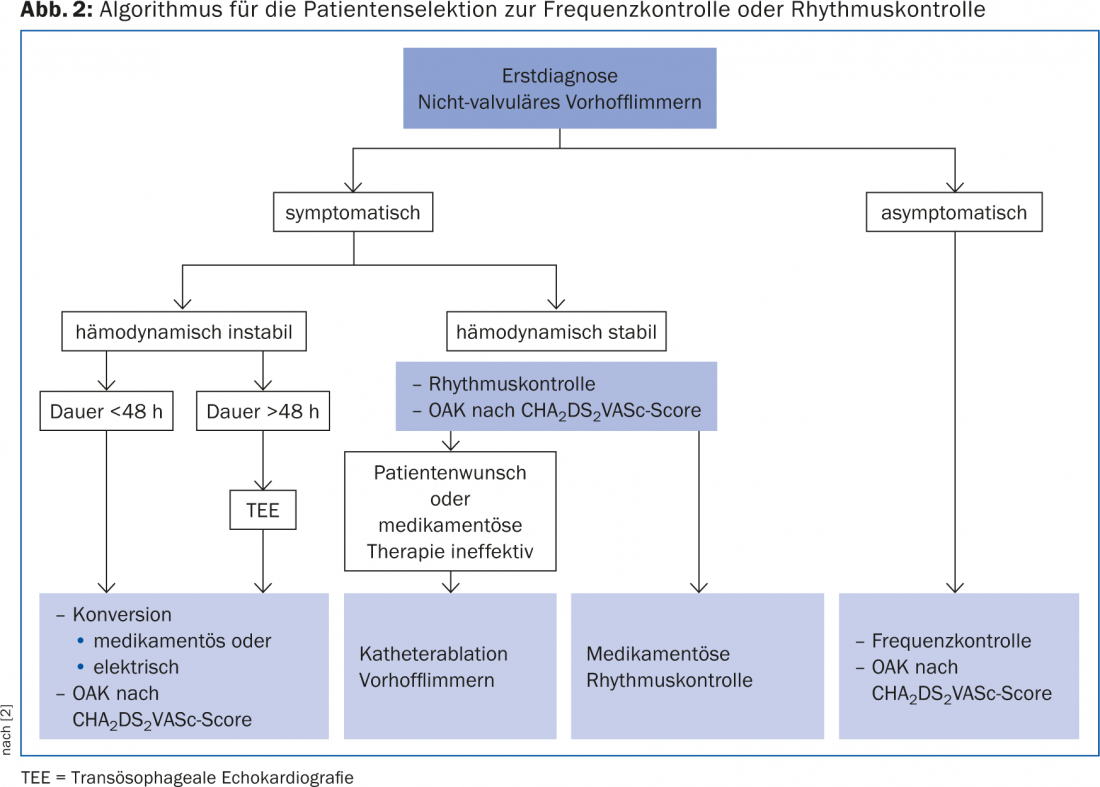
Hasta ahora, no se han encontrado diferencias significativas en la mortalidad o la tasa de ictus entre los pacientes con control de la frecuencia o del ritmo [9]. Que se deba intentar controlar la frecuencia o el ritmo en casos individuales depende en gran medida de los síntomas respectivos y de la disposición del paciente a tomar una medicación permanente que puede tener efectos secundarios o a aceptar una intervención. La figura 2 muestra un posible algoritmo para la decisión terapéutica sobre el control del ritmo o la frecuencia.
Síntomas de la fibrilación auricular: Los síntomas típicos de la fibrilación auricular están causados por una hemodinámica alterada. El llenado ventricular irregular provoca palpitaciones y un déficit de pulso periférico. La pérdida de contracción auricular junto con el acortamiento del llenado ventricular en la taquicardia puede provocar una disminución del “gasto cardíaco” del 5-15%, lo que puede causar disnea, intolerancia a la potencia, hipotensión y mareos hasta llegar al presíncope. Los pacientes con una distensibilidad del VI reducida (por ejemplo, hipertrofia del VI en hipertensión arterial o estenosis grave de la válvula aórtica) o insuficiencia cardiaca grave preexistente toleran estos cambios hemodinámicos especialmente mal. Debido al acortamiento de la diástole durante la taquicardia, el flujo coronario se reduce y pueden aparecer síntomas de AP, especialmente en presencia de una esclerosis coronaria preexistente [3]. Todos los síntomas enumerados aquí pueden ser también la manifestación inicial de la fibrilación auricular y deben conducir al diagnóstico mediante ECG si no tienen explicación.
Control de la frecuencia: Muchos síntomas de la fibrilación auricular pueden minimizarse con un buen control de la frecuencia. Además, la cardiomiopatía inducida por taquicardia puede producirse con frecuencias ventriculares sostenidas >120 lpm (latidos por minuto = frecuencia cardiaca). La normalización de la frecuencia cardiaca suele conducir a la recuperación de la función del VI [10]. Inicialmente, debe aspirarse a una frecuencia en reposo de <110/min. Si la FA sigue siendo sintomática, debe aspirarse a un control más estricto de la frecuencia <80 lpm en reposo y <110 lpm en carga [3]. Para comprobar la seguridad y la eficacia del control de la frecuencia, debe realizarse una monitorización del ECG de 24 horas después de ajustar la terapia. En los pacientes más jóvenes, son preferibles los betabloqueantes y los antagonistas del calcio del tipo no dihidropiridínico, ya que regulan la frecuencia cardiaca en reposo y durante el ejercicio [3]. Debe tenerse precaución en pacientes con preexcitación, que puede no ser visible en el ECG de 12 derivaciones. La administración de fármacos bradicardizantes ralentiza la conducción del nodo AV, pero no afecta a la conducción de la excitación en la aurícula. Así, si existe una vía accesoria, las frecuencias auriculares rápidas pueden transmitirse a los ventrículos sin frenado [3].
Ablación del nodo AV: En la ablación del nodo AV, éste se oblitera bajo control de catéter tras la implantación de un marcapasos, induciendo así un bloqueo AV total. En pacientes con fibrilación auricular sintomática que no consiguen controlar la frecuencia incluso con una terapia farmacológica combinada, la ablación del nódulo AV es una opción de tratamiento definitiva y fiable. Conlleva una mejora de la calidad de vida y se asocia a un aumento de la función del VI [11].
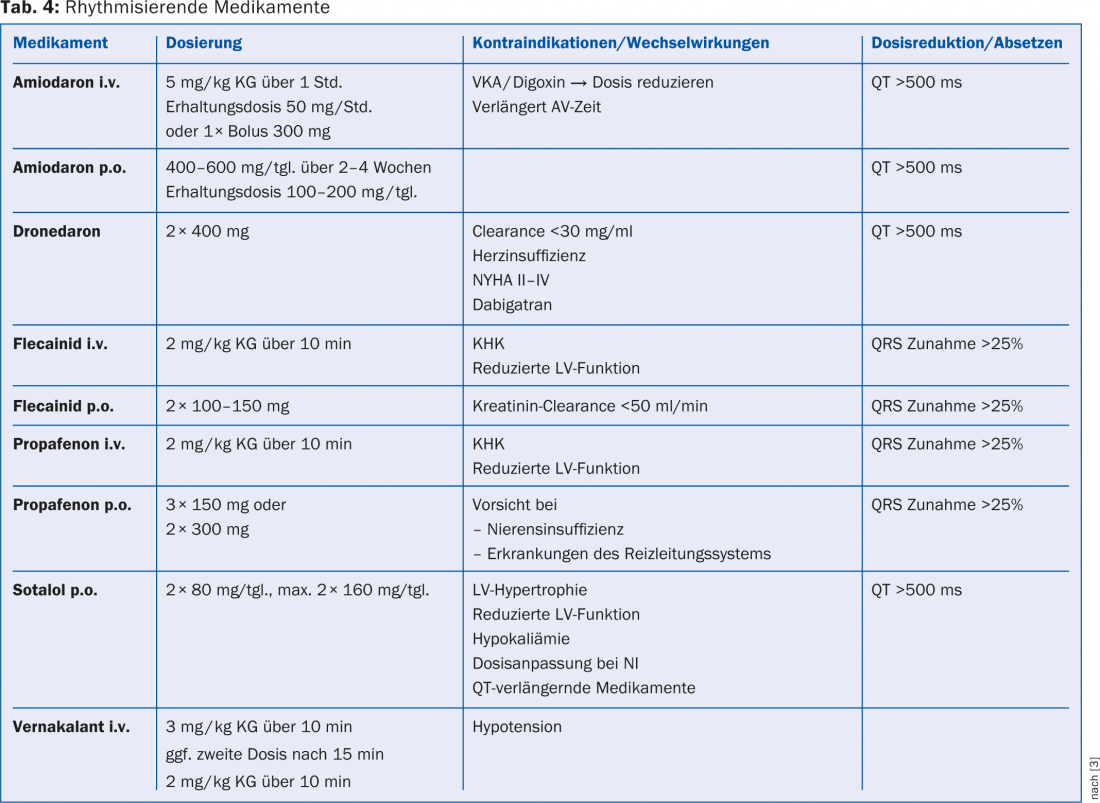
Indicaciones para el control del ritmo: Si un paciente está sintomático incluso bajo un control estricto de la frecuencia, debe buscarse el control del ritmo. Esto puede lograrse en la situación aguda con inestabilidad hemodinámica mediante cardioversión. Para la terapia a largo plazo, se dispone de la ablación con catéter o de la terapia farmacológica antiarrítmica a largo plazo. Si la fibrilación auricular está presente <48 h, la terapia puede iniciarse sin demora. Sin embargo, si la puntuación CHA2DS2-VASc es ≥1, existe una indicación para iniciar la anticoagulación terapéutica al mismo tiempo. Si la fibrilación auricular persiste >48 h, deben excluirse los trombos intracardíacos mediante ecocardiografía transesofágica (ETE) o debe realizarse una anticoagulación terapéutica durante tres semanas antes de iniciar la terapia rítmica [3]. Independientemente del método de control del ritmo elegido, debe realizarse una monitorización periódica del ECG para comprobar el éxito de la terapia [3]. Una visión general de los fármacos y las dosis respectivas que son adecuados para la ritmización la proporciona Tabla 4: Si se prefiere la terapia rítmica al control de la frecuencia, debe iniciarse lo antes posible tras el diagnóstico de FA, ya que cuanto más tiempo haya estado presente la FA, más difícil será mantener el ritmo sinusal [12,13].
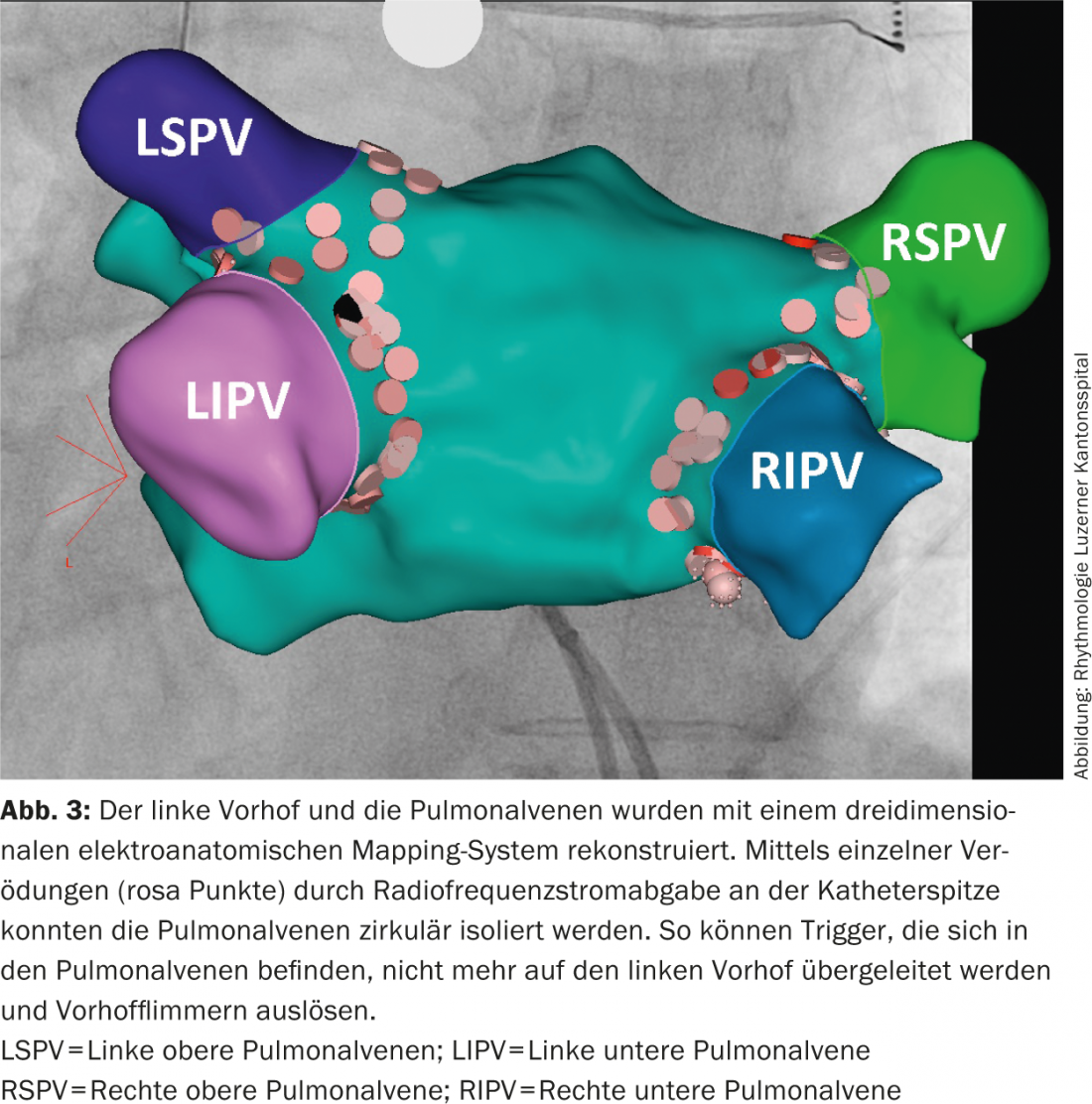
Terapia farmacológica a largo plazo frente a ablación: En pacientes sintomáticos con fibrilación auricular, la ablación con catéter puede ofrecerse como terapia de primera línea como alternativa a la terapia farmacológica con fármacos antiarrítmicos (Fig. 3) [2]. Cuando la ablación de la fibrilación auricular se realiza en un centro con experiencia, más pacientes tienen un ritmo sinusal estable tras la ablación con catéter que con una terapia antiarrítmica a largo plazo e informan de una mejor calidad de vida [14,15]. La ablación con catéter también es una buena alternativa en caso de fracaso o intolerancia de la terapia antiarrítmica. La ablación es una terapia eficaz especialmente en pacientes sin cardiopatía estructural y con sólo FA paroxística o que persiste durante menos de un año.
Literatura:
- Heeringa J, et al: Prevalencia, incidencia y riesgo de fibrilación auricular a lo largo de la vida: el estudio de Rotterdam. Eur Heart J 2006; 27: 949-953.
- Camm AJ, et al: Actualización centrada de 2012 de las directrices de la ESC para el tratamiento de la fibrilación auricular. Una actualización de las directrices de la ESC de 2010 para el tratamiento de la fibrilación auricular. Eur Heart J 2012; 33: 2719-2747.
- Camm AJ, et al: Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC).European Heart Rhythm Association; European Association for Cardio-Thoracic Surgery. Eur Heart J 2010 Oct; 31(19): 2369-2429.
- Van Walraven C, et al: Efecto de la edad en la terapia de prevención del ictus en pacientes con fibrilación auricular. Ictus 2009; 40: 1410-1416.
- Coppens M, et al: Eficacia y seguridad del apixabán comparado con la aspirina en pacientes que previamente probaron pero fracasaron en el tratamiento con antagonistas de la vitamina K: resultados del ensayo AVERROES. Eur Heart J 2014 Jul 21; 35(28): 1856-1863.
- Mant J, et al: Warfarinvversus aspirin for stroke prevention in an elderly community populationvwith atrial fibrillation (the Birmingham Atrial Fibrillation Treatment of thevAged Study, BAFTA): a randomised controlled trial. Lancet 2007; 370: 493-503.
- Heidbuchel H, et al: Guía práctica de la EHRA sobre el uso de nuevos anticoagulantes orales en pacientes con fibrilación auricular no valvular: resumen ejecutivo. Revista Europea del Corazón 2013; 34: 2094-2106.
- Watson T, Shantsila E, Lip GY: Mecanismos de la trombogénesis en la fibrilación auricular: la tríada de Virchow revisitada. Lancet 2009; 373: 155-166.
- AFFIRM Investigators: Una comparación del control de la frecuencia y el control del ritmo en pacientes con fibrilación auricular. N Engl J Med 2002; 347: 1825-1833.
- Packer DL, et al: Cardiomiopatía inducida por taquicardia: una forma reversible de disfunción ventricular izquierda. Am J Cardiol 1986; 57: 563-570.
- Kay GN, et al: The Ablate and Pace Trial: a prospective study of catheter ablation of the AV conduction system and permanent pacemaker implantation for treatment of atrial fibrillation. Investigadores de la APT. Interv Card Electrophysiol 1998 Jun; 2(2): 121-135.
- Cosio FG, et al: El retraso en el control del ritmo de la fibrilación auricular puede ser una causa de fracaso en la prevención de recurrencias: razones para cambiar a un tratamiento antiarrítmico activo en el momento del primer episodio detectado. Europace 2008; 10: 21-27.
- Kirchhof P: ¿Podemos mejorar los resultados en pacientes con fibrilación auricular mediante una terapia precoz? BMC Med 2009; 7: 72.
- Cosedis Nielsen J, et al: Ablación por radiofrecuencia como terapia inicial en la fibrilación auricular paroxística. N Engl J Med 2012; 367(17): 1587-1595.
- Wazni OM, et al: Ablación por radiofrecuencia frente a fármacos antiarrítmicos como tratamiento de primera línea de la fibrilación auricular sintomática: Un ensayo aleatorizado. JAMA 2005; 293: 2634-2640.
- Steinberg BA, Pinccini JP: Anticoagulación en la fibrilación auricular. BMJ 2014; 348: g2116.
CONCLUSIÓN PARA LA PRÁCTICA
- Todos los pacientes mayores de 65 años deben someterse a un cribado de fibrilación auricular mediante palpación del pulso. Si el pulso es irregular, el diagnóstico debe verificarse mediante ECG.
- Todo paciente mayor de 65 años con fibrilación auricular tiene una indicación de anticoagulación oral (ACO).
- Los pacientes con una puntuación CHA2DS2VAScde 0 puntos no necesitan OAK ni antiagregantes plaquetarios para la profilaxis embólica. El sexo femenino con una edad inferior a 65 años y la ausencia de otros factores de riesgo no justifica la OAK.
- En la fibrilación auricular asintomática, intente alcanzar una frecuencia de <110/min en reposo y monitorícela mediante ECG Holter. Si el rendimiento se deteriora durante la fibrilación auricular, debe considerarse la posibilidad de una miocardiopatía inducida por taquicardia. En pacientes sintomáticos, la frecuencia en reposo debe ser <80/min.
- En la fibrilación auricular sintomática, debe buscarse el control del ritmo. Para la FA paroxística sin cardiopatía estructural, las directrices actuales permiten la ablación por radiofrecuencia de la FA como terapia de primera línea.
PRÁCTICA GP 2014; 9 (9): 11-17