“Cuanto más bajo, mejor”: el planteamiento de reducir al máximo los niveles de colesterol en los pacientes con riesgo cardiovascular es más pertinente que nunca, según la actualización de las directrices suizas AGLA y las nuevas directrices ESC/ESA. De hecho, una reducción del LDL-C de 1 mmol/l reduce el riesgo de eventos cardiovasculares en una quinta parte. Sin embargo, estas reducciones de LDL son difíciles en algunos pacientes. Además, surgen las preguntas: ¿Cuándo remitir al especialista y cuándo hacer un estudio genético?
“Cuanto más bajo, mejor”: el planteamiento de reducir al máximo los niveles de colesterol en los pacientes con riesgo cardiovascular es más pertinente que nunca, según la actualización de las directrices suizas AGLA y las nuevas directrices ESC/ESA. De hecho, una reducción del LDL-C de 1 mmol/l reduce el riesgo de eventos cardiovasculares en una quinta parte. Sin embargo, estas reducciones de LDL son difíciles en algunos pacientes. Además, surgen las preguntas: ¿Cuándo remitir al especialista y cuándo hacer un estudio genético?
La dislipidemia es una de las principales causas de enfermedad cardiovascular. La atención se centra especialmente en el colesterol LDL (“colesterol de lipoproteínas de baja densidad”). Diversos estudios realizados en las últimas décadas demuestran claramente que la reducción de las concentraciones de LDL-C se asocia a un menor riesgo de episodios cardiovasculares [1,2]. Las causas de la dislipidemia son múltiples. Según la Fundación Suiza del Corazón, la hipercolesterolemia familiar (HF) afecta aproximadamente a una de cada 200 personas en este país [3]. Por ejemplo, alrededor del 30% de los pacientes jóvenes con enfermedad coronaria (EC) o infarto de miocardio tienen HF [4]. Además, se sabe que el estilo de vida y enfermedades como el hipotiroidismo, las enfermedades hepáticas, la obesidad, la insuficiencia renal crónica, la diabetes mellitus insuficientemente controlada o los efectos secundarios de ciertos fármacos (por ejemplo, los antivirales) influyen a veces considerablemente en los cambios del metabolismo de las grasas. Estos factores de riesgo hacen que hoy en día alrededor de una de cada tres personas en Suiza tenga un perfil lipídico desfavorable [5].

Aunque solo han pasado unos años desde la publicación de las últimas directrices de la Sociedad Europea de Cardiología (ESC) y la Sociedad Europea de Aterosclerosis (EAS) sobre el tratamiento de la dislipidemia en 2016, un gran número de nuevos hallazgos científicos y el desarrollo de nuevas opciones terapéuticas hicieron necesaria la actualización de las directrices [6]. Estas nuevas “Directrices de la ESC/EAS para el tratamiento de las dislipidemias” presentadas en 2019 fueron revisadas y adaptadas al año siguiente por el Grupo de Trabajo sobre Lípidos y Aterosclerosis (AGLA) con vistas a su aplicación en Suiza [7,8]. El objetivo de este resumen es informar a los médicos de cabecera sobre las directrices actualizadas y ayudarles a decidir cuándo remitir a qué pacientes a un especialista.
Evaluación de riesgos
No cabe duda de que unos niveles elevados de colesterol-te-rina están asociados a un mayor riesgo cardiovascular. La evaluación de los factores de riesgo es un componente central del cálculo del riesgo. Por ejemplo, no sólo es decisivo el nivel de lípidos, sino también la duración de la exposición [6]. Según las directrices de la ESC/EAS, se clasifican cuatro categorías de riesgo diferentes, a saber, riesgo muy alto, alto, moderado y bajo (resumen 1).
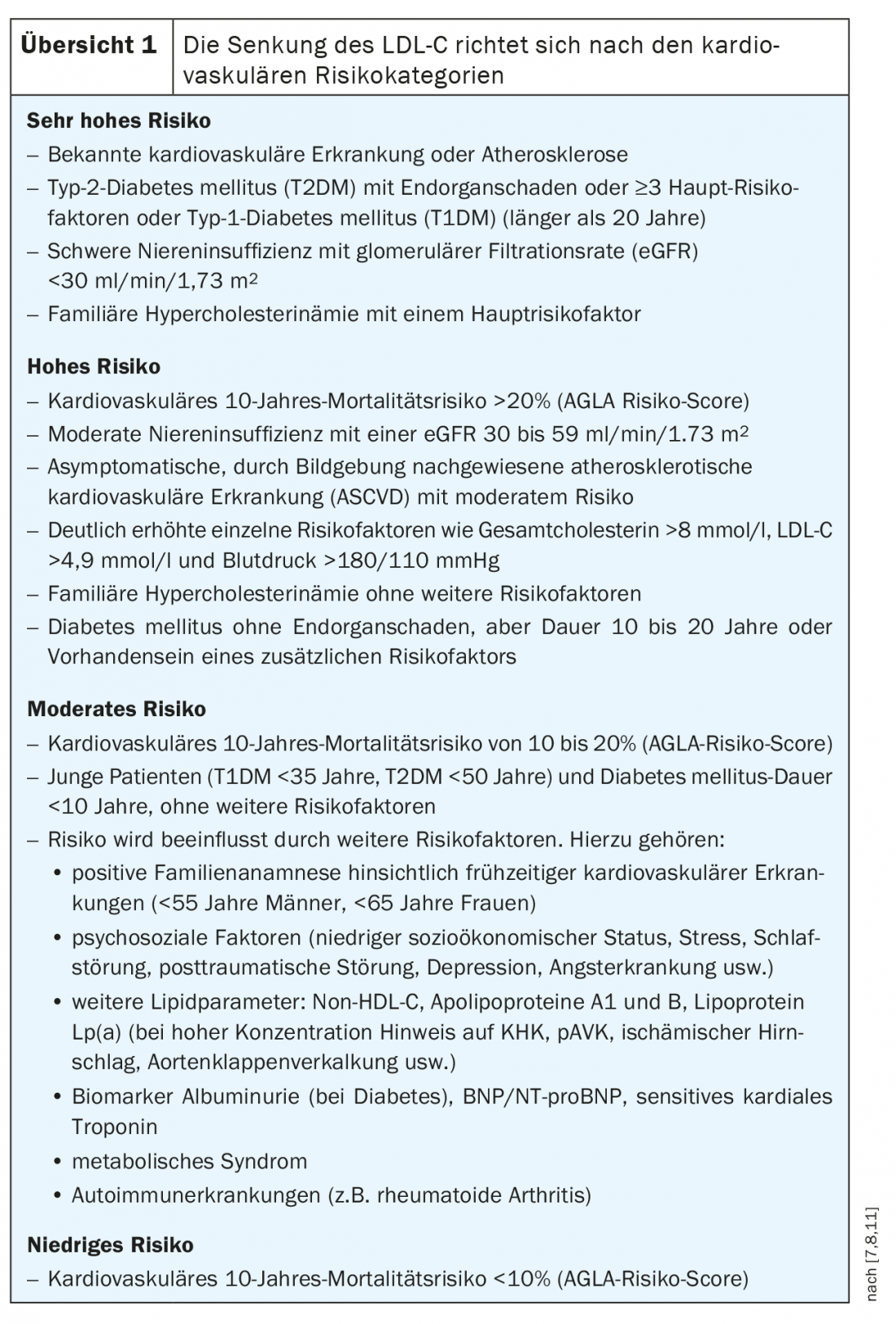
En Suiza se ha establecido la calculadora de riesgo AGLA para calcular el riesgo individual. Puede utilizarse en línea para calcular fácilmente el riesgo absoluto a lo largo de diez años de sufrir un acontecimiento coronario mortal o un infarto de miocardio no mortal (www.agla.ch/de/rechner-und-tools/agla-risikorechner) [8]. La calculadora AGLA tiene en cuenta parámetros como la edad, los antecedentes familiares, el tabaquismo, la tensión arterial, el colesterol LDL, el colesterol HDL o los niveles de triglicéridos. Sin embargo, no se tienen en cuenta la actividad física, la radioterapia, etc.
El ESC/EAS-SCORE también puede utilizarse para estimar el riesgo de mortalidad cardiovascular a 10 años (www.scores.bnk.de/esc.html). Suiza se considera una región de bajo riesgo cardiovascular, por lo que se utiliza la “variante ESC-SCORE de bajo riesgo”.
Para la prevención primaria, la AGLA recomienda una evaluación inicial del riesgo en hombres asintomáticos mayores de 40 años y mujeres mayores de 50 años. Si el riesgo es bajo, debe reevaluarse cada cinco años, y si el riesgo es moderado, debe reevaluarse cada dos a cinco años. Para las personas que ya muestran un riesgo alto o muy alto en la evaluación inicial, no es necesaria una estimación con una calculadora de riesgo, ya que estos pacientes se clasifican automáticamente como pacientes de alto riesgo. Esto se aplica a:
- Enfermedades cardiovasculares documentadas (por ejemplo, infarto de miocardio o síndrome coronario agudo, 2 enfermedades con al menos una oclusión de la arteria coronaria). 50% de estenosis en el TAC cardiaco, ictus isquémico, enfermedad arterial periférica (EAP) o antecedentes de revascularización coronaria/arterial).
- Diabetes mellitus con daño en los órganos finales, larga duración de la enfermedad o al menos 3 factores de riesgo
- insuficiencia renal de moderada a grave (grado KDIGO ≥3)
- Factores de riesgo individuales pronunciados (LDL-C >4,9 mmol/l, colesterol total >8 mmol/l, tensión arterial >180/110 mmHg)
- hipercolesterolemia familiar
- Fuerte aumento de la lipoproteína Lp(a)
Modificadores del riesgo
Para los pacientes con un riesgo bajo y, sobre todo, moderado, se introdujeron de nuevo criterios adicionales de evaluación del riesgo como posible herramienta complementaria. Estos “modificadores del riesgo” pueden ayudar a ajustar la estimación del riesgo cardiovascular. Los pacientes que en realidad se encuentran en una categoría de riesgo más baja pueden entonces ser colocados en un nivel de riesgo más alto. Tales modificadores incluyen:
- Privación social, estrés psicosocial, agotamiento vital, enfermedad psiquiátrica grave
- Imágenes cardiovasculares no invasivas: medición de la puntuación de calcio en la arteria coronaria (CAC) en el TAC cardiaco (puntuación CAC, puntuación Agatston), ecografía de la arteria femoral y de la arteria carótida para la detección de placas (IIbB).
- Antecedentes familiares positivos de enfermedad cardiovascular precoz (varones <55 años, mujeres <60 años).
- Inactividad física, obesidad (medida por el índice de masa corporal o la medida del perímetro abdominal).
- Enfermedad inflamatoria crónica inmunomediada
- Tratamiento de la infección por VIH
- Fibrilación auricular
- Hipertrofia ventricular izquierda
- Insuficiencia renal crónica
- Síndrome de apnea obstructiva del sueño
- Hígado graso no alcohólico
- Lipoproteína Lp(a)
Valores objetivo de LDL-C
Existe una asociación significativa entre la reducción del colesterol LDL y la reducción del riesgo cardiovascular [10]. Por este motivo, las nuevas directrices de la ESC (y, en consecuencia, las directrices actuales de la AGLA) fueron más allá de las recomendaciones de las directrices anteriores al formular los nuevos objetivos de reducción del LDL-C. En principio, el LDL-C debe reducirse lo máximo posible (“cuanto más bajo, mejor”), sobre todo en caso de riesgo alto y muy alto. Cuanto mayor sea el riesgo cardiovascular, menores serán los valores objetivo (Tab. 1) .
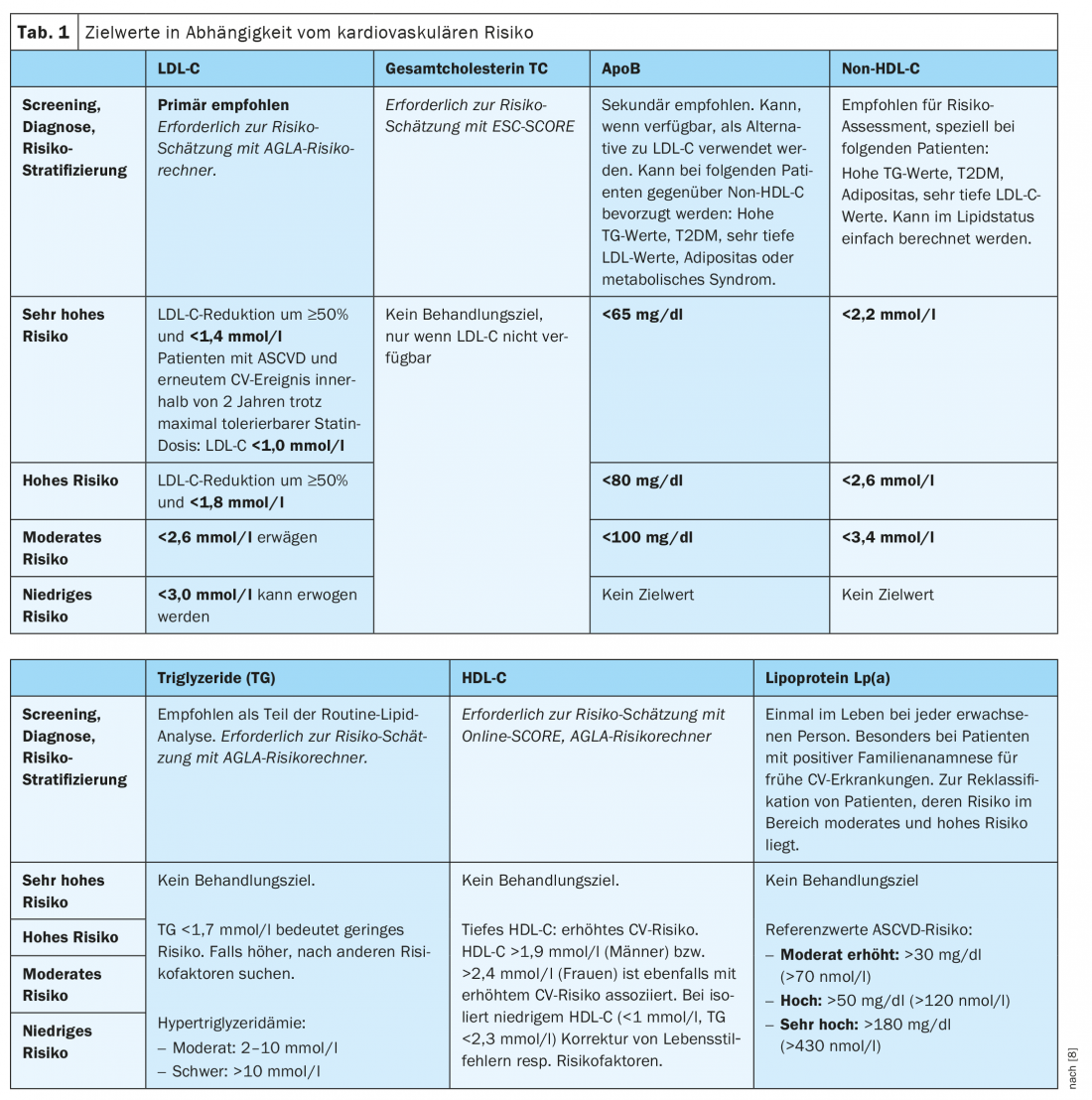
Los pacientes con un riesgo muy elevado deben aspirar a una reducción del 50% del LDL-C y a un valor objetivo de LDL-C <1,4 mmol/l. Además de una reducción del 50%, se recomienda un valor objetivo de <1,8 mmol/l para el riesgo alto y de <2,6 mmol/l para el riesgo moderado. Por último, se puede apuntar a un nivel de bajo riesgo de <3,0 mmol/l. Los pacientes con HF con ASCVD u otro factor de riesgo se consideran de muy alto riesgo (véase más adelante). Según la AGLA, el estado lipídico del plasma sin ayunar es suficiente para la evaluación en la mayoría de los casos. Sin embargo, se recomienda la extracción de sangre en ayunas en las siguientes situaciones:
- Síndrome metabólico
- Triglicéridos no en ayunas >5 mmol/l
- Hipertrigliceridemia conocida
- Tras una pancreatitis inducida por hipertrigliceridemia
- Antes de iniciar el tratamiento farmacológico con hipertrigliceridemia grave como posible efecto secundario
- Si se requieren análisis adicionales que deban determinarse en ayunas, por ejemplo, glucosa en ayunas, monitorización de fármacos terapéuticos
Hipercolesterolemia familiar
Si el perfil lipídico muestra alteraciones significativas, la HF también puede estar presente. Los afectados por un colesterol LDL genéticamente elevado tienen un riesgo cardiovascular mucho mayor que los pacientes con LDL adquirido al mismo nivel [8]. Por ejemplo, en la HF, el riesgo de infarto de miocardio a 10 años sin tratamiento es superior al 50%. Las indicaciones de HF para adultos son la cardiopatía coronaria en hombres menores de 55 años o mujeres menores de 60 años. Además, se recomienda aclarar los niveles elevados de colesterol, es decir, un colesterol total de ≥8mmol/l o LDL ≥5,0 mmol/l o triglicéridos ≥5,0 mmol/l (niños/adolescentes correspondientemente más bajos). La aterosclerosis prematura o, en los menores de 45 años, los xantomas tendinosos o el arcus cornealis, así como la hiperlipidemia genética en otros miembros de la familia, también podrían indicar HF. Si se sospecha HF, ésta debe aclararse según los “Criterios de la Red Clínica Holandesa de Lípidos” (www.agla.ch/de/rechner-und-tools/agla-fh-rechner). Si se confirma la sospecha, debe tratarse como de “alto riesgo” y con un factor de riesgo adicional como de “muy alto riesgo”. La HF debe diagnosticarse clínicamente si es posible y confirmarse genéticamente, y está indicado el cribado familiar de los pacientes con HF. Si se detecta la mutación, suele mejorar el cumplimiento terapéutico.
Terapia
El tratamiento de la dislipidemia depende del riesgo cardiovascular global y de los valores objetivo de LDL para los pacientes en función de éste. La base de una terapia de este tipo es un cambio en el estilo de vida, especialmente con un ajuste de la dieta, la reducción del consumo de alcohol, más ejercicio, pérdida de peso y dejar de fumar. Si además de alcanzar el objetivo terapéutico según la categoría de riesgo es necesario reducir los lípidos, las estatinas son los fármacos de primera elección. Es decir: en la primera fase, se utilizan estatinas muy eficaces en la dosis máxima tolerable. Si los valores objetivo siguen sin alcanzarse, se recomienda la combinación con el inhibidor de la absorción del colesterol ezetimiba. Si hay intolerancia a las estatinas, también debe considerarse la ezetimiba. Puede utilizarse un inhibidor de la PCSK9 además de la ezetimiba.
Si los pacientes con un riesgo muy elevado no alcanzan su objetivo terapéutico a pesar de la dosis máxima de estatina más ezetimiba, pueden ser tratados adicionalmente con un inhibidor de la PCSK9 en prevención primaria. También puede considerarse una combinación con un anticuerpo PCSK9 de este tipo para pacientes con un riesgo muy elevado en prevención secundaria, es decir, cuando no se alcanza el objetivo terapéutico a pesar de la máxima estatina tolerable más ezetimiba. Para los pacientes con HF de muy alto riesgo y en los que ha fracasado el tratamiento con la dosis más alta de estatina más ezetimiba, también se sugiere una combinación con un inhibidor de PCSK9. En el futuro, se dispondrá de otras sustancias, como el ácido bempedoico (inhibidor de la citrato liasa ATP, sólo eficaz en el hígado), el Inclisiran (una molécula de ARNsi que inhibe la PCSK9) o los anticuerpos ANGPTL3 en pacientes con triglicéridos elevados.
Los fármacos más importantes para reducir los lípidos
Con una terapia intensiva con estatinas, es posible reducir las concentraciones de LDL en más de un 50%, y con una terapia moderada en más de un 30-50%. La intensidad de esta reducción depende, por un lado, de las estatinas utilizadas (la atorvastatina, la rosuvastatina y la pitavastatina se consideran estatinas potentes) y, por otro, de la dosis y de la predisposición genética del paciente. Por ejemplo, un gran metaanálisis demostró que reducir el LDL-C en 1 mmol/l reduce el riesgo relativo de eventos cardiovasculares en un 22% a lo largo de cinco años [2]. Las estatinas también reducen los triglicéridos entre un 10 y un 20%, pero sólo aumentan ligeramente las HDL (entre un 1 y un 10%). En cambio, la concentración de Lp(a) no se ve influida o lo hace muy ligeramente. Los efectos secundarios del tratamiento con estatinas pueden incluir miopatía, miositis y rabdomiólisis. Estos síntomas musculares suelen comenzar unas semanas después del inicio de la terapia. Además, especialmente en los pacientes de más edad, el riesgo de desarrollar diabetes mellitus de tipo 2 aumenta ligeramente con las dosis altas de estatinas [11]. Aún no se ha demostrado sin lugar a dudas si el riesgo de accidentes cerebrovasculares hemorrágicos también aumenta ligeramente. Se recomienda precaución con las interacciones. Algunas estatinas reaccionan con determinados fármacos, como los inmunosupresores, los inhibidores de la proteasa del VIH, los macrólidos, los antifúngicos azólicos, las benzodiacepinas o los antagonistas del calcio.
Los inhibidores de la absorción del colesterol también son herramientas importantes para la reducción de la grasa en sangre. La ezetimiba bloquea la absorción del colesterol en el intestino, reduciendo los niveles de LDL en un 18,5% aproximadamente. La ezetimiba actúa a través de la proteína 1 similar a la Niemann-Pick C1 (NPC1L1), pero no reduce la absorción de los alimentos liposolubles.
Los triglicéridos también se reducen, concretamente en un 8%, mientras que se produce un aumento mínimo de las HDL [12]. Se ha demostrado que la combinación de ezetimiba con estatinas reduce aún más los eventos cardiovasculares. Los efectos secundarios más comunes de esta terapia combinada son dolor de cabeza, dolor muscular y un aumento de las transaminasas GOT y GPT.
La disminución de la concentración de PCSK9 (proproteína convertasa subtilisina/kexina tipo 9) favorece la expresión de los receptores de LDL y, por tanto, la captación de LDL en las células hepáticas. Esto conduce a una reducción significativa de los niveles de LDL-C de alrededor del 60%, en combinación con dosis máximas de estatinas de hasta un 73% [6]. La concentración de triglicéridos y Lp(a) también se reduce en aproximadamente una cuarta parte, mientras que el nivel de HDL aumenta ligeramente. Los inhibidores de la PCSK9 (evolocumab, alirocumab) muestran una reducción significativa del riesgo cardiovascular debido a estos efectos. Están indicados en Suiza para los pacientes con un riesgo cardiovascular muy elevado cuyos cambios en la dieta y el tratamiento de las LDL con estatinas a la dosis máxima tolerada (con o sin ezetimiba) no han permitido alcanzar los valores objetivo. Además, debe controlarse la presión arterial y, en el caso de la diabetes mellitus, el valor de HbA1c debe ser <8% y debe procurarse la abstinencia de nicotina. Es obligatorio obtener una consulta de costes de la aseguradora sanitaria.
Para la prevención secundaria, son elegibles para el tratamiento con inhibidores de la PCSK9: pacientes de alto riesgo con eventos cardiovasculares isquémicos ateroscleróticos y un LDL-C de >2,6 mmol/l, adultos con HF heterocigota y -para evolocumab- adultos y adolescentes a partir de 12 años con HF homocigota. En prevención primaria, los inhibidores de la PCSK9 están indicados en pacientes adultos y adolescentes de alto riesgo mayores de 12 años con HF heterocigota u homocigota grave y un LDL-C de >5,0 mmol/l. También existe una indicación para pacientes con HF heterocigota grave, un LDL-C de >4,5 mmol/l y al menos uno de los siguientes factores de riesgo: diabetes mellitus, Lp(a) >120 nmol/l o hipertensión grave.
El diagnóstico y la prescripción inicial, así como los controles periódicos, deben ser realizados por un FMH especialista en angiología, diabetología/endocrinología, cardiología, nefrología, neurología o por expertos en hipercolesterolemia designados. El tratamiento con inhibidores de la PCSK9 sólo debe continuarse si tiene éxito. Esto significa que, en un control realizado en los seis meses siguientes al inicio del tratamiento, el LDL-C debería haberse reducido al menos un 40% respecto al valor basal con el tratamiento hipolipemiante de máxima intensidad o debería haberse alcanzado un valor de LDL <1,8 mmol/l. Esto no se aplica a las personas con HF homocigótica.
Mensajes para llevarse a casa
- El LDL-C es una de las principales causas del desarrollo de enfermedades cardiovasculares.
- En los pacientes con un riesgo cardiovascular muy elevado, el tratamiento intensivo debe tener como objetivo una reducción del 50% del LDL-C y un valor objetivo de LDL-C de <1,4 mmol/l; en los pacientes con un riesgo elevado, también debe perseguirse una reducción del 50% y un valor objetivo de <1,8 mmol/l. Cabe señalar que la duración de la exposición a la hipercolesterolemia también es crucial.
- Si no se alcanzan los niveles objetivo con estatinas y ezetimiba a la dosis máxima tolerable durante al menos tres meses, deben utilizarse inhibidores de la PCSK9 en pacientes con un riesgo cardiovascular muy elevado.
- Los pacientes con hipercolesterolemia familiar y al menos un factor de riesgo cardiovascular se consideran de alto riesgo. También deben recibir un tratamiento intensivo (estatinas, ezetimiba e inhibidores de la PCSK9) con un LDL-C >5,0 mmol/l o >4,5 mmol/l más otros factores de riesgo.
- Debe remitirse a un especialista si fracasa el tratamiento intensivo con LDL, en pacientes de riesgo alto o muy alto, o en pacientes con hipercolesterolemia familiar, o si están presentes determinados factores de riesgo cardiovascular.
- En caso de hipercolesterolemia familiar, el cribado familiar es obligatorio y se recomienda el esclarecimiento genético.

Literatura:
- Carballo D, Mach F: Reducción intensiva del colesterol LDL e inhibición de la inflamación para reducir aún más el riesgo cardiovascular. Medicina cardiovascular 2018; 21(12): 310-315.
- Baigent C, et al.: Cholesterol Treatment Trialists Collaboration: Efficacy and safety of more intensive lowering of LDL cholesterol: a metaanalysis of data from 170.000 participants in 26 randomised trials. Lancet 2010; 376: 1670-1681.
- www.swissheart.ch/de/herzkrankheiten-hirnschlag/erkrankungen/familiaere-hypercholesterinaemie.html.
- Rodondi N: ¿Se debe examinar a los pacientes para detectar la hipercolesterolemia familiar en la consulta del médico? Foro Med Suiza 2014; 14(19): 377.
- www.swissheart.ch.
- Riesen WF et al: Nuevas directrices sobre dislipidemia de la ESC/EAS. Foro Médico Suizo 2020; 20(9-10): 140-148.
- Mach F, et al: 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Revista Europea del Corazón 2019; doi: 10.1093/eurheartj/ehz455.
- AGLA: Prevención de la aterosclerosis Enfoque en la dislipidemia 2020; www.agla.ch.
- Weingärtner O, et al: Comentario de las directrices ESC/EAS (2019) sobre el diagnóstico y el tratamiento de las dislipidemias. Cardiólogo 2020; 14: 256-266.
- McCormack T, et al: Los niveles muy bajos de LDL-C pueden proporcionar con seguridad un beneficio cardiovascular clínico adicional: las pruebas hasta la fecha. Int J Clin Pract 2016; 70(11): 886-897; doi: 10.1111/ijcp.12881.
- Sattar N, et al: Estatinas y riesgo de diabetes incidente: un metaanálisis colaborativo de ensayos aleatorizados de estatinas. 2010 Feb 27; 375(9716): 735-742.
- Pandor A, et al: Monoterapia con ezetimiba para la reducción del colesterol en 2.722 personas: revisión sistemática y metaanálisis de ensayos controlados aleatorizados. J Intern Med 2009; 265(5): 568-580; doi: 10.1111/j.1365-2796.2008.02062.x.
PRÁCTICA GP 2021; 16(10): 9-13