El tratamiento de la artritis reumatoide (AR) ha progresado notablemente en los últimos años, pero la terapia sigue siendo un reto para muchos pacientes: hasta el 60% de los afectados no responden al tratamiento inicial o pierden su respuesta a la terapia con el paso del tiempo [2]. Los inhibidores del TNF (TNFi) se siguen utilizando a menudo de forma rutinaria como terapias de primera línea tras los (cs)DMARD sintéticos convencionales y, en caso de respuesta insuficiente cambiaron a un segundo TNFi, lo que se conoce como ciclo de TNFi [3]. Los datos actuales sugieren ahora que esta práctica debería reconsiderarse: en lugar de otro ciclo de TNFi, el cambio a sustancias con un mecanismo de acción diferente, como los inhibidores de la Janus quinasa (JAKi), podría ser beneficioso para los pacientes [1].
En las recomendaciones actuales para el tratamiento de la AR, la remisión clínica es el objetivo principal del tratamiento [4]. [5-7] La remisión es de vital importancia para los pacientes, ya que no sólo ralentiza la progresión del daño articular, sino que también mejora significativamente el bienestar psicológico y el funcionamiento físico de los afectados . [8-10] La remisión precoz, en particular, es crucial para los efectos a largo plazo de la enfermedad . Los datos de los estudios y losresultados comunicados por los pacientes(PRO) muestran que la remisión precoz está asociada a la remisión a largo plazo [8, 9]. No obstante, alrededor del 30-40 % de los pacientes con AR que inician una terapia de primera línea con TNFi interrumpen el tratamiento debido a un fracaso primario, una falta de respuesta secundaria o una intolerancia [1]. En estos casos, es especialmente importante cambiar rápidamente a una terapia alternativa conjunta para mantener la posibilidad de una remisión duradera y no perder el control de la enfermedad.
Ciclismo vs. conmutación
El Colegio Americano de Reumatología (ACR) recomienda el cambio a un bDMARD o tsDMARD de otra clase de fármacos en la AR tras el fracaso de un agente terapéutico biológico o específico de diana inicial (bDMARD o tsDMARD), mientras que la Alianza Europea de Asociaciones de Reumatología (EULAR) recomienda el cambio a otro mecanismo de acción y el ciclado [4, 11]. [12] Tanto el tratamiento cíclico con TNFi como el cambio a un mecanismo de acción alternativo se utilizan con frecuencia cuando fracasa la terapia con TNFi . [13] Sin embargo, los datos de los estudios demuestran que los pacientes que se someten a varios ciclos de TNFi tienen más probabilidades de fracasar en la terapia y volver a cambiar . [14,15] Sin embargo, el cambio a un mecanismo de acción diferente se asociaría a una mayor probabilidad de mejoría clínica y a una menor tasa de abandonos .
Upadacitinib favorable para el cambio
Un estudio multinacional que analizó los datos del registro de 503 pacientes con AR tras el fracaso de la terapia con TNFi de primera línea investigó el éxito de diferentes terapias de seguimiento [1]. Se comparó a los pacientes con un cambio al JAKi upadacitinib (RINVOQ®, UPA, n=261), un segundo TNFi (n=128) o un DMARD con un mecanismo de acción diferente (n=114) [1, 16]. Los pacientes que cambiaron de un TNFi a un UPA obtuvieron resultados clínicos significativamente mejores que los que recibieron un segundo TNFi. Por ejemplo, el 67,7 % de los pacientes con UPA alcanzaron la remisión en comparación con el 40,3 % de los que recibieron un segundo TNFi (p=0,002). La ausencia de dolor fue mayor con UPA (55,7 % frente a 25,4 %, p=0,001) y la adherencia fue del 60 % frente al 34,2 % entre los pacientes con TNFi (p=0,005) (Fig. 1) [1]. El AUP también fue superior a un FAME con un mecanismo de acción diferente en los tres aspectos. [17] Además, los datos a 5 años del estudio SELECT-COMPARE publicados recientemente subrayan que un cambio de mecanismo de acción parece ser beneficioso para los pacientes con AR que no alcanzaron su objetivo de tratamiento y que esta ventaja puede mantenerse a largo plazo . [17] El estudio mostró diferencias numéricas principalmente a favor de los pacientes que cambiaron de ADA a UPA . Sin embargo, no sólo en la AR, sino también en la artritis psoriásica (APs) y la espondiloartritis axial (axEspA), los datos de los estudios indican que los pacientes responden peor a un segundo o tercer TNFi que al primero [12, 18, 19].
El upadacitinib también es beneficioso como terapia de primera línea tras los csDMARD
La eficacia de UPA frente a TNFi como tratamiento de primera línea se comparó en los estudios cara a cara del programa SELECT-COMPARE [20, 21]. UPA + metotrexato (MTX) mostraron una eficacia significativamente mayor que adalimumab (ADA) + MTX en diversos parámetros como DAS28≤2,6, ACR50, cambio en HAQ-DI y alivio del dolor desde las 12 semanas [20, 21]. [21] También se pudo demostrar una mayor remisión sostenida con UPA + MTX en comparación con ADA + MTX a lo largo de 5 años . En la actualidad, varios estudios reales han demostrado también la buena eficacia y la larga duración del tratamiento con upadacitinib en la práctica diaria [22, 23]. [24] Además, los datos de hasta 7,5 años publicados en EULAR 2024 confirman el conocido perfil de seguridad de UPA en más de 4.700 pacientes .
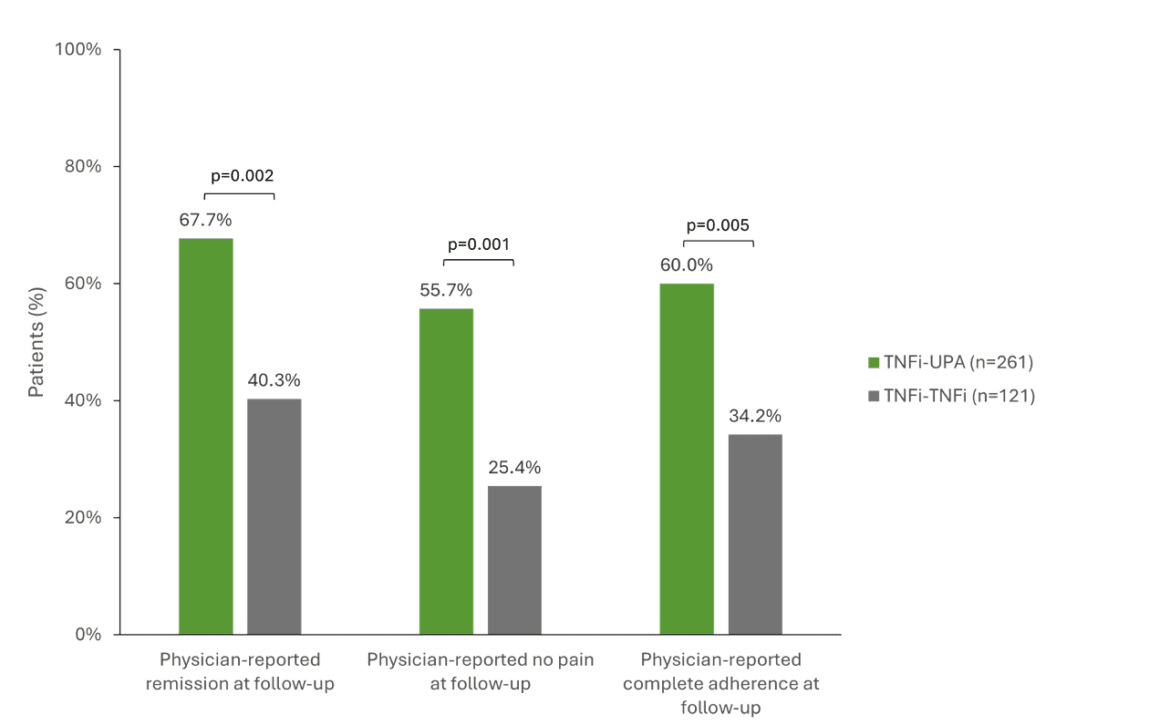
Fig. 1: Resultados clínicos significativamente mejores al cambiar a UPA (TNFi-UPA) en comparación con un segundo TNFi (TNFi-TNFi). TNFi = inhibidor del TNF, UPA = upadacitinib. Adaptado de [1].
Conclusión
Los datos disponibles sugieren que el cambio de TNFi a UPA puede ser una opción de tratamiento favorable para los pacientes con AR que no han respondido adecuadamente o no toleran el tratamiento inicial con TNFi [1]. En comparación con el ciclo con TNFi, el cambio a AUP con un mecanismo de acción alternativo ofrece mejores posibilidades de remisión, ausencia de dolor y adherencia al tratamiento [1]. Estos hallazgos respaldan la recomendación de cambiar a un mecanismo de acción alternativo en una fase temprana para mejorar los resultados del tratamiento a largo plazo de los pacientes con AR y aumentar las posibilidades de una remisión duradera.
Abreviaturas: ACR = Colegio Americano de Reumatología; ACR50 = respuesta ACR con una mejoría ≥50%; ADA = adalimumab; axSpA = espondiloartritis axial; csDMARD = DMARD sintético convencional; DAS28 = puntuación de la actividad de la enfermedad 28; DMARD = fármacos antirreumáticos modificadores de la enfermedad; EULAR = Alianza Europea de Asociaciones de Reumatología; HAQ-DI = Índice de Discapacidad del Cuestionario de Evaluación de la Salud; JAK = Janus quinasa; JAKi = inhibidor de JAK; MTX = metotrexato; PRO = resultados comunicados por los pacientes; APs = artritis psoriásica; AR = artritis reumatoide; T2T = tratamiento según objetivo; TNF = factor de necrosis tumoral; TNFi = inhibidor del TNF; UPA = upadacitinib.
Breve información técnica RINVOQ

Este artículo se ha elaborado con el apoyo financiero de AbbVie AG, Alte Steinhauserstrasse 14, 6330 Cham.
Este artículo se ha publicado en alemán. Texto: Dr sc. nat.
Stefanie Jovanovic CH-RNQ-240019 11/2024
Literatura
1 Caporali, R., et al, A Real-World Comparison of Clinical Effectiveness in Patients with Rheumatoid Arthritis Treated with Upadacitinib, Tumour Necrosis Factor Inhibitors, and Other Advanced Therapies After Switching from an Initial Tumour Necrosis Factor Inhibitor. Adv Ther, 2024. 41(9): p. 3706-3721.
2 Vallejo-Yague, E., et al, Eficacia comparativa de los biológicos en pacientes con artritis reumatoide estratificados por el índice de masa corporal: un estudio de cohortes en un registro suizo. BMJ Open, 2024. 14(2): p. e074864.
3 Edgerton, C., et al, Real-World Treatment and Care Patterns in Patients With Rheumatoid Arthritis Initiating First-Line Tumour Necrosis Factor Inhibitor Therapy in the United States. ACR Open Rheumatol, 2024. 6(4): p. 179-188.
4 Smolen, J.S., et al, Recomendaciones de la EULAR para el tratamiento de la artritis reumatoide con fármacos antirreumáticos modificadores de la enfermedad sintéticos y biológicos: actualización de 20 22. Ann Rheum Dis, 2023. 82(1): p. 3-18.
5 Lillegraven, S., et al, Remisión y resultado radiográfico en la artritis reumatoide: aplicación de los criterios de remisión ACR/EULAR 2011 en una cohorte observacional. Ann Rheum Dis, 2012. 71(5): p. 681-6.
6 McInnes, I.B. y G. Schett, La patogénesis de la artritis reumatoide. N Engl J Med, 2011. 365(23): p. 2205-19.
7 Einarsson, J.T., et al, La remisión sostenida mejora la función física en pacientes con artritis reumatoide establecida y debería ser un objetivo del tratamiento: un estudio de cohortes observacional prospectivo del sur de Suecia. J Rheumatol, 2016. 43(6): p. 1017-23.
8 Ten Klooster, P.M., et al, Long-term clinical, functional, and cost outcomes for early rheumatoid arthritis patients who did or did not achieve early remission in a real-world treat-to-target strategy. Clin Rheumatol, 2019. 38(10): p. 2727-2736.
9 Xie, W., J. Li, y Z. Zhang, El impacto de diferentes conjuntos de criterios en la remisión precoz y la identificación de sus predictores en la artritis reumatoide: resultados de una cohorte observacional (2009-2018). Clin Rheumatol, 2020. 39(2): p. 381-389.
10 Snoeck Henkemans, S.V.J., et al, Resultados comunicados por los pacientes y progresión radiográfica en pacientes con artritis reumatoide en remisión sostenida frente a baja actividad de la enfermedad. RMD Open, 2024. 10(1).
11 Fraenkel, L., et al, 2021 American College of Rheumatology Guideline for the Treatment of Rheumatoid Arthritis. Arthritis Care Res (Hoboken), 2021. 73(7): p. 924-939.
12 Bogas, P., et al, Comparación de la eficacia a largo plazo entre agentes biológicos tras el fracaso del inhibidor del factor de necrosis tumoral en pacientes con artritis reumatoide: un estudio prospectivo de cohortes. Ther Adv Musculoskelet Dis, 2021. 13: p. 1759720×211060910.
13 Wei, W., et al, Treatment Persistence and Clinical Outcomes of Tumour Necrosis Factor Inhibitor Cycling or Switching to a New Mechanism of Action: Real-world Observational Study of Rheumatoid Arthritis Patients in the United States with Prior Tumour Necrosis Factor Inhibitor Therapy. Adv Ther, 2017. 34(8): p. 1936-1952.
14 Migliore, A., et al, Ciclado de los inhibidores del factor de necrosis tumoral frente al cambio a una terapia de mecanismo de acción diferente en pacientes con artritis reumatoide con respuesta inadecuada a los inhibidores del factor de necrosis tumoral: un metaanálisis de red bayesiano. Ther Adv Musculoskelet Dis, 2021. 13: p. 1759720×211002682.
15 Mann, H., et al, Switching to a Targeted Drug with a Different Mode of Action After Discontinuation of the First TNF Inhibitor Is Associated with Better Drug Survival Compared to a Second TNF Inhibitor in Rheumatoid Arthritis: A Propensity Score-matched Analysis from the Czech ATTRA Registry. Resumen 2277, presentado en la ACR Convergence, del 14 al 19 de noviembre de 2024, Washington DC, EE. UU.
16 Resumen actual de las características del producto de RINVOQ® (upadacitinib) en www.swissmedicinfo.ch.
17 Fleischmann, R., et al, Eficacia y seguridad a largo plazo tras el cambio entre upadacitinib y adalimumab en pacientes con artritis reumatoide: datos a 5 años de SELECT-COMPARE. Rheumatol Ther, 2024. 11(3): p. 599-615.
18 Linde, L., et al, Segundos y terceros inhibidores del TNF en pacientes europeos con espondiloartritis axial: eficacia e impacto del motivo del cambio. Reumatología (Oxford), 2024. 63(7): p. 1882-1892.
19 Ørnbjerg, L.M., et al, Eficacia farmacológica de los inhibidores del TNF 2º y 3º en la artritis psoriásica – relación con el motivo de abandono del tratamiento anterior. Joint Bone Spine, 2024. 91(4): p. 105729.
20 Fleischmann, R., et al, Upadacitinib Versus Placebo or Adalimumab in Patients With Rheumatoid Arthritis and an Inadequate Response to Methotrexate: Results of a Phase III, Double-Blind, Randomised Controlled Trial. Arthritis Rheumatol, 2019. 71(11): p. 1788-1800.
21 Fleischmann, R., et al, Seguridad y eficacia a largo plazo de upadacitinib frente a adalimumab en pacientes con artritis reumatoide: datos a 5 años del estudio de fase 3 aleatorizado SELECT-COMPARE. RMD Open, 2024. 10(2).
22 Witte, T., et al, El impacto de los niveles de proteína C reactiva en la eficacia del upadacitinib en pacientes con artritis reumatoide: un estudio alemán prospectivo y no intervencionista de 12 meses de duración. Clin Exp Rheumatol, 2024. 42(3): p. 726-735.
23 Bessette, L., et al, Real-World Effectiveness of Upadacitinib for Treatment of Rheumatoid Arthritis in Canadian Patients: Interim Results from the Prospective Observational CLOSE-UP Study. Rheumatol Ther, 2024. 11(3): p. 563-582.
24 Burmester GR, et al, Safety of Upadacitinib Across Rheumatoid Arthritis, Psoriatic Arthritis, and Axial Spondyloarthritis Encompassing 15,000 Patient-Years of Clinical Trial Data. Presentado en el Congreso Europeo de Reumatología (EULAR), 12-15 de junio de 2024, Viena, Austria. POS0894.
Los profesionales pueden solicitar las referencias en medinfo.ch@abbvie.com.











