El metilfenidato se utiliza en el tratamiento del TDAH desde hace décadas. Existen diferentes hipótesis sobre cómo despliega exactamente sus efectos este psicoestimulante. Una de ellas se refiere a que el metilfenidato afecta a la neurotransmisión dopaminérgica en el núcleo accumbens y las redes neuronales asociadas. Para averiguarlo, un equipo de investigación llevó a cabo un estudio de imagen.
El metilfenidato (MPH) es el fármaco de elección para el tratamiento del trastorno por déficit de atención con hiperactividad (TDAH) clínicamente relevante [1]. Ritalin® es el nombre comercial del preparado de HMP más antiguo y común. Otros medicamentos utilizados en Suiza que también contienen el principio activo MPH son Medikinet MR®, Equasym®, Focalin® y Concerta® [2]. Se distingue entre preparados de acción corta y prolongada. A menudo, se utiliza un preparado de MPH de acción corta al inicio del tratamiento, por ejemplo, el comprimido Ritalin® de 10 mg. El MPH en esta forma es absorbido rápidamente por el cuerpo y comienza a hacer efecto después de unos 30 minutos. Después de 3-4 horas, el efecto desaparece rápidamente. Además, existe la posibilidad de administrar estimulantes en forma de acción prolongada. En este caso, el principio activo se libera del comprimido con retraso y el efecto se mantiene de 7 a un máximo de 14 horas, según el preparado. Sin embargo, la información sobre la duración de la acción es sólo orientativa; la terapia puede adaptarse lo mejor posible a las necesidades del niño [3].
Examen por resonancia magnética en un diseño cruzado
Los investigadores llevaron a cabo un estudio cruzado aleatorizado, controlado con placebo y a doble ciego en el Hospital Universitario de Fukui (Japón) [4]. La edad media de los 27 niños con TDAH era de 10,6 años (DE 1,8; intervalo de edad: 7,3-15,5 años). En los 49 sujetos de control sin TDAH, la edad media era de 11,1 años (DE 2,3; rango de edad 6,1-15,6 años). Los criterios de inclusión se muestran en el recuadro. Los niños con TDAH fueron escaneados dos veces con resonancia magnética funcional en reposo en condiciones de metilfenidato y placebo. Durante la primera cita, se les administró MPH (1,0 ± 0,1 mg/kg) o placebo (lactosa) con liberación osmótica (OROS), como en estudios anteriores en condiciones de doble ciego. Entre cinco y ocho horas después de la administración, cuando la concentración de MPH en la sangre es máxima, los niños se sometieron a un examen de IRMf en estado de reposo y realizaron una prueba estandarizada de rendimiento continuo fuera del escáner de IRM. En la segunda cita (entre 1 y 6 semanas después de la primera cita), los niños con TDAH se sometieron a una RMf en estado de reposo y realizaron la prueba de rendimiento después de tomar la segunda medicación: los niños que habían tomado OROS-MPH en la primera cita recibieron el placebo en la segunda cita en condiciones de doble ciego y viceversa.
El grupo de control, es decir, los participantes del estudio sin TDAH, completaron el mismo escáner fMRI en reposo una vez sin OROS-MPH ni placebo.

Se ha demostrado que el metilfenidato modula la actividad neuronal
Se demostró que el metilfenidato (MPH) aumenta la actividad neuronal espontánea en el núcleo accumbens y en las redes de saliencia y modo por defecto [4].
- En la prueba de rendimiento, el MPH redujo significativamente los errores de omisión, el tiempo medio de reacción y la variabilidad de respuesta intraindividual durante una tarea (IIRV) en el grupo con TDAH (cada uno p<0,001).
- La modulación inducida por el metilfenidato de la actividad neuronal espontánea en la red de modo por defecto predijo el efecto del tratamiento en términos de variabilidad de la respuesta intraindividual (IIRV) (r=-0,46, p=0,016).
- En cuanto a los efectos del MPH sobre la actividad neuronal espontánea en el núcleo accumbens, la amplitud de las fluctuaciones de baja frecuencia (ALFF) en el núcleo accumbens derecho fue significativamente mayor en la condición TDAH-MPH que en la condición TDAH-placebo (p<0,05, corregido por Bonferroni, d de Cohen=0,55).
- El ALFF fue significativamente mayor en las redes de saliencia (SN) y en la red de modos por defecto (DMN) en la condición TDAH-MPH que en la condición TDAH-placebo (SN: p<0,05, d de Cohen=0,57; DMN: p<0,01, d de Cohen=0,66; corregido por Bonferroni en cada caso). No hubo diferencias significativas en la red frontoparietal izquierda y derecha (p>0,05). El análisis de regresión lineal múltiple reveló que sólo la modulación por MPH del patrón de similitud ALFF dentro de la red de modos por defecto se asoció significativamente con los efectos del fármaco sobre la variabilidad de la respuesta intraindividual (Tabla 1) . Esto indica que se trata de un mecanismo de acción neurobiológico crucial.
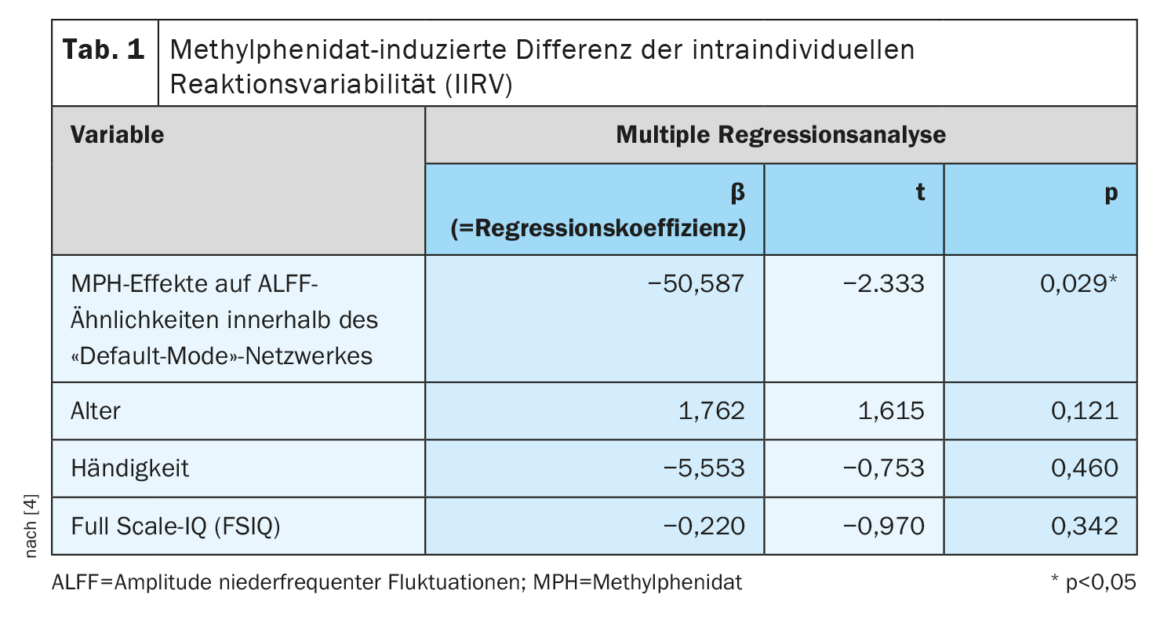
Estos hallazgos amplían la comprensión actual de los mecanismos neurobiológicos que subyacen al tratamiento con MPH en niños con TDAH y, según los autores del estudio, podrían permitir en el futuro derivar biomarcadores clínicamente útiles para evaluar el éxito del tratamiento.
Literatura:
- Praxis Suchtmedizin Schweiz, www.praxis-suchtmedizin.ch/praxis-suchtmedizin/index.php/de/medikamente/einleitung-mh, (último acceso 10.02.2023)
- Swissmedic: Arzneimittelinformation, www.swissmedicinfo.ch, (último acceso 10.02.2023)
- «Die medikamentöse Behandlung von Kindern und Jugendlichen mit einer Aufmerksamkeitsdefizit-Hyperaktivitätsstörung ADHS», März 2022,
www.pukzh.ch/sites/default/assets/File/
Informationen%20Stimulanzien%20und%20Ritalin.pdf, (último acceso 10.02.2023) - Mizuno Y, et al.: Methylphenidate Enhances Spontaneous Fluctuations in Reward and Cognitive Control Networks in Children With Attention-Deficit/Hyperactivity Disorder. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, available online 23 October 2022, www.sciencedirect.com/science/article/pii/S2451902222002476, (último acceso 10.02.2023)
HAUSARZT PRAXIS 2023; 18(2): 24–25
InFo NEUROLOGIE & PSYCHIATRIE 2023; 21(2): 30–31