La terapia de la leucemia linfocítica crónica (LLC) está experimentando actualmente rápidos cambios. Cada vez más, la quimioinmunoterapia, habitual hasta ahora, está siendo sustituida por métodos de tratamiento más específicos. Además de nuevos agentes activos como el inhibidor de la BTK acalabrutinib, también son objeto de estudios actuales diversas terapias combinadas y secuencias de tratamiento.
Al ser la enfermedad leucémica más común en Europa Central, la LLC afecta especialmente a las personas mayores. Éstos podrían beneficiarse pronto de nuevos conocimientos sobre la estrategia de tratamiento óptima. En el contexto del cambio demográfico, que sugiere un nuevo aumento del número de casos en casi un 30% en los próximos 25 años, también es deseable un progreso en la terapia a nivel epidemiológico [1].
Centrarse en las vías de señalización
Desde hace varios años, la vía de señalización del receptor de células B desempeña un papel importante en el tratamiento de la LLC. El crecimiento maligno depende en gran medida de su activación y el bloqueo de quinasas críticas como la BTK (tirosina quinasa de Bruton) y la PI3K (fosfoinsoditida 3 quinasa) puede utilizarse terapéuticamente. El bloqueante de PI3K idelalisib se utiliza principalmente en las últimas líneas de terapia [1]. Los inhibidores de la BTK, por su parte, han llegado ahora a la terapia de primera línea como monoterapia o en combinación con anticuerpos anti-CD20, independientemente del estado de la mutación y de la edad (Fig. 1) [1]. Mientras que el ibrutinib está aprobado en Suiza desde 2014, el inhibidor de BTK de segunda generación acalabrutinib aún no ha sido aprobado en este país [2]. La Agencia Europea del Medicamento ha dado luz verde al acalabrutinib en 2020 [3].
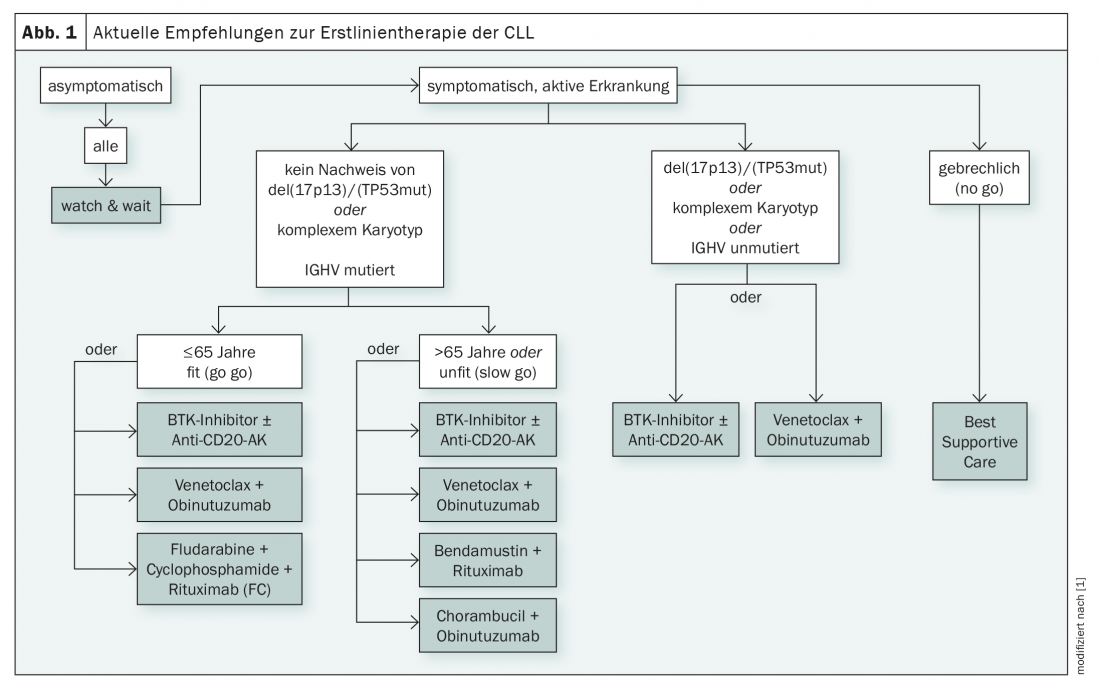
Además de la vía de señalización del receptor de células B, las vías de transducción dependientes de BCL-2 también son patogénicamente significativas para la LLC. El efecto pro-apoptótico de los miméticos deBH3 (Bcl2-dominio-homológico-3)puede contrarrestar este mecanismo causante de la enfermedad. El venetoclax es un agente pontente que se utiliza junto con el anticuerpo anti-CD20 obinutuzumab en la primera línea de tratamiento [1].
Con el gran número de opciones terapéuticas disponibles en la actualidad, elegir el mejor tratamiento no siempre es fácil. Para complicar las cosas, existe una avalancha algo opaca de nuevos datos que probablemente darán forma a las directrices en los próximos años.
Los nuevos inhibidores de la BTK se muestran prometedores en los estudios
En particular, recientemente se han publicado datos interesantes sobre el inhibidor de la BTK acalabrutinib, que ya ha sido aprobado por la Agencia Europea del Medicamento. Mientras que el nuevo agente se probó en pacientes no tratados previamente en el ensayo ELEVATE TN2, el ensayo ASCEND3 probó su uso en la LLC recidivante o refractaria [4,5].
En la terapia de primera línea, el acalabrutinib como monoterapia así como en combinación con obinutuzumab mostró una prolongación significativa de la supervivencia libre de progresión en comparación con la quimioterapia estándar con clorambucil y obinutuzumab. La terapia combinada dio lugar a una reducción del riesgo de progresión de la enfermedad del 90%, mientras que la monoterapia dio lugar a una reducción del riesgo correspondiente del 80%. Después de 24 meses, la tasa de supervivencia sin progresión con acalabrutinib-obinutuzumab fue del 93%, mientras que la de la monoterapia con acalabrutinib fue del 87%. En comparación, sólo el 47% de los pacientes que recibieron quimioterapia estándar seguían sin progresión al cabo de dos años [4].
Al igual que en la primera línea, la nueva sustancia también ofreció resultados prometedores en las líneas de tratamiento posteriores. En el estudio ASCEND, el 88% de los pacientes en tratamiento con acalabrutinib permanecían libres de progresión de la enfermedad al cabo de un año, frente al 68% en el brazo de control. La monoterapia con acalabrutinib se comparó con la terapia de combinación idelalisib/rituximab o bendamustina/rituximab [5]. Ambos estudios mostraron un perfil de seguridad aceptable, en consonancia con hallazgos anteriores.
Aunque aún faltan resultados a largo plazo y datos sobre la supervivencia global, el acalabrutinib es un candidato candente para su uso generalizado en la LLC en un futuro próximo, también en Suiza. En la actualidad, se están llevando a cabo más de 70 estudios sobre la nueva sustancia activa. Entre ellos se incluyen estudios sobre aplicaciones en otras neoplasias de células B, como el linfoma de células del manto o el linfoma no Hodgkin, así como sobre diversas combinaciones de fármacos [6].
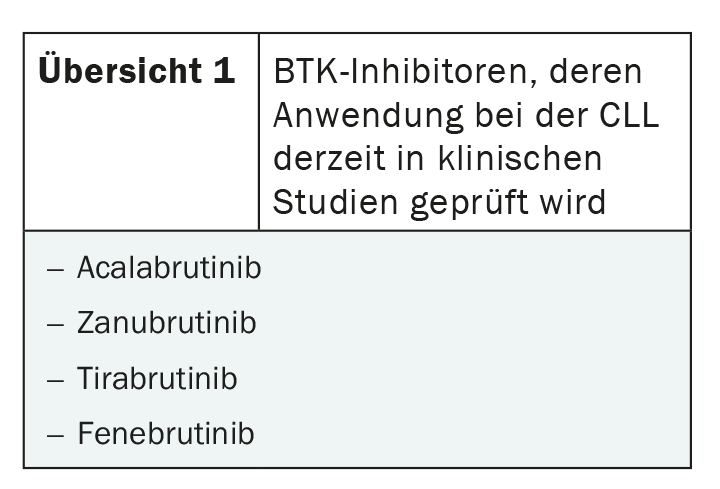
Junto con el zanubrutinib, el tirabrutinib y el fenebrutinib, existen otros nuevos inhibidores de la BTK cuyo uso se está probando actualmente en la LLC (resumen 1). Un estudio chino de fase II concluyó que el zanubrutinib era bien tolerado en las últimas líneas de terapia y mostró altas tasas de respuesta del 84,6% [7]. Se están realizando más estudios, por ejemplo sobre el uso en pacientes que ya han sufrido una progresión bajo terapia con inhibidores de la BTK, pero también sobre el uso en primera línea [6,8]. Al igual que el zanubrutinib, el tirabrutinib se ha examinado hasta ahora especialmente en la LLC refractaria y recidivante. En combinación con idelalisib y con o sin obinutuzumab, se observaron tasas de respuesta global del 60% en la combinación de dos fármacos y superiores al 90% en la combinación de tres fármacos en el estudio de fase II CLLRUmbrella1 [9]. Aún no se han publicado resultados sobre el uso de fenebrutinib en la LLC, que actualmente se está investigando en ensayos de fase I.
¿Qué más hay en proyecto?
No sólo los inhibidores de la BTK son objeto de la investigación actual, sino también otras diversas sustancias activas. Por ejemplo, actualmente se está investigando el uso de primera línea del antagonista del receptor de interleucina-1 anakinra en un ensayo de fase I [10]. Esta sustancia, que hasta ahora se ha utilizado principalmente para la artritis reumatoide, tampoco está aprobada aún en Suiza. Además, se están realizando estudios sobre el nuevo inhibidor de PI3K umbralisib en diferentes estadios de la enfermedad y combinaciones de fármacos [6]. Se espera que la FDA apruebe este fármaco este mismo año [11]. La metformina, el inhibidor de BCL-2 navitoclax (ABT-263), varias vacunas como Oncoquest-CLL, IO103 e IO120, el anticuerpo monoclonal anti-CD20 ofatumumab y varios agentes más podrían desempeñar pronto un papel en el tratamiento [6]. Al igual que en otras áreas de la oncología, también se están investigando enfoques inmunoterapéuticos para el tratamiento de la LLC, incluido el anticuerpo biespecífico epcoritamab [12].
Con la abrumadora cantidad de nuevos agentes potenciales y ya aprobados para el tratamiento de la LLC, se plantea cada vez más la cuestión de las combinaciones y secuencias terapéuticas óptimas, así como de los biomarcadores para seleccionar la mejor población posible de pacientes. Actualmente se están llevando a cabo investigaciones diligentes a este respecto y cabe esperar los primeros resultados en un futuro próximo.
¿El trasplante de células madre pronto quedará obsoleto?
El único enfoque curativo de la LLC sigue siendo el trasplante alogénico de células madre, pero con la disponibilidad de terapias moleculares altamente eficaces, éste está pasando cada vez más a un segundo plano. Hoy en día, sólo es una opción en situaciones cuyo pronóstico es desfavorable, incluso con las nuevas opciones de tratamiento disponibles. El desarrollo de agentes innovadores y la investigación de distintos regímenes terapéuticos podrían impulsar aún más el trasplante alogénico de células madre para la LLC en un futuro próximo. Esperemos que así sea.
Literatura:
- Wendtner C-M, et al: Leucemia linfocítica crónica (LLC) – Onkopedia. Septiembre de 2020. www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html (última consulta: 24.01.2021).
- swissmedic Schweizerisches Heilmittelinstitut: Arzneimittelinformation. www.swissmedicinfo.ch/ (fecha de acceso: 24.01.2021)
- EMA: Calquence. www.ema.europa.eu/en/medicines/human/EPAR/calquence (fecha de acceso: 24.01.2021)
- Sharman JP, et al: Acalabrutinib con o sin obinutuzumab frente a clorambucil y obinutuzmab para la leucemia linfocítica crónica sin tratamiento (ELEVATE TN): un ensayo aleatorizado, controlado, de fase 3. Lancet. 2020; 395(10232): 1278-91.
- Ghia P, et al: ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol. 2020; 38(25): 2849-61.
- ClinicalTrials.gov. www.clinicaltrials.gov (fecha de acceso: 24.01.2021)
- Xu W, et al: Treatment of relapsed/refractory chronic lymphocytic leukemia/small lymphocytic lymphoma with the BTK inhibitor zanubrutinib: phase 2, single-arm, multicenter study. Revista de hematología y oncología. 2020; 13(1): 48.
- Tam CS, et al: Monoterapia con zanubrutinib para pacientes con leucemia linfocítica crónica naïve al tratamiento y deleción 17p. Haematologica. 2020; Epub en línea antes de impresión.
- Seguridad y eficacia de la combinación de tirabrutinib e idelalisib con y sin obinutuzumab en adultos con leucemia linfocítica crónica (LLC) recidivante o resistente al tratamiento – Resultados del estudio – ClinicalTrials.gov. https://clinicaltrials.gov/ct2/show/results/NCT02968563 (fecha de acceso: 24.01.2021)
- Anakinra en pacientes con leucemia linfocítica crónica no tratados previamente – Full Text View – ClinicalTrials.gov. https://clinicaltrials.gov/ct2/show/NCT04691765 (fecha de acceso: 24.01.2021)
- Rai-Roche S.: Es probable que el umbralisib y el ublituximab de TG Therapeutics se enfrenten a obstáculos en el mercado, pero la aprobación de la FDA es muy esperada. Tecnología farmacéutica. 2020. www.pharmaceutical-technology.com/comment/tg-therapeutics-umbralisib-ublituximab-likely-to-face-market-hurdles-but-fda-approval-highly-expected/ (última consulta: 24.01.2021).
- Estudio de seguridad y eficacia de epcoritamab en sujetos con leucemia linfocítica crónica recidivante/refractaria – Full Text View – ClinicalTrials.gov. https://clinicaltrials.gov/ct2/show/NCT04623541 (fecha de acceso: 24.01.2021)
InFo ONCOLOGÍA Y HEMATOLOGÍA 2021; 9(1): 24-25