¿Qué beneficios pueden esperar los pacientes con esclerosis múltiple remitente-recurrente (EMR) del tratamiento de primera línea con ofatumumab (KESIMPTA®)? La respuesta a esta pregunta la proporcionó un análisis de subgrupos de los datos de los pacientes sin tratamiento de los dos ensayos ASCLEPIOS. Aquí se demostró que los pacientes que tomaban ofatumumab tenían una menor actividad de la enfermedad y una progresión más lenta en comparación con la teriflunomida. La tolerabilidad fue comparable a la de la población general del estudio y la adherencia fue correspondientemente alta.
Cada vez hay más datos que sugieren que el uso precoz de una terapia de alta eficacia (TRH) tiene un impacto más positivo en la progresión de la enfermedad que empezar con una opción moderadamente eficaz e ir aumentando la terapia a medida que la enfermedad empeora. Por ejemplo, un análisis de 592 pacientes británicos descubrió que el uso precoz de la THS producía mejores resultados en cuanto a la tasa anual de recaídas, la puntuación de la Escala Expandida del Estado de Discapacidad (EDSS) y la acumulación de discapacidad sostenida durante un periodo de cinco años en comparación con la terapia de intensificación.1 Los anticuerpos monoclonales se consideraron TRH, al resto de terapias modificadoras de la enfermedad se les asignó una eficacia moderada. Además, en un análisis retrospectivo, se comparó a 213 pacientes con THS precoz (iniciada en los 2 años siguientes al inicio de la enfermedad) con un grupo emparejado de 253 pacientes que iniciaron la THS sólo entre 4 y 6 años después del inicio de la enfermedad.2 Esto demostró que las pacientes que empezaron la THS pronto tenían una puntuación media de EDSS significativamente más baja después de 6 a 10 años que las pacientes que empezaron la THS más tarde (2,3 frente a 3,5 después de 10 años; p < 0,0001). Sin embargo, estas opciones tempranas también deben tener un buen perfil de seguridad y no suponer una carga para los pacientes y su adherencia con las frecuentes citas de tratamiento y seguimiento y cualquier tratamiento previo necesario.
ASCLEPIOS I y II: Análisis de subgrupos de pacientes sin tratamiento previo
El anticuerpo anti-CD20 totalmente humano ofatumumab es una opción nueva y muy eficaz para el tratamiento de primera línea del EMR.3,4 La eficacia y seguridad del ofatumumab en el tratamiento de pacientes con EMR se investigó en los dos estudios multicéntricos, de diseño idéntico, doble ciego, con control activo, doble simulación y de grupos paralelos ASCLEPIOS I (n = 927) y ASCLEPIOS II (n = 955).5 Se eligió la teriflunomida como comparador. Los pacientes incluidos en el brazo de ofatumumab recibieron una dosis inicial de 20 mg de ofatumumab por vía subcutánea (s.c.) los días 0, 7 y 14, seguida de una dosis mensual de mantenimiento (también de 20 mg) y placebo por vía oral. La terapia de mantenimiento podría ser aplicada por los propios pacientes en casa. El grupo de comparación fue tratado con 14 mg de teriflunomida al día y placebo s.c.. La duración del estudio fue flexible y de un máximo de 30 meses.
En un análisis de subgrupos, se investigó el perfil beneficio-riesgo del tratamiento con ofatumumab en pacientes con enfermedad en estadio temprano (≤ 3 años desde el diagnóstico).6 Esto suponía aproximadamente un tercio de la población total de ASCLEPIOS (314 pacientes con ofatumumab, 301 pacientes con teriflunomida). La mediana de edad de estos pacientes era de 36 años y la mediana de tiempo transcurrido desde el diagnóstico era de 0,35 años.
Pacientes sin tratamiento: Resultados coherentes con la población total de ASCLEPIOS
El análisis de los datos de los pacientes sin tratamiento demostró que el tratamiento con ofatumumab condujo a una reducción significativa de la tasa anualizada de recaídas (TRA) del 50,3% en comparación con la teriflu- nomida (p < 0,001).6 Además, el empeoramiento confirmado de la discapacidad (CDW) a lo largo de 6 meses se redujo en un 46% con ofatumumab en comparación con teriflunomida (p=0,044). Este resultado, así como el de la TDC a 3 meses (38% de reducción del riesgo; p=0,065), fue coherente con el de la población general. El análisis de diversos parámetros de imagen confirmó la superioridad del ofatumumab (Fig. 1). Así, el número de lesiones T1 positivas al gadolinio (Gd) por exploración se redujo significativamente en un 95,4% con el ofatumumab en comparación con la teriflunomida (p <0,001). El número de lesiones T2 nuevas/ampliadas también disminuyó significativamente en un 82,0% al año (p < 0,001). En el segundo año de tratamiento, se observó una reducción del 97,1% de las lesiones T2 con ofatumumab en comparación con la teriflunomida (p < 0,001).
 Fig. 1. El ofatumumab consiguió resultados significativamente mejores en pacientes con EM sin tratamiento en comparación con la teriflunomida en varios parámetros de imagen.6
Fig. 1. El ofatumumab consiguió resultados significativamente mejores en pacientes con EM sin tratamiento en comparación con la teriflunomida en varios parámetros de imagen.6
Uno de los objetivos del éxito del tratamiento de la EM es la NEDA (No Evidencia de Actividad de la Enfermedad).7 La NEDA-3 se define por la ausencia de recaídas (1), progresión de la discapacidad (2) y actividad radiológica (3). Resultó que la probabilidad de lograr NEDA-3 con el tratamiento con ofatumumab fue más de 3 veces superior que con teriflunomida en el primer año de tratamiento e incluso más de 14 veces superior en el segundo año de tratamiento para los pacientes sin tratamiento en los dos estudios ASCLEPIOS (Fig. 2).6
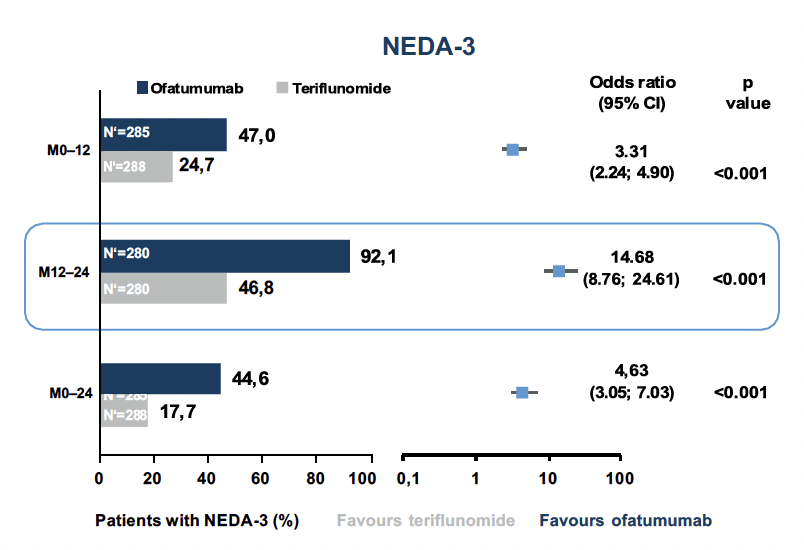 Fig. 2 La probabilidad de lograr NEDA-3 fue significativamente mayor con ofatumumab que con teriflunomida.6
Fig. 2 La probabilidad de lograr NEDA-3 fue significativamente mayor con ofatumumab que con teriflunomida.6
Perfil favorable de efectos secundarios
El análisis de los efectos secundarios dejó claro que la buena eficacia del ofatumumab no va en detrimento de la tolerabilidad. En la población global de los dos estudios ASCLEPIOS, se produjeron acontecimientos adversos en el 83,6% de los pacientes que recibieron ofatumumab y en el 84,2% de los pacientes que recibieron teriflunomida.5 Se registraron acontecimientos graves en el 9,1% y el 7,9% de los pacientes, respectivamente. Las reacciones asociadas a la inyección fueron las más comunes. Se produjeron en el 20,2% de los pacientes del grupo de ofatumumab y en el 15,0% de los pacientes del grupo de teriflunomida. Las reacciones sistémicas a la inyección fueron leves o moderadas en más del 99% de los casos. Se produjeron principalmente tras la primera inyección y disminuyeron significativamente con las aplicaciones posteriores. Se registraron infecciones en el 51,6% de los pacientes tratados con Ofa- tumumab y en el 52,7% de los tratados con teriflunomida. Las más comunes fueron la na- faringitis (18% ofatumumab, 16,7% teriflunomida), las infecciones de las vías respiratorias superiores (10,3% frente a 12,8%) y las infecciones de las vías urinarias (10,3% frente a 8,3%).
El análisis del grupo de pacientes sin tratamiento mostró una incidencia equilibrada de acontecimientos adversos entre los dos grupos de tratamiento.6 La tasa de acontecimientos adversos graves fue menor en el grupo sin tratamiento que en la población general, pero siguió siendo comparable entre los grupos de ofatumumab y teriflunomida. No se registraron casos de infecciones oportunistas como la LMP (leucoencefalopatía multifocal progresiva) o la reactivación de la hepatitis B. La adherencia al ofatumumab en los pacientes tratados fue alta, del 98,8%, y casi idéntica a la adherencia en la población general de ASCLEPIOS (98,3%).
Conclusión
Cada vez hay más datos que sugieren que el uso precoz de una terapia altamente eficaz tiene un impacto más positivo en el curso de la enfermedad que la intensificación de la terapia cuando la enfermedad empeora. Sin embargo, las terapias altamente eficaces suelen ir asociadas a un perfil de seguridad limitado. Como demostraron los dos estudios ASCLEPIOS, el ofatumumab demostró ser muy eficaz no sólo en la población general, sino especialmente en pacientes no tratados previamente en una fase temprana de la enfermedad. Además, el perfil de efectos secundarios en los pacientes sin tratamiento previo fue comparativamente favorable que en los pacientes ya pretratados. Tras iniciar la terapia bajo la supervisión del médico tratante, los pacientes pueden autoadministrarse fácilmente KESIMPTA® (ofatumumab), una vez al mes con una pluma autoinyectora subcutánea. Además, no es necesaria ninguna premedicación, ninguna estancia hospitalaria ni ninguna fase de observación posterior durante la aplicación. La adherencia de los pacientes sin tratamiento, así como de la población total, fue superior al 95% en los estudios ASCLEPIOS.
Este artículo ha sido elaborado por Novartis Pharma Schweiz AG, Suurstoffi 14, 6343 Rotkreuz, Suiza.
NO55104/04.2021