En el Congreso Europeo sobre el Cáncer celebrado en Viena se presentaron nuevos hallazgos sobre la posible etiología del linfoma de Hodgkin. Además, se presentó una comparación europea exhaustiva de la atención oncológica. En el campo del melanoma metastásico, se respondió a dos preguntas: ¿En qué medida los pacientes con factores de mal pronóstico se benefician de la inmunoterapia combinada? ¿Y cómo deben interpretarse los datos actuales de supervivencia del estudio COMBI-v?
Para comprender mejor la etiología del linfoma de Hodgkin (LH) en niños y adultos jóvenes, un equipo inglés estudió 621 casos registrados de LH en pacientes de 0 a 24 años (años 1968-2003). 247 de ellos eran del subtipo esclerosante nodular, 105 eran del tipo mixto, 58 eran LH rico en linfocitos (tipo con mejor pronóstico), 68 entraban en la categoría “otros” y 143 en la categoría “sin especificar más”.
En general, había más pacientes varones con LH. Esto también fue cierto para el subtipo de LH esclerosante nodular, con 130 varones frente a 117 mujeres afectados. Curiosamente, sin embargo, se produjo un cambio relacionado con la edad en la proporción de sexos: en el grupo de 20-24 años predominaron las mujeres (72 frente a 55 personas). Entre los hombres jóvenes, las tasas específicas por edad fueron de 14,26 (por millón de personas/año), mientras que la cifra correspondiente a las mujeres jóvenes fue de 18,79.
Además del género, las privaciones también influyeron. Los investigadores los definieron a través de cuatro factores: Hogares con alta densidad de población, desempleo, sin vivienda en propiedad, hogares sin coche. La privación se asoció notablemente con tasas de incidencia más bajas del subtipo esclerosante nodular. Con cada aumento del 1% en el factor “densidad de personas en el hogar”, se produjo una reducción significativa del riesgo del 12% (RR 0,88; IC 95%: 0,82-0,94). Se observó una tendencia inversa en los tipos que no se especificaron más. Aquí el RR fue de 1,17. Para los demás subtipos, la privación no tuvo ningún efecto sobre la incidencia.
¿Cómo pueden explicarse los resultados?
Los datos son reveladores en varios aspectos. Por un lado, la inversión de la proporción de sexos podría explicarse por factores hormonales que intervienen durante la pubertad femenina, incluidos los estrógenos. Es posible que la etiología del subtipo esclerosante nodular también esté relacionada con los cambios hormonales femeninos, además de otros factores. Esta podría ser la razón por la que la incidencia en las mujeres aumenta después de la pubertad. Muchos genes están regulados directamente (pero también indirectamente) por las hormonas sexuales.
La menor incidencia de este subtipo en hogares hacinados también puede indicar un factor ambiental etiológico. Cuando las personas viven cerca unas de otras, hay más agentes infecciosos presentes. Las personas que se exponen a diferentes agentes patógenos a una edad temprana y pasan por múltiples infecciones pueden desarrollar un sistema inmunológico más fuerte y capaz de responder mejor a futuras infecciones y células cancerosas en la edad adulta. Esto supone una ventaja en el área de HL. Los individuos con susceptibilidad genética al HL que viven en condiciones a gran escala durante la infancia y experimentan menos infecciones serían, según esta teoría, más susceptibles al subtipo más adelante porque sus sistemas inmunitarios están menos desarrollados. Según los autores, la inversión de la tendencia en los tipos no especificados es más difícil de explicar, pero también podría ser una coincidencia.
Atención a los enfermos de cáncer en Europa
EUROCARE, el mayor estudio de registro de cáncer basado en la población de Europa, lleva en marcha desde finales de la década de 1990. En el congreso se presentaron nuevos resultados con implicaciones transnacionales. Se evaluaron los datos de más de diez millones de pacientes de cáncer mayores de 15 años de 29 países europeos y un total de 107 registros con respecto a la supervivencia a 5 años, entre otras cosas. Esta cifra se ajustó en función de las muertes por causas distintas al cáncer y de las diferencias de edad. Se incluyeron los diagnósticos hasta 2007.
En general, las tasas de supervivencia son bajas en Europa del Este, pero altas en Europa del Norte y Central. Surgieron otras diferencias geográficas, que se resumen en la tabla 1 . Las diferencias más drásticas se encontraron en la leucemia mieloide y linfocítica crónica (LMC/LCL), el linfoma folicular y difuso de células B grandes y el mieloma múltiple. La LMC mostró una supervivencia media a 5 años del 53%, pero una enorme variación en los distintos grupos de edad. De todos los cánceres hematológicos, las diferencias regionales fueron mayores en el caso de la LMC: 33,4% en Europa del Este frente a 51-58% en el resto de Europa. También se encontraron diferencias geográficas en los cánceres de mal pronóstico, como los de ovario, pulmón, páncreas, esófago y estómago, los tumores cerebrales y el linfoma de Hodgkin, pero en general fueron algo menos pronunciadas.
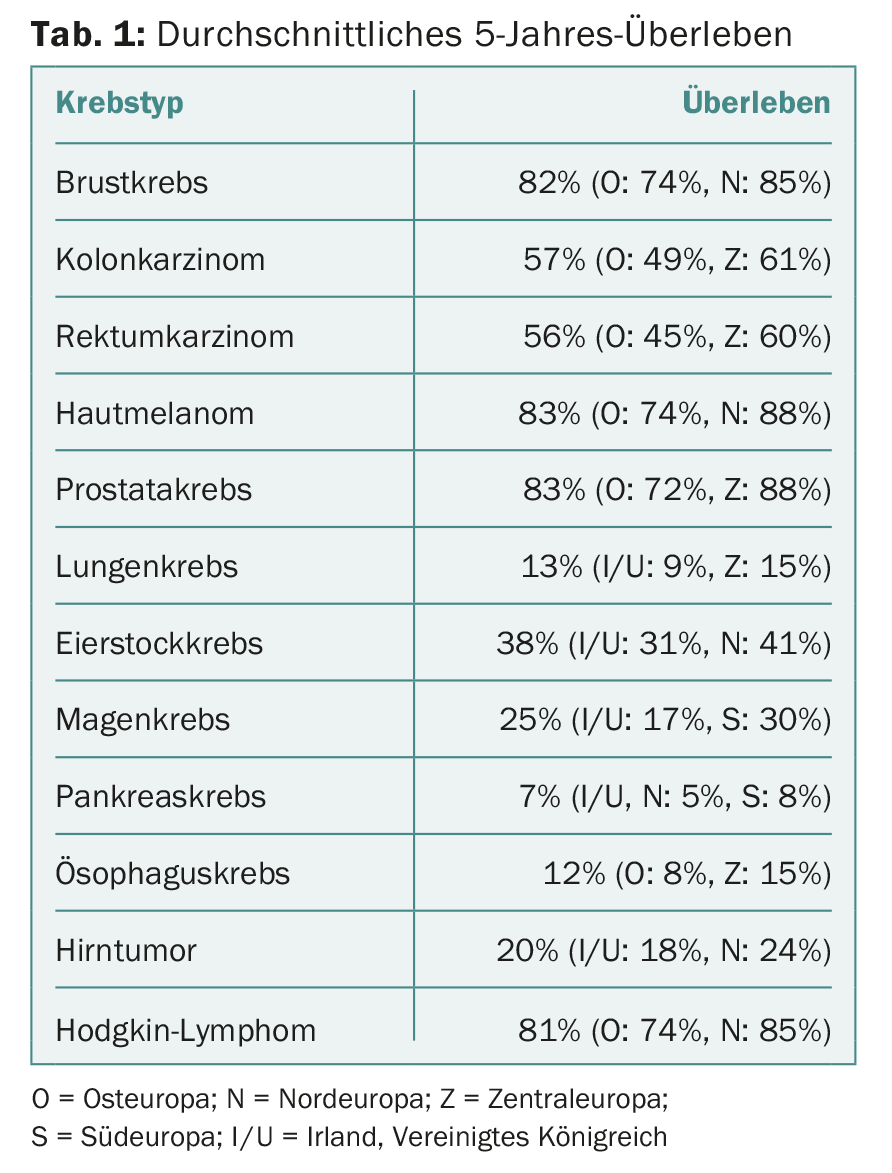
Las tasas de supervivencia a 5 años aumentaron en toda Europa durante el periodo de observación, especialmente en Europa del Este. En concreto, las tasas aumentaron para los tumores de mama, cuello de útero, hígado, biliar y cabeza/cuello (excluyendo el cáncer de laringe), por ejemplo. Los mayores aumentos entre 1999-2001 y 2005-2007 se observaron en los cánceres de LMC (32-54%), próstata (73-82%) y recto (52-58%). También se produjo un ligero aumento de la supervivencia en los melanomas cutáneos. Las tasas se mantuvieron estables en los cánceres de esófago, páncreas, pene y testículos.
Las tasas combinadas de supervivencia a 5 años de todos los tipos de cáncer se correlacionaron positivamente con el producto interior bruto y el gasto sanitario nacional total. Los estados con aumentos recientemente superiores en ambos parámetros tuvieron aumentos correspondientemente superiores en las tasas de supervivencia. Sin embargo, esto no siempre fue así: países como el Reino Unido y Dinamarca deberían haber alcanzado mejores tasas dado su elevado gasto sanitario.
Las variaciones geográficas pueden explicarse, entre otras cosas, por los diferentes esfuerzos de diagnóstico o la calidad y la existencia de programas nacionales de cribado (cáncer de próstata, de mama, colorrectal). Además del diagnóstico precoz, el acceso a un tratamiento multidisciplinar, la buena calidad de los cuidados, el estilo de vida y el estado de salud y socioeconómico de la población respectiva desempeñan un papel importante en la supervivencia. Queda por ver si los resultados se traducirán en esfuerzos políticos concretos.
Las terapias combinadas para el melanoma siguen convenciendo
CheckMate 067: Los puntos de control CTLA-4 y PD-1 son utilizados por las células cancerosas para anular la respuesta inmunitaria específica del cáncer del organismo. Se pueden utilizar inhibidores para bloquear los puntos de control, lo que activa el sistema inmunitario o provoca un aumento de la actividad de las células T. CheckMate 067 es un ensayo de fase III que comparó el inhibidor del punto de control PD-1 nivolumab solo o en combinación con el inhibidor del punto de control CTLA-4 ipilimumab con la monoterapia con ipilimumab. La población del estudio estaba formada por 945 pacientes con melanoma avanzado no tratados previamente. La combinación fue significativamente superior a la monoterapia con ipilumumab en términos de supervivencia libre de progresión (SLP) y tasa de respuesta objetiva. Los resultados de un análisis de subgrupos preespecificado se presentaron en el congreso ECCO/ESMO: ¿Sigue siendo superior la combinación independientemente de la edad, el estado genético o la extensión del tumor? De particular interés fue cómo les fue a los pacientes con factores de mal pronóstico. Los subgrupos diferían en cuanto a metástasis, niveles séricos de lactato deshidrogenasa (LDH), estado de la mutación BRAF y edad.
Los parámetros mencionados se distribuyeron por igual en los tres brazos de tratamiento. La SLP fue de 11,5 meses (combinación) frente a 2,9 meses (monoterapia con ipilimumab; reducción significativa del riesgo del 58%) frente a 6,9 meses (monoterapia con nivolumab; reducción significativa del riesgo del 43%).
Los resultados de los subgrupos mencionados se muestran en la tabla 2. En general, la SLP fue siempre mayor con la combinación. Tampoco hubo diferencias en el perfil de seguridad (en comparación con la población general).
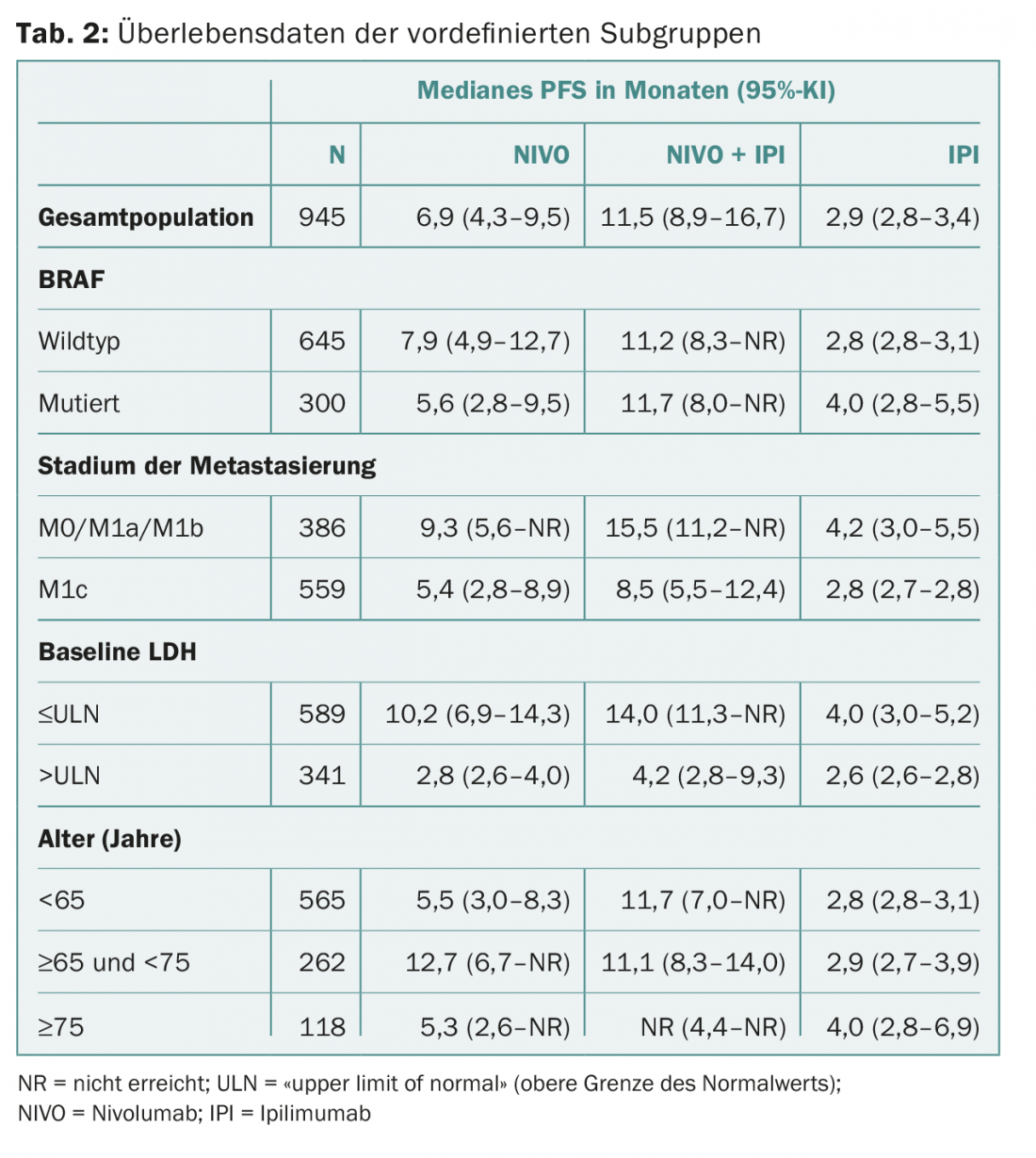
Los autores concluyen que la combinación de nivolumab e ipilimumab es significativamente superior a las monoterapias incluso en pacientes con factores de mal pronóstico y es controlable en cuanto al perfil de seguridad. En la práctica, esto podría conducir a una toma de decisiones más rápida y sencilla en cuanto al uso de la terapia combinada en el futuro. Sobre todo porque los investigadores estudiaron deliberadamente los subgrupos más relevantes para el clínico. Saber si determinados pacientes no se benefician de la combinación es importante, porque a pesar de toda la euforia, no hay que olvidar que las terapias pueden ir acompañadas de un número relativamente elevado de efectos secundarios.
COMBI-v: En este ensayo de fase III, la combinación del inhibidor de la quinasa BRAF dabrafenib y el inhibidor de MEK trametinib (brazo 1) con el inhibidor de BRAF vemurafenib (brazo 2) en comparación. La población del estudio estaba formada por 704 pacientes no tratados previamente con melanoma metastásico, no resecable y avanzado en estadio IIIC/IV con mutación BRAF V600E/K. Según los resultados publicados en el New England Journal of Medicine en enero de 2015 [1], la tasa de supervivencia global, el criterio de valoración primario, fue del 72% en el brazo 1 y del 65% en el brazo 2 después de 12 meses (HR 0,69; IC 95% 0,53-0,89; p=0,005). Las tasas de efectos secundarios fueron comparables en ambos brazos. Debido a los resultados convincentes, el estudio se detuvo en julio de 2014. Sin embargo, como los pacientes tenían la opción de seguir con la terapia respectiva, los investigadores tuvieron la oportunidad de realizar un seguimiento prolongado. En el congreso se presentó una actualización que incluía datos hasta el 13 de marzo de 2015:
- La mediana de la supervivencia global fue de 25,6 frente a 18 meses, lo que corresponde a una reducción significativa del riesgo de mortalidad del 34%.
- La mediana de la SLP fue de 12,6 frente a 7,3 meses, lo que corresponde a una reducción significativa del riesgo de muerte o progresión del 39%.
- Al cabo de dos años, el 51 frente al 38% de los pacientes estaban vivos.
- No hubo nuevos efectos secundarios sorprendentes en el seguimiento prolongado.
- Otro subanálisis presentado en el congreso también demostró que la combinación mejoraba significativamente la calidad de vida.
La actualización confirmó así los convincentes resultados del análisis publicado once meses antes. Por ello, la UE aprobó la combinación de dabrafenib y trametinib para esta indicación a principios de septiembre de 2015.
Fuente: Congreso Europeo del Cáncer(18º ECCO, 40º ESMO), 25-29 de septiembre de 2015, Viena.
Literatura:
- Robert C, et al: Mejora de la supervivencia global en el melanoma con la combinación de dabrafenib y trametinib. N Engl J Med 2015 Ene 1; 372(1): 30-39.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2015; 3(11-12): 32-34