Según la clasificación actual, la insuficiencia cardiaca con fracción de eyección reducida (IC-FEr) se caracteriza por una fracción de eyección del ventrículo izquierdo (FEVI) en el rango ≤40%, la insuficiencia cardiaca con fracción de eyección preservada (IC-FEP) por una FEVI en el rango ≥50%. Desde el punto de vista terapéutico, ¡esta diferenciación marca una gran diferencia!
La insuficiencia cardiaca (IC) no es un diagnóstico único, sino un síndrome clínico causado por la incapacidad del corazón para satisfacer las demandas fisiológicas de los órganos del cuerpo. Esto provoca o bien sistemas de sobrecarga de volumen, como disnea, hinchazón de tobillos, fatiga y signos clínicos de sobrecarga de volumen, o bien un bajo gasto cardiaco, o ambas cosas, debido a una anomalía estructural y/o funcional del corazón. Entre los factores de riesgo se encuentran el sedentarismo, la obesidad, la hipertensión, el tabaquismo, el consumo excesivo de alcohol, así como la dislipidemia, la diabetes o las enfermedades coronarias. Que puede modificarse mediante cambios en el estilo de vida, una terapia médica óptima para la hipertensión, la diabetes y la dislipidemia, y vacunas preventivas.
La hipertensión arterial es uno de los principales factores de riesgo
La hipertensión, en particular, es uno de los principales factores de riesgo para desarrollar IC. Dos tercios de todos los pacientes con IC la padecen, y hasta el 90% de los pacientes con IC-FEM. Sin embargo, la hipertensión no controlada en pacientes tratados con un tratamiento médico óptimo de la IC es más bien rara debido al solapamiento entre los medicamentos para la IC y para la hipertensión. Aún se desconocen los objetivos óptimos de presión arterial tanto para la IC-FEr como para la IC-FEp, por lo que se suelen tener en cuenta los objetivos individuales, teniendo en cuenta la edad y las enfermedades concomitantes (diabetes, enfermedad renal, cardiopatía coronaria, valvulopatía, ictus). No obstante, como norma general, apueste por objetivos de medicación basados en la evidencia en la IC-FEr, a pesar de una hipotensión leve; por el contrario, evite la hipotensión en la IC-FEp con hipertrofia ventricular izquierda y reserva de precarga limitada.
Además, el diagnóstico de insuficiencia cardiaca requiere la presencia de síntomas y/o signos de IC, así como pruebas objetivas de disfunción cardiaca, como falta de aliento, fatiga e hinchazón de tobillos. Si están presentes, se recomiendan las siguientes pruebas diagnósticas para la evaluación de pacientes con sospecha de IC crónica: El electrocardiograma (ECG) puede revelar anomalías como fibrilación auricular, ondas Q, hipertrofia del VI (HVI) y un complejo QRS ensanchado, que pueden aumentar la probabilidad de un diagnóstico de IC y también orientar la terapia. Si está disponible, se recomienda la medición de los péptidos natriuréticos (PN). Una concentración plasmática de péptido natriurético tipo B (BNP) <35 pg/ml, de péptido natriurético tipo pro-B N-terminal (NT-proBNP) <125 pg/ml o de péptido natriurético auricular medio (MR-proANP) <40 pmol/L68 hacen poco probable el diagnóstico de IC. Se recomiendan investigaciones básicas como la urea y los electrolitos séricos, la creatinina, el hemograma completo y las pruebas de función hepática y tiroidea para diferenciar la IC de otras enfermedades, proporcionar información pronóstica y orientar la posible terapia. La ecocardiografía se recomienda como el examen más importante para evaluar la función cardiaca. Además de determinar la FEVI, la ecocardiografía también proporciona información sobre otros parámetros como el tamaño ventricular, la HVI excéntrica o concéntrica, las anomalías regionales del movimiento de la pared (que pueden indicar una EAC subyacente, el síndrome de Takotsubo o miocarditis), la función del VD, la hipertensión pulmonar, la función valvular y los marcadores de la función diastólica.
La insuficiencia cardíaca puede producirse independientemente de la fracción de eyección del VI
Las causas de la IC pueden variar, pero las miocardiopatías isquémicas son relativamente frecuentes. La IC isquémica está causada por trastornos circulatorios en el corazón, por ejemplo a consecuencia de una cardiopatía coronaria. Por lo tanto, la cuestión decisiva en el diagnóstico inicial de la IC es siempre si existe una cardiopatía coronaria no detectada previamente. Para responder a esta pregunta se suele utilizar una prueba de isquemia no invasiva, como la resonancia magnética de estrés. Se trata de un método completo para evaluar la función global y regional, valorar si ya existe isquemia o infarto de miocardio y caracterizar el tejido (edema miocárdico, zona de riesgo, trombo ventricular, miocardiopatía). La sensibilidad para detectar el infarto es del 94-99%; la sensibilidad para la isquemia es del 91% y la especificidad para la isquemia es del 83%. Si hay una RM de estrés positiva o equívoca, con evidencia de isquemia relevante (≥10%) o patrones de IC isquémica, el siguiente paso es la angiografía invasiva. cuyo resultado, o bien confirma la IC isquémica y hace necesaria una angioplastia coronaria transluminal percutánea (ACTP) o un injerto de derivación de la arteria coronaria (CABG), o bien demuestra una EAC circunstancial. En caso de una IRM de esfuerzo no concluyente, con isquemia limitada (<10%), nachweislich kleinen Infarkten oder sehr jungen Patienten, sollte ein Kalzium-Score (Ca-Score) und eventuell eine computertomografische Koronarangiografie (CTCA) durchgeführt werden. Bei fortgeschrittener HF und einem Ca-Score=0, kann eine ischämische HF ausgeschlossen werden; bei einem Ca-Score>0, debe realizarse también una ACTC para excluir o confirmar una EAC estenótica y una IC isquémica. Si es positiva, se recomienda de nuevo la angiografía invasiva. cuyo resultado confirma la IC isquémica o prueba la cardiopatía isquémica bystander y requiere las terapias apropiadas.
Beneficio pronóstico de los fármacos clásicos para la HFrEF
En la actualidad, se distinguen dos grupos principales de pacientes en función de la fracción de eyección del ventrículo izquierdo: los pacientes con una función de bombeo del corazón deteriorada (≤40%) que padecen insuficiencia cardiaca sistólica (ICrEF) y los pacientes con insuficiencia cardiaca con una potencia de bombeo del corazón preservada (≥50%) (ICpEF). La diferenciación marca una gran diferencia desde el punto de vista terapéutico, porque para los pacientes con IC-FEr, la investigación clínica ha desarrollado ahora un arsenal de opciones de tratamiento basadas en pruebas para reducir la morbilidad y la mortalidad. En concreto, los llamados “Cuatro Fantásticos” (ARNI/ACE-I/ARB, BB, ARM, SGLT2-I) reducen la morbilidad y la mortalidad a las cuatro semanas de iniciar el tratamiento.
Según las directrices de la Sociedad Europea de Cardiología , la terapia estándar común para la insuficiencia cardiaca con fracción de eyección reducida (IC-FEr) incluye inicialmente el uso de un inhibidor de la enzima convertidora de angiotensina (IECA) o del receptor de angiotensina II tipo 1 (AT1) y un betabloqueante (BB). Si la presión arterial es adecuada y la TFGe ≥30 ml/min/m², puede cambiarse a sacubtril/valsartán. Los inhibidores de la ECA o los bloqueantes AT1 deben suspenderse antes de la administración. Para evitar el angioedema, deben transcurrir al menos 36 horas entre la última administración de inhibidores de la ECA y el inicio de la administración de ARNI. En caso de intolerancia a los IECA o a los IRA, pueden utilizarse los SRA/Sartán. Tanto los RAAS-I como los ARNI y los SGLT2-I pueden reducir temporalmente la TFGe. Un aumento de la creatinina <50% y una disminución de la TFGe <10% con respecto al valor basal es aceptable, la función renal se recupera. Los SGLT2-I en particular han mostrado un beneficio en la supervivencia independiente del estado de la diabetes/HbA1c.
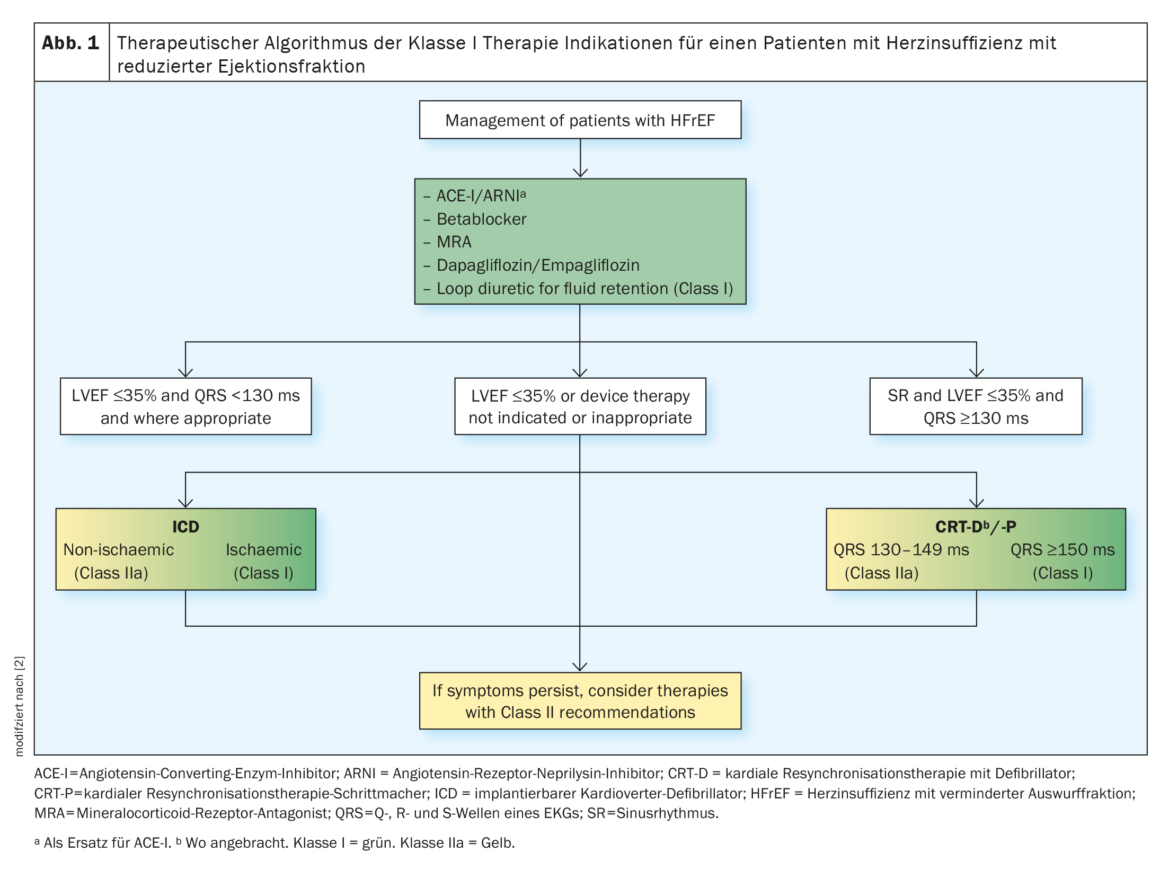
Los pacientes con IC isquémica tienen de media un mayor riesgo de muerte súbita cardiaca (MSC) que los pacientes con IC no isquémica. En presencia de factores de riesgo de MSC, como una clasificación II-III de la NYHA** y una FEVI ≤35% a pesar de ≥3 meses de tratamiento médico óptimo establecido y una supervivencia >de 1 año, existe una indicación de DAI# de clase I para los pacientes con IC isquémica y una indicación de clase IIa para todos los pacientes con IC no isquémica. Los pacientes con clasificación IV de la NYHA que son refractarios a la terapia farmacológica (supervivencia <1 año) reciben una indicación de clase III. La terapia de resincronización cardiaca (TRC) se recomienda a los pacientes con IC sintomática, una FEVI ≤35% a pesar de un tratamiento farmacológico óptimo y un bloqueo de rama izquierda del haz de His (BRIHH) en ritmo sinusal y una duración del QRS ≥150 ms (fig. 1) [2].
** NYHA = Asociación Cardiaca de Nueva York
# ICD = Desfibrilador cardioversor implantable
Exámenes preventivos y tratamiento de enfermedades subyacentes
En los pacientes con IC-FEM, se carece de terapias que mejoren el pronóstico a pesar de los numerosos estudios realizados. Hasta ahora, no se ha demostrado que ningún tratamiento reduzca la mortalidad y la morbilidad. En este caso, la única opción que queda sigue siendo el intento empírico de aliviar los síntomas de los pacientes con diuréticos (de asa) y lograr el cambio a un estilo de vida saludable. La falta de una terapia general hace aún más importante el cribado y el tratamiento de enfermedades subyacentes como la hipertensión, la diabetes, la amiloidosis, la cardiopatía coronaria y la valvulopatía en pacientes con IC-FEM, explica el doctor Philip Haaf, médico jefe del Hospital Universitario de Basilea [1]. La gran mayoría de los pacientes con insuficiencia cardiaca pulmonar padecen hipertensión, y muchos tienen también una cardiopatía coronaria subyacente. Debe buscarse la fibrilación auricular, la diabetes, la EPOC, la enfermedad renal, las terapias oncológicas previas, el estado del hierro, la enfermedad cardiaca valvular, la cardiomiopatía hipertrófica y la amiloidosis cardiaca, añadió Haaf.
Muy poco hierro es malo – ¡pero también lo es demasiado!
La miocardiopatía por sobrecarga de hierro se produce principalmente en pacientes con hemocromatosis primaria o hereditaria, secundaria a múltiples transfusiones de sangre. Una resonancia magnética cardiaca puede ayudar cuantificando el contenido de hierro del corazón y el hígado para diagnosticar y supervisar la terapia con quelantes de hierro y la flebotomía. Sin embargo, aún más importante que la sobrecarga de hierro es la deficiencia de hierro en la insuficiencia cardiaca. En los pacientes con IC, la deficiencia de hierro se presenta con una ferritina <100 ng/ml o una ferritina <300 ng/ml con una saturación de transferrina (TSAT) <20%. La carencia de hierro puede presentarse independientemente de la anemia y afecta al 55% de los pacientes con IC crónica y hasta al 80% de los pacientes con IC aguda. La causa exacta de la carencia de hierro en la HF sigue siendo desconocida.
Se recomienda que todos los pacientes con IC e indicaciones de clase I se sometan periódicamente a pruebas de detección de anemia y ferropenia mediante hemograma completo, concentración sérica de ferritina y TSAT. Debe considerarse la suplementación intravenosa de hierro con carboximaltosa férrica en pacientes sintomáticos con IC hospitalizados recientemente por IC con FEVI ≤50% y deficiencia de hierro, definida como ferritina sérica <100 ng/ml o ferritina sérica 100-299 ng/ml con TSAT <20%, para reducir el riesgo de hospitalización por IC. No se recomienda el tratamiento de la anemia en la IC con agentes estimulantes de la eritropoyetina en ausencia de otras indicaciones terapéuticas.
Los problemas con las válvulas son frecuentes
La estenosis aórtica provoca una sobrecarga del ventrículo izquierdo, lo que puede provocar hipertrofia cardiaca e insuficiencia cardiaca. Se habla de estenosis aórtica grave cuando el área de apertura de la válvula es ≤1 cm² o cuando la presión media es ≥40 mmHg. Esto provoca un aumento de la poscarga del VI e hipertrofia y remodelación del VI, lo que a su vez empeora la IC. Cuando utilice vasodilatadores, debe tener cuidado para evitar la hipotensión. La sustitución quirúrgica se recomienda a todos los pacientes <75 Jahren empfohlen, die zusätzlich ein geringes chirurgisches Risiko aufweisen. Die Transkatheter-Aortenklappen-Implantation (TAVI) wird bei Patienten>de 75 años que presenten un riesgo quirúrgico elevado. Debido a la suavidad del procedimiento, la TAVI también se utiliza cada vez más en pacientes jóvenes.
La insuficiencia aórtica también puede convertirse con el tiempo en insuficiencia cardiaca. La regurgitación aórtica se considera grave cuando existe un gran volumen de regurgitación y reflujo hacia la aorta. Esto provoca una dilatación progresiva del VI y la consiguiente disfunción, que a su vez empeora la IC. Los betabloqueantes deben utilizarse con precaución, ya que pueden prolongar la diástole y empeorar la regurgitación aórtica. El abordaje quirúrgico se considera el estándar para la regurgitación aórtica, pero la TAVI también se utiliza cada vez más, especialmente en casos de riesgo quirúrgico alto/prohibitivo.
La regurgitación mitral (RM) grave también puede causar insuficiencia cardiaca. Se recomienda la intervención quirúrgica, preferiblemente la reparación, en pacientes con IM primaria grave y síntomas de IC. Si la cirugía está contraindicada o se considera de alto riesgo, puede considerarse la reparación percutánea. En pacientes con IM secundaria grave e ICrEF que requieran revascularización, debe considerarse la cirugía de la válvula mitral y el injerto de bypass arterial coronario (CABG). La cirugía aislada de la válvula mitral puede considerarse en pacientes sintomáticos con IM secundaria grave a pesar de una terapia óptima y un riesgo quirúrgico bajo
La regurgitación tricuspídea (RT) puede estar causada o ser consecuencia de una disfunción del VD y de la IC. El tratamiento de la IC con TR incluye terapia farmacológica (diuréticos, antagonistas neurohormonales). En casos seleccionados, puede considerarse la terapia transcatéter y la cirugía. La cirugía de la válvula tricúspide se recomienda para pacientes con TR grave que requieran cirugía cardíaca izquierda. También debe considerarse en pacientes con IT moderada y dilatación de la válvula tricúspide que requieran cirugía cardiaca izquierda y en pacientes sintomáticos con IT grave aislada. Las técnicas transcatéter han surgido recientemente como posibles opciones de tratamiento para la TR. Los resultados preliminares muestran una mejora de la gravedad y los síntomas de la TR con bajas tasas de complicaciones.

La amiloidosis cardiaca sigue siendo una causa infradiagnosticada
Normalmente, uno de cada seis pacientes con hipertrofia ventricular izquierda inexplicada y/o IC-FEp padece amiloidosis cardiaca (AC). Las dos formas más comunes son la inmunoglobulina de cadena ligera (AL) y la amiloidosis por transtiretina (ATTR). Una edad >65 años e IC junto con un grosor de la pared del VI >12 mm en la ecocardiografía son los principales criterios para sospechar una AC. Para el diagnóstico de la AL-CA en pacientes con pruebas hematológicas anormales se requieren pruebas de imagen cardiaca y biopsia endomiocárdica (BEM) o biopsia extracardiaca. La gammagrafía 99mTc-PYP## o DPD$ o HMDP& marcada con tecnecio con imágenes planares y SPECT*** tiene una especificidad y un valor predictivo positivo para ATTR-CA de hasta el 100%. En cambio, la RMC£ tiene una sensibilidad y una especificidad del 85% y el 92% respectivamente. Sin embargo, la BEM sigue siendo el patrón oro para el diagnóstico de ATTR-CA con una sensibilidad y especificidad de casi el 100%.
## mTc-PYP=Pirofosfato 99mTcmarcado con tecnecio
$ DPD=ácido 3,3-difosfono-1,2-propanedicarboxílico
& HMDP=Difosfonato de hidroximetileno
*** SPECT = Tomografía Computarizada por Emisión de Fotón Único
£ CMR = resonancia magnética cardiaca
Literatura:
- PD Dr. med. Philip Haaf: Herzinsuffizienz mit reduzierter und erhaltener EF. Forum Medizin Fortbildung (FomF), Update Refresher 2023, Kardiologie I, 24.01.2023.
- McDonagh TA, et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal, Volume 42, Issue 36, 21 September 2021, Pages 3599–3726, https://doi.org/10.1093/eurheartj/ehab368.
Para saber más:
- Zeppenfeld K, et al.: 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. European Heart Journal, Volume 43, Issue 40, 21 October 2022, Pages 3997–4126, https://doi.org/10.1093/eurheartj/ehac262.
HAUSARZT PRAXIS 2023; 18(2): 20–21
CARDIOVASC 2023; 22(1): 26–28











