Las terapias sistémicas para la psoriasis han cambiado mucho en los últimos años. En el pasado, se utilizaba sobre todo la fototerapia o las terapias sistémicas convencionales como el metotrexato, la acitretina, la ciclosporina A y los ésteres del ácido fumárico. Hoy en día, éstos son sustituidos cada vez más en el curso de la terapia por el tratamiento con los biológicos más recientes y el grupo de las moléculas pequeñas.
Dada su importancia en el desencadenamiento de los brotes de la enfermedad, los factores precipitantes de la psoriasis deben eliminarse sistemáticamente: En primer lugar, se encuentran las infecciones, el estrés, la medicación y un cuidado inadecuado de la piel.
Además de las infecciones estreptocócicas, a las que a menudo se atribuye la causa, el estrés psicológico también se considera un importante factor de provocación, especialmente en la infancia y la adolescencia. Los jóvenes sufren con mayor frecuencia la estigmatización, lo que puede dar lugar a importantes situaciones de conflicto psicosocial, especialmente durante la pubertad. Los jóvenes sufren la misma pérdida de calidad de vida por la psoriasis que por el acné.
Medicamentos como los β2-bloqueantes, los inhibidores de la ECA, los antipalúdicos, el litio y los AINE también pueden provocar psoriasis, por lo que es importante realizar un historial exhaustivo de la medicación.
Por último, pero no por ello menos importante, hay que cuidar la piel incluso cuando no hay aparición o la expresión de la enfermedad es mínima. El uso regular de preparados para el cuidado de la piel no sólo ayuda a restaurar la función de barrera alterada de la piel, sino que también tiene el propósito de prevenir la aparición de nuevos síntomas cutáneos debidos a irritaciones como la deshidratación (baños o duchas frecuentes, estancia en habitaciones con calefacción y poca humedad). Por lo tanto, la piel debe cuidarse a diario con productos adecuados.
Las series completas para el cuidado de la piel especialmente desarrolladas para pacientes con psoriasis (por ejemplo, Aqeo®), pero también las fórmulas dermatológicas de eficacia probada u otros productos para el cuidado de la piel son adecuados para el cuidado diario de la piel, siempre que sean bien tolerados por el paciente.
Terapia tópica
En el caso de las placas de descamación infiltradas, resulta útil en primer lugar una terapia desincrustante con queratolíticos, sobre todo para mejorar la penetración de los agentes activos. Aquí se recomienda utilizar ácido salicílico en concentraciones entre el 5 y el 10%, según la localización, en una base de vaselina, carbowax o aceite. Otros queratolíticos son la urea, el ácido láctico y el azufre coloidal.
Mientras que el ácido salicílico se utiliza esencialmente para eliminar la caspa, la urea (en concentraciones entre el 8 y el 12%), el ácido láctico (2,5-10%) y el azufre son adecuados para el cuidado y el tratamiento en forma de aditivos en cremas, lociones o baños de aceite de azufre.
En niños menores de 12 años, la aplicación local de gran superficie de preparados tópicos que contienen ácido salicílico puede provocar toxicidad resortiva (salicilismo) con daños en el sistema nervioso central y los riñones. Por ello, se recomienda el uso de cremas emulsionantes como Unguentum emulsificans aquosum, si es necesario con la adición de urea (5%), para la descamación en niños.
Una vez descamadas las placas, se utilizan corticosteroides tópicos. Éstas se encuentran entre las terapias locales más utilizadas para la psoriasis. Se caracterizan por una eficacia y una tolerabilidad muy buenas, así como -cuando se utilizan correctamente- unos efectos indeseables bajos, con una relación calidad-precio comparativamente favorable.
La evaluación negativa de la cortisona en la población carece de base médico-dermatológica. Sólo si la duración de la terapia es demasiado larga (terapia ininterrumpida durante más de seis semanas) se produce atrofia cutánea, aunque en muchos casos puede ser irreversible. Normalmente, los esteroides de clase III-IV que son a la vez antiinflamatorios y antiproliferativos, como el dipropionato de clobetasol (Dermovate®), la betametasona (Betnovate®) o, especialmente en niños, el furoato de mometasona (Elocom®) son bien eficaces, preferiblemente en combinación con análogos tópicos de la vitamina D como el calcipotriol (Daivobet®), el tacalcitol (Curatoderm®) y el calcitriol (Silkis®). También están disponibles en combinaciones fijas de betametasona y calcipotriol tanto para aplicación cutánea (Daivobet®) como en el cuero cabelludo (Xamiol®) [1]. En el caso de focos localizados, los corticosteroides también pueden aplicarse de forma oclusiva para aumentar su eficacia, por ejemplo en forma de parche (Betesil®).
En principio, no se recomienda la terapia ininterrumpida con corticosteroides más allá de un mes, por un lado por la atrofia y otros efectos secundarios cutáneos, y por otro por la absorción y el riesgo de atrofia de la corteza suprarrenal. Como alternativa a los preparados de corticosteroides, los inhibidores tópicos de la calcineurina tacrolimus o pimecrolimus (Protopic®, Elidel®) son adecuados en las zonas intertriginosas (psoriasis inversa).
Fototerapia
La fototerapia es muy valorada en el tratamiento de la psoriasis moderada y grave. Es fácil de usar, cosméticamente aceptable, no muy costoso y barato. Por último, puede combinarse ventajosamente con tratamientos tópicos. En la actualidad, se utilizan principalmente lámparas UVB que emiten 311 nm [2]. Los rayos UVA de longitud de onda más larga también pueden ser muy eficaces en combinación con psoralenos fotosensibilizantes y retinoides [3].
Terapia sistémica
Las terapias sistémicas están indicadas para los casos moderados a graves de psoriasis que no pueden controlarse adecuadamente con medidas locales y fototerapia, y para la artritis psoriásica. Se distingue entre las terapias sistémicas estándar con metotrexato, acitretina, ciclosporina A y los ésteres del ácido fumárico y el tratamiento con los biológicos más recientes.
El metotrexato (MTX) es una opción rentable con perspectivas limitadas a largo plazo. Dosificación baja (de 7,5 a máx. 30 mg/semana), el MTX muestra un efecto especialmente bueno en todas las formas pustulosas de psoriasis, eritrodermia psoriásica así como artritis psoriásica, pero también en la psoriasis extensa en forma de placas. El MTX tiene un efecto antiproliferativo y antiinflamatorio al inhibir la enzima dihidrofolato reductasa, impidiendo así la formación del importante metabolito ácido tetrahidrofólico a partir del ácido fólico. Produce una mejora del 75% de la psoriasis superficial en aproximadamente el 60% de los casos (60% PASI75) [4,5]. Se observa una respuesta en un plazo de dos a seis semanas [6]. La administración inicial es de 7,5 mg/semana, debido a la cinética de absorción variable con la administración oral, se prefiere la forma parenteral. En las dos primeras semanas, la dosis debe aumentarse hasta la dosis normal de mantenimiento de 10-15 mg semanales, ajustando la dosis cada tres o cuatro semanas. La administración de 5 mg de ácido fólico p.o. 24-48 horas después mejora la tolerancia. El principal inconveniente del MTX es la dosis acumulativa limitada de aproximadamente 1,5 g, que suele alcanzarse al cabo de dos a cuatro años. En este límite, se recomiendan ahora las determinaciones de procolágeno III o las biopsias hepáticas para excluir la fibrosis hepática.
Los retinoides son análogos de la vital vitamina A liposoluble. Tienen un efecto antiproliferativo e inmunomodulador. El retinoide sistémico más utilizado, la acitretina (Neotigason®) a una dosis de 20-75 mg muestra un PASI75 en el 25-41% de los pacientes en un plazo de ocho a doce semanas [7,8]. Las dosis más bajas no muestran ningún efecto. La acitretina se prefiere para las formas pustulosas de la psoriasis y la eritrodermia psoriásica. La dosis inicial suele ser de 0,5-1 mg/kg/d. Tras la respuesta, puede reducirse a 0,3-0,5 mg/kg/d como terapia de mantenimiento. Dado que se producen efectos secundarios frecuentes, aunque en su mayoría reversibles, y que el fármaco es inferior a los demás preparados como monoterapéutico, casi sólo se utiliza como preparado combinado para la fotoquimioterapia. Aquí se alcanzan tasas de remisión superiores al 94% [3]. En cualquier caso, los pacientes deben ser informados del efecto teratógeno y se les prescribe un anticonceptivo eficaz durante dos años.
El péptido entérico ciclosporina A (Sandimmun Neoral®), derivado del moho del suelo Tolypocladium inflatum, inhibe los factores de transcripción nuclear en las células T. Con ello se consigue una rápida inmunosupresión celular. Con la administración oral de 2,5-3 mg/kgKG/d en dos dosis únicas (la dosis más baja descrita para el tratamiento a largo plazo [9,10]), se consigue un PASI75 en el 50-70% de los casos tras 8-16 semanas de terapia [11,12]. La ciclosporina A tiene la desventaja de numerosos efectos secundarios, como el desarrollo de hipertensión arterial, insuficiencia renal, temblores, infecciones e hipertricosis. Normalmente no puede utilizarse durante más de unos meses, por lo que no suele ser adecuado como terapia a largo plazo para los pacientes psoriásicos. En la actualidad, se utiliza principalmente como terapia de rescate en situaciones en las que el estado de la piel debe mejorar rápidamente (en un plazo de cuatro semanas), como en la psoriasis eritrodermática.
Los ésteres de ácido fumárico (Fumaderm®) han demostrado su eficacia en estudios doble ciego desde su desarrollo por Schweckendiek, un químico afectado él mismo de psoriasis [13–15]. Esta clase de sustancias es un subproducto del ciclo del citrato y tiene la ventaja de un perfil de eficacia muy seguro, aunque a menudo se manifiesta con molestos efectos secundarios al inicio de la terapia, como rubor, dolor de cabeza, náuseas, diarrea y linfopenia pasiva. Sin embargo, si se tolera, puede tomarse durante décadas y suprimir completamente la psoriasis. El PASI75 se alcanza en el 50-70% de los pacientes tras 16 semanas [13–15]. No está aprobado en Suiza, pero puede obtenerse fácilmente en farmacias internacionales tras obtener la aprobación de la compañía de seguros médicos.
Biológicos
Dado que la psoriasis se considera una enfermedad inmunitaria mediada por células T en la que las citocinas también desempeñan un papel esencial, surgen puntos de partida específicos para la terapia. Los productos biológicos, en concreto los anticuerpos recombinantes o los receptores solubles, pueden inhibir eficazmente las citocinas activadoras de las células T. Los antagonistas del factor de necrosis tumoral (TNF)-α infliximab (Remicade®), etanercept (Enbrel®) y adalimumab (Humira®), el bloqueante de la IL-12/23 ustekinumab (Stelara®) y el antagonista de la IL-17A secukinumab (Cosentyx®) están aprobados actualmente en Suiza para el tratamiento de la psoriasis en placas de moderada a grave en adultos bajo ciertas condiciones.
Antagonistas del TN F-α: En la actualidad, los fármacos biológicos más utilizados para el tratamiento de la psoriasis y la artritis psoriásica son los antagonistas del TNF-α.
El etanercept (Enbrel®) es un receptor soluble del TNF-α que se administra s.c.. Utilice 50 mg semanalmente, o 50 mg dos veces por semana para los casos graves. El fármaco produce una mejora del 75% del PASI en el 30% de los pacientes en doce semanas [16]. Es el único biológico también aprobado para la psoriasis pediátrica [17]. La pregunta para el futuro, especialmente para la artritis psoriásica en la infancia, es hasta qué punto el tratamiento precoz con etanercept puede evitar un curso destructivo e invalidante.
Infliximab (Remicade®) es un anticuerpo quimérico ratón-humano contra el TNF-α, que se administra en infusión cada ocho semanas tras la dosis inicial. El infliximab es adecuado para pacientes con sobrepeso, ya que puede administrarse adaptado a su peso. Actualmente es uno de los biológicos más eficaces, pero tiene el inconveniente de que su efecto disminuye con el tiempo debido a la formación de anticuerpos.
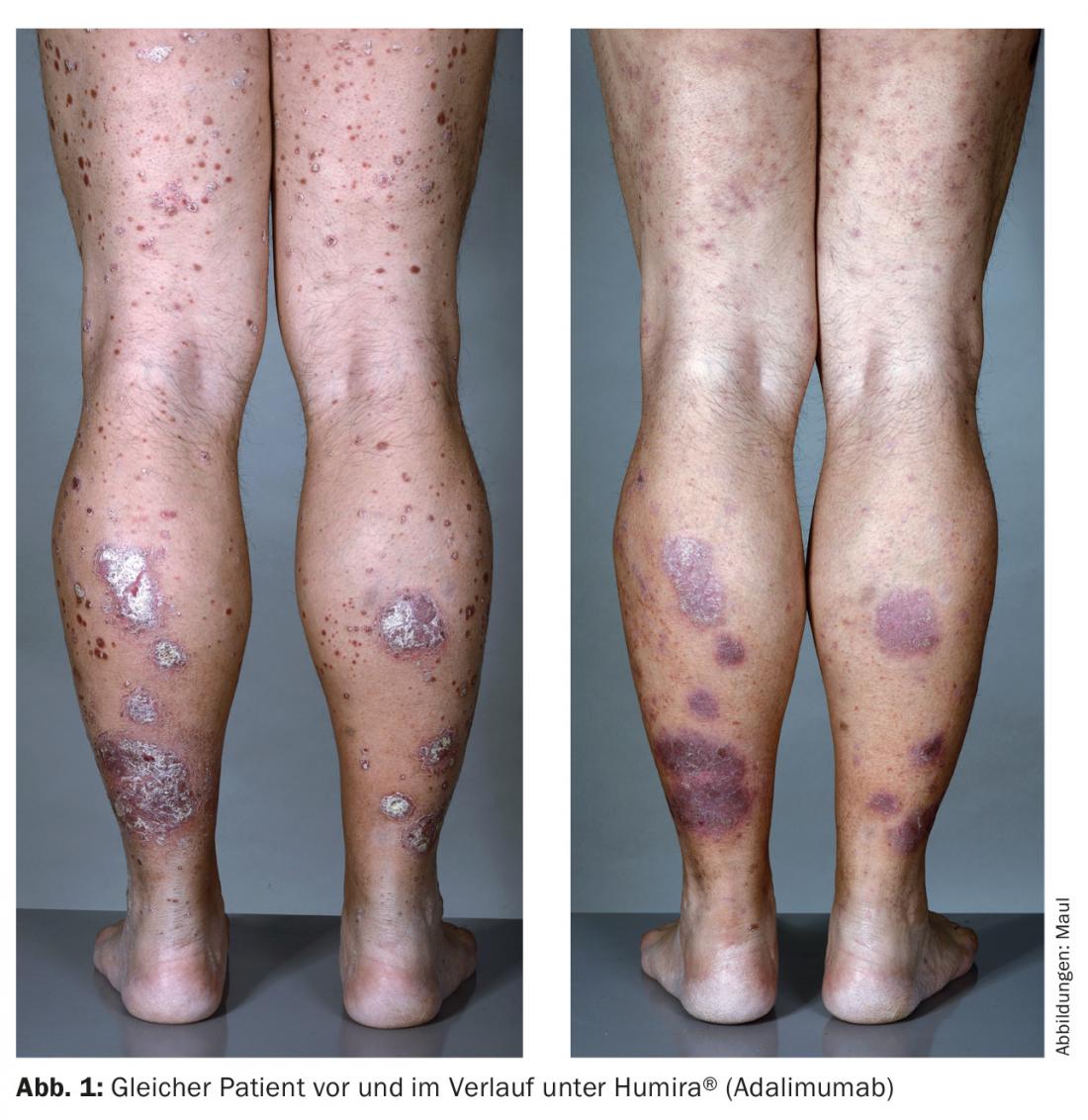
El adalimumab (Humira®) es un anticuerpo anti-TNF-α totalmente humanizado que se inyecta s.c. cada quince días y combina una buena eficacia con una gran autonomía del paciente (Fig. 1). Tanto el infliximab como el adalimumab son superiores al etanercept en eficacia.
Bloqueante de IL-12/23: El bloqueante de IL-12/23 ustekinumab (Stelara®) es un anticuerpo totalmente humanizado que se une a la subunidad común de IL-12 y -23. Estas citocinas son importantes en las respuestas inmunitarias locales. Aunque son esenciales para el desarrollo de las lesiones cutáneas psoriásicas, no parecen serlo para la inmunidad normal, ya que en los estudios no se han producido efectos adversos significativos en comparación con el placebo. Los estudios a largo plazo tampoco mostraron un aumento de las tasas de infección, lo que convierte al fármaco en una de las terapias para la psoriasis más seguras disponibles [18,19].
Antagonista de la IL-17A: Un nuevo biológico que salió al mercado en 2015 es el bloqueante de la IL-17A secukinumab (Cosentyx®). La IL-17A es una sustancia mensajera producida por el subgrupo de células T ayudantes Th17, entre otras, y es responsable muy específicamente de la inflamación local al reclutar granulocitos neutrófilos y monocitos localmente en los focos de inflamación. La ventaja de esta inhibición selectiva de la respuesta inmunitaria es que los efectos secundarios son limitados debido a la inhibición de estas citocinas. Secukinumab se administra 300 mg s.c. semanalmente durante el primer mes, a partir de la semana 5 se administra mensualmente. Dos ensayos de fase III de secukinumab en la psoriasis de moderada a grave demostraron que la mejora del PASI75 en la semana 12 del tratamiento de la psoriasis (en comparación con el estado previo al tratamiento) se alcanzó en el 77,1-81,6% de todos los pacientes [20]. En un estudio comparativo, se comparó el tratamiento con etanercept frente al placebo; aquí, sólo el 44,0% de los pacientes alcanzaron un PASI75 en la semana 12 con etanercept, mientras que el placebo logró este criterio de valoración en menos del 5% de los casos en cada caso. En la semana 52, se observó una respuesta PASI90 en el 39% de los pacientes que tomaban Enbrel® frente al 70,6% que tomaban secukinumab 300 mg. Los efectos secundarios de los antagonistas de la IL-17 se han investigado en ensayos de fase III [20]. El fármaco mostró un perfil de seguridad y efectos secundarios similar al de los biológicos más antiguos. En comparación con el placebo, el periodo de inducción mostró una incidencia ligeramente mayor de efectos adversos, especialmente los de naturaleza infecciosa no peligrosa. La IL-17 desempeña un papel clave en la defensa contra los patógenos microbianos mucocutáneos. Entre otras cosas, éstos son defendidos por los granulocitos neutrófilos, para los que la IL-17-A desempeña un papel importante en la migración y la granulopoyesis. Esto explica por qué la incidencia de las infecciones por Candida no complicadas aumenta de forma dependiente de la dosis. Todas las infecciones por Candida pudieron tratarse con la terapéutica estándar y no dieron lugar a una interrupción de la terapia biológica. Además, se produjeron algunas neutropenias que, sin embargo, desaparecieron espontáneamente.
Los estudios han demostrado que el secukinumab también es una buena terapia alternativa para la artritis psoriásica. El criterio de valoración utilizado es el ACR20, una puntuación estándar que mide la mejora del 20% en los síntomas de la artritis psoriásica. En la semana 24, ésta había alcanzado aprox. 50% de los pacientes tratados con secukinumab frente al 18% de los pacientes tratados con placebo. En un segundo estudio, el 39% de los pacientes tratados con 300 mg de secukinumab lograron un ACR20 frente al 15% del grupo placebo [21].
Moléculas pequeñas
Otro fármaco aprobado en Suiza en 2015 es el apremilast (Otezla®), una pequeña molécula oral inhibidora de la fosfodiesterasa 4 (PDE4) para el tratamiento de la psoriasis (PsO) y la artritis psoriásica (PsA), que pertenece al grupo de las “pequeñas moléculas dirigidas”. El inhibidor de la PDE4 apremilast regula intracelularmente la producción de citoquinas inflamatorias, que desempeñan un papel en la inmunopatofisiología de la PsO, al elevar los niveles intracelulares de AMPc. Se reduce la producción de citocinas proinflamatorias (como TNF-α, IL-23, IL-17), mientras que se promueve la producción de citocinas antiinflamatorias. En los ensayos ESTEEM 1 y 2, aproximadamente seis veces más pacientes lograron una respuesta PASI75 en la semana 16 con apremilast que con placebo (concretamente, un tercio de los pacientes con apremilast presentaron una mejora del 75% de la psoriasis en 16 semanas). La respuesta se mantuvo durante 52 semanas. El 22% de los pacientes tratados con apremilast también lograron una curación casi completa de la PsO después de 16 semanas (sPGA: 21,7% frente a 3,9%). Además, el apremilast mostró buenos resultados en zonas difíciles de tratar como el cuero cabelludo (scPGA) y la infestación de las uñas (NAPSI) ya en la semana 16. El picor disminuyó más durante este tiempo que con el placebo, pero también en este caso los biológicos individuales tienen un efecto más rápido y posiblemente más fuerte. La calidad de vida mejoró clínicamente de forma significativa en comparación con el grupo placebo (reducción del DLQI ≥5: 70% frente a 34%) [22]. El tratamiento con Apremilast fue bien tolerado (sin aumento del riesgo de infecciones) y, en consecuencia, dio lugar a una menor tasa de interrupción del tratamiento. Los efectos secundarios experimentados incluyeron: Diarrea, náuseas, dolor de cabeza e infecciones de las vías respiratorias superiores, sobre todo durante las dos primeras semanas de tratamiento. En general, los síntomas de la diarrea desaparecieron en cuatro semanas sin intervención médica con un tratamiento continuado con Otezla® [22,23]. El apremilast se aumenta inicialmente como una titulación durante cinco días (paquete de titulación de 10/20/30 mg), después se administra como terapia de mantenimiento a 30 mg 2×/d. El apremilast también puede utilizarse para tratar la artritis psoriásica, como se demostró en el estudio PALACE1 (n=504). El tratamiento con apremilast dio lugar a una respuesta ACR20 significativamente mayor (38,1% frente a 19,0%) en comparación con el placebo en la semana 16. La tasa de respuesta ACR20 mejoró progresivamente entre la semana 24 y la semana 52 hasta el 63% (apremilast 20 mg BID) y el 55% (apremilast 30 mg BID), respectivamente. Apremilast también mostró una mejora significativa de los síntomas de la APs (hinchazón, dolor, entesitis, dactilitis), el funcionamiento físico y la calidad de vida (SF36, HAQ-DI). Las mejoras en los parámetros relevantes se mantuvieron hasta la semana 52 [23].
Outlook
Con los avances de la inmunología en la comprensión de la patogénesis de la psoriasis, el desarrollo de fármacos con mayor selectividad y el reconocimiento de la naturaleza sistémica de la psoriasis, la terapia ha mejorado. Al mismo tiempo, se complicó. En particular, la integración de biológicos y pequeñas moléculas en el tratamiento de la psoriasis grave ha supuesto un cambio de paradigma en dermatología: La piel vuelve a formar parte de todo el organismo, que se ve igualmente afectado por la psoriasis en el área de la psique, el sistema cardiovascular o el sistema musculoesquelético como en el tegumento. Sobre todo debido a los ensayos clínicos con biológicos, aumentó la atención prestada a los instrumentos de calidad de vida como otra medida del éxito del tratamiento. Tenemos gran curiosidad por ver hasta qué punto el uso de biológicos tendrá también un efecto favorable sobre las comorbilidades y la esperanza de vida a largo plazo. Ya sea en la clínica o en la consulta dermatológica: los factores decisivos en cada caso concreto son la indicación médica y la falta de alternativas terapéuticas genuinas más baratas. La psoriasis y la artritis psoriásica deben tratarse en un equipo formado por dermatólogos, reumatólogos y médicos generalistas.
Es de gran importancia reconocer tanto las manifestaciones cutáneas de la psoriasis como las comorbilidades de la psoriasis en una fase temprana y tratarlas eficazmente.
Literatura:
- Jemec GB, et al: Una nueva formulación para el cuero cabelludo de calcipotrieno más betametasona comparada con sus principios activos y el vehículo en el tratamiento de la psoriasis del cuero cabelludo. Un ensayo aleatorizado, doble ciego y controlado. J Am Acad Dermatol 2008; 59: 455-463.
- Barbagallo J, et al: Fototerapia UVB de banda estrecha para el tratamiento de la psoriasis. Una revisión y actualización. Cutis 2001; 68: 345-347.
- Saurat JH, et al: Estudio multicéntrico doble ciego aleatorizado que compara acitretina-PUVA, etretinato-PUVA y placebo-PUVA en el tratamiento de la psoriasis grave. Dermatologica 1988; 177: 218-224.
- Heydendael VM, et al: Metotrexato frente a ciclosporina en la psoriasis crónica en placas de moderada a grave. N Engl J Med 2003; 349: 658-665.
- Nyfors A: Beneficios y experiencias farmacológicas adversas durante el tratamiento a largo plazo con metotrexato de 248 psoriásicos. Dan Med Bull 1978; 25: 208-211.
- Trüeb RM: Recomendaciones de consenso metotrexato. Gebro Pharma 2008.
- van de Kerkhof PC, et al: Efecto de la adición de calcipotriol en pomada (50 microgramos/g) al tratamiento con acitretina en la psoriasis. Br J Dermatol 1998; 138: 84-89.
- Gupta AK, et al: Perfil de efectos secundarios del tratamiento con acitretina en la psoriasis. J Am Acad Dermatol 1989; 20: 1088-1093.
- Griffiths CE, et al: Eliminación de la psoriasis con dosis bajas de ciclosporina. Br Med J (Clin Res Ed) 1986; 293: 731-732.
- Lowe NJ, et al: Tratamiento a largo plazo con dosis bajas de ciclosporina para la psoriasis grave. Efectos sobre la función y la estructura renales. J Am Acad Dermatol 1996; 35: 710-719.
- Koo J: Estudio aleatorizado, doble ciego, que compara la eficacia, la seguridad y la dosis óptima de dos formulaciones de ciclosporina, Neoral y Sandimmun, en pacientes con psoriasis grave. Grupo de estudio OLP302. Br J Dermatol 1998; 139: 88-95.
- Laburte C, et al: Eficacia y seguridad de la ciclosporina A oral (CyA; Sandimmun) para el tratamiento a largo plazo de la psoriasis en placas crónica grave. Br J Dermatol 1994; 130: 366-375.
- Altmeyer PJ, et al.: Efecto antipsoriásico de los derivados del ácido fumárico. Resultados de un estudio multicéntrico doble ciego en 100 pacientes. J Am Acad Dermatol 1994; 30: 977-981.
- Gollnick H, et al: El calcipotriol tópico más ácido fumárico oral es más eficaz y de acción más rápida que la monoterapia con ácido fumárico oral en el tratamiento de la psoriasis vulgar en placas crónica grave. Dermatología 2002; 205: 46-53.
- Altmeyer P, Hartwig R, Matthes U: [Perfil de eficacia y seguridad de los ésteres de ácido fumárico en el tratamiento oral a largo plazo de la psoriasis vulgar grave refractaria al tratamiento. Un estudio de 83 pacientes]. Dermatólogo 1996; 47: 190-196.
- Gottlieb AB, et al: Un ensayo aleatorizado de etanercept como monoterapia para la psoriasis. Arch Dermatol 2003; 139: 1627-1632; discusión 32.
- Paller AS, et al: Tratamiento con etanercept en niños y adolescentes con psoriasis en placas. N Engl J Med 2008; 358: 241-251.
- Leonardi CL, et al: Eficacia y seguridad del ustekinumab, un anticuerpo monoclonal contra la interleucina-12/23 humana, en pacientes con psoriasis: resultados de 76 semanas de un ensayo aleatorizado, doble ciego y controlado con placebo (PHOENIX 1). Lancet 2008; 371: 1665-1674.
- Papp KA, et al: Eficacia y seguridad del ustekinumab, un anticuerpo monoclonal contra la interleucina-12/23 humana, en pacientes con psoriasis: resultados de 52 semanas de un ensayo aleatorizado, doble ciego y controlado con placebo (PHOENIX 2). Lancet 2008; 371: 1675-1684.
- Langley RG, et al: Secukinumab in plaque psoriasis-results of two phase 3 trials. N Engl J Med 2014; 371: 326-338.
- McInnes IB, et al: Eficacia y seguridad del secukinumab, un anticuerpo monoclonal anti-interleucina-17A totalmente humano, en pacientes con artritis psoriásica de moderada a grave: un ensayo de prueba de concepto de fase II, aleatorizado, doble ciego y controlado con placebo, de 24 semanas de duración. Ann Rheum Dis 2014; 73: 349-356.
- Papp K, et al.: Apremilast, un inhibidor oral de la fosfodiesterasa 4 (PDE4), en pacientes con psoriasis en placas de moderada a grave. Resultados de un ensayo de fase III, aleatorizado y controlado (Ensayo de eficacia y seguridad que evalúa los efectos del apremilast en la psoriasis [ESTEEM] 1). J Am Acad Dermatol 2015; 73: 37-49.
- Schafer PH, et al: El impacto farmacodinámico del apremilast, un inhibidor oral de la fosfodiesterasa 4, en los niveles circulantes de biomarcadores inflamatorios en pacientes con artritis psoriásica. Resultados de un subestudio de fase III, aleatorizado y controlado con placebo (PALACE 1). J Immunol Res 2015; 2015: 906349.
PRÁCTICA DERMATOLÓGICA 2016: 26(2): 10-16