Los inhibidores orales de la cinasa Janus (JAKi) están ganando terreno en el tratamiento de las enfermedades reumatoides inflamatorias, por lo que también fueron un tema muy debatido en el congreso anual de este año de la Sociedad Suiza de Reumatología (SGR). La Prof. Dra. med. Andrea Rubbert-Roth y el Prof. Dr. med. Gerd Burmester informaron sobre los avances actuales.
“Lo que siempre quiso saber sobre JAKi”. Este fue el título del Simposio Satélite de AbbVie celebrado el 8 de septiembre en Interlaken, moderado por la Prof. Andrea Rubbert-Roth, de St. Gallen, y el Prof. Gerd Burmester, de Berlín. Los participantes no esperaban una conferencia frontal clásica, sino un “juego de dados” interactivo. Un cubo de tela de gran tamaño decidía qué enfoque temático en torno al JAKi debía debatirse; a continuación, los participantes votaban la pregunta concreta al experto. Se prestó especial atención al inhibidor selectivo de JAK upadacitinib (UPA; RINVOQ®), que actualmente es el único JAKi en Suiza que puede utilizarse en las tres indicaciones espondiloartritis anquilosante (EA), artritis psoriásica (APs) y artritis reumatoide (AR) [1-3].

Prof. Dr med. Andrea Rubbert-Roth y Prof. Dr med. Gerd Burmester en el Congreso de la SGR 2022.
¿Son los eventos cardiovasculares un efecto de clase del JAKi?
La primera tirada: un 6 – ¡Pregunta Joker! El estrangulador del público quiere saber: “¿Son los eventos cardiovasculares un problema general de JAKi?”. Prof. A este respecto, Burmester habla en primer lugar del estudio prospectivo, aleatorizado, abierto y de vigilancia ORAL posterior a la comercialización, que investigó la no inferioridad del JAKi tofacitinib frente a los inhibidores del factor de necrosis tumoral (TNFi) etanercept o adalimumab (ADA) en lo que respecta a la aparición de acontecimientos cardiovasculares graves (MACE) y neoplasias malignas en 4.362 pacientes mayores de 50 años con artritis reumatoide (AR) y al menos otro factor de riesgo cardiovascular. El resultado: el tofacitinib mostró un mayor riesgo de MACE y neoplasias malignas que el TNFi de comparación [4]. ¿Es esto ahora un efecto de clase del JAKi? “Sabemos que los JAKi tienen propiedades diferentes, como su semivida, su metabolización y su selectividad”, afirma el Prof. Burmester. Además, hay algunos puntos importantes que deben tenerse en cuenta a la hora de interpretar los datos de vigilancia ORAL, por ejemplo, la elevadísima actividad de la enfermedad, la duración a menudo larga de la enfermedad y el pretratamiento mayoritariamente subóptimo de la población de pacientes, en su mayoría estadounidenses. Si estos resultados pueden trasladarse a las poblaciones europeas debe investigarse en análisis posteriores, por ejemplo con registros.
Discutir los objetivos de la terapia y alinear las expectativas al inicio del tratamiento
A continuación, surge una pregunta práctica: “¿Qué puntos importantes discute con los pacientes al iniciar la terapia?” El profesor Rubbert-Roth señala las posibles discrepancias entre el paciente y el médico con respecto al objetivo de la terapia. “Los parámetros importantes para los pacientes son sobre todo el dolor, la capacidad funcional, la fatiga y el sueño. Los médicos, por su parte, tienden a centrarse más en las medidas objetivas, como los parámetros inflamatorios y las imágenes [5-10].” El Prof. Burmester añade: “A lo largo de los años, los resultados relacionados con los pacientes (PRO) también han cobrado cada vez más importancia para mí. Con los relojes de fitness disponibles hoy en día, podemos medir objetivamente parámetros sencillos como la calidad del sueño o el número de pasos diarios.” Además, las expectativas de los pacientes sobre el éxito de la terapia han aumentado considerablemente, según el Prof. Burmester: “En el pasado, lo importante era no acabar en una silla de ruedas. Hoy, el objetivo principal es poder jugar un tercer set de tenis. Tenemos que respetar estas altas expectativas e intentar cumplirlas”.
Perfil de seguridad del AUP en relación con las infecciones graves y la malignidad
“¿Qué pasa con las infecciones graves bajo la UPA?”, quieren saber ahora los participantes. El Prof. Rubbert-Roth muestra los resultados de un análisis integrado de la seguridad de la UPA en la AR, la EA y la APs (figura 1). Su conclusión: Las tasas de infecciones graves e infecciones oportunistas fueron en general similares en todos los grupos de tratamiento dentro de cada indicación. El Prof. Burmester subraya el buen perfil de riesgo especialmente en pacientes con EA [11]. En cuanto al aumento de las tasas de herpes zóster entre los UPA, también hace un llamamiento a la vacunación con Shingrix®, con la que se puede minimizar en gran medida el riesgo de herpes zóster. También en términos de malignidad, el análisis integrado de seguridad no mostró diferencias significativas entre el AUP y el ADA o el metotrexato (MTX) en la AR y la APs, respectivamente [11]. “Estamos en lo cierto al suponer que aquí no hay señal. En la EA, que suele afectar a pacientes más jóvenes, las tasas de malignidad son incluso más bajas que en la AR y la APs”, comenta el Prof. Rubbert-Roth.
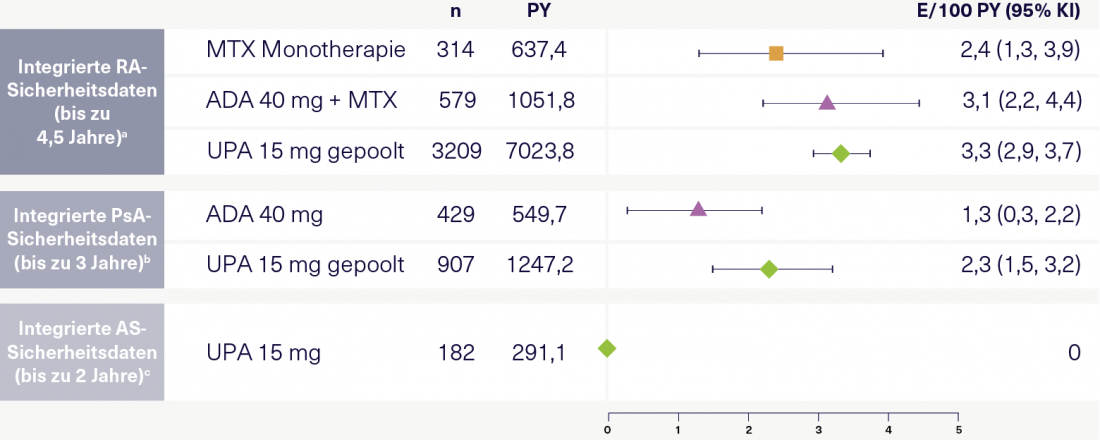
Figura 1: Infecciones graves por cada 100 pacientes-año en AR, APs y EA según el análisis integrado de seguridad UPA. Adaptado según [11].
a Incluye 6 ensayos aleatorizados UPA-RA del programa de ensayos SELECT. Los datos se agruparon según el tratamiento y/o el régimen de dosificación. b Pacientes con respuesta inadecuada o intolerancia a ≥ 1 FAME no biológico (SELECT-PsA 1) o ≥ 1 FAME biológico (SELECT-PsA-2). c Pacientes de SELECT-AXIS 1. ADA, adalimumab; AS, espondilitis anquilosante; bDMARD, fármaco antirreumático modificador de la enfermedad biológico; KI, intervalo de confianza; E, acontecimiento; MTX, metotrexato; PsA, artritis psoriásica; PY, pacientes-año; AR, artritis reumatoide; UPA, upadacitinib.
¿Cuándo puede utilizarse el AUP como monoterapia?
“Cada vez son más los pacientes que se quejan de intolerancia al MTX y ya no quieren tomarlo”, informa el Prof. Burmester. Por ello, una monoterapia eficaz y tolerable resulta cada vez más atractiva. En el ensayo aleatorizado y doble ciego de fase III SELECT-MONOTHERAPY, los pacientes con AR con una respuesta inadecuada al MTX en monoterapia con UPA (15 mg, 1 vez al día) alcanzaron una tasa de remisión del DAS28-CRP (<2,6) del 28% a las 14 semanas, en comparación con el 8% en monoterapia con MTX (p ≤ 0,0001) [12]. En el ensayo aleatorizado y doble ciego de fase III SELECT-COMPARE, las tasas de remisión a las 12 semanas fueron del 29% con UPA (15 mg, 1 vez al día) + MTX, del 6% con placebo + MTX y del 18% con ADA (40 mg, quincenalmente) + MTX (ambas p ≤ 0,001) [13]. Prof. Burmester: "No se aprecia una gran diferencia si el UPA se combina con MTX o no. Si un paciente ya está recibiendo MTX bajo JAKi y lo tolera bien, el MTX también puede continuarse". "A menudo, los pacientes deciden cambiar ellos mismos a la monoterapia", añade el Prof. Rubbert-Roth.
¿Hasta qué punto es eficaz el UPA en pacientes con APs y EA con una respuesta inadecuada a los biológicos?
La eficacia del AUP (15 mg, 1 vez al día) en la APs se investigó en dos ensayos aleatorizados de fase III [14, 15]. SELECT PsA 1 incluyó a pacientes sin tratamiento biológico y SELECT PsA 2 a pacientes con respuesta inadecuada a los biológicos. En ambos estudios, el UPA mostró una respuesta significativamente mejor en términos de actividad mínima de la enfermedad (MDA) en comparación con el placebo después de 24 semanas (Figura 2). “La diferencia con el placebo es comparable en ambos estudios, lo que habla en favor de una buena eficacia del UPA en pacientes con APs que no respondieron a los biológicos”, valoración del Prof. Rubbert-Roth. La situación es similar en el caso de la EA (Figura 2) [16, 17]: “También en este caso, la eficacia de la UPA en términos de inactividad de la enfermedad(Puntuación de la actividad de la enfermedad de la espondilitis anquilosante-Enfermedad inactivaASDAS-ID) en los dos estudios de fase III, aleatorizados y controlados con placebo SELECT AXIS 1 con pacientes sin tratamiento biológico y SELECT AXIS 2 con pacientes con respuesta inadecuada a los biológicos comparable -quizá marginalmente mejor en los pacientes sin tratamiento biológico”. Para el Prof. Burmester, el UPA “ofrece una buena alternativa a los inhibidores del TNF y la IL-17 precisamente por su ventajoso perfil de seguridad, que es fácilmente aceptado por los pacientes”.
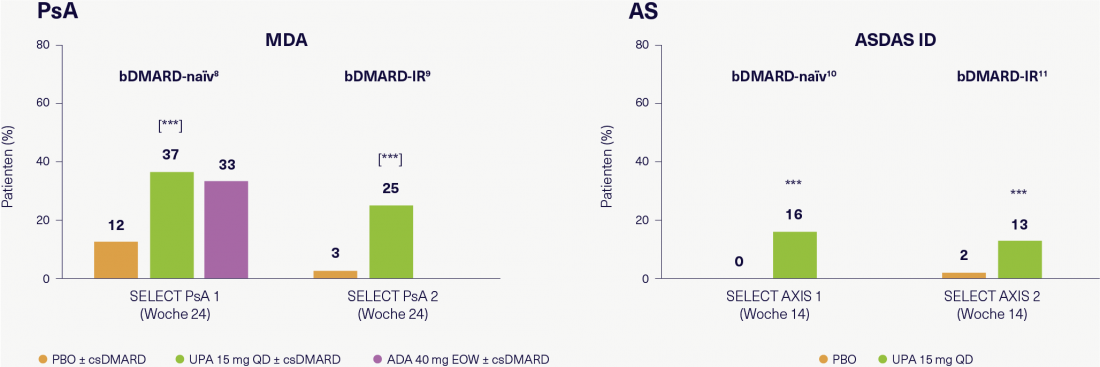
Figura 2: Eficacia del UPA en pacientes sin tratamiento biológico y pacientes con respuesta inadecuada a los biológicos en los ensayos clínicos de APs y EA. Adaptado según [14-17].
*** p ≤ 0,001 frente a PBO; [] = comparaciones ajustadas por multiplicidad. Todos los análisis se realizaron con NRI (imputación de no respondedores). ADA: adalimumab; AS: espondilitis anquilosante; ASDAS: puntuación de la actividad de la enfermedad de la espondilitis anquilosante; ADME: fármaco antirreumático modificador de la enfermedad biológico; ADMEc: fármaco antirreumático sintético convencional; EOW: quincenal; ID: enfermedad inactiva; IR: respuesta inadecuada; MDA: actividad mínima de la enfermedad; PBO: placebo; APs: artritis psoriásica; QD: una vez al día; UPA: upadacitinib.
¿Cómo se comporta la AUP en la práctica en comparación con los ensayos clínicos?
Sobre la cuestión final del rendimiento del AUP en condiciones reales, el Prof. Burmester presenta los resultados provisionales del estudio observacional postcomercialización UPwArds, que investiga la eficacia y seguridad del AUP como monoterapia o en combinación con MTX en pacientes con AR de moderada a grave en la práctica clínica en Alemania [18]. Tras un periodo de observación de 6 meses, el 65% de los pacientes había alcanzado un valor DAS28-CRP <2,6, y también se observaron mejoras en el dolor y la fatiga. "Esto nos proporciona datos que concuerdan bien con los resultados de los ensayos clínicos", concluye el experto.
Referencias
Los profesionales pueden solicitar las referencias en medinfo.ch@abbvie.com.
Informe y entrevista: Dr. sc. nat. Jennifer Keim
A la breve información técnica de RINVOQ
Este artículo ha sido elaborado con el apoyo financiero de AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-RNQR-220089_10/2022
Artículo en línea desde el 17.11.2022












