En hemostasisología, se ha producido un aumento revolucionario de los conocimientos en los últimos años, tanto desde el punto de vista preclínico en la investigación básica como desde el punto de vista clínico con el desarrollo de estrategias de tratamiento innovadoras. El paciente como vara de medir significa poner de relieve los últimos avances en la investigación hemostática en función de su repercusión en la atención actual y futura de los pacientes. La conferencia anual de este año estuvo a la altura de esta afirmación.
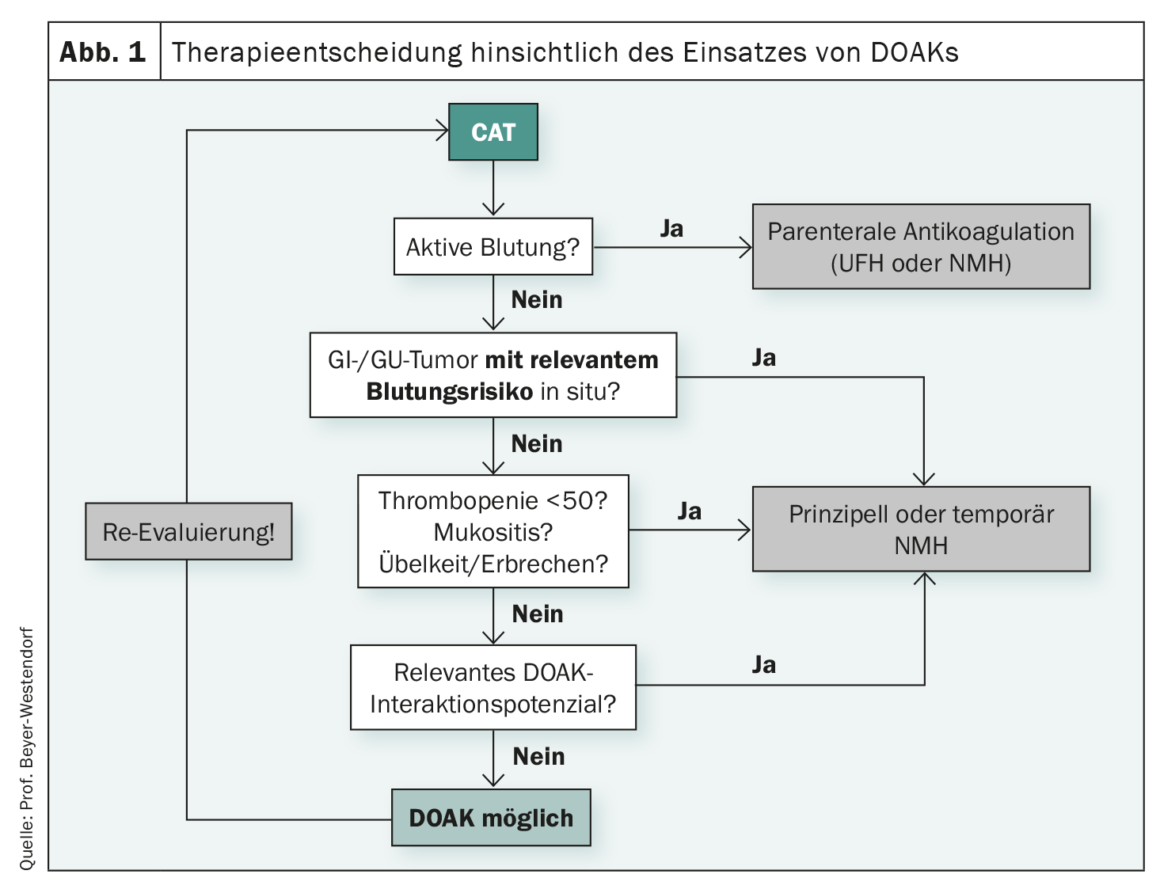
Las directrices están diseñadas para simplificar las decisiones en la práctica diaria. Pero no siempre es así, como demostró el Prof. Dr. med. Jan Beyer-Westendorf, de Dresde (D), utilizando la anticoagulación en el tromboembolismo venoso asociado a tumores (TEV tumoral). Si se va a iniciar la anticoagulación en pacientes con tumores, se sabe que el riesgo de recidiva, así como de hemorragia, es muy elevado. Con el tratamiento con antagonistas de la vitamina K (AVK), se observó una TEV recurrente en el 6,8% de los pacientes no oncológicos y en el 20,7% de los pacientes con cáncer. El riesgo de hemorragia grave para los pacientes tumorales en tratamiento con AVK es del 12,4%, para los pacientes sin enfermedad oncológica del 4,9%. Para empeorar las cosas, el riesgo de TEV cambia con el tiempo. En consecuencia, la evaluación riesgo-beneficio de la anticoagulación en pacientes con tromboembolismo asociado al cáncer (TAC) es especialmente difícil, subrayó el experto. Si se consultan ahora las directrices, las recomendaciones actuales son que se utilicen DOAK y NMH para la terapia de la ETV tumoral. Esto refleja un cambio de paradigma, porque ya no se trata de si hay que anticoagular en absoluto, la heparina no fraccionada y los antagonistas de la vitamina K sólo desempeñan un papel en contadas ocasiones y el estándar terapéutico de los últimos 20 años con heparinas de bajo peso molecular (HBPM) se complementa ahora con anticoagulantes orales directos (ACOD). La verdadera cuestión clave hoy en día es más bien cuándo utilizar NMH y cuándo es mejor utilizar DOAK. La selección de pacientes de los estudios DOAC-CAT puede dar una pista. Aquí, los pacientes trombopénicos, los afectados por tumores cerebrales y los que padecían tumores del tracto gastrointestinal superior estaban generalmente excluidos o infrarrepresentados. Además, existe un mayor riesgo de hemorragia en los DOAK y el riesgo de hemorragia varía en función del tipo de tumor. También debe tenerse en cuenta el potencial de interacción con otros medicamentos, dijo. Según su experiencia, la terapia DOAK alcanza sus límites clínicos en pacientes con disfagia, lesiones mucosas y náuseas o vómitos, y cuando se requiere anticoagulación a pesar de los estigmas hemorrágicos y la trombocitopenia clínicamente relevante. (Fig. 1). En principio, sin embargo, Beyer-Westendorf está convencida de que la NMH y el DOAK son opciones equivalentes e importantes “codo con codo” para los pacientes tumorales con ETV, que muchos pacientes también pueden beneficiarse de la sencillez del uso del DOAK, pero que debe considerarse cuidadosamente cuando, entre otras cosas, las contraindicaciones complican o incluso impiden su uso.
Aspectos específicos de la mujer en el CAT
La incidencia de la TEV en las enfermedades tumorales es elevada, especialmente en el cáncer de ovario. Además, la incidencia depende del estadio. Mientras que el carcinoma pancreático sigue ocupando el primer lugar en los estadios I y II y el carcinoma ovárico el segundo, éstos son superados por el carcinoma endometrial en el estadio IV. Si se dirige la atención a los efectos de la ETV sobre la mortalidad, éstos muestran efectos claros en el carcinoma de endometrio y de mama, como explicó el doctor Christian Pfrepper, de Leipzig (D). Por consiguiente, la profilaxis de la trombosis desempeña un papel completamente diferente en los tumores ginecológicos. Esto debe hacerse durante la quimioterapia en pacientes de alto riesgo con apixaban, rivaroxaban o NMH. Para las operaciones tumorales en el abdomen/pelvis, debe administrarse HNM, HNF o apixabán durante cuatro semanas, a menos que exista un alto riesgo de hemorragia.
La doctora Sandra Marten, de Dresde (D), añadió que la principal indicación de la anticoagulación en pacientes menores de 50 años es la prevención y el tratamiento de la TEV. Los DOAK se utilizan en gran medida con este fin, cada vez más también en mujeres en edad reproductiva. Esto plantea nuevos retos en relación con el efecto de la terapia sobre la hemorragia menstrual, la prevención o planificación del embarazo y el riesgo de exposición al DOAK durante el embarazo y la lactancia. Hay muchas discusiones de pacientes en Internet sobre el aumento del sangrado menstrual bajo DOAK. Así lo demuestran también los amplios estudios en los que se observó hipermenorrea o menstruación prolongada. Sólo el dabigatrán no mostró esta señal. Esto se debe, por un lado, a la alteración del estado hormonal debido a un cambio en la anticoncepción o a la terapia hormonal después de una ETV y, por otro, al efecto directo de los DOAK sobre los factores de coagulación, la pared uterina, así como al sinergismo con los anticoagulantes naturales, necesarios para la hemorragia menstrual, según el experto. Si se produce hipermenorrea o hemorragia uterina atípica, debe reducirse la dosis de DOAK o cambiarse a dabigatrán, o debe interrumpirse el tratamiento y cambiarse a AAS.
La siguiente pregunta se refiere a la evitación o planificación del embarazo durante la terapia con DOAC. La anticoncepción adecuada es sin duda el enfoque correcto, afirma el experto. El aumento del riesgo de TEV recurrente debido a los anticonceptivos hormonales parece ser pequeño, y el beneficio es superior al riesgo. Antes de desescalar la terapia DOAK, es aconsejable una reevaluación que incluya el cambio de la píldora que contiene estrógenos a una alternativa más segura.
Con respecto a un embarazo planeado, debe considerarse el cambio a otro anticoagulante. El cambio a NMH es seguro, eficaz y no hay signos de embriotoxicidad. Sin embargo, el tratamiento es desagradable y está asociado a riesgos como la HIT y la osteoporosis. El cambio a AVK es posible hasta que se produzca el embarazo debido a la conocida embriotoxicidad. Por lo demás, la terapia oral es eficaz y se dispone de datos y recomendaciones válidos. El tiempo crítico de exposición en la semana seis a doce del embarazo y el frecuente solapamiento debido a la detección del embarazo y la semivida del AVK no deben subestimarse. En principio, la paciente también podría seguir con la terapia DOAK hasta que se confirme el embarazo. El tratamiento también es oral, eficaz y los DOAK tienen una semivida muy corta. Sin embargo, el riesgo desconocido de embriotoxicidad y la falta de recomendaciones hasta el momento hablan en contra, resumió Marten su visión de conjunto.
Durante el embarazo, por el contrario, debe cambiarse en cualquier caso de DOAK a NMH. No obstante, la exposición al DOAK no es motivo para interrumpir un embarazo. Sin embargo, se recomienda una cogestión ginecológica precoz y un seguimiento fetal. La terapia DOAK durante la lactancia tampoco está indicada. Por lo tanto, en función de la evaluación de riesgos y beneficios, se debe interrumpir la lactancia materna o pasar a la NMH.
Congreso: 67. Jahrestagung der Gesellschaft für Thrombose- und Hämostaseforschung (GTH) 2023
InFo ONKOLOGIE & HÄMATOLOGIE 2023; 11(2): 20–21