Con el oligonucleótido en antisentido nusinersen, se aprobó en 2017 el primer fármaco para el tratamiento causal de pacientes con atrofia muscular espinal asociada a 5q (5q-SMA) [1]. El fármaco se dirige a la causa de la enfermedad, la falta de la proteína SMN [1]. Amplios estudios clínicos y en condiciones reales han demostrado que el nusinersén puede conducir a la estabilización e incluso a la mejora de la función motora – en todos los grupos de edad y en los tipos I-III de AME [2-7].
La 5q-SMA es una enfermedad neomuscular progresiva autosómica recesiva [8]. Si no se trata, los pacientes corren el riesgo de sufrir una degeneración progresiva de las motoneuronas, lo que provoca una debilidad y atrofia crecientes de los músculos [8]. Hasta la introducción de una terapia farmacológica causalmente eficaz, la forma infantil de 5q-SMA, en la que los síntomas ya son perceptibles en los primeros 6 meses de vida, se consideraba una de las causas genéticas más comunes de muerte en bebés y niños pequeños [8]. Con el nusinersén (SPINRAZA®), se dispone de una opción terapéutica que permite mantener o incluso aumentar la fuerza muscular [1-7].
El nusinersén conduce a la formación de mayores cantidades de proteína SMN [9].
La causa de la denervación progresiva de los músculos esqueléticos es una deficiencia de la proteína “motoneurona de supervivencia” (SMN), vital para las motoneuronas. Debido a mutaciones o deleciones en el gen SMN1, en los pacientes con 5q-SMA se produce muy poca proteína SMN [8].
El nusinersén contribuye a la producción de una proteína SMN más funcional y garantiza así la supervivencia de las motoneuronas [9]. Esto puede ralentizar o incluso detener el curso de la enfermedad. Los pacientes se benefician de la conservación o mejora de la función muscular. Se ha demostrado la eficacia del nusinersén en todas las edades y estados de la enfermedad: bebés con AME 5q presintomática, niños y adolescentes sintomáticos y adultos [2-7].
Los niños con 5q-SMA se benefician de la terapia presintomática
En los ensayos clínicos, muchos niños con AME 5q tratados con nusinersén pudieron alcanzar importantes hitos motores no observados en pacientes con AME 5q no tratados [2-4]. Esto demostró que la terapia temprana con SPINRAZA puede permitir un desarrollo adecuado a la edad en niños con 5q-SMA. La mayoría de los pacientes con diagnóstico genético de 5q-SMA que fueron tratados de forma presintomática con nusinersén en el ensayo clínico NURTURE habían alcanzado los hitos motores adecuados a su edad en la evaluación intermedia del estudio (Tab. 1) [10].
Tabla 1: Evaluación provisional del estudio NURTURE en febrero de 2020; edad media de los participantes en el estudio 3,8 años (n = 25) [10]
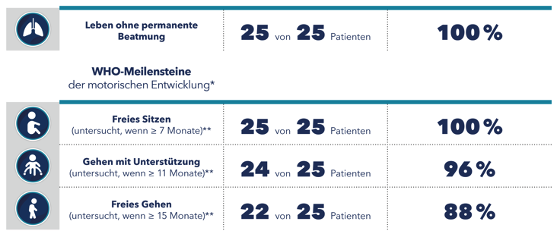





* Edad a la que los niños sanos alcanzan normalmente estos hitos.
** La hora del examen estaba dentro del margen de tiempo especificado por la OMS [11]
También se observaron mejoras significativas en las funciones bulbares, necesarias para masticar y tragar [12]. Mientras que muchos pacientes no tratados con 5q-SMA se cansan al masticar, se atragantan con la comida o necesitan una sonda de alimentación [13-16], el tratamiento presintomático con nusinersen en el estudio NURTURE consiguió que el 92% de los niños siguieran tragando y el 84% se las arreglara sin una sonda de alimentación [12]. En consecuencia, los padres de los niños con 5q-SMA tratados con nusinersen no estaban preocupados en general por la deglución, la alimentación y el peso de sus hijos. [12].
La eficacia del nusinersén también se ha demostrado en adultos
Amplios datos de estudios observacionales en pacientes adultos con 5q-SMA demuestran que el tratamiento con nusinersén puede conducir a mejoras significativas en todas las escalas de función motora utilizadas (HFMSE, RULM, distancia de 6 minutos andando) [5-7].
En un estudio prospectivo y multicéntrico en el que participaron 139 pacientes de 10 centros clínicos de Alemania, una elevada proporción de pacientes con 5q-SMA tipo II o III mostraron mejoras clínicamente relevantes en la función motora. En todos los puntos temporales del estudio, los pacientes lograron mejoras estadísticamente significativas en la puntuación HFMSE de media. Ésta había aumentado 3,12 puntos al cabo de 14 meses. Sin embargo, en el curso natural de la enfermedad, la puntuación HFMSE disminuye una media de 0,5-1,0 puntos al año [6]. En los adultos se observó una mejora comparable en la puntuación HFMSE que en los niños (Tab. 2) [6].
Tabla 2: Cambios medios en la puntuación HFMSE desde el inicio: Comparación de 126 niños con aparición tardía de la enfermedad 5q-SMA del estudio CHERISH y 173 pacientes adultos del estudio Hagenacker et al. Publicación [3,6].

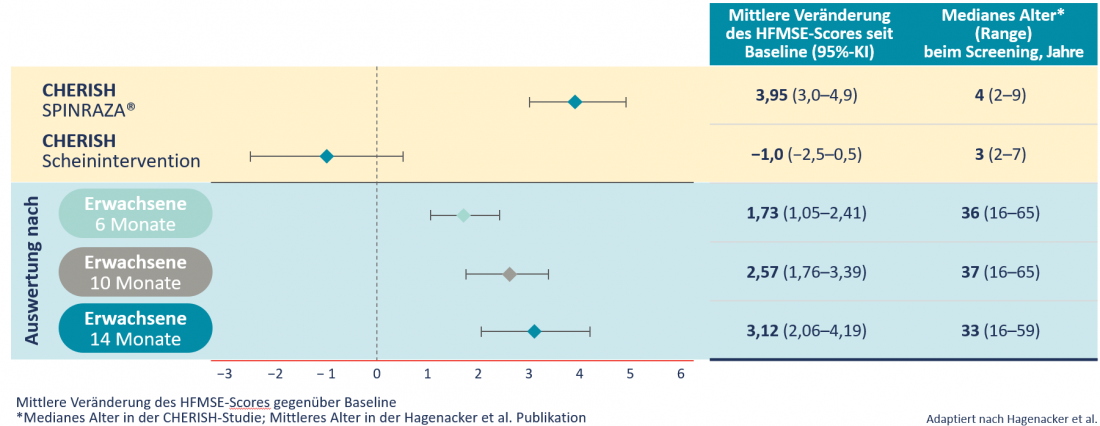
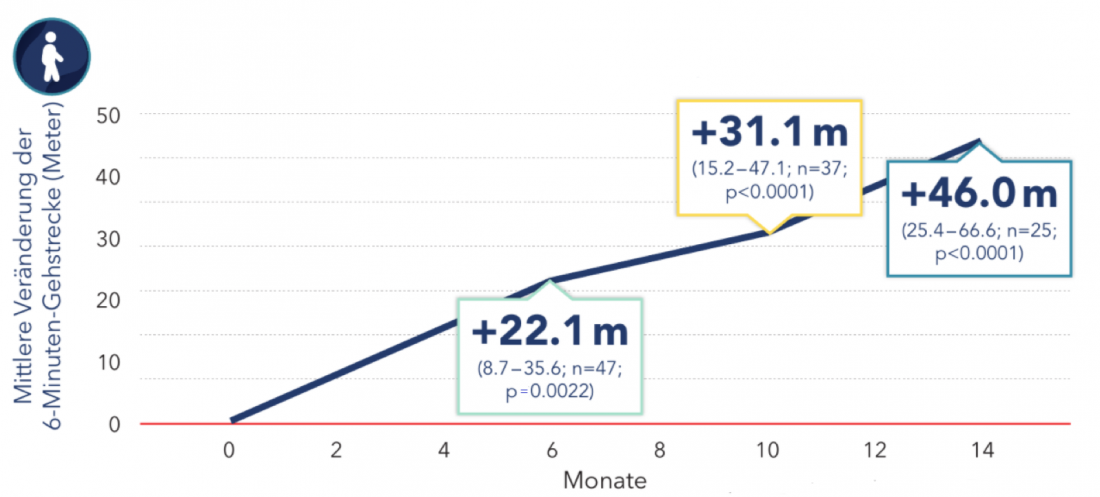
La puntuación RULM, que mide la función de las extremidades superiores, mostró una mejora significativa de 1,09 puntos de media tras 14 meses en el estudio. Además, los pacientes consiguieron recorrer una media de 403 metros en 6 minutos. Por término medio, fueron capaces de caminar 46 metros más que antes del inicio de la terapia (Fig. 2) [6].
La edad de los pacientes no influyó en los resultados. Sin embargo, el alcance de las mejoras dependía de la función motora residual del paciente al inicio del estudio. Cuanto mayor sea el nivel de función motora residual antes del inicio de la terapia, mayor será el efecto esperado de la terapia con nusinersén [6].
Figura 2: Cambio en la distancia caminada de 6 minutos en adultos con terapia de nusinersen. Los recuadros muestran la media y el IC del 95% [6]. Modificado según Hagenacker T et al. [6].
Los pacientes quieren participar en la vida normal
Muchos pacientes adultos desean mantener su fuerza para poder sentarse, levantarse y caminar de forma independiente [17]. Las funciones de las manos y los brazos son indispensables para las tareas cotidianas, como poder lavarse o vestirse de forma independiente. La motricidad fina también desempeña un papel importante en el entorno social de los pacientes, que se manifiesta en el uso de un smartphone o un ordenador portátil.
Sin embargo, en el curso natural de la 5q-SMA, se produce una debilidad muscular progresiva y una pérdida de la función motora [8]. El tratamiento con nusinersén puede dar esperanzas de futuro a los adultos con 5q-SMA. De este modo, los pacientes no sólo pueden conseguir una estabilización a más largo plazo del statu quo funcional, sino que muchos de ellos experimentan mejoras relevantes en las funciones motoras, tienen más fuerza en manos y dedos y pueden levantarse mejor, permanecer más tiempo de pie y caminar más lejos [5-7].
Efecto dirigido – Central al SNC
Al hacerlo, el Nusinersen se dirige a la causa de 5q-SMA. Se une de forma reversible al pre-mRNA del gen SMN2 paralógico, que se utiliza para la formación de la proteína SMN en pacientes con 5q-SMA. Esto desplaza los factores de empalme y el exón 7 permanece en el ARNm SMN2 maduro, de modo que se puede formar una proteína SMN más funcional (Fig. 3) [1, 9].
Figura 3: Mecanismo de acción dirigido del nusinersén [9].

El nusinersén se administra por vía intratecal a través de una punción lumbar, por lo que llega directamente a donde se supone que debe actuar: el sistema nervioso central [1]. La aplicación intratecal garantiza que el nusinersén llegue directamente al lugar central de acción, donde puede ejercer su efecto dirigido y específico sobre el ARNpre-m del gen SMN2 [1]. El efecto del nusinersén se establece rápidamente, tan pronto como de 1 a 3 días después de la inyección [18]. La alta especificidad del nusinersén y su aplicación dirigida al sistema nervioso central han demostrado ser seguras en su uso a largo plazo y también han dado lugar a un efecto sostenido sobre la función motora en una amplia gama de pacientes con AME 5q [5-7,10,19-23].
Al mismo tiempo, la aplicación intratecal presenta ventajas en términos de adherencia. Los datos hasta la fecha muestran que la mayoría de los pacientes están recibiendo sus dosis de nusinersén según lo previsto [24]. Para otras enfermedades, se ha demostrado que el cumplimiento es mayor para las terapias administradas en una clínica que para las terapias orales diarias [25,26]. Por lo tanto, es razonable suponer que, gracias a la administración intratecal, los médicos pueden estar seguros de que los pacientes reciben la dosis correcta de nusinersén en el momento adecuado y de que su salud y su respuesta al tratamiento pueden controlarse de forma rutinaria.
No se esperan efectos secundarios sistémicos
Una ventaja importante del uso intratecal del nusinersén es la exposición específica al compartimento, que hace improbables los efectos secundarios sistémicos. Esto se confirmó tanto en estudios clínicos como en estudios reales. La cefalea, el dolor de espalda y los vómitos son los acontecimientos adversos más frecuentemente observados asociados a la administración intratecal [1]. Pueden producirse poco después de la administración de nusinersén y se deben en gran medida al síndrome postpunción que puede aparecer tras las punciones lumbares incluso sin la aplicación de sustancias medicamentosas [6]. El perfil de seguridad del nusinersén está bien documentado a lo largo de 7 años [19].
También puede utilizarse para la escoliosis
Incluso en los casos de escoliosis pronunciada u otras deformidades graves de la columna vertebral, que son frecuentes en los pacientes con AME 5q, la inyección intratecal de nusinersén puede ser generalmente exitosa, segura y rápida [27]. Si es necesario, la inyección en el espacio del LCR debe realizarse bajo control por imagen mediante tomografía computarizada (TC) [27].
Conclusión
La aplicación central de nusinersén proporciona un efecto selectivo directamente donde se necesita. La eficacia del nusinersén ha quedado demostrada en amplios ensayos clínicos y en estudios reales para todas las edades y severidades de la AME 5q [2-7]. Los pacientes adultos con 5q-SMA también pueden beneficiarse de la terapia y lograr una estabilización clínicamente significativa o mejoras en la función motora [5-7].
El beneficio del nusinersén también se refleja en la satisfacción de los pacientes: en un estudio observacional prospectivo de pacientes adultos realizado en Alemania, el 95,7% declaró estar satisfecho con el nusinersén – independientemente de la edad y la gravedad de la enfermedad [28].
Mientras tanto, existe una amplia experiencia de la práctica clínica diaria. Más de 11.000 pacientes en todo el mundo han sido tratados con nusinersén hasta la fecha [29].
Literatura
- Información técnica de SPINRAZA®, a partir de agosto de 2019 (www.swissmedicinfo.ch)
- Finkel RS, Mercuri E, Darras BT, et al. Nusinersenversus Sham Control in Infantile-Onset Spinal Muscular Atrophy. N Eangl J Med. 2017;377:1723-32.
- Mercuri E, Darras BT, Chiriboga CA, et al. Nusinersen versus Sham Control in Later-Onset Spinal Muscular Atrophy. N Engl J Med. 2018;378:625-35.
- De Vivo DC, Bertini E, Swoboda KJ, et al. Nusinersen iniciado en lactantes durante la fase presintomática de la atrofia muscular espinal: Resultados provisionales de eficacia y seguridad del estudio de fase 2 NURTURE. Neuromuscul Disord. 2019;29:842-56.
- Walter MC, Wenniger S, Thiele S, et al. Safety and Treatment Effects of Nusinersen in Longstanding Adult 5q-SMA Type 3 – A Prospective Observational Study. J Neuromuscul Dis. 2019;6:453-65.
- Hagenacker T, Wurster CD, Günther R, et al. Nusinersen en adultos con atrofia muscular espinal 5q: un estudio de cohortes observacional, multicéntrico y no intervencionista. Lancet Neurol. 2020;19:317-25.
- Maggi L, Bello L, Bonanno S, et al. Nusinersensafety and effects on motor function in adult spinal muscular atrophy type 2 and 3. J Neurol Neurosurg Psychiatry. 2020;91(11):1166-74.
- Lunn MR, Wang CH. Atrofia muscular espinal. Lancet. 2008;371:2120-33.
- Goodkey K, Ashley T, Maruyama R, et al. Nusinersen en el tratamiento de la atrofia muscular espinal. Methods Mol Biol. 2018; 1828: 69-76.
- Swoboda KJ, Kirschner J, Finkel RS, et al; Grupo de estudio NURTURE. Efecto del nusinersén en lactantes que inician el tratamiento en una fase presintomática de la AME: resultados de NURTURE. Conferencia Virtual de AME Cure SMA 2020; 8-12 de junio de 2020; https://curesma2020.biogenscicomm.com/curesma2020/sma/swoboda/#home. Recuperado en septiembre de 2021.
- Grupo de estudio multicéntrico de referencia sobre el crecimiento de la OMS. Estudio del desarrollo motor de la OMS: ventanas de logro para seis hitos del desarrollo motor grueso. Acta Pediatr Suppl. 2006; 450: 86 – 95.
- Swoboda KJ, Sansone VA, De Vivo DC, et al. Función de deglución conservada en bebés que iniciaron el tratamiento con nusinersen en la fase presintomática de la AME: resultados del estudio NURTURE. Presentado en la Conferencia Clínica y Científica 2021 de la MDA, 15-18 de marzo de 2021.
- Van der Heul AMB, Wijngaarde CA, Wadman RI, et al. Problemas bulbares autoreportados por niños y adultos con atrofia muscular espinal. J Neuromuscul Dis. 2019;6:361-8.
- Finkel RS, McDermott MP, Kaufmann P, et al. Estudio observacional de la atrofia muscular espinal tipo I e implicaciones para los ensayos clínicos. Neurología. 2014;83:810-7.
- Van der Heul AMB, Cuppen I, Wadman RI, et al. Problemas de alimentación y deglución en bebés con atrofia muscular espinal tipo 1: un estudio observacional. J Neuromuscul Dis. 2020;7:323-30.
- Choi YA, Suh DI, Chae JH, et al. Trayectoria del cambio en el estado de la deglución en la atrofia muscular espinal tipo I. Int J Pediatr Otorhinolaryngol. 2020;130:109818.
- Burbridge C, Kelly K, García L, et al. PND74 Mapeo de una exploración cualitativa del cambio significativo en la atrofia muscular espinal de aparición tardía (tipo II o III) en la Escala motora funcional ampliada de Hammersmith (HFMSE). Valor en salud. 2019; 22, Suppl 2, p284.
- Mazur C, Powers B, Zasadny K, et al. Farmacología cerebral de los oligonucleótidos antisentido intratecales revelada mediante imágenes multimodales. JCI Insight. 2019;4:e129240.
- Claborn MK, Stevens DL, Walker CK, et al. Nusinersen: Un tratamiento para la atrofia muscular espinal. Ann Pharmacother. 2019; 53(1): 61-69.
- Castro D, Finkel RS, Farrar MA, et al. Nusinersén en la atrofia muscular espinal de inicio infantil: resultados del tratamiento a largo plazo del estudio de extensión SHINE de etiqueta abierta. Neurología. 2020; 94(15):1640.
- Chiriboga CA, et al. Tratamiento a largo plazo con nusinersén: resultados en la atrofia muscular espinal de aparición tardía del estudio shine. Presentado en la AAN 2020; 25. abril-1. mayo 2020; https://www.neurologylive.com/view/nusinersen-shows-efficacy-in-infantile-and-lateonset-spinal-muscular-atrophy; consultado en septiembre de 2021.
- Acsadi G, Crawford TO, Müller-Felber W, et al. Seguridad y eficacia del nusinersén en la atrofia muscular espinal: El estudio EMBRACE. Nervio muscular. 2021;63:668-77.
- Duong T, Wolford C, McDermott, MP, et al. Tratamiento con nusinersén en adultos con atrofia muscular espinal. Neurol Clin Pract. 2021; 11(3): e317-27.
- Paradis A, et al. Experiencia con Nusinersen en la atrofia muscular espinal de aparición tardía. Presentado en WMS 2020.
- Seal BS, Anderson S, Shermock KM, et al. Factores asociados a las tasas de adherencia a la terapia anticancerosa oral e intravenosa en pacientes con cáncer de colon metastásico asegurados comercialmente. J Manag Care Spec Pharm. 2016;22:227-35.
- Moran K, Null K, Huang Z, et al. Retrospective Claims Analysis Indirectly Comparing Medication Adherence and Persistence Between Intravenous Biologics and Oral Small-Molecule Therapies in Inflammatory Bowel Diseases. Adv Ther. 2019;36:2260-72.
- Cordts I, Lingor B, Friedrich P, et al. Administración de nusinersén intratecal en pacientes adultos con atrofia muscular espinal con anatomía espinal compleja. Ther Adv Neurol Disord 2020; 13: 1756286419887616
- Meyer T, Maier, A, Uzelac Z, et al. Expectativas de tratamiento y percepción de la terapia en pacientes adultos con atrofia muscular espinal que reciben nusinersen. Eur J Neurol. 2021; 28(8): 2582-95.
- Nuevos datos en Cure SMA 2021; Biogen, https://investors.biogen.com/news-releases/news-release-details/new-data-cure-sma-2021-highlight-long-term-efficacy-spinrazar; Último acceso: septiembre de 2021
Resumen abreviado de la información del producto SPINRAZA® Z: Un vial contiene 12 mg de nusinersén en 5 ml de líquido cefalorraquídeo artificial. I: Tratamiento de la atrofia muscular espinal (AME) asociada a 5q D: Aplicación intratecal por punción lumbar (PL). 4 Dosis de saturación de 12 mg (5ml) por aplicación los días 0, 14, 28, 63; terapia de mantenimiento cada 4 meses 12 mg (5ml). Spinraza sólo debe administrarse en centros neuromusculares hospitalarios especializados. Es obligatorio que el personal médico tratante tenga experiencia en el diagnóstico y tratamiento de pacientes con atrofia muscular espinal y en la realización de PL. KI: Hipersensibilidad a la sustancia activa o a los excipientes. VM: No hay datos de seguridad a largo plazo. Riesgo de efectos secundarios asociados a la PL. Dificultades de la PL en pacientes muy jóvenes/pacientes con escoliosis. Examen de las plaquetas y de la coagulación antes y regularmente durante la terapia. Control de las proteínas en la orina antes y regularmente durante la terapia. ECG antes de empezar y regularmente durante la terapia. Posible neurotoxicidad a dosis elevadas y/o uso prolongado. En pacientes con alteraciones de la consciencia, considere la posibilidad de investigar la hidrocefalia. S: No se recomienda durante el S. UW: Forma infantil: Infecciones respiratorias, nasofaringitis, infecciones del tracto urinario, infecciones de oído, gripe, estreñimiento, flatulencia, pérdida de peso, erupciones cutáneas. Aparición más tardía de la enfermedad: fiebre, dolor de cabeza, vómitos, epistaxis, congestión de las vías respiratorias, alergia estacional, dolor de espalda, caída. Posible reducción del crecimiento. Incidencia baja de anticuerpos antifármaco (ADA), no se observó ningún impacto aparente del desarrollo de ADA en la respuesta clínica, los acontecimientos adversos o el perfil farmacocinético del nusinersén. Poscomercialización: Infecciones graves como meningitis, hidrocefalia comunicante, meningitis aséptica, hipersensibilidad (por ejemplo, angioedema, urticaria, erupción cutánea). IA: Sin interacción con CYP450, interacción debida a unión competitiva a proteínas plasmáticas, efecto competitivo o inhibición de transportadores baja. Lista A. La información profesional completa se publica en www.swissmedicinfo.ch. Biogen Suiza AG, 6340 Baar. Estado de la información: agosto de 2019. Biogen-29360_09.2020
Biogen Suiza AG
Neuhofstrasse 30
6340 Baar
www.biogen.ch
Biogen-128051_09.2021