La hemoglobinuria paroxística nocturna (HPN) reduce la esperanza de vida de los pacientes afectados y a menudo limita drásticamente su calidad de vida. El diagnóstico lo más precoz posible es extremadamente importante, porque hoy en día, con el eculizumab, se dispone de una terapia dirigida que mejora significativamente el pronóstico. Por desgracia, los síntomas de la HPN son inespecíficos. No obstante, los proveedores de atención primaria pueden contribuir en gran medida a un diagnóstico más rápido reflexionando sobre el cuadro clínico de la HPN.
La hemoglobinuria paroxística nocturna (HPN) es un trastorno raro de la hematopoyesis. Debido a una mutación genética adquirida y no hereditaria en las células madre hematopoyéticas, faltan ciertas proteínas en la superficie celular de los eritrocitos, que protegen a las células sanguíneas contra los ataques del sistema del complemento. Como resultado, los eritrocitos se destruyen intravasalmente.
La HPN provoca diversos síntomas, pero sólo inespecíficos. Los síntomas típicos son fatiga crónica, dolor abdominal, de cabeza y de pecho, disnea, disfagia y, en los hombres, disfunción eréctil (tab. 1) . Como estos síntomas son tan inespecíficos, los pacientes suelen recibir un tratamiento inadecuado e inapropiado durante meses y años. Es mortal porque la enfermedad es crónicamente progresiva y el riesgo de complicaciones aumenta con la duración de la enfermedad.

Mortalidad y morbilidad elevadas
Como consecuencia de la hemólisis crónica, puede producirse una sobrecarga de hierro y daños hepáticos y renales. Además, la HPN está asociada a la trombofilia, lo que aumenta enormemente el riesgo de episodios tromboembólicos: entre el 28 y el 49% de todos los pacientes con HPN experimentan al menos un tromboembolismo durante el curso de la enfermedad, con las correspondientes consecuencias como ictus, infarto de miocardio, embolia pulmonar, isquemia abdominal, trombosis venosa profunda, etc. El tromboembolismo es también la causa más común de muerte en pacientes con HPN, siendo la segunda más común la insuficiencia renal crónica. El 35% de los pacientes con HPN mueren en los primeros cinco años tras el diagnóstico y el 50% en los primeros diez años. La morbilidad de los pacientes suele ser considerable debido a la fatiga y el dolor crónicos, y muchos son hospitalizados con frecuencia e incapaces de trabajar.
Diagnóstico: la anemia no siempre está presente
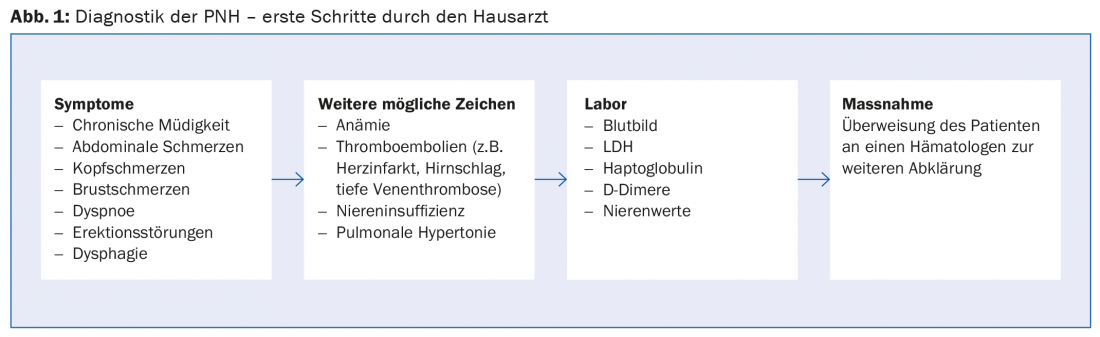
Dado que la HPN es muy poco frecuente y los síntomas son inespecíficos, a menudo transcurren años hasta que se realiza un diagnóstico correcto. Para hacer el diagnóstico, hay una cosa que se aplica sobre todo a los proveedores de atención primaria: ¡pensar en la posibilidad de la HPN! Si hay síntomas sospechosos o Si existen enfermedades, se aconsejan las siguientes pruebas de laboratorio:
- LDH: aumento de la concentración
- Haptoglobina: disminución de la concentración
- D-dímeros: la concentración aumenta en los acontecimientos tromboembólicos
- A veces hay anemia, ¡pero no siempre!
Si se sospecha HPN, el paciente debe ser remitido a un hematólogo (Fig. 1) . La regla de oro para confirmar el diagnóstico de HPN es el análisis por citometría de flujo de los eritrocitos y granulocitos de una muestra de sangre periférica para detectar la ausencia de proteínas de superficie en las células sanguíneas.
Terapia con eculizumab
Para tratar la HPN se utilizan medidas de apoyo como transfusiones, analgésicos y anticoagulación. Desde hace algunos años, en Suiza desde 2010, también se dispone de una terapia dirigida en forma de eculizumab (Soliris®). El eculizumab es un anticuerpo monoclonal contra el factor del complemento C5. El tratamiento con eculizumab reduce la hemólisis intravascular y disminuye drásticamente el riesgo de tromboembolismo en los pacientes con HPN.
Estos efectos tienen un impacto decisivo en el pronóstico de los pacientes con HPN: los estudios demuestran que su esperanza de vida aumenta significativamente con el tratamiento con eculizumab: La tasa de supervivencia a 5 años es del 95,5% en los pacientes tratados y del 66,8% en los no tratados. Los pacientes tratados alcanzan así una esperanza de vida que ya no difiere de la de la población general.
En Suiza, la indicación de la terapia debe darse en un hospital universitario o en uno de los hospitales cantonales de Aarau, Bellinzona, Lucerna o Lucerna. Gallen. Los controles de los pacientes en el marco de los registros también deben realizarse en estos centros. La administración de eculizumab entre estos controles puede realizarse en un hospital local.
Para saber más:
- Compendio suizo de medicamentos, resumen de las características del producto Soliris.
- Audebert HJ, et al: J Neurol 2005; 252(11): 1379-1386.
- Borowitz MJ, et al: Citometría B Clin Cytom 2010; 78(4): 211-230.
- Brodsky RA: HPN. Hematol. Princ. básico Pract. 4ª Ed. Filadelfia: Elsevier Churchill Livingstone; 2005; 419-427.
- Oficina Federal de Salud Pública, lista de especialidades Soliris.
- Gerber B, et al: BMJ Case Rep 2011; 2011.
- Hill A, et al: Br J Haematol 2010; 149(3): 414-425.
- Hill A, et al: Br J Haematol 2007; 137: 181-192.
- Hill A, et al: Blood (ASH Annual Meeting Abstracts) 2006; 108: 985.
- Hill A, et al: Blood 2013; 121(25): 4985-4996, quiz 5105.
- Hillmen P, et al: Blood 2007; 110(12): 4123-4128.
- Hillmen P, et al: Am J Hematol 2010; 85(8): 553-559.
- Hillmen P, et al: Br J Haematol 2013; 162(1): 62-73.
- Hillmen P, et al: N Engl J Med 1995; 333(19): 1253-1258.
- Kelly RJ, et al: Blood 2011; 117(25): 6786-6792.
- Lee JW, et al: Int J Hematol 2013; 97(6): 749-757.
- Meyers G, et al: Blood (ASH Annual Meeting Abstracts) 2007; 110: 3683.
- Moyo VM, et al: Br J Haematol 2004; 126(1): 133-138.
- Parker C, et al: Blood 2005; 106(12): 3699-3709.
- Rother RP, et al: JAMA 2005; 293(13): 1653-1662.
- Schrezenmeier H, et al: Haematologica 2014; 99(5): 922-929.
- Socié G, et al: Lancet 1996; 348(9027): 573-577.
PRÁCTICA GP 2015; 10(4): 25-26