El carcinoma endometrial es el sexto cáncer más frecuente en las mujeres de todo el mundo y tiene un mal pronóstico, sobre todo en cuanto a los resultados a largo plazo. La mediana del tiempo de supervivencia global es inferior a tres años. El tratamiento terapéutico eficaz está especialmente indicado para las pacientes con carcinoma endometrial primario avanzado o recidivante. Ahora, los resultados de un estudio alimentan la esperanza de un nuevo tratamiento combinado.
El carcinoma endometrial (CE) es un tumor maligno del útero que se origina en la capa mucosa interna del útero. La enfermedad afecta predominantemente a mujeres posmenopáusicas, con un pico de edad entre los 65 y los 85 años. La menarquia precoz, la menopausia tardía, la baja paridad o el síndrome de ovario poliquístico se describen como factores de riesgo endógenos. Los factores de riesgo exógenos incluyen la terapia de sustitución estrogénica no cíclica sola, la terapia con tamoxifeno y la radioterapia previa. La CE suele afectar a los adenocarcinomas del revestimiento uterino. Los adenocarcinomas serosos y de células claras o los carcinomas de células escamosas sólo se dan en raras ocasiones. Se distingue entre carcinoma de tipo I dependiente de estrógenos y carcinoma de tipo II independiente de estrógenos. Sin embargo, los marcadores inmunohistoquímicos y moleculares también desempeñan un papel cada vez más importante.
La tipificación molecular permite una terapia más precisa
La subtipificación molecular permite una estratificación individualizada del riesgo y una elección más precisa de la terapia. Como parte del proyecto The Cancer Genome Atlas (TCGA), se identificaron cuatro subtipos moleculares de CE mediante secuenciación de nueva generación (NGS):
- POLE: gen de la polimerasa épsilon (POLE) mutado, función de corrección de pruebas alterada durante la replicación del ADN, fenotipo ultramutado
- MSI-H/dMMR: reparación deficiente del emparejamiento erróneo (dMMR) debido a mutaciones, alta inestabilidad de microsatélites (MSI-H), fenotipo hipermutado
- Número de copias elevado/TP53abn: número elevado de alteraciones somáticas del número de copias, en su mayoría mutaciones TP53 (TP53 anormal)
- Número de copias bajo/NSMP: varias mutaciones, sin perfil molecular específico (NSMP)
Partiendo de esta base, en los últimos años se han desarrollado sustancias dirigidas (por ejemplo, Dostarlimab, Lenvatinib). Los tumores MSI-H representan el 25-30% de los carcinomas endometriales. La mayor expresión del receptor de muerte celular programada 1 (PD-1) y sus ligandos (PD-L1 y PD-L2) y la elevada carga de mutaciones tumorales asociadas a los tumores dMMR-MSI-H los hacen potencialmente susceptibles a las terapias anti-PD-1 y anti-PD-L1.
CE primario avanzado o recurrente
El carboplatino más paclitaxel es la quimioterapia estándar para el tratamiento de primera línea del CE primario avanzado o recidivante. Sin embargo, los resultados a largo plazo siguen sin ser satisfactorios. Antes de la aprobación de los agentes dirigidos, no existían estrategias de tratamiento eficaces para las pacientes en las que había fracasado la quimioterapia basada en platino. El dostarlimab es un inhibidor activo del punto de control inmunitario que se dirige al receptor PD-1. Basándose en los resultados del estudio GARNET, el fármaco fue aprobado para el cáncer de endometrio avanzado o recurrente dMMR-MSI-H. Los investigadores han ido ahora un paso más allá: la quimioterapia citotóxica puede tener efectos inmunomoduladores, como la interrupción de las vías de señalización inmunosupresoras y un aumento de la respuesta de las células T citotóxicas. Por tanto, era razonable suponer que la combinación de quimioterapia e inmunoterapia podría tener un efecto sinérgico en el microentorno tumoral. Por ello, el estudio ENGOT-EN-6-NSGO/GOG-3031/RUBY investigó la eficacia y seguridad de dostarlimab en combinación con carboplatino y paclitaxel en comparación con placebo más carboplatino y paclitaxel en pacientes con CE primario avanzado o recurrente.
En el estudio de fase III, doble ciego y multicéntrico, 494 pacientes (118 de los cuales tenían dMMR-MSI-H-EC) fueron aleatorizados en una proporción de 1:1 y recibieron 500 mg de dostarlimab o placebo por vía intravenosa en combinación con carboplatino y paclitaxel cada tres semanas durante los seis primeros ciclos, seguidos de 1000 mg de dostarlimab o placebo por vía intravenosa cada seis semanas durante un máximo de tres años o hasta la progresión de la enfermedad, la interrupción del tratamiento debido a efectos tóxicos, la retirada del paciente, la decisión del investigador de retirarlo o la muerte. Los criterios de valoración primarios fueron la supervivencia sin progresión en pacientes con dMMR-MSI-H-EC primario avanzado o recurrente y en la población general, así como la supervivencia global en la población general. Los criterios de valoración secundarios incluían la supervivencia sin progresión determinada por una revisión central ciega e independiente, la respuesta objetiva, el control de la enfermedad, la duración de la respuesta, el tiempo hasta la segunda progresión de la enfermedad, los resultados comunicados por los pacientes y los análisis farmacocinéticos y de inmunogenicidad.
Supervivencia sin progresión prolongada
La tasa de supervivencia global a los 24 meses fue del 71,3% con dostarlimab y del 56,0% con placebo. En la población dMMR-MSI-H, la supervivencia libre de progresión estimada fue del 61,4% en el grupo del suero y del 15,7% en el grupo del placebo. En la población total, fue del 36,1% frente al 18,1%. Los efectos adversos más frecuentes fueron náuseas (53,9% frente a 45,9%), alopecia (53,5% y 50,0%) y fatiga (51,9% y 54,5%). Por lo tanto, se demostró que las pacientes con CE primaria avanzada o recurrente se benefician significativamente de la combinación de dostarlimab, carboplatino y paclitaxel en términos de un menor riesgo de progresión de la enfermedad.
Para saber más:
- Mirza MR, Chase DM, Slomovitz BM, et al.: Dostarlimab for Primary Advanced or Recurrent Endometrial Cancer. N Engl J Med 2023; 388: 2145–2158.
- www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/LL_Endometriumkarzinom_Langversion_3.01_.pdf (fecha de consulta: 05.01.2024)
- www.gelbe-liste.de/krankheiten/endometriumkarzinom (fecha de consulta: 05.01.2024)
- www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/krebsarten/andere-krebsarten/gebaermutterkoerperkrebs.html (fecha de acceso: 05/01/2024).
HAUSARZT PRAXIS 2024; 19(1): 41
InFo ONKOLOGIE & HÄMATOLOGIE 2024; 12(1): 26
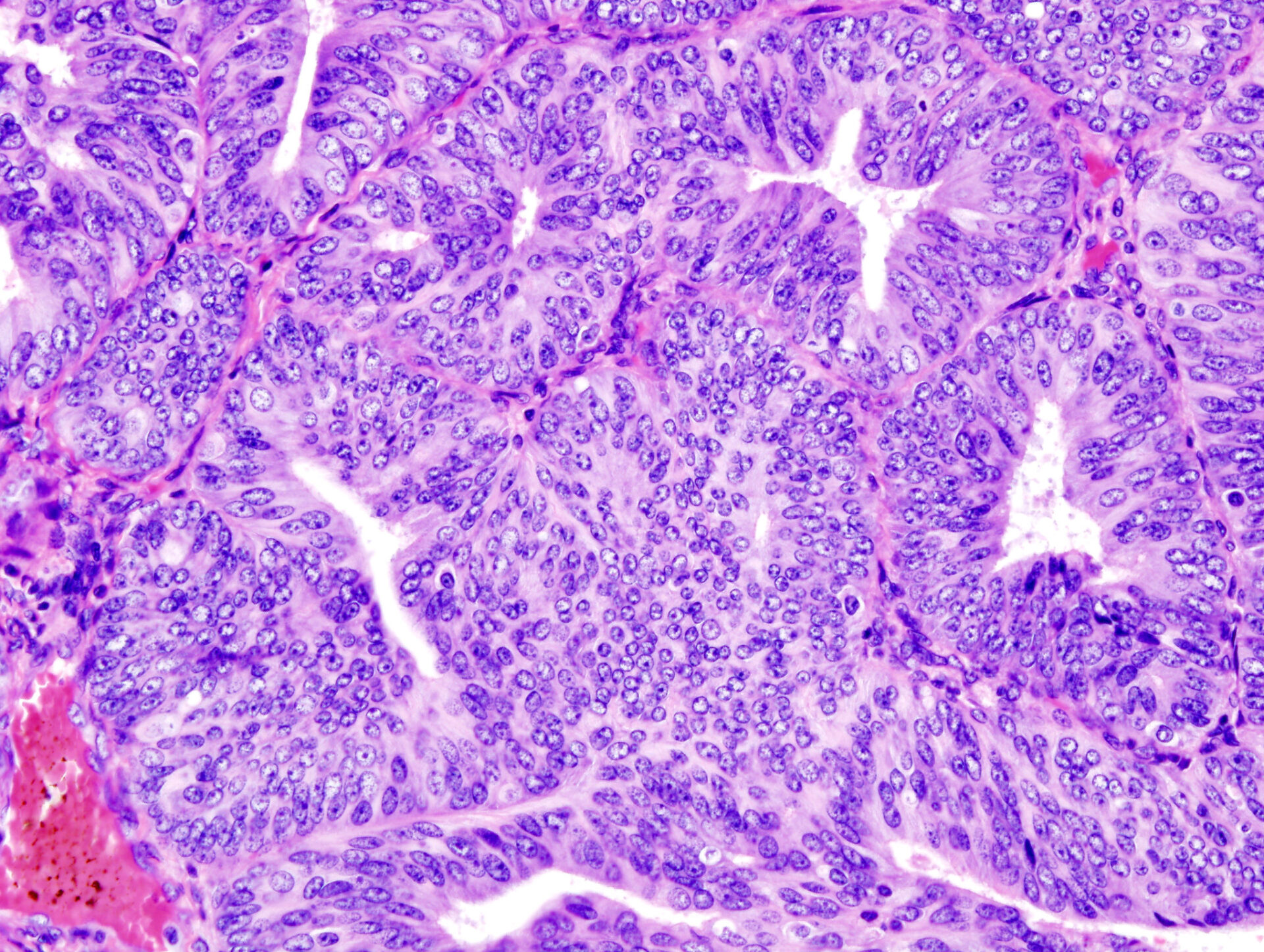
Foto de portada: Representación histopatológica de un adenocarcinoma endometrioide demostrado en una biopsia endometrial. Tinción de hematoxilina-eosina.
© KGH, wikimedia