En los últimos años, el espectro terapéutico para los pacientes con enfermedad inflamatoria intestinal (EII) se ha ampliado considerablemente. Partiendo del conocimiento de que la inflamación crónica y no tratada influye desfavorablemente en la evolución de la enfermedad, hoy en día se propugna una intervención farmacológica precoz y un seguimiento intensivo para prevenir las complicaciones.
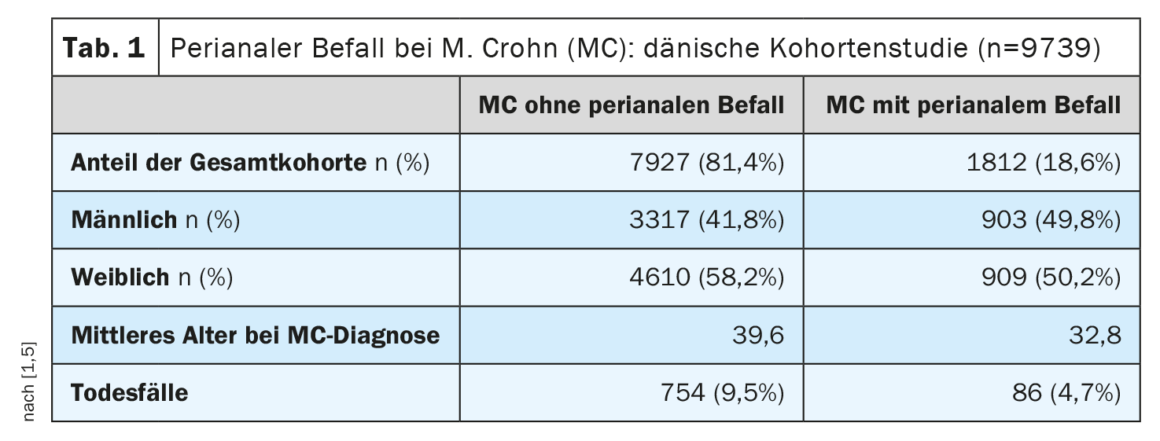
La enfermedad de Crohn (MC) se caracteriza por un cuadro heterogéneo de diferentes fenotipos [1]. La evaluación de la actividad y la gravedad de la CM se basa principalmente en parámetros de laboratorio, así como en información clínica y anamnésica (por ejemplo, frecuencia de las deposiciones, estado, dolor). Estos parámetros se han resumido en diversas puntuaciones clínicas, siendo el índice de actividad de la enfermedad de Crohn (CDAI) el más común [2]. El valor de corte para MC de moderada a grave según FDA/EMA es CDAI ≥220 [3]. El profesor David T. Rubin, MD, de la Universidad de Chicago, señaló que los pacientes con MC leve pero enfermedad perianal también deben clasificarse como de moderados a graves en cuanto al tratamiento. [4,5]La infestación perianal se produce en aproximadamente el 20% de los pacientes con MC durante el curso de la enfermedad . Así lo demuestra, entre otros, un estudio de cohortes danés a gran escala (Tab. 1).
Seguimiento de la evolución de la enfermedad y del tratamiento
La terapia tiene como objetivo inicial inducir la remisión. A largo plazo, el objetivo es mantener la remisión. El control de la enfermedad se entiende como un constructo multidimensional en MC (recuadro) . La gama de opciones de tratamiento farmacológico se ha ampliado considerablemente. A la introducción de anticuerpos contra el factor de necrosis tumoral (TNF)-α le siguieron el anticuerpo α4β7 vedolizumab y el anticuerpo (IL)-12/ IL-23 ustekinumab. Es importante evaluar el curso de la enfermedad y el tratamiento teniendo en cuenta la dimensión temporal, afirma el Prof. Rubin. [1,6,7]Varios análisis post hoc han demostrado que la respuesta de los pacientes con MC con una duración de la enfermedad más corta al tratamiento con anticuerpos contra el TNF-α, ustekinumab y vedolizumab es mejor que con una duración de la enfermedad más larga .
| Decisión terapéutica basada en la evidencia La elección de la terapia se basa en una evaluación de riesgos y beneficios, en la que deben tenerse en cuenta diversos factores y también situaciones especiales de tratamiento. Una interpretación adecuada de los datos es un requisito previo para tomar decisiones de tratamiento basadas en pruebas. Los ensayos controlados aleatorios se califican como pruebas empíricas sólidas, seguidos en orden descendente de evidencia por los estudios cara a cara, los datos posteriores a la comercialización, los metanálisis de redes, los datos del mundo real, los informes de casos y, por último, la opinión de expertos. |
Por ejemplo, un metaanálisis publicado en 2020 que incluía a 18.471 pacientes demostró que el uso precoz de biológicos (es decir, en los dos años siguientes al diagnóstico) se asociaba a una probabilidad entre dos y tres veces mayor de remisión clínica a los 6-12 meses. en los dos años siguientes al diagnóstico) se asoció con una probabilidad entre dos y tres veces mayor de remisión clínica a los 6-12 meses (OR 2,10 [IC 95%: 1,69-2,60], n=2763, p<0,00001) y mayores tasas de curación de la mucosa (OR 2,37 [IC 95%: 1,78-3,16], n=994, p<0,00001) [8].
Vedolizumab y ustekinumab: datos de estudios actuales
En el estudio SEAVUE, se compararon frente a frente ustekinumab y adalimumab [9]. Se trató de un ensayo aleatorizado, doble ciego, con control activo y un diseño de grupos paralelos. En total, se dispuso de resultados evaluables de 386 pacientes sin tratamiento biológico tratados con ustekinumab (n=191) o adalimumab (n=195). No hubo diferencias significativas entre los dos biológicos en el criterio de valoración clínico en la semana 52: las tasas de respuesta del adalimumab y el ustekinumab fueron del 61,0% y el 64,9%, respectivamente (p=0,417), con remisión clínica operacionalizada como CDAI <150 en la semana 52. Sin embargo, en términos de tolerabilidad, ustekinumab obtuvo resultados ligeramente mejores.
En un análisis secundario publicado en 2022, ustekinumab demostró ser superior a vedolizumab en el contexto de segunda línea (tras la terapia anti-TNF). El análisis se basó en 5 estudios (4 retrospectivos y 1 prospectivo) en pacientes MC con tratamiento anti-TNF fallido. [10]En la fase de mantenimiento, ustekinumab funcionó mejor que vedolizumab, y en la fase de inducción, los dos anticuerpos monoclonales mostraron efectos similares en el tratamiento .
Opciones de tratamiento de los gases de escape
Actualmente se están investigando otras terapias biológicas en ensayos de registro, como el risankizumab, por ejemplo. Este anticuerpo se une a la subunidad p19 de la interleucina-23 humana (IL-23), inhibiendo la interacción con su receptor. [11]En los ensayos clínicos, el risankizumab demostró su eficacia tanto en pacientes de primera línea como en pacientes con experiencia en biológicos . También se observó una buena respuesta al risankizumab en pacientes que habían sido tratados previamente con ustekinumab. Según el ponente, el risankizumab es adecuado en una fase temprana del tratamiento debido a su buena seguridad y tolerabilidad. Según los datos actuales, también tiene sentido utilizarlo en secuencias de tratamiento posteriores.
El control de la enfermedad como constructo multidimensionalLos factores importantes relacionados con el paciente para la evaluación del control de la enfermedad son, por ejemplo, el IMC, el sexo, la nutrición, la farmacogenómica, la adherencia, el tabaquismo. Además de la gravedad y la actividad de la enfermedad, los factores relacionados con la enfermedad también incluyen la latencia diagnóstica, el fenotipo, los factores extraintestinales y los intentos previos de tratamiento. Los factores relacionados con la terapia se refieren a las propiedades farmacocinéticas y farmacodinámicas de la sustancia activa, así como a la vía de administración y al perfil general beneficio-riesgo. Los predictores de un curso complejo de la CM en términos de factores de riesgo independientes en el momento del diagnóstico (tabla 2 ) incluían una edad más joven, manifestaciones perianales y la necesidad de una terapia esteroidea precoz. |
| según [3] |
En cuanto a la secuencia de la terapia con biológicos y la intervención quirúrgica, las recomendaciones de las directrices actuales aconsejan no interrumpir la terapia con biológicos a largo plazo, sino programar la cirugía al final del intervalo normal de administración de biológicos, siempre que la actividad de la enfermedad lo permita [1].
En moléculas pequeñas, el inhibidor de la quinasa Janus (JAK) tofacitinib sólo ha sido aprobado hasta ahora para la colitis ulcerosa. [12]El upadacitinib, también un inhibidor de JAK, se está investigando actualmente en ensayos clínicos de fase III para el tratamiento de la enfermedad de Crohn .
Congreso: Organización Europea de Crohn y Colitis
Literatura:
- “Diagnóstico y terapia de la enfermedad de Crohn”, Sociedad Alemana de Gastroenterología, Enfermedades Digestivas y Metabólicas (DGVS), directriz S3 actualizada, agosto de 2021 – Número de registro AWMF: 021-004.
- Best WR, et al: Desarrollo de un índice de actividad de la enfermedad de Crohn. Estudio cooperativo nacional sobre la enfermedad de Crohn. Gastroenterología 1976; 70: 439-444.
- “Secuenciación del tratamiento en la EC de moderada a grave: ¿Quién es el primero y quién el último?”, Prof. David T. Rubin, MD, ECCO, Copenhague, 1-4 de marzo de 2023.
- Eglinton TW, et al: Factores de riesgo clínicos y genéticos de la enfermedad de Crohn perianal en una cohorte de base poblacional. Am J Gastroenterol 2012; 107: 589-596.
- Wewer MD, et al: La incidencia y el curso de la enfermedad de Crohn perianal: un estudio de cohorte nacional danés, 1997-2015. J Crohns Colitis 2020; 15: 5-13.
- Alric H, et al: La eficacia de ustekinumab o vedolizumab en 239 pacientes con enfermedad de Crohn refractaria al factor de necrosis antitumoral. Aliment Pharmacol Ther 2020; 51: 948-957.
- Hamdeh S, et al: Uso precoz frente a tardío de la terapia anti-TNFa en pacientes adultos con enfermedad de Crohn: una revisión sistemática y metaanálisis. Inflamm Bowel Dis 2020; 26: 1808-1818.
- ngaro RC, et al: Revisión sistemática y metaanálisis: eficacia y seguridad del tratamiento biológico precoz en pacientes adultos y pediátricos con enfermedad de Crohn. Aliment Pharmacol Ther 2020; 51(9): 831-842.
- Sands BE, et al: Grupo de estudio SEAVUE. Ustekinumab frente a adalimumab para el tratamiento de inducción y mantenimiento en pacientes sin tratamiento biológico con enfermedad de Crohn de moderada a gravemente activa: ensayo multicéntrico, aleatorizado, doble ciego, de grupos paralelos, de fase 3b. Lancet 2022; 399(10342): 2200-2211.
- Parrot L, et al: Revisión sistemática con metaanálisis: la eficacia de ustekinumab o vedolizumab en pacientes con enfermedad de Crohn refractaria al factor de necrosis antitumoral. Aliment Pharmacol Ther 2022; 55(4): 380-388.
- Farrante M, et al: Presentado en UEGW. Oct 2022. OP128.
- Chugh R, et al: Experiencia real multicéntrica de upadacitinib en el tratamiento de la enfermedad de Crohn. J Crohns Colitis 2023; 17(4): 504-512.
- (ACG) Lichtenstein GR, et al: Directrices clínicas del ACG: Manejo de la enfermedad de Crohn en adultos. Am J Gastroenterol 2018; 113: 481-517.
HAUSARZT PRAXIS 2023; 18(5): 37-38 (publicado el 25.5.23, antes de impresión).