En el congreso de la DGIM se debatieron las distintas opciones terapéuticas para el síndrome del intestino irritable. Al parecer, los médicos alemanes favorecen principalmente los probióticos, los espasmolíticos y los fitoterapéuticos en el tratamiento. ¿De qué otras medidas disponemos?
Según los conocimientos actuales, en el SII, una alteración del eje intestino-cerebro conduce a un aumento de la percepción del dolor visceral y de la motilidad intestinal. Un cambio en el microbioma parece desempeñar un papel causal. El SII suele ir asociado a hinchazón, diarrea o estreñimiento y dolor abdominal. Los síntomas suelen ir acompañados de un estado de ánimo depresivo.
Según una encuesta presentada como póster en el congreso, los médicos alemanes prefieren el tratamiento con probióticos, espasmolíticos y fitoterapéuticos. Así, los proveedores de atención primaria consideraron más eficaces las tres clases de fármacos para las que existen las pruebas más débiles en los estudios, según el Prof. Stefan Müller-Lissner, MD, Park-Klinik Weissensee, Berlín. Las incertidumbres en el diagnóstico del SII (32 enfermedades diferentes) y en su terapia diferencial farmacológica (Fig. 1) no facilitan el manejo de los pacientes afectados. El síndrome del intestino irritable no tiene una fisiopatología uniforme, lo que ya sugiere la clasificación en los subtipos síndrome del intestino irritable de tipo diarrea-dominante y estreñimiento-dominante o con alternancia de deposiciones.
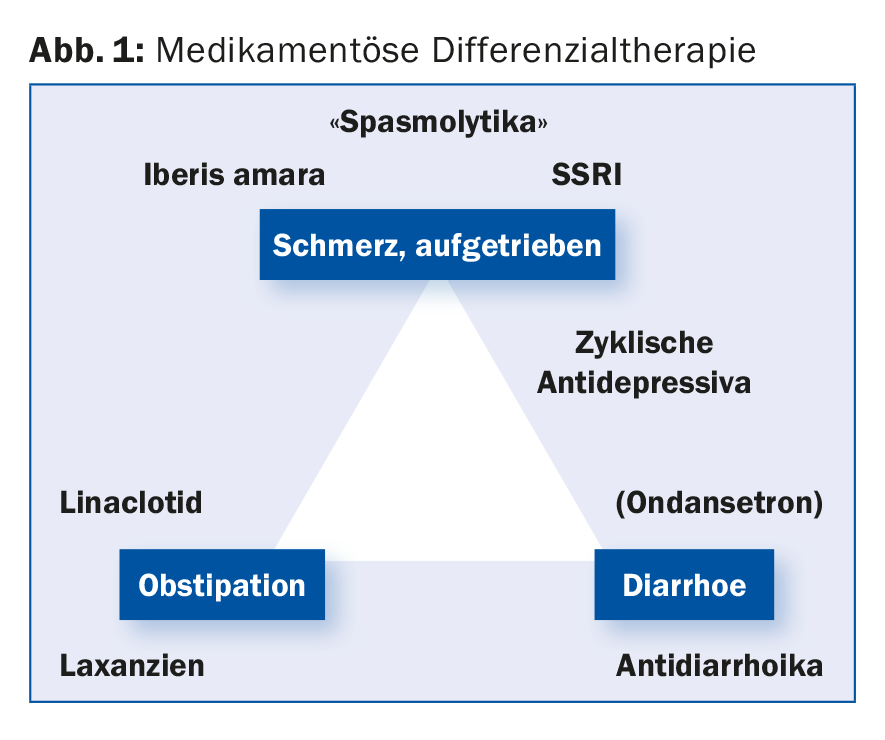
Sin embargo, el SII se asocia a trastornos periféricos y sistémicos definidos, afirmó el Prof. Dr. Michael Schemann, de la Universidad Técnica de Múnich, en la reunión anual de la Sociedad Alemana de Medicina Interna (DGIM). Conocemos las vías de señalización alteradas en el cerebro, pero esto no significa que la enfermedad sólo se produzca en el SNC. Ejemplos de correlatos orgánicos (mensurables) en el SII son los trastornos de la motilidad intestinal o el síndrome de acidosis biliar. Con la ayuda de los biomarcadores, ahora es posible identificar los subtipos de SDR y tratarlos de forma más específica. Actualmente, los biomarcadores de una patología tratable son el tránsito colónico de 48 h (trastorno de la motilidad) y las proteasas en el sobrenadante de la mucosa (trastornos sensoriomotores periféricos). El análisis de muestras de heces o la medición de mediadores inmunitarios pueden considerarse otros candidatos a biomarcadores. Sin embargo, estos marcadores no se utilizan de forma rutinaria.
Terapia: medicación, dieta y probióticos
Una condición para la aparición de los síntomas del intestino irritable es la evaluación afectiva de los síntomas por parte del paciente. “Necesita una señal periférica como desencadenante inicial”, dijo la profesora Müller-Lissner. Los desencadenantes pueden ser la motilidad (anormal), ciertos componentes de los alimentos, las bacterias o la formación de gases. Estos desencadenantes también pueden utilizarse para clasificar los diferentes enfoques terapéuticos: Dieta, probióticos y terapias farmacológicas. En general, no existe ninguna terapia innovadora; en la modulación del dolor, los antidepresivos tricíclicos o los ISRS aportan alivio, con el inconveniente de que deben tomarse a largo plazo (en lugar de “a demanda” como otras terapéuticas), afirma el experto.
Dieta: Fibra dietética y FODMAP
La recomendación de favorecer una dieta rica en fibra, por ejemplo con salvado de trigo y cáscaras de psilio, sólo ha podido demostrar hasta ahora un beneficio limítrofe en los estudios, afirma la Prof. Müller-Lissner. En los últimos años ha surgido como más eficaz la llamada dieta FODMAP, es decir, una dieta que evita ciertos tipos de frutas y verduras. Las siglas significan “Fructanos, Oligosacáridos, Disacáridos, Monosacáridos (y) Polioles”. Estos hidratos de carbono y alcoholes de azúcar se encuentran en muchos alimentos y se descomponen y absorben casi por completo en el intestino delgado en las personas sanas. En los pacientes con intestino irritable, es posible que no se descompongan por completo y acaben en el colon. Aumentan la afluencia de agua al intestino y, una vez que llegan al colon, son fermentados por las bacterias intestinales. Esto conduce a la formación de gas. El resultado puede ser una desagradable flatulencia, diarrea o un dolor abdominal poco claro. Entre las fuentes de FODMAP se encuentran el brécol, la coliflor, los guisantes, las patatas, los puerros y las cebollas, así como las manzanas, los albaricoques, las cerezas, las peras, las ciruelas y los frutos secos.
Motilidad anormal: espasmolíticos, aceite de menta y laxantes
La motilidad anormal en el tracto gastrointestinal puede manifestarse como dolor abdominal. Como espasmolítico antiguo pero menos conocido, el aceite de menta puede utilizarse con buena eficacia en pacientes con intestino irritable. Esto se debe a la alta biodisponibilidad del aceite de menta. El anticolinérgico hioscina (Buscopan®) es casi igual de eficaz para tratar el dolor abdominal tipo cólico en el síndrome del intestino irritable. En cambio, en el caso de la mebeverina, los metaanálisis no han demostrado un efecto significativo.
Los laxantes pueden utilizarse para tratar el estreñimiento y la hinchazón. El agonista del receptor de la guanilato ciclasa C linaclotida, que se utiliza para tratar el síndrome del intestino irritable con estreñimiento, también demostró tener un efecto analgésico en ratones hipersensibles.
Microbiomodulación: probióticos y antibióticos
La descomposición de la fibra alimentaria por la microbiota da lugar a la formación de gases; por el contrario, se han encontrado anomalías en la colonización bacteriana del intestino en pacientes con meteorismo. Sin embargo, se ha demostrado que los probióticos tienen poco efecto sobre la hinchazón y el dolor abdominal. El antibiótico no absorbible rifaximina resultó ser superior al placebo en la mejora del meteorismo.
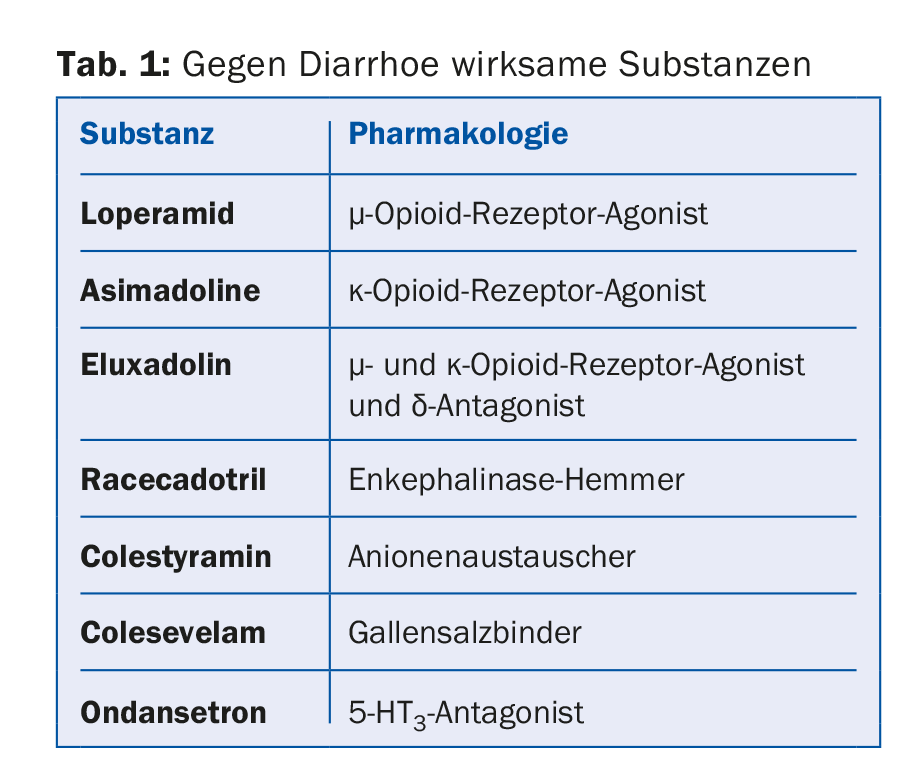
Diarrea: Loperamida y nuevas sustancias (Tab. 1)
Además de los conocidos agentes antidiarreicos, los aglutinantes de ácidos biliares pueden utilizarse en el tratamiento del síndrome del intestino irritable. Los ácidos biliares estimulan la motilidad y la secreción en el colon, lo que acorta el tiempo de tránsito y favorece la diarrea. La terapia con un aglutinante de ácidos biliares como la colestiramina o el colesevelam puede retrasar el vaciado colónico en pacientes con SII de tipo diarreico.
Síntomas generales de intestino irritable: Iberis amara
Para el cóctel de hierbas Iberogast®, compuesto por flor de trébol amargo (Iberis amara) y los otros ocho asociados combinados manzanilla, alcaravea, melisa, menta piperita, celidonia, regaliz, angélica y cardo mariano, existe un estudio original que demuestra una mejora del dolor parámetro así como de la sintomatología global. El mecanismo de acción es, entre otras cosas, una influencia sobre el umbral periférico de los estímulos de la mucosa. El preparado está aprobado para la indicación “síndrome del intestino irritable”.
Fuente: Congreso de la DGIM, 14-17 de abril de 2018, Mannheim
Para saber más:
- Enck P, et al.: Síndrome del intestino irritable: disección de una enfermedad. Una polémica de 13 pasos. Z Gastroenterol 2017 Jul; 55(7): 679-684.
- Ford AC, et al: Monografía del Colegio Americano de Gastroenterología sobre el tratamiento del síndrome del intestino irritable y el estreñimiento crónico idiopático. Am J Gastroenterol 2014 Ago; 109(Suppl 1): S2-26.
- Wong BS, et al: El aumento de la biosíntesis de ácidos biliares se asocia al síndrome del intestino irritable con diarrea. Clin
- Gastroenterol Hepatol 2012; 10: 1009-1015.
- Madisch A, et al: Tratamiento del síndrome del intestino irritable con preparados a base de plantas: resultados de un ensayo multicéntrico doble ciego, aleatorizado y controlado con placebo. Aliment Pharmacol Ther 2004 Feb 1; 19(3): 271-279.
PRÁCTICA GP 2018; 13(5): 43-44











