El espectro de terapias modificadoras de la enfermedad (TME) para pacientes con EM no ha dejado de ampliarse en los últimos años. Esto también se ha incorporado a la nueva edición de la directriz DGN. Los beneficios y los riesgos de las distintas opciones terapéuticas deben evaluarse individualmente. Varios medicamentos del campo de los DMT también han sido aprobados recientemente en Suiza.
La esclerosis múltiple (EM) se caracteriza por lesiones desmielinizantes inflamatorias focales y crónicas de las fibras nerviosas del SNC. Éstas van acompañadas de daño axonal, cicatrización tisular persistente (gliosis) y atrofia cerebral a medida que progresa la enfermedad [1]. Se cree que la desmielinización se inicia por diferentes factores celulares y humorales del sistema inmunitario innato y adquirido. La inflamación crónica altera la transmisión normal de las señales nerviosas, lo que provoca diversos síntomas y también puede causar daños permanentes o discapacidades a largo plazo. Hoy en día sigue siendo una enfermedad incurable. El objetivo de la terapia es reducir la actividad de la enfermedad y ralentizar su progresión. El tratamiento de la EM se basa en tres pilares: la intervención en las recaídas, la terapia modificadora del curso y el alivio de los síntomas. Las modernas terapias antiinflamatorias o inmunoterapias pueden modificar el curso de la enfermedad y reducir la frecuencia de las recaídas.
¿Cuáles son las innovaciones más importantes de la directriz DGN?
En la actualidad se dispone de más de una docena de sustancias para la inmunoterapia modificadora de la enfermedad de la EM, con diferentes mecanismos de acción, espectros de efectos secundarios y formas de dosificación (inyección, infusión, comprimidos). Entre otras cosas, es nueva la información específica sobre si están indicadas las inmunoterapias modificadoras del curso, cuándo y cuáles [2]. Los fármacos modificadores de la enfermedad (TME) se dividieron en tres categorías de eficacia – en lugar del esquema anterior de niveles de tratamiento. La agrupación se basó en la reducción de la tasa de recaída de los ensayos pivotales. Los preparados de acción más suave también tienen perfiles de efectos secundarios más favorables. Un criterio importante para la elección de la categoría de eficacia es el grado de actividad de la enfermedad.
- Categoría de eficacia 1: interferones beta, dimetilfumarato, glatirameroides y teriflunomida
- Categoría de eficacia 2: Cladribina, Fingolimod, Ozanimod
- Categoría de eficacia 3: Alemtuzumab , anticuerpo CD20 (ocrelizumab, rituximab off label) Natalizumab
El tratamiento inmunoterapéutico se asigna a la actividad de la enfermedad. También se presentan escenarios definidos de entrada, cambio y también de salida, y se abordan situaciones especiales (por ejemplo, el embarazo y la lactancia, así como la EM en ancianos y niños/adolescentes). El diagnóstico se simplificó con la revisión de los criterios diagnósticos de McDonald en 2017 (examen del LCR, así como examen por IRM con secuencias definidas; diagnósticos de laboratorio ampliados sólo en caso de sospecha clínica correspondiente). Las enfermedades relacionadas con la EM, como las enfermedades del espectro de la neuromielitis óptica (NMOSD) y las enfermedades asociadas a MOG-IgG, se incluyeron por primera vez como entidades patológicas independientes.
¿Qué medicamentos para la esclerosis múltiple están aprobados en Suiza?
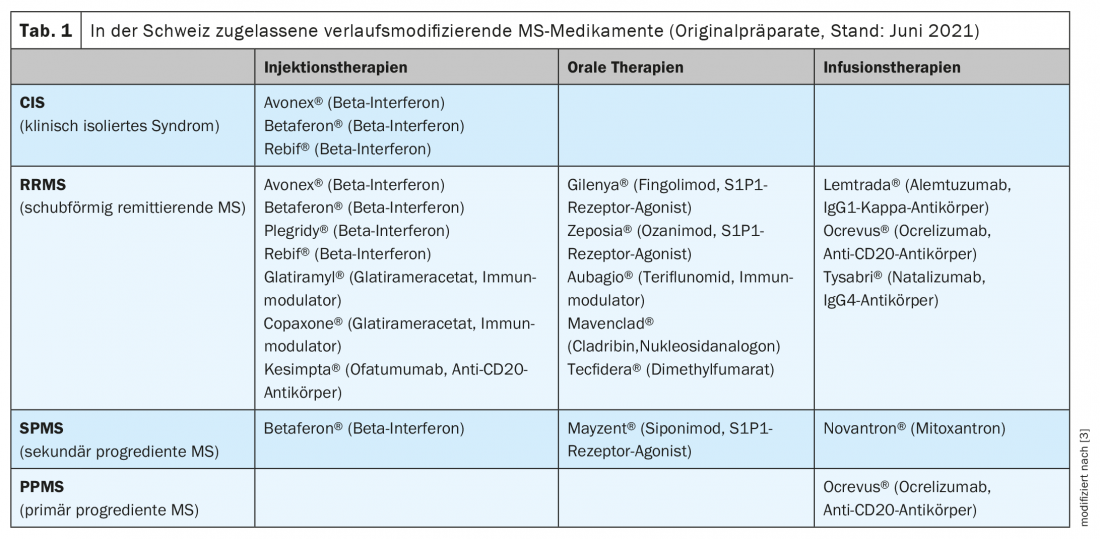
Los preparados originales autorizados actualmente en Suiza figuran en la tabla 1 [3,4]. La autorización de Swissmedic difiere en parte para algunas sustancias de la autorización en los países vecinos (Agencia Europea del Medicamento, EMA) [5]. Además, en Suiza, las limitaciones que figuran en la lista de especialidades de la Oficina Federal de Salud Pública (OFSP) tienen un impacto significativo en su uso en la práctica clínica diaria. Uno de los TME aprobados recientemente es Kesimpta® (ofatumumab) [4]. Este medicamento se aplica bajo la piel una vez al mes (pluma precargada) tras una fase de dosificación. Desde el 1 de junio de 2021, los costes de esta preparación están cubiertos por el seguro básico de enfermedad [6].
Otras aprobaciones recientes afectan a dos representantes del grupo de los moduladores del receptor de la esfingosina 1 fosfato (S1P): Zeposia® (Ozanimod) y Mayzent® (Siponimod). Mientras que Zeposia® puede utilizarse en adultos con EM recurrente-remitente (EMRR), Mayzent® está aprobado para personas con EM secundaria progresiva (EMSP) con actividad inflamatoria de la enfermedad (evidenciada por recaídas o los correspondientes cambios en las imágenes)(Tab. 1) [3,4,7].
|
“Las opciones disponibles hoy en día permiten una |
Determinar individualmente la estrategia de tratamiento
Mientras que en la terapia escalonada el tratamiento se realiza inicialmente con un TME de eficacia más bien moderada y sólo después se cambia a un fármaco modificador del curso con un efecto más potente, el principio de la terapia de alta eficacia (“Highly Effective Therapy”) consiste en que se aprovecha una “ventana de oportunidad terapéutica” temprana utilizando un fármaco muy potente desde el principio. La elección de la estrategia de tratamiento es a menudo un compromiso entre alta eficacia y seguridad/tolerabilidad. Los estudios actuales indican que la terapia intensiva temprana tiene un efecto positivo sobre la discapacidad a medio plazo [8].
¿Cuál es el mecanismo de acción de los biológicos altamente potentes? Estudios recientes sobre el papel de las células B en la progresión de la enfermedad han demostrado que la función de las células B independiente de los anticuerpos desempeña un papel importante en la patogénesis de la EM [9,10]. Este es el objetivo terapéutico de los anticuerpos. Ya está disponible un anticuerpo CD20 para la esclerosis múltiple primaria progresiva (EMPP), que hasta hace poco se consideraba intratable. En el estudio pivotal del ocrelizumab, el riesgo de progresión de la discapacidad se redujo en un 25% [11].
Aunque los TME pueden modificar el curso de la enfermedad y reducir la frecuencia de las recaídas, una recaída aguda de la EM sigue tratándose con cortisona a corto plazo. La norma establecida de tratamiento es la administración intravenosa de altas dosis de glucocorticosteroides. El tratamiento debe administrarse lo antes posible tras la aparición de los síntomas (metilprednisolona 500-1000 mg /d durante 3-5 días).
El tercer pilar de la terapia de la EM son las medidas no farmacológicas. La fisioterapia, la terapia ocupacional, la logopedia y otras opciones de tratamiento pueden contribuir a aliviar los síntomas y compensar las deficiencias funcionales.
Literatura:
- Mayo L, Quintana FJ, Weiner HL: Immunol Rev 2012; 248(1): 170-187.
- Hemmer, B et al: Diagnosis and therapy of multiple sclerosis, neuromyelitis optica spectrum disorders and MOG-IgG-associated diseases, S2k-Leitlinie, 2021, en: Deutsche Gesellschaft für Neurologie (ed.), www.dgn.org/leitlinien, (última consulta: 15.07.2021).
- Sociedad Suiza de Esclerosis Múltiple, www.multiplesklerose.ch/PDF/de/Infoblaetter/01_Medizinische_und_therapeutische_Fragen/MS-Info_Behandlung_der_Multiplen_Sklerose.pdf (última consulta: 15.07.2021)
- Información sobre medicamentos, www.swissmedicinfo.ch, (último acceso 15.07.2021)
- Achtnichts L, et al: Especificidades de la inmunoterapia para la esclerosis múltiple en Suiza, Swiss Medical Forum 2019; 41-42.
- Sociedad Suiza de Esclerosis Múltiple, www.multiplesklerose.ch/de/aktuelles/detail/kesimptar-ofatumumab-kassenzulaessig-in-der-grundversicherung (última consulta: 15.07.2021)
- Sociedad Suiza de Esclerosis Múltiple, www.multiplesklerose.ch/de/aktuelles/detail/neue-therapien
- Harding K, et al: Clinical Outcomes of Escalation vs Early Intensive Disease-Modifying Therapy in Patients With Multiple Sclerosis. JAMA Neurología 2019; 76(5): 536-541.
- Fraussen J, et al: Células B y anticuerpos en la esclerosis múltiple progresiva: Contribución a la neurodegeneración y la progresión. Autoinmune Rev 2016; 15: 896-899.
- Jelcic I, et al: Las células B de memoria activan las células T CD4+ autoreactivas que se dirigen al cerebro en la esclerosis múltiple. Cell 2018; 175: 85-100.
- Montalban X, et al; ORATORIO Clinical Investigators: Ocrelizumab versus Placebo in Primary Progressive Multiple Sclerosis. N Engl J Med 2017; 376(3): 209-220.
- DGN: “Neue S2k-Leitlinie für Diagnostik und Therapie der Multiplen Sklerose”, Sociedad Alemana de Neurología, 10.05.2021
PRÁCTICA GP 2021; 16(8): 26-27