Antes temerario, ahora terapia estandarizada: el trasplante ortotópico de hígado da a muchos pacientes la esperanza de una vida normal.
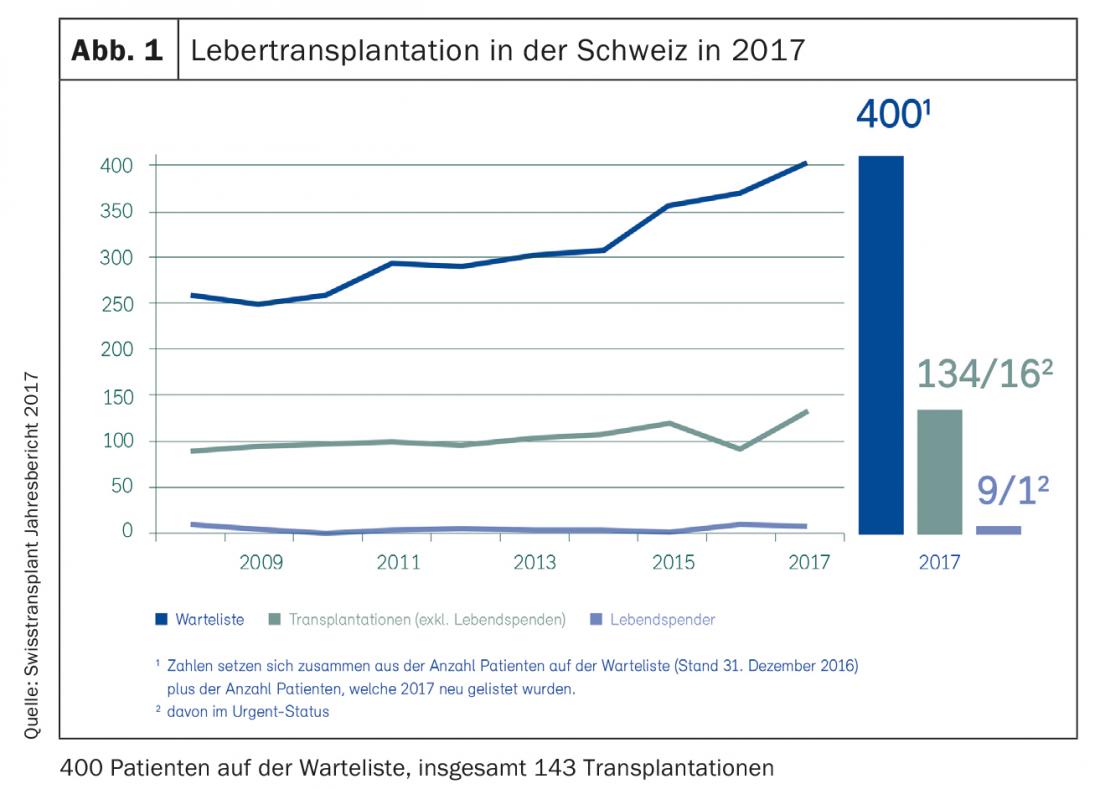
En Europa se realizan más de 10.000 trasplantes de hígado al año y en Suiza unos 150 (Fig. 1) [1]. El número de pacientes en lista de espera no deja de aumentar, al igual que el número de los que fallecen en ella porque no se dispuso a tiempo de un órgano de un donante adecuado. Aunque hace 30 años el trasplante ortotópico de hígado (TOL) requería cirujanos temerarios y pacientes valientes, los avances en la técnica quirúrgica, el tratamiento perioperatorio y la terapia inmunosupresora han hecho del TOL una terapia segura y altamente estandarizada. Los receptores y donantes multimórbidos y de edad considerablemente avanzada han configurado y modificado el perfil de riesgo en los últimos años. No obstante, la OLT sigue siendo la única oportunidad para muchos pacientes de volver a llevar una vida normal.
Indicaciones para el trasplante de hígado
Las indicaciones de la OLT pueden dividirse en insuficiencia hepática aguda, complicaciones de la hepatopatía crónica en la fase avanzada de la cirrosis hepática y enfermedades metabólicas hepáticas con manifestación sistémica. (Tab. 1). El diagnóstico de cirrosis no implica necesariamente la necesidad de OLT, sino que la indicación debe hacerse en función de la evolución clínica, teniendo en cuenta las complicaciones y su tratabilidad [2].

La asignación de órganos de donantes en Suiza se lleva a cabo de forma centralizada por Swisstransplant y está regulada por ley. En Alemania, Austria y Suiza, la puntuación MELD, compuesta por el cociente internacional normalizado (INR), la bilirrubina y la creatinina, se utiliza para la asignación de trasplantes. Además de estos parámetros, existen numerosos síntomas en la práctica clínica diaria que provocan una reducción considerable de la calidad de vida (por ejemplo, prurito, ascitis refractaria a la terapia) o que se asocian a un aumento de la mortalidad en lista de espera (especialmente la hiponatremia en pacientes cirróticos). Tras una evaluación individual, esto puede justificar la solicitud de un reglamento especial. Algunas indicaciones reciben una puntuación alta independientemente de la puntuación MELD calculada, en particular el carcinoma hepatocelular (CHC) y algunas complicaciones sistémicas y enfermedades metabólicas (por ejemplo, el síndrome hepatopulmonar, la polineuropatía amiloide familiar).
En general, los pacientes cirróticos deben ser remitidos a un centro de trasplantes tras la aparición de la primera descompensación (por ejemplo, hemorragia varicosa, ascitis, encefalopatía hepática), ya que en este caso el pronóstico de la enfermedad se deteriora considerablemente. En el caso de un declive constante de la función de síntesis hepática, debe realizarse una presentación como muy tarde cuando se alcance una puntuación MELD de >10. A partir de un MELD de ≥15, los beneficios de una OLT superan los riesgos asociados, por lo que la inclusión en la lista de espera puede tener sentido. El tiempo de espera es muy variable en función del curso clínico, pero en general puede esperarse un periodo de algo menos de un año. En caso de insuficiencia hepática aguda con deterioro rápido de la función de síntesis hepática, también se considera una inclusión en la lista de urgencia. Si se sospecha una insuficiencia hepática aguda en el curso clínico, debe ponerse en contacto con un centro de trasplantes lo antes posible. Esto debe distinguirse de la exacerbación aguda de una hepatopatía crónica, en la que no es posible un listado de alta urgencia.
En el caso de un listado regular, las aclaraciones necesarias de antemano para el listado activo son organizadas y coordinadas por la coordinación de trasplantes. En el ámbito ambulatorio, deben observarse en particular las recomendaciones infectológicas relativas a las vacunaciones o terapias que deben realizarse antes de un posible trasplante.
Medidas durante la fase de espera
Cuando se atienda a pacientes incluidos en la lista OLT, debe procurarse realizar un cribado ecográfico del CHC cada seis meses. Las terapias puente, que evitan la progresión en el intervalo previo a la TMO, deben considerarse obligatoriamente en el caso del CHC [3]. La malnutrición y el metabolismo catabólico con pérdida de tejido muscular, también en pacientes obesos (palabra clave “obesidad sarcopénica”), también deben examinarse como parte del seguimiento clínico [4]. Una intervención temprana y agresiva con la optimización del estado nutricional o la mejora de la función muscular puede mejorar significativamente el resultado tras la OLT (palabra clave “prehabilitación”). Lo que se necesita aquí es un equipo bien coordinado de hepatólogos y cirujanos de trasplantes, anestesistas y médicos de cuidados intensivos, coordinadores de trasplantes, enfermería especializada, asesoramiento nutricional y fisioterapeutas, así como el médico de cabecera, la familia y, por último pero no menos importante, el paciente.
Cualquier descompensación o deterioro del estado general debe sugerir una infección y debe aclararse en este sentido. En caso de deterioro de la función de síntesis hepática, así como de descompensación, es indispensable informar rápidamente al centro de trasplante responsable.
Esto es especialmente importante ya que una infección sistémica o sepsis es una contraindicación absoluta para la OLT, también en vista de la inmunosupresión posterior necesaria. Del mismo modo, la OLT está contraindicada en presencia de una neoplasia extrahepática activa o de una neoplasia intrahepática localmente avanzada o diseminada. Por otro lado, las comorbilidades psiquiátricas, incluido el abuso de alcohol, con la condición de una abstinencia de alcohol de al menos seis meses, no representan contraindicaciones absolutas y deben examinarse de forma interdisciplinar en casos individuales.
Aspectos quirúrgicos generales
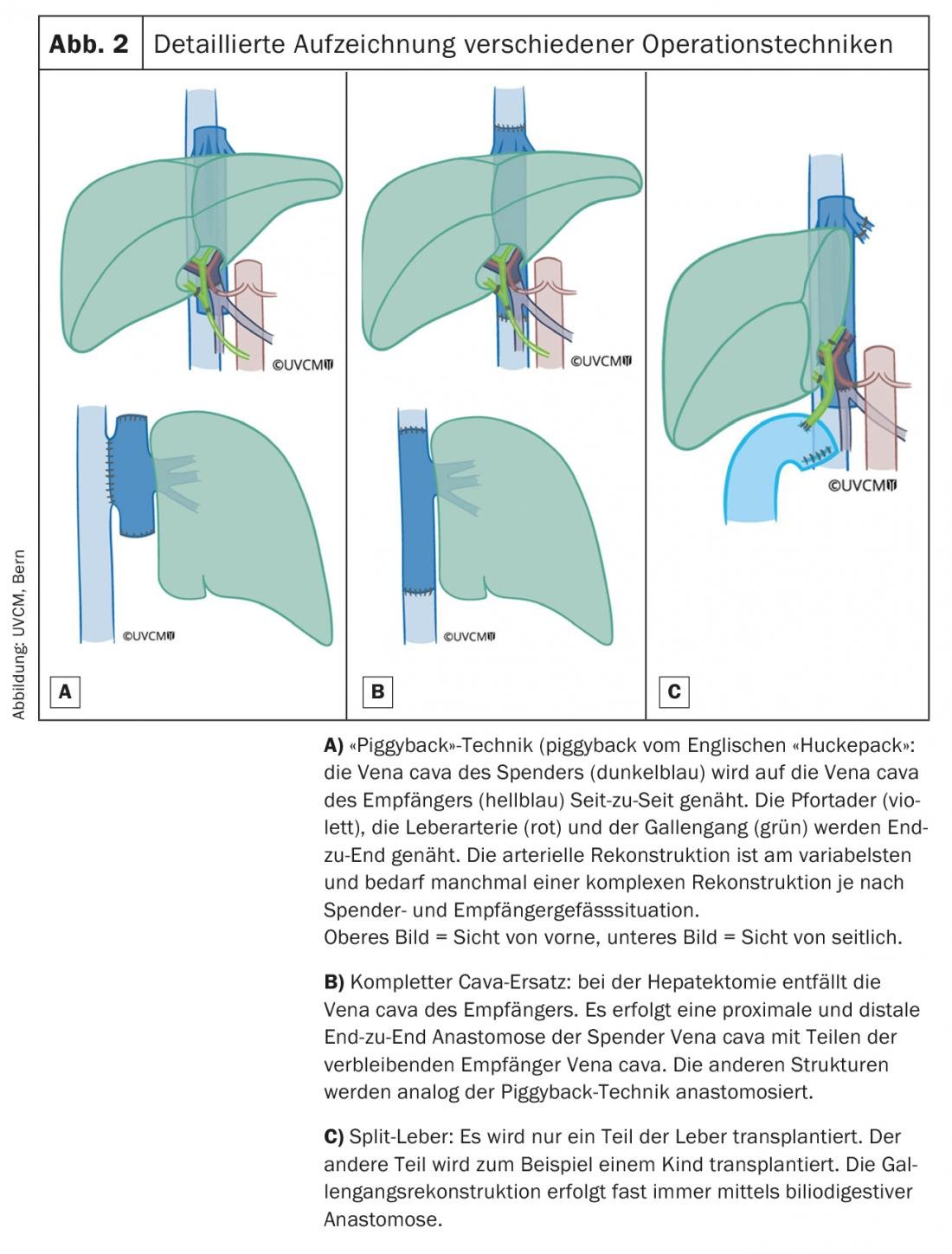
En los últimos años, no sólo ha mejorado significativamente la supervivencia tras la OLT (supervivencia a 1 año del 83%, supervivencia a 5 años del 71%), sino también el tiempo hasta la recuperación completa [5]. Los tiempos de operación significativamente más cortos (4 h frente a las 12 h anteriores de >) y la mejora de la gestión perioperatoria significan que la extubación puede realizarse a menudo muy rápidamente con una estancia correspondientemente corta en la unidad de cuidados intensivos. En 2018, la mediana de la estancia postoperatoria en la unidad de cuidados intensivos del Inselspital Bern <fue de 24 horas, y la mediana de la estancia hospitalaria de 8 días. Salvo contadas excepciones, los pacientes suelen poder regresar directamente a su entorno familiar. La figura 2 ofrece una visión detallada de las técnicas quirúrgicas que se utilizan para la colocación del órgano del donante.
Tipo de hígado donado
En Suiza, la gran mayoría de los pacientes reciben un hígado de un donante fallecido. Suele tratarse de un donante con daño o enfermedad cerebral primaria, con pérdida irreversible de la función de todo el cerebro, incluido el tronco encefálico (la llamada muerte encefálica; también conocida como “donación tras muerte encefálica”, donante “DBD”). Otra posibilidad es la extracción de un hígado de un donante con parada circulatoria persistente, que secundariamente conduce a la muerte debido a la falta de perfusión del cerebro y el tronco encefálico. Se trata de un donante denominado “DCD”, “donación tras muerte circulatoria”. En la donación de hígado en vida, sólo se extrae una parte del hígado. Esto se lleva a cabo principalmente en países en los que, por exigencias legales, religiosas y culturales, se rechaza la donación cadavérica.
La donación de hígado en vida también es muy adecuada para los programas de trasplantes pediátricos, ya que de otro modo los niños tendrían que esperar mucho tiempo para conseguir un órgano donado adecuado. En Suiza, la donación de hígado en vida rara vez se realiza. Una posibilidad para ampliar la reserva de donantes es el uso de órganos de donantes marginales (“donante con criterios ampliados”), es decir, el trasplante de órganos de mayor edad (>65-70 años), órganos con un mayor grado de esteatosis o donantes que hayan sido positivos a la hepatitis C, etc. Los hígados DCD también entran en esta categoría. Se están realizando esfuerzos en todo el mundo para reducir el riesgo en estas situaciones con el uso de diversas máquinas de perfusión, la mayoría ex situ. Existen protocolos basados en la hipotermia (+/- adición de oxígeno) según los cuales se preacondiciona el hígado para prevenir complicaciones postoperatorias como la colangiopatía isquémica. Otros grupos utilizan la perfusión en máquina normotérmica para evaluar mejor la función de los órganos antes del implante. Los informes iniciales son prometedores, pero aún está por ver qué protocolos prevalecerán finalmente y si ambos procedimientos (en todas sus variantes) son equivalentes [6].
Complicaciones postoperatorias tempranas
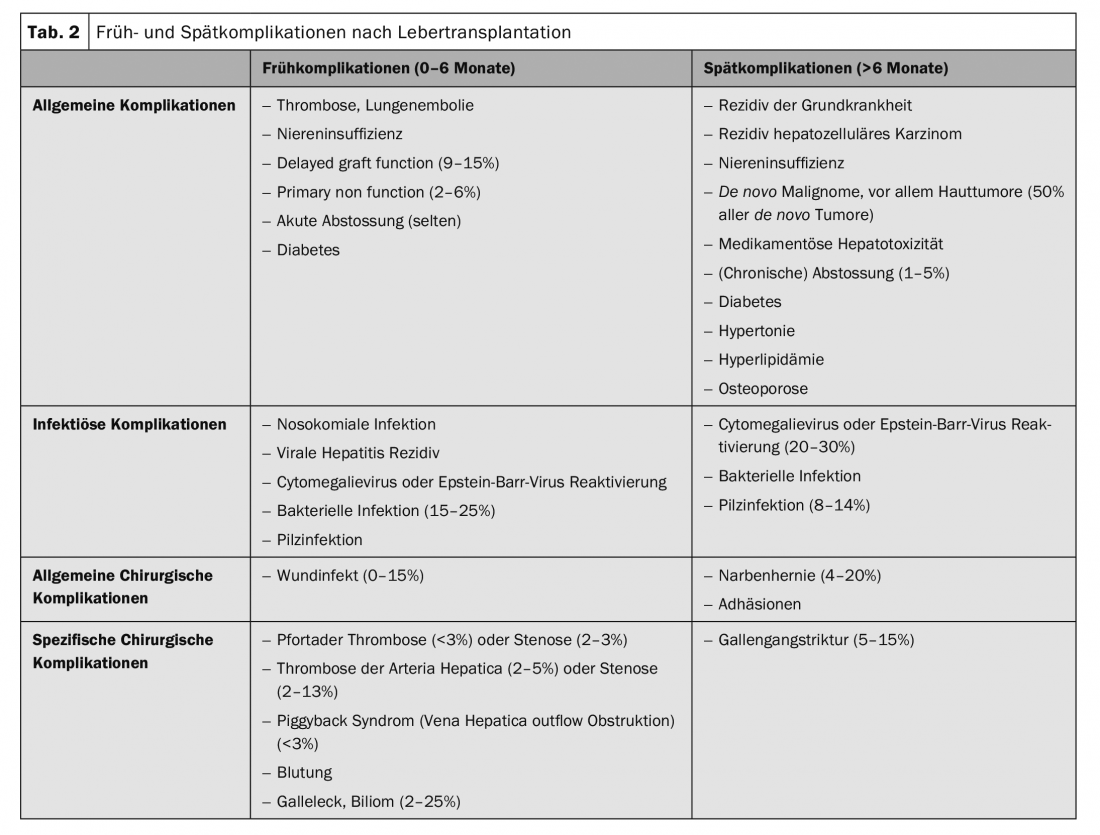
Aunque la OLT se ha vuelto mucho más segura en los últimos años, aún existen posibles obstáculos que superar. La tabla 2 ofrece una visión general de las complicaciones tempranas más frecuentes tras la OLT [7–9]. En general, la morbilidad postoperatoria es de hasta el 78%, con una mortalidad a los 30 días del 5,7% [7]. Además, los problemas de las vías biliares y las infecciones siguen siendo el talón de Aquiles de la OLT. Esta última puede reducirse significativamente utilizando la dosis más baja posible de inmunosupresores y vacunaciones adecuadas. En la gran mayoría de los casos, las estenosis del conducto biliar pueden tratarse por vía endoscópica mediante papilotomía, dilatación y colocación de endoprótesis. Sin embargo, en ausencia de respuesta, la revisión quirúrgica con la inserción de una hepaticoyeyunostomía suele ser la única solución definitiva. Difícil es la terapia de los problemas difusos de la vía biliar intrahepática. Un fenómeno que puede darse con mayor frecuencia en los trasplantes DCD (colangiopatía difusa isquémica). En determinadas circunstancias, un retrasplante es la única opción terapéutica sensata en esta situación.
Especialmente para los pacientes recién trasplantados, es esencial ponerse en contacto con el centro de trasplantes en una fase temprana si se sospechan complicaciones, para discutir el procedimiento posterior.
Seguimiento a largo plazo
Las complicaciones a largo plazo, que pueden producirse en el periodo de meses a años tras el TMO, deben tenerse en cuenta en el cuidado de los pacientes trasplantados, ya que influyen significativamente en el pronóstico a largo plazo. Los sistemas orgánicos más importantes afectados y las medidas recomendadas se resumen en la tabla 3 [10].
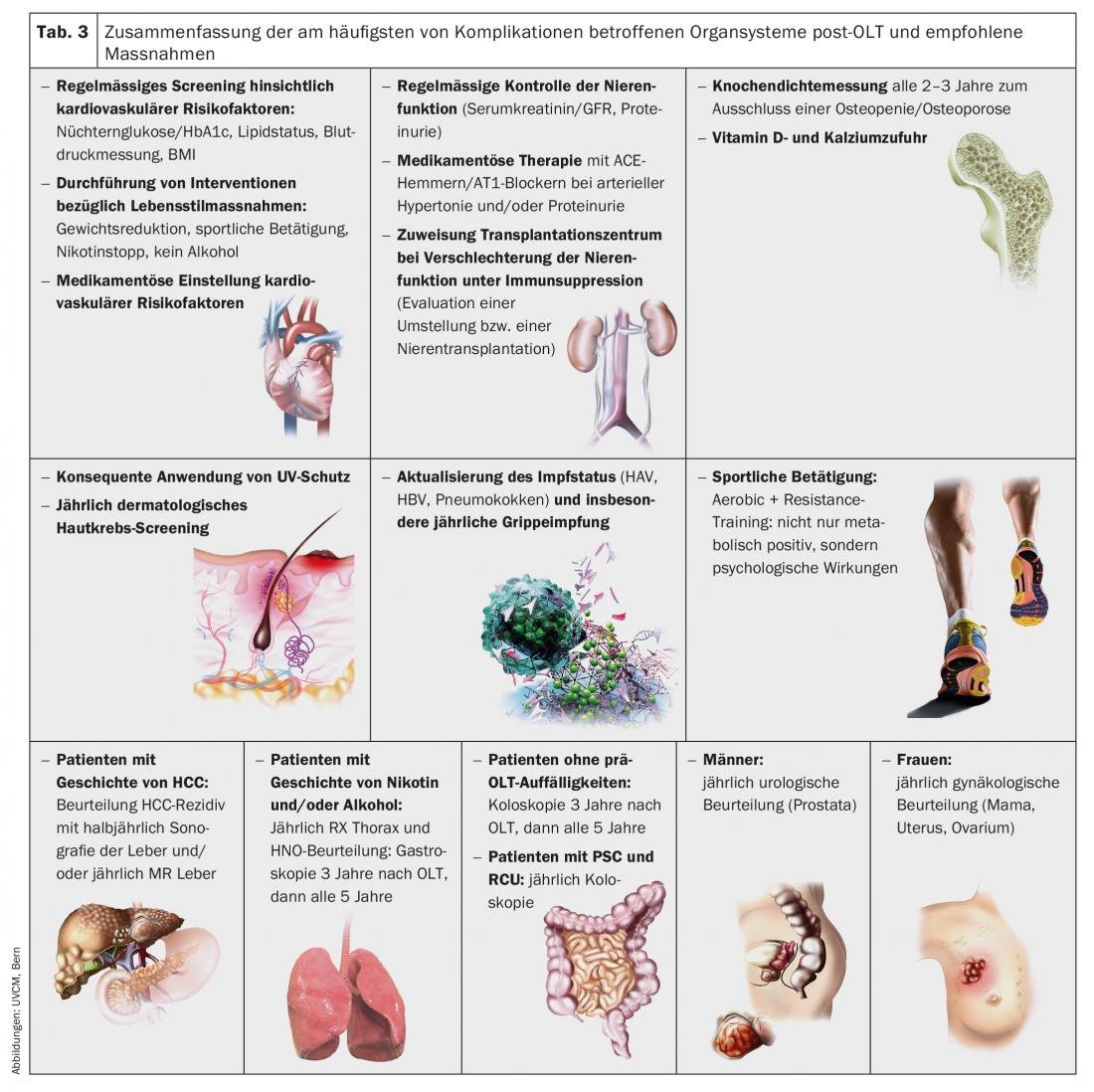
La prevención constante y el ajuste estricto de los factores de riesgo cardiovascular tienen una influencia relevante en la supervivencia a largo plazo tras el TMO. En particular, la presencia de diabetes mellitus e hipertensión arterial debe comprobarse regularmente y tratarse a un nivel bajo mediante medidas de estilo de vida o medicación. Si existen factores de riesgo como la obesidad o el abuso de nicotina, está indicado el asesoramiento sobre el ajuste del estilo de vida, si es necesario mediante un asesoramiento dietético específico o para dejar de fumar.
Objetivo de la terapia: Aumento de la calidad de vida
La OLT puede considerarse hoy en día un “procedimiento rutinario” altamente especializado con una baja mortalidad perioperatoria y, si está correctamente indicada, un resultado muy bueno a largo plazo. El objetivo final no es sólo aliviar al paciente de su enfermedad crónica a corto plazo, sino también permitirle una buena calidad de vida sin restricciones significativas en su vida cotidiana a largo plazo. Sin embargo, en caso de deficiencia persistente del órgano, es de esperar que en el futuro otras terapias, como la terapia celular con células madre o el uso de hígados “bioartificiales”, sustituyan la necesidad de la OLT “clásica”.
Mensajes para llevarse a casa
- Los pacientes cirróticos deben ser remitidos a un centro de trasplantes tras producirse la primera descompensación, o como muy tarde cuando se alcance una puntuación MELD >10.
- La “prehabilitación” con una optimización temprana y agresiva del estado nutricional y la función muscular mejora decisivamente los resultados tras la OLT.
- Los avances en la cirugía, la anestesia y el tratamiento perioperatorio de los pacientes tras un TMO han permitido una reducción significativa del riesgo, con una recuperación normalmente rápida y tiempos de hospitalización cortos.
- Los problemas de las vías biliares y las infecciones son las complicaciones postoperatorias más importantes y está absolutamente indicada una rápida remisión al centro de trasplantes.
- Debe realizarse un ajuste estricto de los factores de riesgo cardiovascular, ya que esto afecta significativamente a la supervivencia a largo plazo tras el TMO.
Literatura:
- Swisstransplant. Informe anual 2017. www.swisstransplant.org/fileadmin/user_upload/Swisstransplant/Jahresbericht/SWT_Geschaeftsbericht_A4_2017_de_def_web.pdf, consultado el 17.12.2018
- Martin P, et al: Evaluación para el trasplante de hígado en adultos: directriz práctica de 2013 de la Asociación Americana para el Estudio de las Enfermedades Hepáticas y la Sociedad Americana de Trasplantes. Hepatología 2014; 59(3): 1144-1165
- Asociación Europea para el Estudio del Hígado. Guías de práctica clínica de la EASL: Manejo del carcinoma hepatocelular. Revista de hepatología 2018; 69(1): 182-236.
- Asociación Europea para el Estudio del Hígado. Guías de práctica clínica de la EASL sobre nutrición en la enfermedad hepática crónica. Revista de hepatología 2019; 70(1): 172-193.
- Registro Europeo de Trasplantes Hepáticos, datos del receptor. www.eltr.org, último acceso 03 Ene. 2019.
- Jia JJ, et al: Perfusión mecánica para el trasplante hepático: una revisión concisa de los ensayos clínicos. Hepatobiliary & pancreatic diseases international. HBPD INT 2018; 17(5): 387-391.
- Agopian V, et al: Evolución del trasplante hepático durante 3 décadas: análisis de 5.347 trasplantes hepáticos consecutivos en un único centro. Ann Surg 2013; 258(3): 409-421.
- Kochhar G, et al: World J Gastroenterol 2013; 19(19): 2841-2846.
- Piardi T, et al: World J Hepatol 2016; 8(1): 36-57.
- Lucey MR, et al: Gestión a largo plazo del trasplante hepático en adultos con éxito: directriz práctica de 2012 de la Asociación Americana para el Estudio de las Enfermedades Hepáticas y la Sociedad Americana de Trasplantes. Trasplante hepático 2013; 19(1): 3-26.
CARDIOVASC 2019; 18(1): 20-25