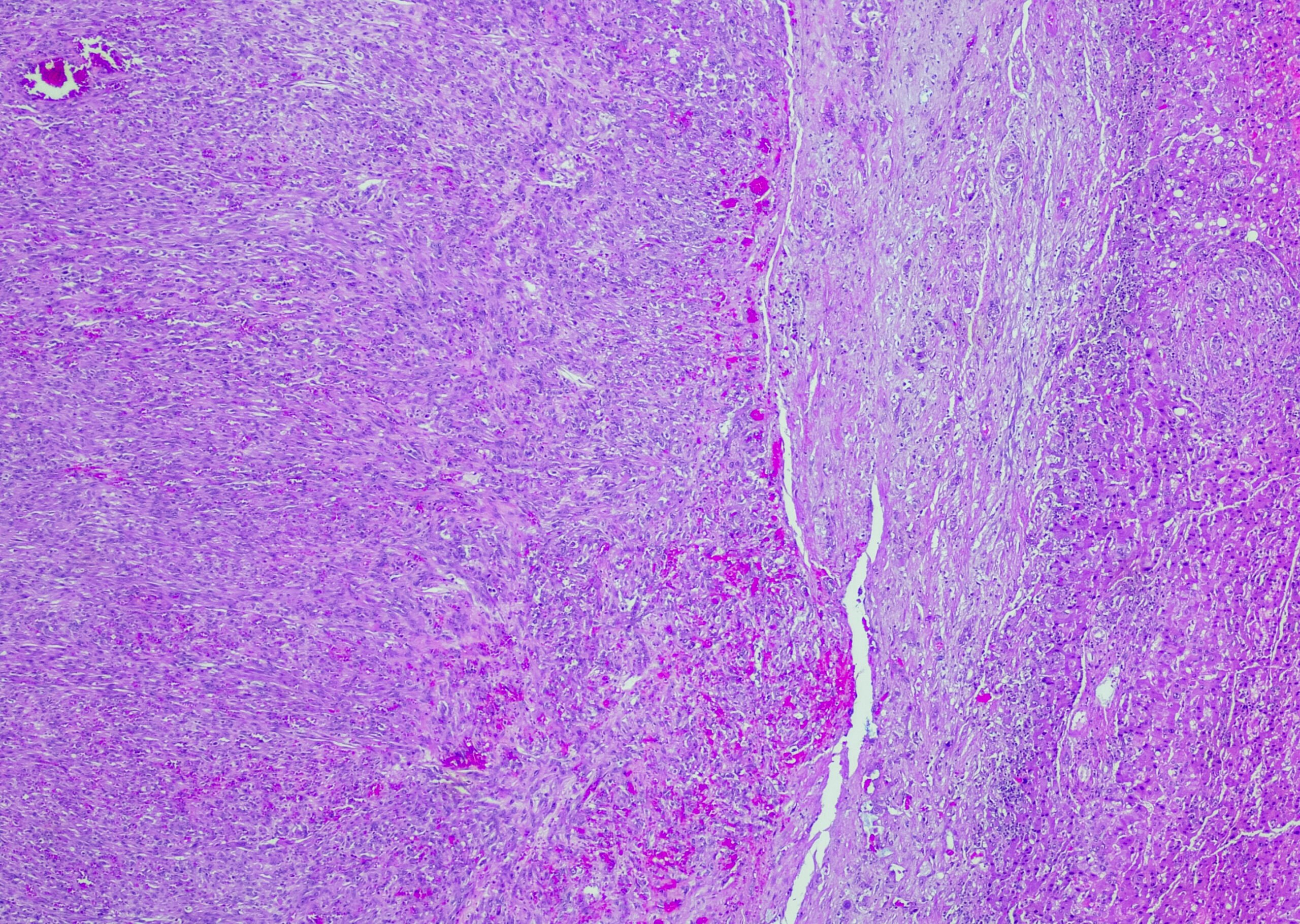
As formas pustulares da psoríase são relativamente raras. Uma mutação da IL-36RN é mais comum no subtipo generalizado (GPP) do que no subtipo restrito palmoplantar (PPP). Ambas as entidades patológicas podem ocorrer independentemente da psoríase vulgar. Em contraste com os PPC, os PPC estão associados ao consumo de nicotina. Este e muitos outros factos interessantes sobre estas doenças auto-inflamatórias da pele foram apresentados pelo Prof. Dr. Alexander Navarini, do Hospital Universitário de Basileia, no Swiss Derma Day.
Segundo o Prof. Navarini [1], o interesse pela psoríase pustulosa aumentou enormemente nos últimos dez anos. Em 2017, a ERASPEN (European Rare And Severe Psoriasis Expert Network) publicou um consenso europeu para os critérios clínicos da psoríase pustulosa palmoplantar (PPP) e da psoríase pustulosa generalizada (PPG) [2]. Desde então, prosseguiu a investigação intensiva, que resultou na autorização de comercialização de um novo ingrediente ativo biológico no GPP [3,4]. A autorização do espesolimab (Spevigo®) baseou-se no estudo Effisayil-1 [4]. De acordo com um estudo que incluiu 863 doentes com formas pustulosas de psoríase, a idade média da primeira manifestação da PPG foi de 31,0 ± 19,7 anos, ligeiramente inferior à da PPP (43,7 ± 14,4 anos) [8].
Psoríase pustulosa palmo-plantar
De acordo com o ERASPEN, a PPP é definida como pústulas epidérmicas primárias persistentes (>3 meses), estéreis e macroscopicamente visíveis na área das palmas das mãos e/ou plantas dos pés (Fig. 1) . Em cerca de 60% dos doentes, tanto as mãos como os pés são afectados e cerca de 10% também têm pústulas na região das unhas [1,5]. “Em termos de sintomas, a dor é o mais importante na primeira apresentação, e cerca de um quinto tem mesmo dificuldade em trabalhar com as mãos e os pés”, relatou o orador [1,5]. A artralgia afecta 13% dos doentes com PPP e 15% mostram uma coincidência com a psoríase em placas em [1,5]. Destes, cerca de um quarto sofre também de artrite psoriática (APS). O Prof. Navarini aconselha que faça um historial completo da psoríase [1].
As pústulas ocorrem de forma transgrediente ou isolada na PPP, o padrão de distribuição é frequentemente bilateral e simétrico. 40% dos doentes têm recaídas recorrentes, 60% têm um curso crónico constante [1,5]. “Há diferentes graus de intensidade”, explica o orador [1]. No decurso da doença, as vesículas tornam-se maiores e podem confluenciar para formar lagos de pus (Fig. 2) . Inicialmente, as pústulas são de cor esbranquiçada, tornando-se amareladas com o tempo e depois acastanhadas. “Se se forma um lago de pus que preenche todo o estrato subcórneo, este é restritivo em termos de elasticidade, rasga-se e pode surgir uma epiderme fresca por baixo”, explica o Prof. As mutações estão presentes em menos de 5% dos casos de PPP. Cerca de três quartos das pessoas que sofrem de PPP são mulheres e cerca de 60% são fumadores activos. O stress, as infecções e certos medicamentos (por exemplo, lítio, inibidores do TNF-alfa) são outros factores desencadeantes [6].
A distinção entre os subtipos A (Andrews) e B (Barber) de PPP é objeto de um debate controverso. Os diagnósticos diferenciais mais importantes da PPP são apresentados na Visão Geral 1. Ao contrário da PPP, uma estratégia terapêutica dirigida contra a IL-36 ainda não provou ser um sucesso retumbante na PPP [1].
Psoríase pustulosa generalizada
Em comparação com o PPP, o GPP (Fig. 3) ocorre com menos frequência. As pústulas primárias estéreis, macroscopicamente visíveis e não foliculares, manifestam-se normalmente na pele eritematosa não acral – com exceção dos casos em que a formação de pústulas se limita às placas psoriásicas (“psoriasis cum pustulatione”). “As pústulas são típicas do tronco, das extremidades e das pregas de flexão”, explica o Prof. Navarini [1]. Numa subclassificação, pode ser feita uma distinção entre PPG com vs. sem inflamação sistémica e com vs. sem psoríase vulgar. Aproximadamente um quarto dos doentes com PPG tem um historial de psoríase em placas [1,7]. O curso clínico da PPG é heterogéneo; é feita uma distinção entre uma forma intermitente (>1 episódio) e uma forma persistente [1]. Os episódios de GPP ocorrem normalmente de forma abrupta e duram aproximadamente 10 dias a 4 semanas. A gravidade dos sintomas pode variar em cada episódio.
Sabe-se, através de estudos de coorte, que pelo menos 50% dos doentes com PPG têm uma mutação na IL-36RN. Esta mutação está normalmente presente nos 30% dos doentes em que a PPG ocorre no primeiro ano de vida. O biólogo espesolimab (Spevigo®) actua na via de sinalização da IL-36 [3]. Nos estudos de aprovação clínica, mais de metade dos doentes apresentaram um desaparecimento completo de todas as pústulas no espaço de uma semana, explicou o Prof. Navarini [1,4].
A inflamação sistémica está presente em cerca de três quartos de todas as pessoas que sofrem de PPG. Os sintomas inflamatórios sistémicos são febre (>38°C), mal-estar, leucocitose, proteína C-reactiva (PCR) elevada. Em termos de envolvimento de órgãos, o fígado ou os rins podem estar envolvidos, mas os sistemas respiratório e cardiovascular também podem ser afectados, o que pode levar à morte, segundo o orador [1].
A PEGA é o diagnóstico diferencial mais importante da PPG [1], sendo um quadro clínico mais frequente que a PPG e que requer uma estratégia terapêutica diferente. Para além dos outros diagnósticos diferenciais apresentados na Visão Geral 2, as infecções virais também podem estar associadas a manifestações pustulosas.
Tal como no caso do PPP, há uma predominância de mulheres no GPP, mas este facto é menos claro (aproximadamente 55-67% de mulheres) [1,7]. Não existe qualquer associação com o tabagismo; muitos doentes nunca fumaram. Para além de uma associação com factores genéticos, o stress (65%), a infeção (53%), a medicação (28%) e a gravidez (<10%) são factores desencadeantes conhecidos [1,7]. Para além da PPP e da GPP, a acrodermatite contínua supurativa Hallopeau também é classificada como uma forma pustulosa de psoríase [2]. Trata-se de uma doença pustulosa rara, inflamatória, frequentemente crónica, da pele e do leito ungueal das falanges distais [1].
Literatura:
- “Psoríase pustulosa”, Prof. Dr. A. Navarini, Dermatoses inflamatórias, Swiss Derma Day e revisões e actualizações STI, 11.01.2024.
- Navarini AA, et al: Rede ERASPEN. Declaração de consenso europeu sobre os fenótipos da psoríase pustulosa. JEADV 2017; 31(11): 1792-1799.
- Swissmedic: Informações sobre o medicamento, www.swissmedicinfo.ch,(último acesso em 13.03.2024)
- Bachelez H, et al: Investigadores do Ensaio Effisayil 1. Ensaio de Spesolimab para Psoríase Pustulosa Generalizada. N Engl J Med 2021; 385(26): 2431-2440.
- Noe MH, et al: Avaliação de uma série de casos de pacientes com pustulose palmoplantar nos Estados Unidos. JAMA Dermatol 2022; 158(1): 68-72.
- Genovese G, et al: Psoríase pustulosa: da fisiopatologia ao tratamento. Biomedicinas 2021; 9(12): 1746.
- Kharawala S, et al: O fardo clínico, humanístico e económico da psoríase pustulosa generalizada: uma revisão estruturada. Expert Rev Clin Immunol 2020; 16(3): 239-252.
- Twelves S, et al: Diferenças clínicas e genéticas entre os subtipos de psoríase pustulosa. J Allergy Clin Immunol 2019; 143: 1021-1026.
DERMATOLOGIE PRAXIS 2024; 34(2): 32-33 (publicado em 26.4.24, antes da impressão)