Los opiáceos forman un grupo farmacológicamente heterogéneo de sustancias activas sintéticas, semisintéticas y naturales cuya característica común es la unión a los receptores opiáceos. En cuanto al desarrollo de los efectos analgésicos, los receptores opioides del sistema nervioso central son decisivos. La activación de los receptores opioides presinápticos en el asta posterior de la médula espinal inhibe la transmisión de los impulsos dolorosos.
El término opioide procede del griego y significa “similar al opio”. Los opiáceos forman un grupo farmacológicamente heterogéneo de sustancias activas sintéticas, semisintéticas y naturales cuya característica común es la unión a los receptores opiáceos. Los receptores opioides se encuentran tanto en el sistema nervioso periférico como en el central. En cuanto al desarrollo de los efectos analgésicos, los receptores opioides del sistema nervioso central son decisivos. Al activar los receptores opioides presinápticos en el asta posterior de la médula espinal, se inhibe la transmisión de los impulsos dolorosos. La activación inducida por opiáceos de los receptores opiáceos en ciertas regiones del tronco encefálico provoca una estimulación adicional de las vías neurales inhibitorias descendentes. Esto inhibe la transmisión de las señales de dolor que llegan al asta posterior. En las regiones subcorticales del sistema límbico, la activación de los receptores opioides conduce a una atenuación del componente emocional-afectivo de la percepción de una sensación de dolor [1].
El propio cuerpo humano produce opioides endógenos, que se liberan en el contexto de reacciones de estrés y conducen a la supresión del dolor y la sensación de hambre. En la práctica médica se utilizan generalmente opiáceos sintéticos. Las diferencias farmacodinámicas entre los distintos opiáceos pueden observarse en la diferente afinidad a los receptores opiáceos o a subtipos individuales de receptores. El conocimiento preciso de estas diferencias farmacodinámicas ayuda en la práctica clínica diaria a poder estimar el efecto esperado de un opioide concreto.
Epidemiología
La Encuesta de Salud Suiza de 2017 mostró que alrededor de 2,5 millones de personas en Suiza sufren dolor crónico. Aproximadamente 0,6 millones de personas padecen dolencias de moderadas a graves que tienen un efecto limitante sobre la actividad y la calidad de vida. Es más probable que las mujeres declaren sufrir dolor crónico [2].
Aunque existen diversos enfoques terapéuticos para el tratamiento del dolor, en Suiza también se prescriben cada vez más opiáceos. El uso de opiáceos está bien reconocido y suele ser muy útil para el tratamiento del dolor agudo intenso, por ejemplo en el entorno perioperatorio. Los opiáceos también suelen ser una opción terapéutica indispensable y reconocida en todo el mundo para el tratamiento del dolor relacionado con tumores [3]. El dolor crónico no oncológico, por el contrario, suele ser una indicación menos buena para el tratamiento a largo plazo con opiáceos. No está claro si el uso de opiáceos muy potentes mejora el control del dolor crónico no oncológico a medio o largo plazo [4].
Precisamente por este motivo resulta alarmante que el 85% de todos los opiáceos que se recetan en la actualidad se utilicen para tratar el dolor no oncológico [5]. Aproximadamente el 25% de los pacientes afectados reciben los opiáceos prescritos durante una duración >90 días. El resultado suele ser un uso prolongado durante años.
Taxonomía de los mecanismos del dolor
El tratamiento farmacológico adecuado y eficaz del dolor puede lograrse de forma más fiable si se acotan al máximo los mecanismos de causalidad del dolor. Una historia clínica detallada y un examen clínico centrado son fundamentales para identificar el mecanismo del dolor. Los exámenes radiológicos, de laboratorio y otros exámenes adicionales son útiles en situaciones específicas. Deben identificarse o excluirse los siguientes mecanismos del dolor:
Dolor nociceptivo: Este mecanismo es responsable del mantenimiento de la integridad corporal y también se entiende como sensación de dolor “normal, habitual”. Las señales nociceptivas del dolor ayudan a prevenir lesiones. El dolor depende del estímulo, suele ser de corta duración y el tejido estimulado permanece intacto. Los estímulos nociceptivos continuados pueden provocar cambios neuronales en el asta posterior de la médula espinal. Estos cambios suelen durar poco y remitir. No se esperan fenómenos persistentes de sensibilización al dolor.
Dolor nociceptivo-inflamatorio: El dolor agudo a subagudo se produce cuando ya se ha producido un daño tisular. Los desencadenantes son los mediadores inflamatorios liberados (por ejemplo, las interleucinas). Por un lado, se produce una activación directa de las terminaciones de las fibras dolorosas periféricas y, por otro, en el transcurso de este proceso se reclutan y sensibilizan adicionalmente nuevas fibras dolorosas previamente inactivas. En general, se produce una disminución del umbral de excitabilidad electrofisiológica. Esto hace posible la formación de fenómenos de sensibilización periférica.
Dolor neuropático: El dolor neuropático también se produce de forma aguda o subaguda. Sin embargo, en este caso la causa de la señal de dolor no es el tejido circundante, sino el propio sistema somatosensorial [6]. El daño a las propias células nerviosas constituye la base del dolor neuropático. Prácticamente siempre se producen fenómenos de sensibilización periférica y central. Por regla general, pueden documentarse fenómenos de sensibilización “positivos” y/o “negativos”. A menudo existe una gran discrepancia entre la intensidad del dolor del que se queja el paciente, la extensión de la zona afectada por el dolor y los hallazgos objetivos que puede determinar el examinador.
Un importante fenómeno de sensibilización es la hiperalgesia. Se da tanto en los cuadros de dolor neuropático como en los inflamatorios. La hiperalgesia puede definirse como una condición durante la cual un estímulo normalmente poco doloroso se experimenta como excesivamente doloroso (por ejemplo, pincharse con un palillo de dientes). La alodinia es otro fenómeno de sensibilización “positiva” y es una exacerbación de la hiperalgesia. En una zona de la piel afectada por la alodinia, un estímulo que en realidad es indoloro se percibe como doloroso (por ejemplo, tocar con un cepillo).
Dolor nociceptivo: El dolor nociceptivo/inflamatorio y el dolor neuropático son, en última instancia, entidades definidas mecanísticamente. La diferencia crucial es que en el contexto de las afecciones de dolor nociceptivo, existe una función normal del sistema somatosensorial, mientras que es precisamente éste el que está dañado en las afecciones de dolor neuropático. Muchos pacientes con dolor crónico no pueden asignarse a ninguna de estas entidades sin lugar a dudas [7]. En estos pacientes, no puede suponerse ni una activación de los nociceptores ni una lesión del sistema somatosensorial. En estos casos, se trata de un problema de dolor nociplásico. Afecta a un amplio grupo de pacientes: Dolor de espalda inespecífico, dolor inespecífico en articulaciones periféricas, fibromialgia, síndrome de dolor regional complejo (SDRC) tipo 1.
Superposición de mecanismos del dolor/”Dolor mixto “: Muy a menudo, en los pacientes con dolor crónico puede detectarse/suponerse una superposición de los mecanismos del dolor antes mencionados. En el “dolor mixto”, todos los mecanismos descritos anteriormente suelen estar implicados en el desarrollo o la modulación de la señal de dolor. Normalmente, uno u otro mecanismo del dolor está en primer plano.
Los opiáceos desempeñan un papel importante en el tratamiento del dolor nociceptivo, pero también pueden contribuir a un buen control del dolor en el dolor neuropático. En el caso de los cuadros de dolor nociplásico, el valor terapéutico de los opiáceos suele ser inexistente.
Los 4 pilares de la analgesia
Para lograr un tratamiento analgésico lo más satisfactorio posible, es fundamental reconocer el dolor y los mecanismos de sensibilización presentados anteriormente. Independientemente de la modalidad terapéutica, una terapia dirigida de las afecciones dolorosas, o la consecución de la “analgesia”, se basa por tanto en los cuatro pilares siguientes: “antinocicepción”, “antiinflamación”, “antihiperalgesia” y “antineuropatía” [8].
Por lo tanto, en el marco de una terapia analgésica farmacológica, es crucial utilizar fármacos de una o varias clases de sustancias que puedan cubrir en la medida de lo posible todo el espectro de los mecanismos del dolor diagnosticados.
Medidas recomendadas antes de iniciar un tratamiento del dolor con un opiáceo
La utilidad o no de un intento de tratamiento con un analgésico opiáceo requiere una cuidadosa consideración conjunta entre médico y paciente. El uso de opiáceos de acción débil o fuerte desempeña un papel secundario. Deben considerarse específicamente los siguientes puntos [9]:
- Deben buscarse e identificarse específicamente los mecanismos subyacentes del problema de dolor.
- Se recomienda realizar una historia psicosocial más detallada y detectar la presencia de influencias psicológicas en el problema del dolor.
- Si es posible, el dolor crónico no oncológico nunca debe tratarse exclusivamente con opiáceos. Los datos científicos indican que los opiáceos no son más eficaces que otros analgésicos para el tratamiento del dolor crónico no oncológico.
- Por lo tanto, antes de plantearse un tratamiento del dolor con opiáceos, deberían haberse tomado ya o al menos intentado otras medidas terapéuticas (físicas, fisioterapéuticas, medicinales, intervencionistas, psicológicas).
- Deben elaborarse objetivos terapéuticos significativos y alcanzables junto con el paciente. Hay que centrarse en objetivos como una reducción del dolor de al menos un 30%, la vuelta al trabajo o también la realización de tareas cotidianas, por ejemplo en el hogar.
- Los pacientes deben ser informados detalladamente sobre los posibles peligros que pueden producirse en el curso de una terapia a largo plazo con opiáceos. Además de los efectos secundarios conocidos como estreñimiento, sequedad de boca, náuseas, malestar, estados de confusión, caídas, también debe prestarse atención a la depresión respiratoria potencialmente mortal como resultado de dosis incorrectas/excesivas.
- Hay que informar a los pacientes de que la terapia con un opiáceo suele provocar dependencia física.
- Durante las primeras 1-2 semanas de terapia, durante la fase de ajuste, cuando se aumenta la dosis o cuando se cambia a otro opiáceo, debe evitarse conducir o manejar maquinaria. Durante este tiempo, son frecuentes los efectos secundarios que limitan la capacidad de respuesta.
¿Cuándo puede considerarse una terapia a largo plazo >120 días con opiáceos?
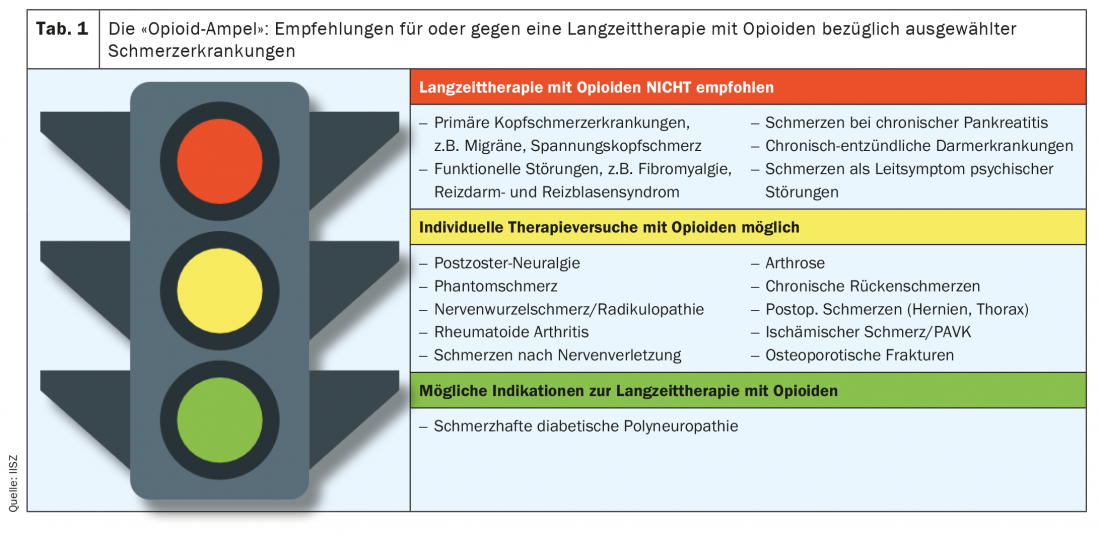
Se aplica el principio de que los opiáceos sólo deben utilizarse para la terapia a largo plazo (>120 días) de un dolor crónico si el paciente afectado ha podido registrar una reducción significativa del dolor y/o una mejora de su estado general durante una terapia de prueba de 4 a 12 semanas. Además, las directrices aplicables a nivel nacional e internacional deben incluirse en las consideraciones en torno a una indicación. Un recurso recomendable es, por ejemplo, la directriz sobre “Uso a largo plazo de opiáceos para el dolor crónico no relacionado con tumores (LONTS)” [9] de la Sociedad Alemana del Dolor. Actualmente, la terapia con opiáceos a largo plazo sólo se recomienda en presencia de una polineuropatía diabética dolorosa. Por el contrario, la terapia a largo plazo con opiáceos se desaconseja incluso específicamente en el caso de otras diversas dolencias crónicas (véase también la Tabla 1).
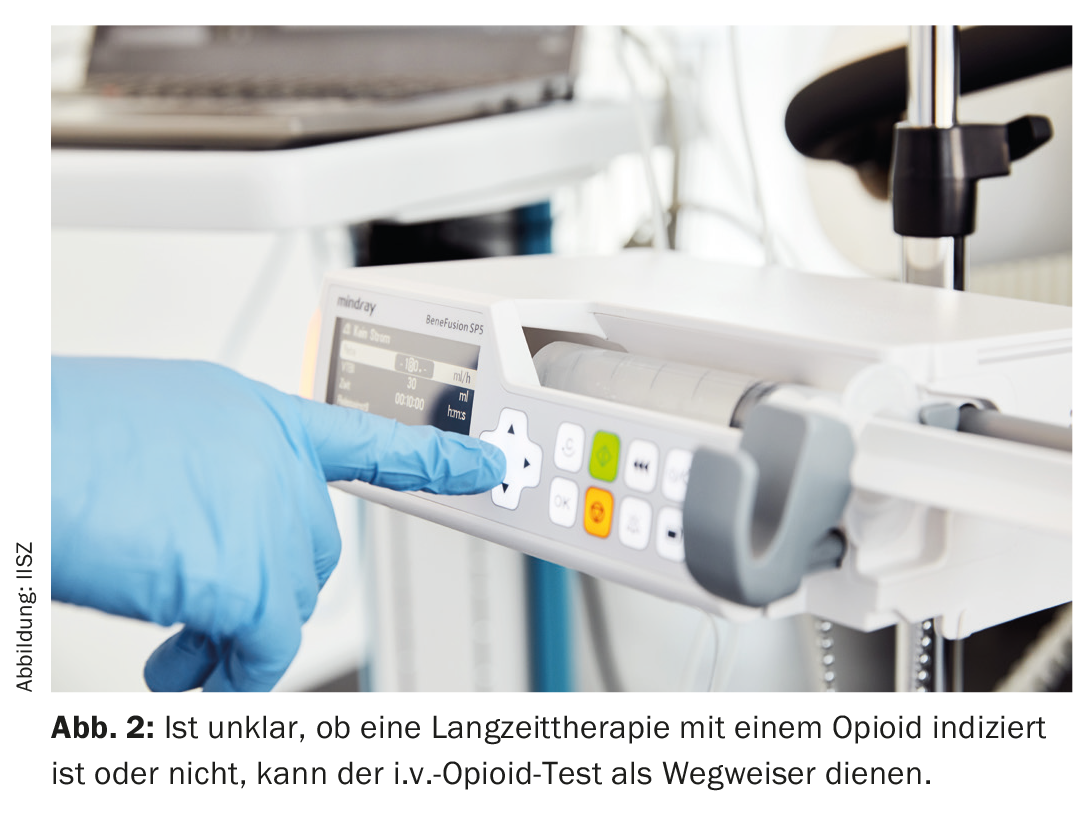
En caso de duda: la prueba de opiáceos i.v. como indicador
Si hay dudas sobre si la terapia del dolor con opiáceos debe continuarse durante más de 12 semanas, una prueba intravenosa (i.v.) de opiáceos realizada en un entorno ambulatorio puede ser útil [10] (Fig. 2). Diversos centros de medicina del dolor de Suiza ofrecen este tipo de pruebas. Mediante la administración i.v. protocolizada de un opiáceo de acción ultracorta, suele ser posible averiguar si un cuadro de dolor puede tratarse eficazmente con un opiáceo o no.
Preparados opiáceos de acción corta frente a los de acción prolongada
Para el tratamiento del dolor crónico deben utilizarse, si es posible, preparados con galénicos de liberación lenta o de larga duración de acción. La ingesta debe seguir un calendario fijo. La experiencia demuestra que de este modo se puede lograr un mejor control del dolor y una mayor adherencia a la terapia. Además, este procedimiento puede reducir el riesgo de complicaciones.
Los opiáceos de acción corta y ultracorta sólo deben utilizarse en casos excepcionales en el tratamiento del dolor crónico no relacionado con tumores. Tampoco se recomiendan como medicación a demanda. La experiencia clínica demuestra que los opiáceos de acción corta también pueden provocar rápidamente una dependencia psicológica. Desgraciadamente, esto a menudo da lugar a un mal uso.
Resultados de la terapia con opiáceos a largo plazo
Las pruebas científicas actualmente disponibles para evaluar la eficacia de la terapia con opiáceos >120 días para el dolor crónico no relacionado con tumores son insuficientes. Esto implica automáticamente unas perspectivas inciertas de éxito [11].
En el contexto del uso crónico de opiáceos, no es infrecuente que la medicación opiácea utilizada disminuya su efecto. Existen varios diagnósticos diferenciales que pueden explicar esta evolución. Incluso en el caso del dolor crónico no relacionado con tumores, puede producirse una progresión de la enfermedad que lleve a una intensificación del problema del dolor. Sin embargo, el tratamiento crónico con opiáceos suele conducir al desarrollo de tolerancia con la consiguiente reducción del efecto analgésico del opiáceo utilizado. Se cree que la causa es una migración de los receptores opioides de la superficie celular al interior de la célula, de modo que ya no están disponibles para el efecto analgésico. Otro fenómeno que puede producirse en relación con un aumento del dolor durante la terapia continuada con opiáceos es la hiperalgesia inducida por opiáceos. Los mecanismos discutidos de la hiperalgesia inducida por opiáceos son complejos y van desde una regulación a la baja de los receptores opiáceos hasta una posible sensibilización central, pasando por una potenciación sináptica a largo plazo.
Efectos adversos con el uso prolongado
El uso prolongado de opioides puede provocar los siguientes efectos adversos:
- Pérdida del deseo sexual
- Impotencia
- Trastornos menstruales en la mujer
- Aumento de la mortalidad por todas las causas
- Pasividad / desgana
- Deterioro de la memoria
- Mayor riesgo de caídas
¿Cuándo debe interrumpirse la terapia con opiáceos a largo plazo?
La terapia a largo plazo con un opioide debe reevaluarse periódicamente. Si no está claro si la terapia con un opiáceo proporciona alivio del dolor, trabaje para interrumpir esta terapia. Se recomienda interrumpir gradualmente la terapia con un opiáceo si:
- En la fase de ajuste (de 4 a 12 semanas), no se pudieron alcanzar los objetivos terapéuticos definidos individualmente y/o se produjeron efectos secundarios significativos.
- En el curso del tratamiento, hay que determinar una pérdida de efecto del opiáceo utilizado y esto no puede evitarse más que con un ajuste moderado de la dosis o un cambio a otro opiáceo.
- Hay indicios de uso indebido durante el tratamiento (aumentos independientes de la dosis, prescripción por varios médicos).
Conclusión
Los opiáceos son una de las clases de sustancias más importantes para el tratamiento del dolor intenso. Nunca se utilizan como opción de primera línea y siempre deben ir acompañados de medidas no farmacológicas. La terapia a largo plazo sólo se lleva a cabo con los pacientes que responden a la terapia, por lo que el efecto debe evaluarse regularmente mediante la definición y el seguimiento de los objetivos de la terapia. Una terapia con opioides que no funcione debe interrumpirse a tiempo.
Mensajes para llevar a casa
- Antes de iniciar una terapia farmacológica contra el dolor en general y un tratamiento con opiáceos en particular, debe acotarse el mecanismo del dolor subyacente.
- Los opiáceos suelen ser el tratamiento de elección para el dolor agudo intenso y el relacionado con tumores.
- Por el contrario, la terapia a largo plazo del dolor crónico no relacionado con tumores sólo debe llevarse a cabo en casos excepcionales y, siempre que sea posible, debe combinarse con medidas no farmacológicas.
- La terapia a largo plazo con opiáceos debe orientarse hacia objetivos mensurables. Si no se logran estos objetivos, debe suspenderse el tratamiento con opiáceos.
- En el contexto de una terapia a largo plazo con opiáceos, siempre se desarrolla una dependencia física, que a veces va acompañada de un componente psicológico, en el sentido de una adicción.
Literatura:
- Ossipov MH, Dussor GO, Porreca F: Modulación central del dolor. J Clin Invest 2010; 120: 3779-3787.
- Encuesta suiza de salud mediante entrevista 2017, Salud y género, Oficina Federal de Estadística, número FSO 213-1718. 2020.
- Wertli MM, Steurer J: Cita en proceso. Práctica 2015; 104(11): 541-542.
- Breivik H, Stubhaug A: La carga de morbilidad suele agravarse con el tratamiento con opiáceos de los pacientes con dolor crónico: Etiología y prevención. DOLOR 2014; 155(12): 2441-2443.
- Wertli M, Held U, Signorell A, et al: Análisis de la evolución de las prácticas de prescripción de medicamentos para el dolor y el sueño entre 2013 y 2018 en Suiza. Hospital Universitario de Berna 2020.
- Jensen T, Baron R, et al: Una nueva definición del dolor neuropático. Dolor 2011; 152: 2204-2205.
- Trouvin AP, Perrot S: Nuevos conceptos del dolor. Mejores prácticas e investigación Reumatología clínica 2019; 33(3).
- Maurer K: Terapia práctica paso a paso para el médico general. El médico informado 2017.
- Uso a largo plazo de opiáceos para el dolor crónico no relacionado con tumores (LONTS), 2ª actualización 2020; registro de directrices de la AWMF nº 145/003.
- Gustorff B: Pruebas de opiáceos intravenosos en pacientes con dolor crónico no oncológico. Eur J Pain 2005; 9(2): 123-125.
- Chou R, Turner JA, et al: The Effectiveness and Risks of Long-Term Opioid Therapy for Chronic Pain: A Systematic Review for a National Institutes of Health Pathways to Prevention Workshop. Ann Int Med 2015; doi: 10.7326/M14-2559.
InFo DOLOR Y GERIATURA 2021; 3(1): 10-14