En el estudio no intervencionista PIONEER REAL Switzerland, los diabéticos adultos de tipo 2 tratados con semaglutida oral como parte de la atención clínica habitual lograron una mejora clínicamente significativa del control glucémico sin que se produjeran nuevas señales de seguridad. Los resultados se presentaron en la Reunión Anual de la SGED y apuntalan los prometedores resultados de los estudios de autorización clínica.
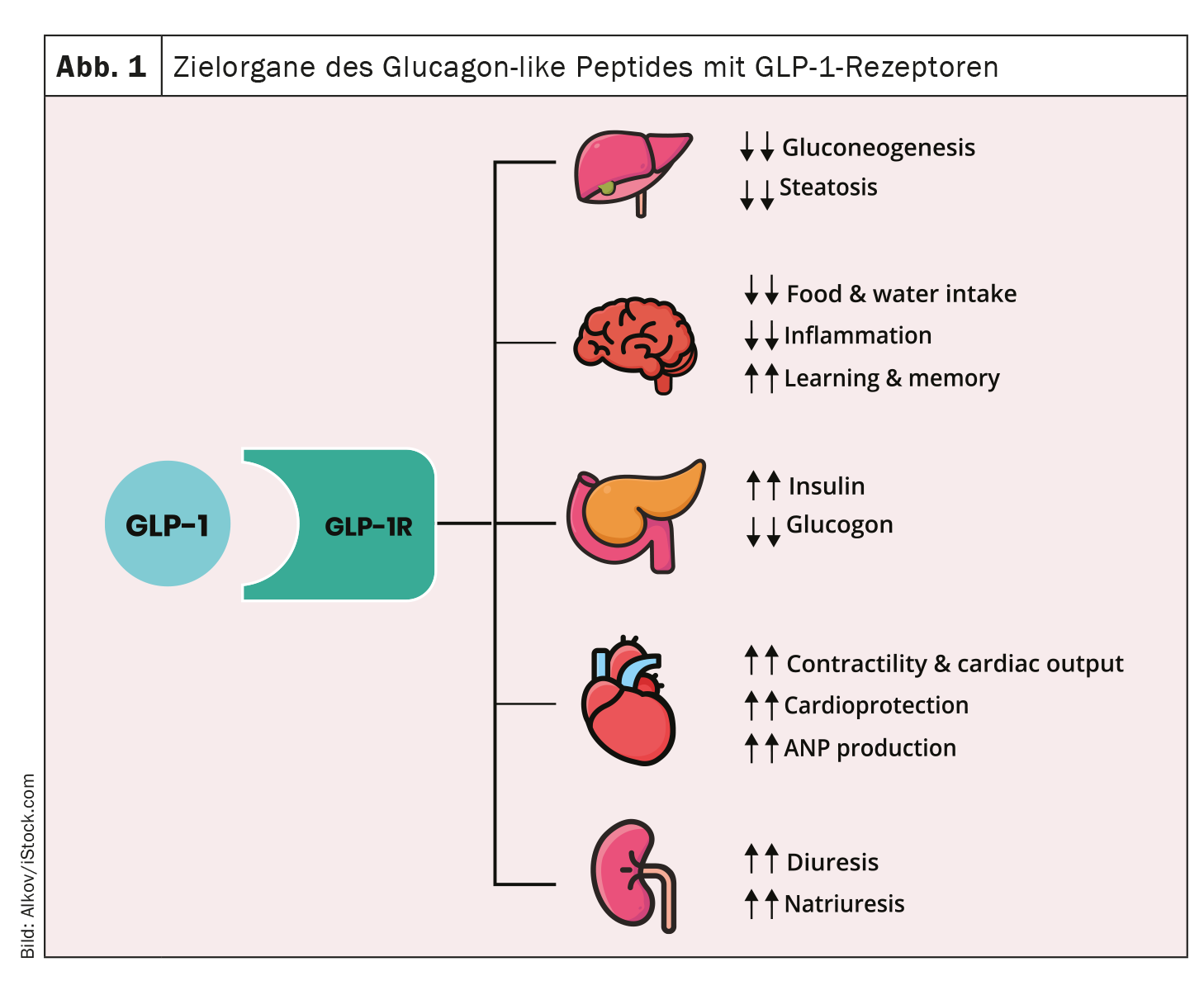
La semaglutida también se comercializa en Suiza para el tratamiento de la diabetes de tipo 2 (DMT2) en forma oral desde 2020, bajo el nombre comercial de Rybelsus® [1]. Al igual que otros agonistas del receptor del péptido-1 similar al glucagón (GLP-1-RA), la semaglutida se une al receptor del GLP-1, promoviendo así la secreción de insulina e inhibiendo la liberación de glucagón. El programa de ensayos PIONEER de fase III tuvo mucho éxito. Uno de los principales estudios demostró que Rybelsus® no sólo mejora el control metabólico y reduce el peso corporal, sino que también provoca menos infartos e incluso menos muertes[1,2]. El objetivo del estudio internacional de fase IV PIONEER REAL es observar sistemáticamente cómo funciona y se tolera el fármaco en condiciones cotidianas [2].
Estudio multicéntrico del mundo real
PIONEER REAL Suiza forma parte de un proyecto de estudio llevado a cabo en 13 países – es un estudio multicéntrico, prospectivo, abierto, de un solo brazo, de 34-44 semanas de duración en adultos con T2D. Los participantes no estaban en tratamiento con terapias inyectables reductoras de la glucosa al inicio del estudio y recibieron semaglutida en forma oral una vez al día como parte de su atención rutinaria habitual [3]. Además de los cambios en la HbA1c (criterio de valoración primario) y el peso corporal (criterio de valoración secundario), se registró la proporción de pacientes que alcanzaron una HbA1c <7% y/o un criterio de valoración compuesto de una reducción de la HbA1c ≥1% acompañada de una reducción del peso corporal (PC) ≥3% o ≥5% al final del estudio.
Resultados importantes de un vistazo
De los 185 participantes incluidos, el 90,8% completó el estudio y el 77,3% permaneció en tratamiento con semaglutida hasta el final del estudio [3]. Al inicio del estudio, la edad media era de 62 (DE 10,4) años, el valor de HbA1c era del 7,7% (DE 1,5%) y el peso corporal era de 95,6 kg (DE 17,6 kg). Se documentó un IMC medio de 33,2 kg/m2 (4,8 kg/m2). El 56,2% de los participantes recibió al mismo tiempo otra medicación para reducir la glucosa.
** DE = desviación estándar
KI=intervalo de confianza
Los cambios medios estimados desde el inicio hasta el final del estudio fueron los siguientes [3]:
- Valores deHbA1c: cambio de -0,9% (IC 95%: -1,1; -0,7, p<0,0001)
- Peso corporal absoluto: cambio de 4,7 kg (IC 95%: -5,6; -3,8, p<0,0001)
- Peso corporal relativo: reducción del -4,9% (IC 95%: -5,7; -4,0, ambos p<0,0001)
- Al final del estudio, el 64,2% de los participantes tenían un valor de HbA1c <7% y el 37,8% y el 28,3% alcanzaron el criterio de valoración compuesto de una reducción de HbA1c ≥1% más una reducción del KG ≥3% y ≥5% respectivamente.
Se notificaron un total de 139 acontecimientos adversos (AA) en 65 participantes (35,1%) [3]. La mayoría fueron leves o moderados, siendo los trastornos gastrointestinales los más frecuentes (89 eventos en 50 participantes). 31 EA en 20 (10,8%) participantes provocaron la interrupción de la semaglutida oral. Se notificaron un total de seis EA graves que probablemente no estaban relacionados con el tratamiento con semaglutida.
Fuente: Novo Nordisk
Literatura:
- Swissmedic: Arzneimittelinformation,
www.swissmedicinfo.ch,(última consulta: 21 de noviembre de 2023) - Husain M, et al.: PIONEER 6 Investigators. Oral Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. NEJM 2019; 381(9): 841–851.
- Kick A, et al.: Real-world use of oral semaglutide in adults with type 2 diabetes: Results from the PIONEER REAL Switzerland multicenter, prospective, observational study. Abstractband, Annual Meeting SGED/SSED, 16. –17.11.2023.
CARDIOVASC 2023; 22(4): 58
HAUSARZT PRAXIS 2023: 18(12): 37