Alrededor del 50% de las causas perioperatorias de muerte en cirugía no cardiaca pueden atribuirse a causas cardiovasculares. Una evaluación preoperatoria adecuada del riesgo cardiovascular puede reducir el riesgo de complicaciones. Para ello, los autores de la directriz 2022 de la ESC han elaborado recomendaciones específicas basadas en una evaluación exhaustiva de la bibliografía actual.
A medida que la población envejece, también aumenta el número de afecciones que requieren cirugía. En consecuencia, es muy probable que se encuentre cada vez más a menudo con pacientes que requieren una evaluación preoperatoria en su propia sala de espera. Se plantea entonces la cuestión de qué exámenes están indicados y son necesarios antes de la operación. ¿Cuáles de nuestros pacientes pueden ser operados sin dudarlo y cuáles pueden necesitar aún terapia antes de la operación propiamente dicha (cirugía)? La “Directriz sobre evaluación y tratamiento cardiovascular antes de intervenciones no cardiacas” de la Sociedad Europea de Cardiología (ESC) [1], publicada en 2022, ofrece orientaciones sobre esta misma cuestión. El objetivo de esta directriz es reducir la mortalidad y la morbilidad perioperatorias mediante un enfoque sistemático estandarizado y basado en pruebas. Si nos fijamos en las causas exactas de la muerte de los cuatro millones de pacientes que fallecen perioperatoriamente cada año, encontramos que alrededor del 50% se deben a causas cardiovasculares [2,3].
Las recomendaciones se especificaron en particular para los pacientes con un nuevo soplo cardíaco, dificultad respiratoria, edema o angina de pecho. Además, se presta especial atención a la evaluación de la fragilidad/frailty de los pacientes y a la obtención de los biomarcadores péptido natriurético cerebral o pro péptido natriurético cerebral N-terminal (en adelante, ambos abreviados como BNP) y troponina. También se hacen recomendaciones para la gestión de la medicación anticoagulante, las hemorragias y las complicaciones cardiovasculares perioperatorias. Por primera vez, la directriz se ocupa de los pacientes con neoplasias malignas subyacentes y con infección por cóvida 19. A continuación se resumen los aspectos más importantes para su rutina clínica diaria.
El primer paso: la evaluación preoperatoria de riesgos
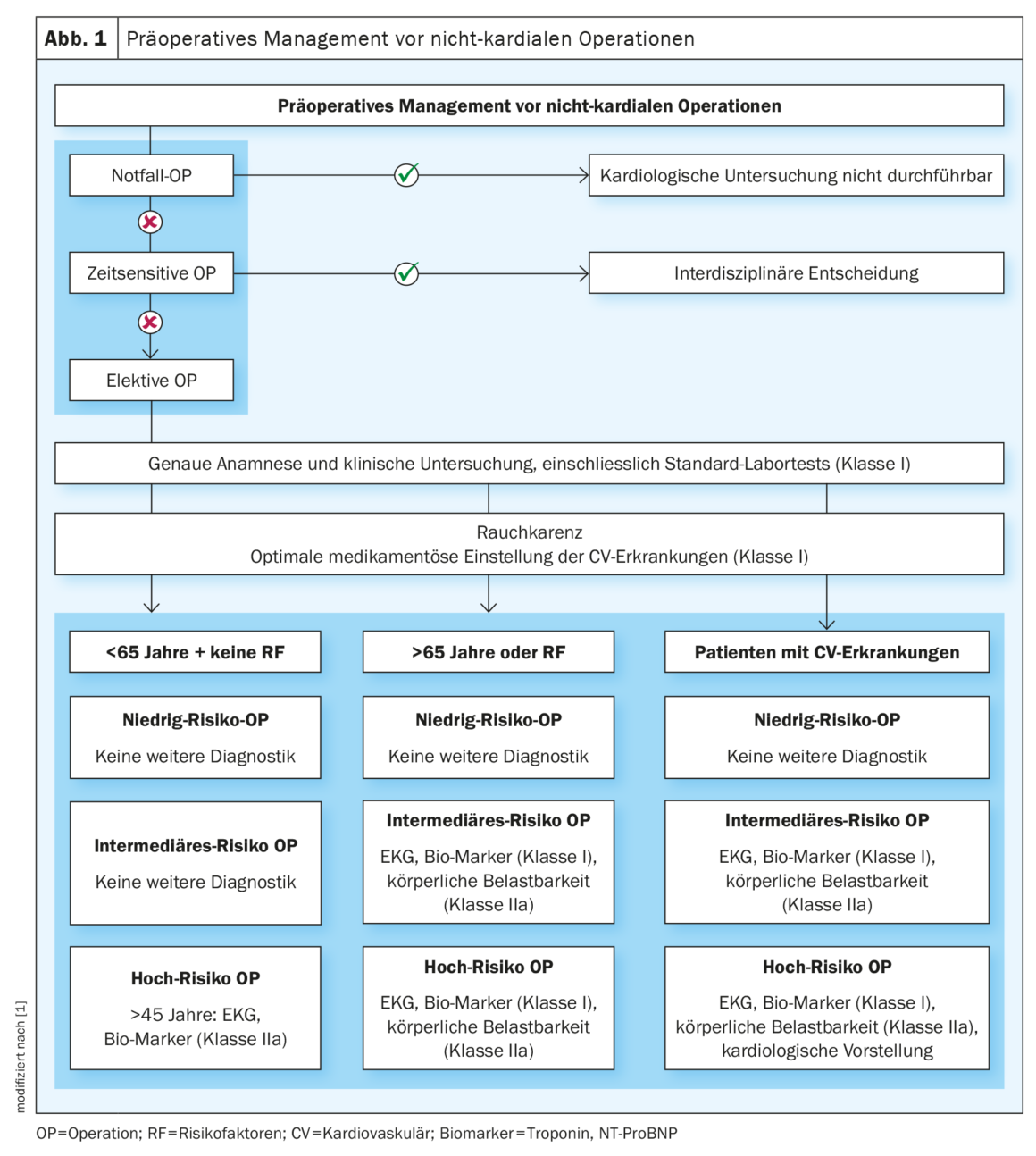
Como se muestra en la figura 1 , el algoritmo recomienda en primer lugar clasificar la urgencia de la operación. Se distingue entre emergencia, urgente, puntual y electiva. En las operaciones de urgencia y emergencia, la posibilidad de estratificar el riesgo es limitada y requiere -si la situación lo permite- una evaluación interdisciplinar a pie de cama. Sin embargo, la mayoría de las circunstancias clínicas permiten el enfoque sistemático recomendado en la directriz. La base de la vía posterior de diagnóstico y tratamiento es la historia clínica, el examen físico clínico y un laboratorio estándar, que debe registrar al menos un hemograma y la función renal.
En todos los pacientes, la optimización de los factores de riesgo cardiovascular es una gran prioridad antes de una intervención quirúrgica programada. Debe aconsejarse una abstinencia preoperatoria de nicotina de al menos cuatro semanas. Esto demostró una mejora significativa de los resultados quirúrgicos, especialmente en lo que respecta a las infecciones de la herida [4]. También es aconsejable el tratamiento farmacológico de la hipertensión arterial, la dislipoproteinemia y la diabetes mellitus, pero no la reducción de peso inmediatamente antes de la cirugía.
Posteriormente, en función del riesgo asociado al paciente y del riesgo de la intervención quirúrgica prevista, pueden adaptarse y complementarse otros diagnósticos preoperatorios, por ejemplo, con un electrocardiograma (ECG) de 12 derivaciones y biomarcadores cardíacos (troponina, BNP). Los datos muestran una asociación pronóstica de los biomarcadores con las complicaciones cardiovasculares postoperatorias [5]. El BNP puede ayudar a diagnosticar la insuficiencia cardiaca no detectada [6] y la troponina puede ayudar a diagnosticar la isquemia cardiaca o el infarto postoperatorio [7].
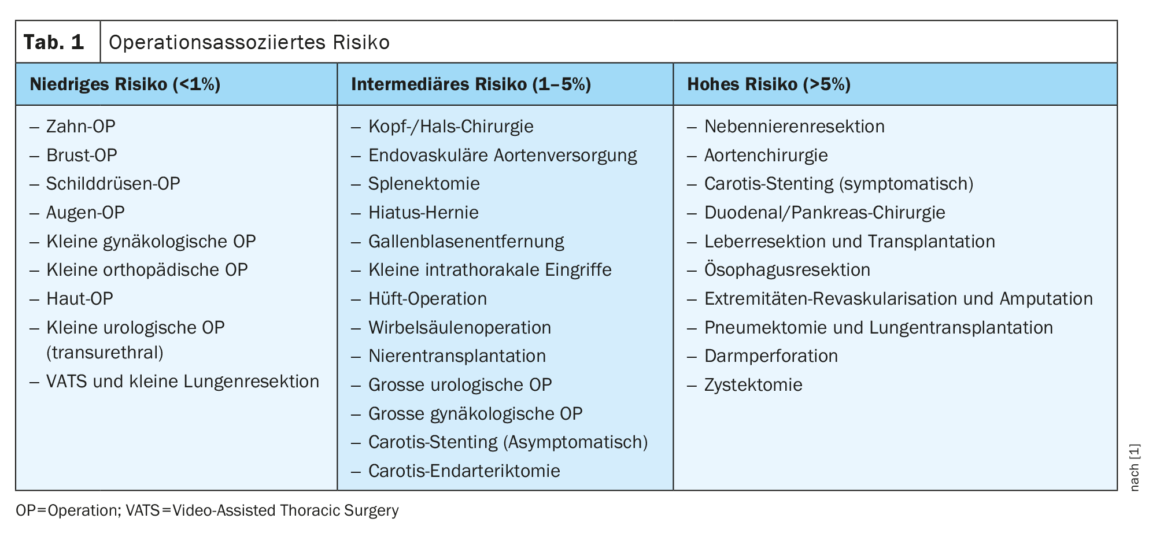
La directriz define tres categorías de pacientes y tres categorías de riesgo quirúrgico: El riesgo quirúrgico se clasifica en riesgo bajo, riesgo intermedio y riesgo alto. La directriz ofrece múltiples ejemplos para cada categoría, como también puede verse en el cuadro 1. En el riesgo asociado al paciente se tienen en cuenta tres factores: La edad, los factores de riesgo cardiovascular y las enfermedades cardiovasculares previas [8,9]. Se divide de la siguiente manera y, en función del riesgo asociado a la cirugía, se proporciona con las correspondientes recomendaciones para diagnósticos posteriores:
- En pacientes de entre 45 y 65 años sin factores de riesgo ni afecciones preexistentes, sólo debe realizarse una evaluación mediante ECG y biomarcadores antes de una intervención quirúrgica de alto riesgo quirúrgico (clase IIa) [8]. Excepción: Si existen antecedentes familiares de miocardiopatía genética, debe realizarse un ECG y una ecocardiografía transtorácica (ETT) en pacientes jóvenes y asintomáticos.
- En pacientes mayores de 65 años o con factores de riesgo existentes (hipertensión, antecedentes de tabaquismo, hiperlipoproteinemia, antecedentes familiares, diabetes mellitus), ya se recomienda la realización de un ECG (clase I) y la toma de biomarcadores (clase I) para las operaciones programadas con riesgo intermedio. Además, debe evaluarse la capacidad física (clase IIa) para detectar posibles enfermedades cardiovasculares. Esto puede determinarse, por ejemplo, mediante el Índice de Estado de Actividad de Duke [10] o la capacidad de subir dos tramos de escaleras. Un ECG de ejercicio bajo tensión ergométrica tiene una especificidad baja y sólo debe utilizarse como alternativa si la capacidad física no puede determinarse de forma válida a partir de la historia clínica [9].
- En pacientes con enfermedad cardiovascular preexistente conocida, se recomiendan todas las recomendaciones enumeradas en 2. Además, en el caso de operaciones de alto riesgo, la decisión sobre el procedimiento posterior debe tomarse de forma interdisciplinar con el cardiólogo tratante, teniendo en cuenta toda la información y los hallazgos.
Diagnóstico avanzado
Hallazgos como un soplo cardiaco, dificultad respiratoria, angina de pecho o edema pueden ser los primeros indicios de una enfermedad cardiovascular relevante y desconocida [9]. Si aparecen en el examen clínico, se recomienda lo siguiente:
Nuevo soplo cardíaco
- Con síntomas: ETT (Clase I)
- Sin síntomas: ETT antes de cirugía de riesgo intermedio o alto (clase IIa)
Angina de pecho
- Optativa OP: Diagnóstico cardiológico avanzado (Clase I)
- OP urgente: ECG, biomarcadores y debate interdisciplinar (Clase I)
Dificultad respiratoria y/o edema periférico
- ECG y biomarcadores (clase I)
- ETT con biomarcadores elevados (Clase I)
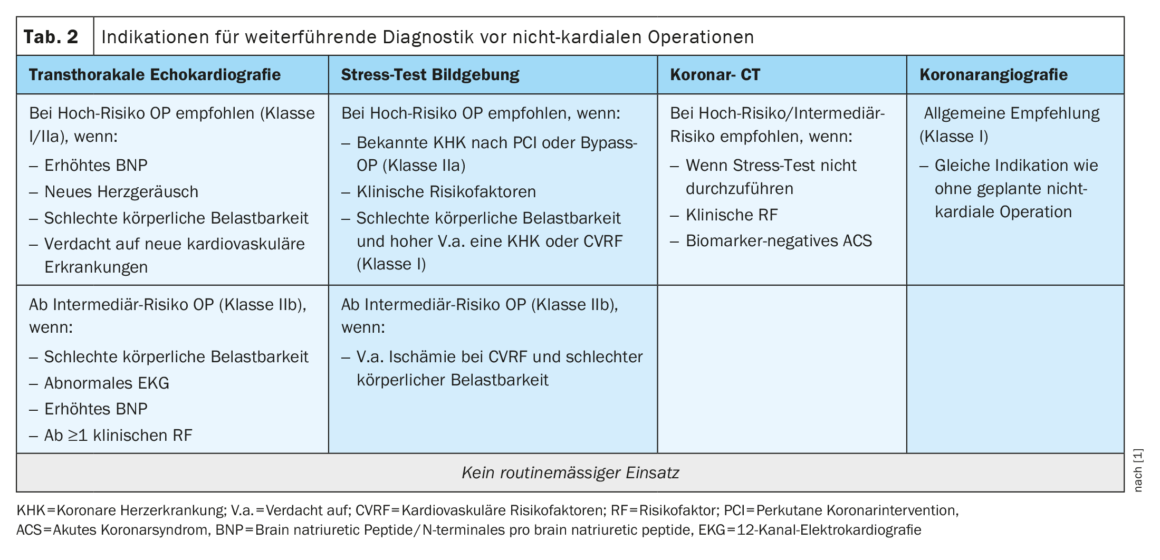
El deterioro de la función ventricular izquierda (VI), la valvulopatía y las miocardiopatías son las tres entidades con mayor potencial de riesgo cardiaco perioperatorio, que se detectan fácilmente mediante ecocardiografía transtorácica [12]. El deterioro de la función del VI (tanto sistólica como diastólica) también desempeña un papel crucial en las complicaciones cardiacas postoperatorias [13]. Sin embargo, la ETT no se asigna a una categoría en la vía diagnóstica central como recomendación general. Sin embargo, la directriz nombra indicaciones específicas para su aplicación (Tab. 2) .
En pacientes con mala tolerancia al ejercicio, factores de riesgo clínicos y ecocardiografía anormal, puede realizarse una prueba de imagen de estrés para profundizar en el diagnóstico [14]. Un déficit de perfusión en las imágenes de estrés muestra una asociación con una mayor tasa de complicaciones cardiacas postoperatorias [15]. Si no es posible obtener imágenes de esfuerzo, puede realizarse una tomografía computarizada (TC) coronaria para excluir una cardiopatía coronaria relevante con una probabilidad pretest baja y una buena calidad de imagen esperada [16]. La angiografía coronaria debe indicarse independientemente de la cirugía electiva prevista siguiendo la directriz de “Revascularización miocárdica” [11].
Infarto/daño de miocardio perioperatorio (PMI)
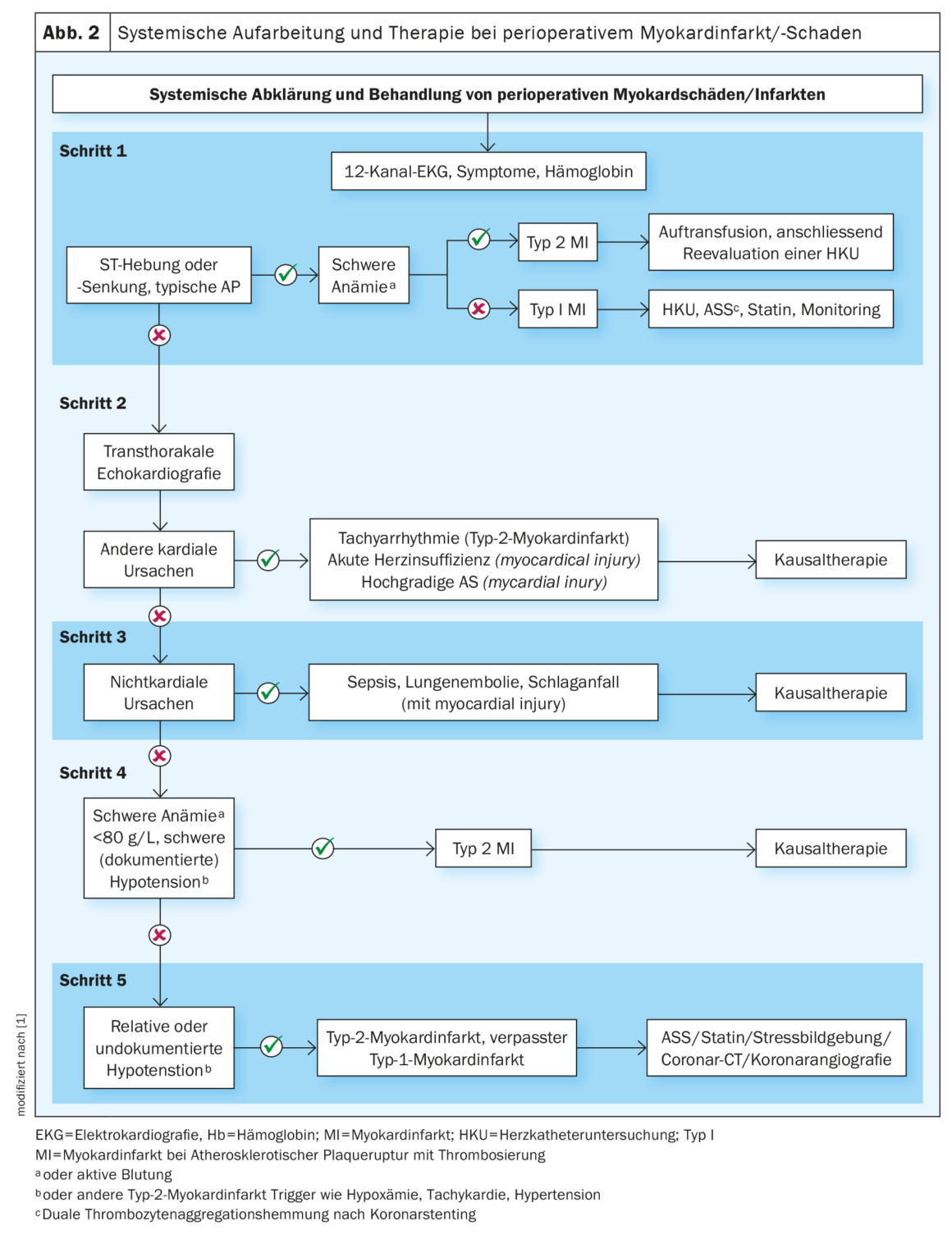
La troponina está generalmente establecida, es favorable, excluye la isquemia cardiaca en valores normales y ayuda en el diagnóstico del infarto/daño de miocardio (IAM) perioperatorio [7]. Esta última es una de las complicaciones cardiovasculares más frecuentemente observadas. En el 90% de los casos, permanece inicialmente asintomática debido a la anestesia y la analgesia postoperatoria o está enmascarada por otros síntomas, como el dolor de la herida, lo que dificulta su diagnóstico [17]. Para contrarrestarlo, se recomienda la toma de muestras de troponina en la población de pacientes adecuada 24 h y 48 h (clase I) después de la cirugía, además de la toma de muestras preoperatoria. Si los valores son elevados, está indicada una mayor clarificación para encontrar la causa. La troponina significativamente elevada se define como un aumento por encima del límite superior del ensayo utilizado en el laboratorio respectivo. El PMI puede deberse a una causa cardiaca, como un infarto de miocardio de tipo I o II, una descompensación aguda o una taquiarritmia, pero también a una causa no cardiaca, como una sepsis grave o una embolia de la arteria pulmonar. Para ello, debe utilizarse el algoritmo que figura en esta directriz y, en función de la causa, debe iniciarse la terapia adecuada (Fig. 2). En los casos de infarto de miocardio altamente probable debido a aterotrombosis, debe realizarse una angiografía coronaria inmediatamente después de descartar una anemia grave. No se recomienda la determinación rutinaria de biomarcadores.
Recomendaciones para el adelgazamiento de la sangre y la inhibición de la agregación plaquetaria
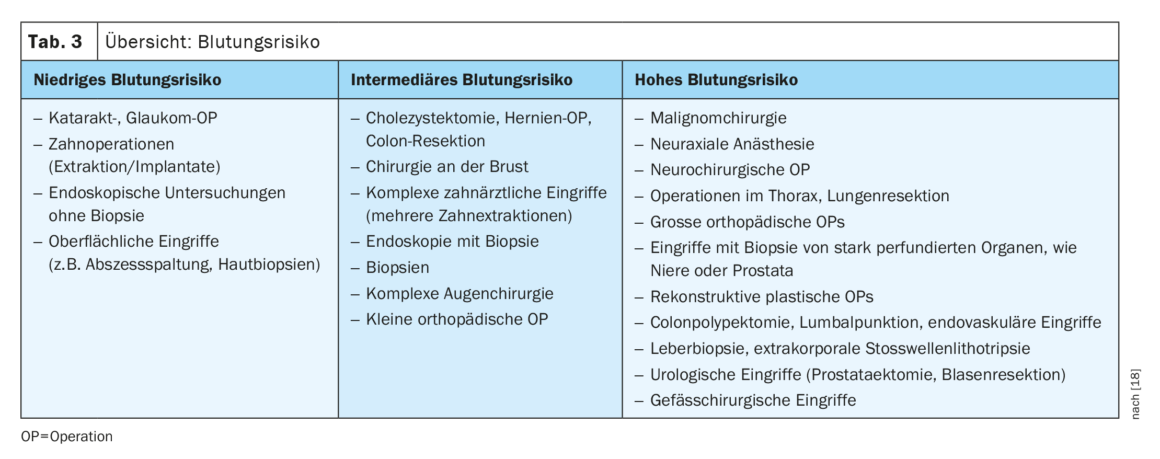
La nueva directriz formula recomendaciones sobre el uso de anticoagulantes plasmáticos y antiagregantes plaquetarios para la reducción del riesgo perioperatorio. El primer paso es evaluar el riesgo de hemorragia perioperatoria (Tab. 3). A continuación debe evaluarse el riesgo trombótico del paciente.
Inhibición de la agregación plaquetaria
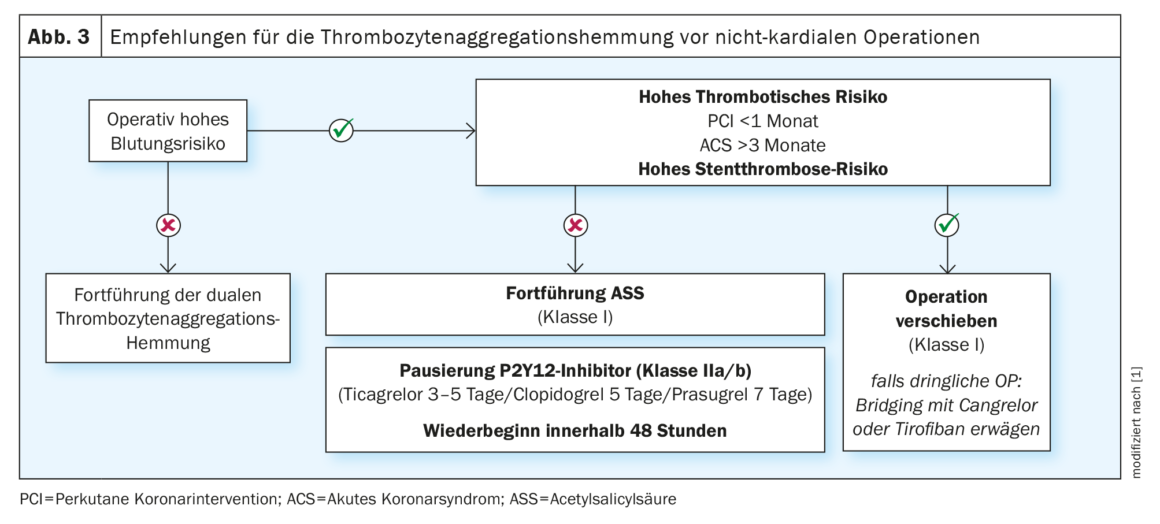
Si se toma ácido acetilsalicílico (AAS) como profiláctico primario, el riesgo de acontecimientos cardiovasculares es bajo y puede pausarse perioperatoriamente [19]. Para un uso profiláctico secundario, en cambio, no se recomienda la pausa (clase III) [20]. Los pacientes con doble terapia antiplaquetaria tras una intervención coronaria percutánea (ICP) tienen un riesgo significativamente mayor de sufrir complicaciones cardiovasculares relevantes del 2-8% [21]. El mayor riesgo en este caso se da en el primer mes tras la ICP, especialmente si la ICP inicial fue en un IAMCEST, se suspendió la terapia antiplaquetaria dual o la lesión coronaria era compleja [22]. Por lo tanto, la cirugía electiva no cardiaca debe posponerse hasta después del cese de la terapia antiplaquetaria dual (seis meses después de una ICP electiva y doce meses después de un síndrome coronario agudo (SCA) o una ICP de alto riesgo [Klasse I]) [23]. Para las indicaciones quirúrgicas urgentes, la terapia antiplaquetaria dual debe haberse tomado durante al menos tres meses (clase IIb) en pacientes de alto riesgo tras una ICP en el contexto de un SCA y durante al menos un mes (clase IIa) tras una ICP electiva. Posteriormente, sólo debe suspenderse el inhibidor de P2Y12 durante tres a siete días en el preoperatorio [24] y reiniciarse con dosis de carga lo antes posible tras la evaluación del riesgo (tabla 3). En constelaciones de alto riesgo tras una ICP, la cirugía no cardiaca debe realizarse en un centro con capacidad de laboratorio de cateterismo cardiaco las 24 horas del día.
Anticoagulación oral
En caso de terapia combinada de antiagregantes plaquetarios y anticoagulación oral, la cirugía electiva debe posponerse hasta el final de la terapia antiagregante plaquetaria (seis meses después de una ICP electiva y doce meses después de un SCA). Cuando se toma un antagonista de la vitamina K, si existe un mayor riesgo de hemorragia y al mismo tiempo un alto riesgo de trombosis (por ejemplo, en pacientes con sustitución valvular mecánica), debe pausarse la toma e iniciarse una terapia puente con heparina [25]. En pacientes con anticoagulación oral para la fibrilación auricular, se ha demostrado que el puenteo tiene un efecto negativo, por lo que sólo debe realizarse cuando el riesgo trombótico sea elevado y se sopese con el riesgo de hemorragia [26]. La reanudación de la OAK puede adaptarse al riesgo a partir de las doce horas postoperatorias. Sin vitamina K
Los antagonistas también deben pausarse antes de la cirugía no cardiaca. La colocación de puentes sólo está indicada en casos excepcionales de alto riesgo trombótico. En caso de deterioro de la función renal, la ingesta debe interrumpirse antes (TFG <50 mL/min al menos 48-72 horas) [27].
Enfermedades especiales
Las enfermedades previas del paciente también deben tenerse en cuenta en el preoperatorio, ya que también favorecen el riesgo perioperatorio: Las enfermedades coronarias aumentan el riesgo perioperatorio. El SCA debe tratarse siempre según la directriz y la cirugía electiva debe posponerse con este fin [28]. En el síndrome coronario crónico, aún no existe una recomendación segura debido a la falta de datos [29]. La insuficiencia cardiaca también influye negativamente en la mortalidad postoperatoria tras una cirugía no cardiaca [30]. Debe iniciarse y continuarse una terapia farmacológica basada en pautas [31]. Un dispositivo de TRC existente no debe desactivarse excepto para la función de desfibrilación.
Las cardiopatías valvulares aumentan el riesgo perioperatorio en función de la gravedad del vitium y, por tanto, plantean un reto importante en el preoperatorio [32]. Por lo tanto, la ETT debe realizarse en todos los pacientes con valvulopatía conocida antes de una intervención quirúrgica no cardiaca de riesgo intermedio a alto. En la directriz se mencionan las siguientes recomendaciones de actuación:
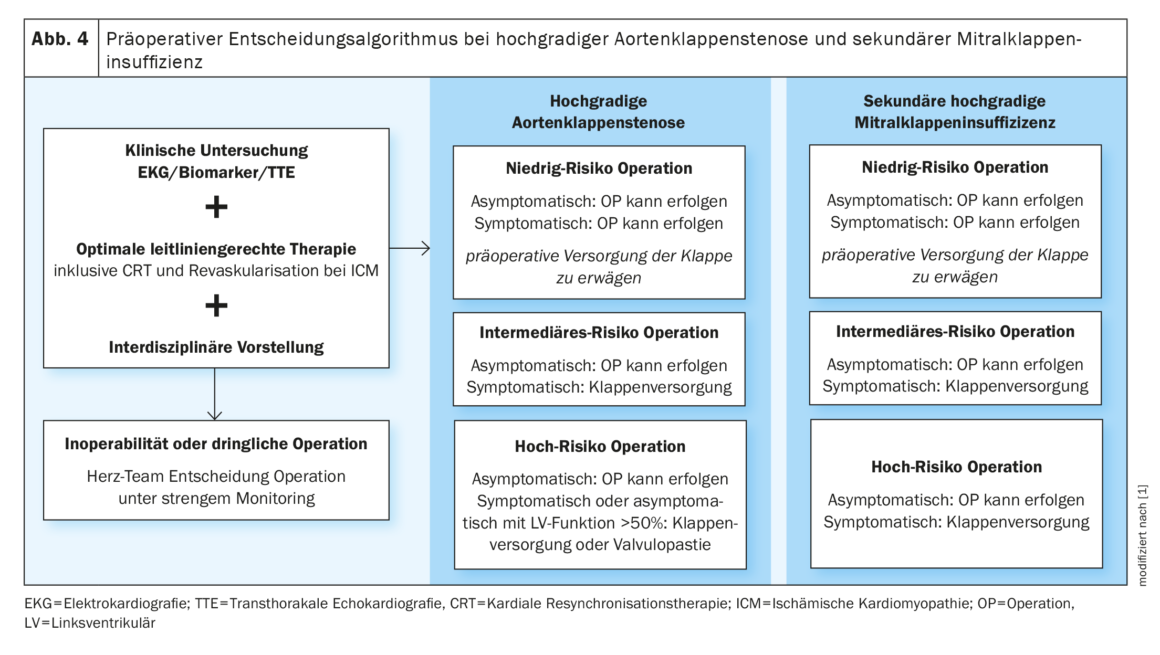
Se ha demostrado que la estenosis aórtica (EA) sintomática de alto grado afecta negativamente a las complicaciones postoperatorias y a la supervivencia a 30 días [33]. Por ello, la cirugía electiva debe posponerse hasta después de la sustitución valvular. En caso de cirugía urgente no cardiaca, la valvuloplastia con balón puede utilizarse como procedimiento puente. Los pacientes con EA asintomática de alto grado con función del VI normal pueden ser autorizados para una cirugía de riesgo bajo e intermedio.
En la regurgitación sintomática de alto grado de la válvula aórtica (IA), así como en la IA asintomática de alto grado (con una DSVI >50 mm o una función ventricular izquierda (FVI) de >50%, debe realizarse un tratamiento valvular guiado por las directrices antes de una cirugía electiva de riesgo intermedio o alto [34].
Se recomienda la valvuloplastia con balón antes de la cirugía de alto riesgo para la estenosis sintomática de grado moderado a alto de la válvula mitral y para una presión arterial pulmonar sistólica >50 mmHg.
En los casos de regurgitación de alto grado de la válvula mitral (IM), el primer paso es aclarar la FVI y la etiología. En presencia de una miocardiopatía isquémica concomitante y de un IM secundario, en este caso también debería realizarse una intervención valvular antes de la cirugía electiva en el contexto de riesgo intermedio o alto [35,36].
La pericarditis activa debe tratarse primero según las directrices antes de la cirugía no cardiaca [37].
Los pacientes con enfermedad pulmonar tienen complicaciones pulmonares, especialmente en el postoperatorio. En pacientes con enfermedad pulmonar obstructiva crónica, debe aprovecharse el periodo preoperatorio para iniciar una terapia antiobstructiva que mejore la función pulmonar.
Si se sospecha de apnea obstructiva del sueño, debe evaluarse la indicación de una terapia de presión positiva continua en las vías respiratorias para reducir el riesgo cardiovascular [38].
En pacientes con hipertensión arterial con un perfil de presión arterial por encima de 180 mmHg sistólica, así como por encima de 110 mmHg diastólica, la cirugía electiva debe posponerse hasta que se consiga un mejor control [38,39].
Los pacientes con enfermedad oclusiva arterial cerebral combinada con síntomas neurológicos en los últimos seis meses deben ser presentados preoperatoriamente a un neurólogo. Los pacientes con estenosis carotídea sintomática (>70%) y accidente isquémico transitorio o ictus en los últimos tres meses deben ser tratados en primer lugar [40].
Si tiene que evaluar preoperatoriamente a un paciente con una enfermedad maligna, debe preguntar, entre otras cosas, por la quimioterapia cardiotóxica y/o la radiación torácica, ya que estos pacientes – a menudo también a una edad temprana – pueden tener una cardiopatía coronaria o una vitiación [41].
En caso de infección actual o reciente por SARS-Cov2, puede observarse un mayor número de tromboembolismos, así como una mayor mortalidad en cirugía no cardiaca. Este riesgo dura hasta siete semanas después del diagnóstico y aumenta especialmente cuando los pacientes siguen siendo sintomáticos [42]. Además, el estrés cardiaco resultante y el daño miocárdico asociado conducen a un mayor riesgo perioperatorio de eventos cardiacos [43]. En consecuencia, la cirugía electiva sólo debe realizarse tras una recuperación completa. Todavía no hay recomendaciones para los pacientes vacunados debido a la falta de datos.
Por último, cabe señalar que para muchas de las recomendaciones de esta directriz, el nivel de evidencia es sólo C y se necesitan más estudios.
Mensajes para llevarse a casa
- Alrededor del 50% de las causas perioperatorias de muerte en cirugía no cardiaca pueden atribuirse a causas cardiovasculares. A través de
Una evaluación preoperatoria adecuada del riesgo cardiovascular puede reducir el riesgo de complicaciones. - Los autores de la directriz de la ESC de 2022 han elaborado 147 recomendaciones específicas basadas en una revisión exhaustiva de la bibliografía actual.
- Se presta especial atención a la obtención de los biomarcadores troponina y NT-ProBNP, ya que muestran una correlación pronóstica con las complicaciones cardiovasculares postoperatorias.
- En caso de daño miocárdico perioperatorio con dinámica de troponina, debe aclararse la causa y posibilitar así una terapia causal
- Una gestión perioperatoria de la terapia de coagulación adaptada individualmente puede prevenir acontecimientos trombóticos y evitar complicaciones hemorrágicas.
- La directriz también ha desarrollado recomendaciones concretas para cuadros clínicos específicos.
Literatura:
- Halvorsen S, Mehilli J, Cassese S, et al.: ESC Scientific Document Group. 2022 ESC Guidelines on cardiovascular as-sessment and management of patients undergoing non-cardiac surgery. Eur Heart J 2022 Oct 14;43(39): 3826–3924.
- Weiser TG, et al.: An estimation of the global volume of surgery: a modelling strategy based on available data. Lancet 2008 Jul 12; 372(9633): 139–144.
- Smilowitz, et al.: Trends in cardiovascular risk factor and disease prevalence in patients undergoing non-cardiac surgery. Heart 2018 Jul; 104(14): 1180–1186.
- Gourgiotis, et al.: The effects of tobacco smoking on the incidence and risk of intraoperative and postopera-tive complications in adults. Surgeon 2011 Aug; 9(4): 225–232.
- Weber, et al.: Incremental value of high-sensitive troponin T in addition to the revised cardiac index for peri-operative risk stratification in non-cardiac surgery. Eur Heart J 2013 Mar; 34(11): 853–862.
- Mueller, et al.: Heart Failure Association of the European Society of Cardiology practical guidance on the use of natriuretic peptide concentration, Eur J Heart Fail 2019;21: 715–731.
- Walter, et al.: Using High-Sensitivity Cardiac Troponin for the Exclusion of Inducible Myocardial Ischemia in Symptomatic Patients: A Cohort Study. Ann Intern Med 2020 Feb 4; 172(3): 175–185.
- Botto, et al.: Myocardial injury after noncardiac surgery: a large, international, prospective cohort study establishing diagnostic criteria, characteristics, predictors, and 30-day outcomes. Anesthesiology 2014 Mar; 120(3): 564–578.
- Visseren, et al.: 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J 2021 Sep 7; 42(34): 3227–3337.
- Wijeysundera, et al.: Assessment of functional capacity before major non-cardiac surgery: an international, prospective cohort study. Lancet 2018 Jun 30; 391(10140): 2631–2640.
- Knuuti, et al.: 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020 Jan 14;41(3): 407–477.
- Steeds, et al.: EACVI appropriateness criteria for the use of transthoracic echocardiography in adults: a re-port of literature and current practice review. Eur Heart J Cardiovasc Imaging 2017; 18: 1191–1204.
- Halm, et al.: Echocardiography for assessing cardiac risk in patients having noncardiac surgery. Study of Perioperative Ischemia Research Group. Ann Intern Med 1996; 125: 433–441.
- Pellikka, et al.: Guidelines for performance, interpretation, and application of stress echocardiography in is-chemic heart disease: from the American Society of Echocardiography. J Am Soc Echocardiogr 2020; 33: 1–41.e8.
- Ballal, et al.: Prognosis of patients with vascular disease after clinical evaluation and dobutamine stress echocardiography; Am Heart J 1999;137: 469–475.
- Sheth T, Chan M, Butler C, et al.: Prognostic capabilities of coronary computed tomographic angiography before on-cardiac surgery: pro-spective cohort study. BMJ 2015; 350: h1907.
- Devereaux, et al.: Cardiac complications in patients undergoing major noncardiac surgery. N Engl J Med 2015; 373: 2258–2269.
- Steffel J, Collins R, Antz M, et al.: Guide on the use of non-vitamin k an-tagonist oral anticoagulants in patients with atrial fibrillation 2021 European Heart Rhythm Association Practical Europace 2021; 23: 1612–1676.
- Zheng, et al.: Association of aspirin use for primary prevention with cardiovascular events and bleeding events: a systematic review and meta-analysis. JAMA 2019; 321: 277–287.
- Graham, et al.: Aspirin in patients with previous percutaneous coronary intervention undergoing noncardiac surgery; Ann Intern Med 2018; 168: 237–244.
- Holcomb CN, Graham LA, Richman JS, et al.: The incremental risk of coronary stents on postoperative adverse events: a matched cohort study. Ann Surg 2016; 263: 924–930.
- Saia, et al.: Risk of adverse cardiac and bleeding events following cardiac and noncardiac surgery in patients with coronary stent: how important is the interplay between stent type and time from stenting to surgery?; Circ Cardiovasc Qual Outcomes 2016; 9: 39–47.
- Knuuti, et al.: 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes, Eur Heart J 2020; 41: 407–477.
- Collet, et al.: 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J 2021; 42: 1289–1367.
- Kuo, et al.: Thromboembolic and bleeding risk of periprocedural bridging anticoagulation: a systematic re-view and meta-analysis; Clin Cardiol 2020; 43: 441–449.
- Douketis JD, Spyropoulos AC, Kaatz S, et al.: Perioperative bridging antico-agulation in patients with atrial fibrillation. N Engl J Med 2015; 373: 823–833.
- Godier A, Dincq AS, Martin AC, et al.: Predictors of pre-procedural concentra-tions of direct oral anticoagulants: a prospective multicentre study. Eur Heart J 2017; 38: 2431–2439.
- Ibanez, et al.: 2017 ESC Guidelines for the management of acute myocardial infarction in patients present-ing with ST-segment elevation: the Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2018; 39: 119–177.
- Illuminati, et al.: Systematic preoperative coronary angiography and stenting improves postoperative results of carotid endarterectomy in patients with asymptomatic coronary artery disease: a randomised controlled trial.; Eur J Vasc Endovasc Surg 2010; 39: 139–145.
- Hammill BG, Curtis LH, Bennett-Guerrero E, et al.: Im-pact of heart failure on patients undergoing major noncardiac surgery, Anesthesiology 2008; 108: 559–567.
- McDonagh, et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure; Eur Heart J 2021; 42: 3599–3726.
- Agarwal, et al.: Impact of aortic stenosis on postoperative outcomes after noncardiac surgeries.; Circ Cardio-vasc Qual Outcomes 2013; 6: 193–200.
- Taniguchi, et al.: Elective non-cardiac surgery in patients with severe aortic stenosis – observations from the CURRENT AS Registry; Circ J 2020; 84: 1173–1182.
- Vahanian, et al.: 2021 ESC/EACTS Guidelines for the management of valvular heart disease; Eur Heart J 2022; 43: 561–632.
- Stone, et al.: Transcatheter mitral-valve repair in patients with heart failure; N Engl J Med 2018; 379: 2307–2318.
- Bauersachs J, et al.: 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Eur Heart J 2022;43: 561–632.
- Adler, et al.: 2015 ESC Guidelines for the diagnosis and management of pericardial diseases: the Task Force for the Diagnosis and Management of Pericardial Diseases of the European Society of Cardiology (ESC). Endorsed by: the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2015; 36: 2921–2964.
- Chau, et al.: Obesity hypoventilation syndrome: a review of epidemiology, pathophysiology, and perioperative considerations. Anesthesiology 2012; 117: 188–205.
- Im, et al.: Association between use of preoperative antihypertensive medication and 90-day mortality after noncardiac surgery: a retrospective cohort study; Am J Hypertens 2020; 33: 534–542.
- Aboyans, et al.: 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS). Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries. Endorsed by: the European Stroke Organization (ESO). The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J 2018;39: 763–816.
- 2022 ESC Guidelines on cardio-oncology ESC. Eur Heart J 2022;
- SARS-CoV-2 infection and venous thromboembolism after surgery: an international prospective cohort study. COVIDSurg Collaborative, GlobalSurg Collaborative. Anaesthesia 2022;77: 28–39.
- Guzik, et al.: COVID-19 and the cardiovascular system: implications for risk assessment, diagnosis, and treatment options. Cardiovasc Res 2020; 116: 1666–1687.
CARDIOVASC 2023; 22(2): 10–17