La demencia vascular (DV) es la segunda causa más común de demencia después de la demencia de Alzheimer y, por tanto, la forma no neurodegenerativa más común de demencia. No se trata de una enfermedad singular. De especial importancia clínica es la microangiopatía cerebral a menudo asociada a la hipertensión, que puede conducir a la demencia vascular isquémica subcortical (DIVS). Ésta es probablemente la forma mejor caracterizada de DVa y se caracteriza menos por el deterioro de la memoria que por alteraciones en las funciones ejecutivas y la velocidad de procesamiento. El diagnóstico se basa sobre todo en exámenes anamnésicos, clínicos y de imagen. En cualquier caso, debería hacerse en una fase temprana.
En un futuro próximo, en el contexto del desarrollo demográfico de las naciones industrializadas occidentales, cabe esperar un aumento de la prevalencia de las enfermedades demenciales. Debido a las consiguientes implicaciones tanto médicas como socioeconómicas, la Oficina Federal de Salud Pública ha adoptado recientemente la “Estrategia nacional contra la demencia 2014-2017” de Suiza [1].
Además de la demencia de Alzheimer (EA), que es la causa más común de demencia, las demencias vasculares (DV) desempeñan un papel importante como segunda forma más común y causa más frecuente de formas no neurodegenerativas de demencia [2,3]. Los hombres -a diferencia de la EA- se ven afectados aproximadamente el doble de veces que las mujeres. Las posibles causas de la DVa se resumen en la Tabla 1 a modo de referencia. La EA y la DVa, así como la demencia mixta, representan hasta el 80% de las demencias. Esta última incluye solapamientos no infrecuentes entre la EA y la DVa. Los procesos vasculares también desempeñan un papel importante en el desarrollo de la demencia en el contexto de la EA [4–7], por lo que hoy en día ambas formas también se consideran un continuo.
Clasificación de la demencia vascular
La DVa no es una enfermedad única, sino un término paraguas para una variedad de enfermedades cerebrovasculares que pueden provocar deterioro cognitivo e incluso demencia (Tabla 1).

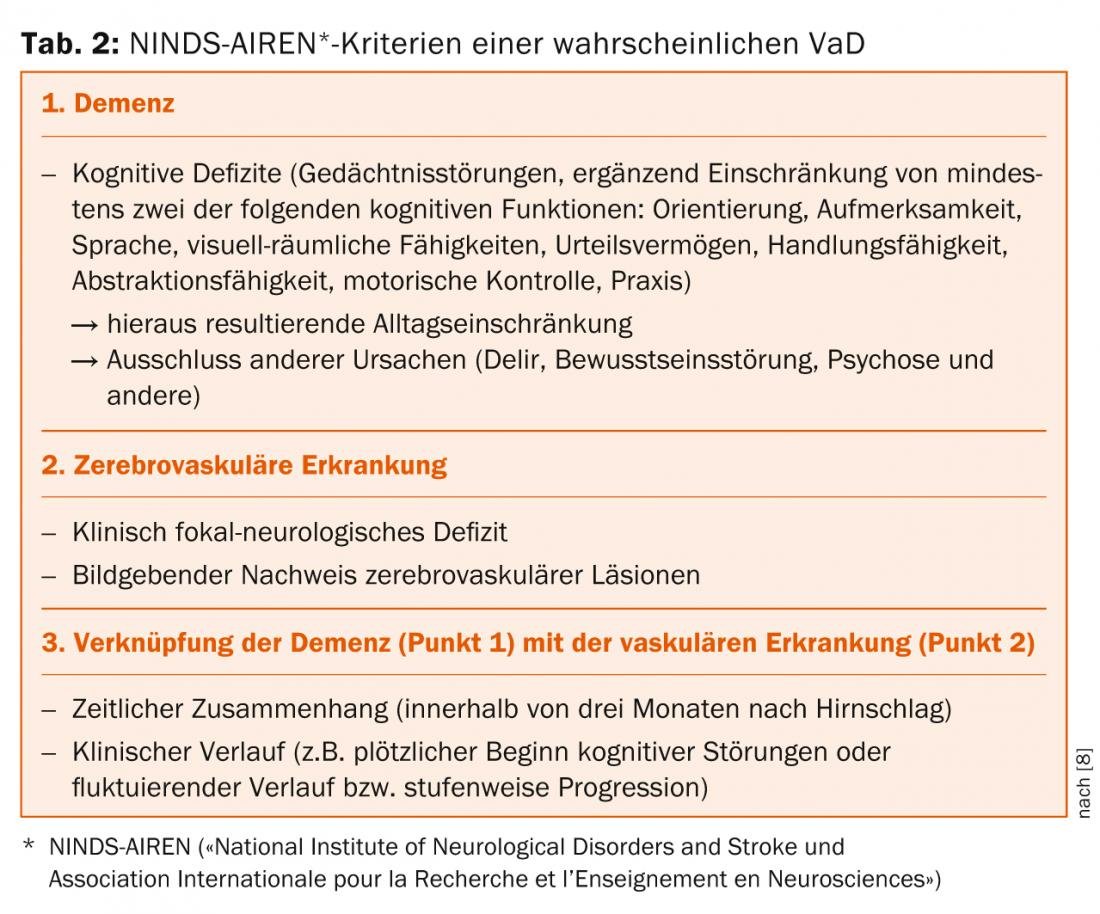
Los llamados criterios NINDS-AIREN [8], que se basan en la presencia de demencia y enfermedad cerebrovascular (Tab. 2 ), se siguen utilizando hoy en día como sistema válido para diagnosticar la DVa. Además, se utilizan criterios estandarizados para la clasificación y el diagnóstico de los trastornos cognitivos vasculares [9].
Microangiopatía cerebral
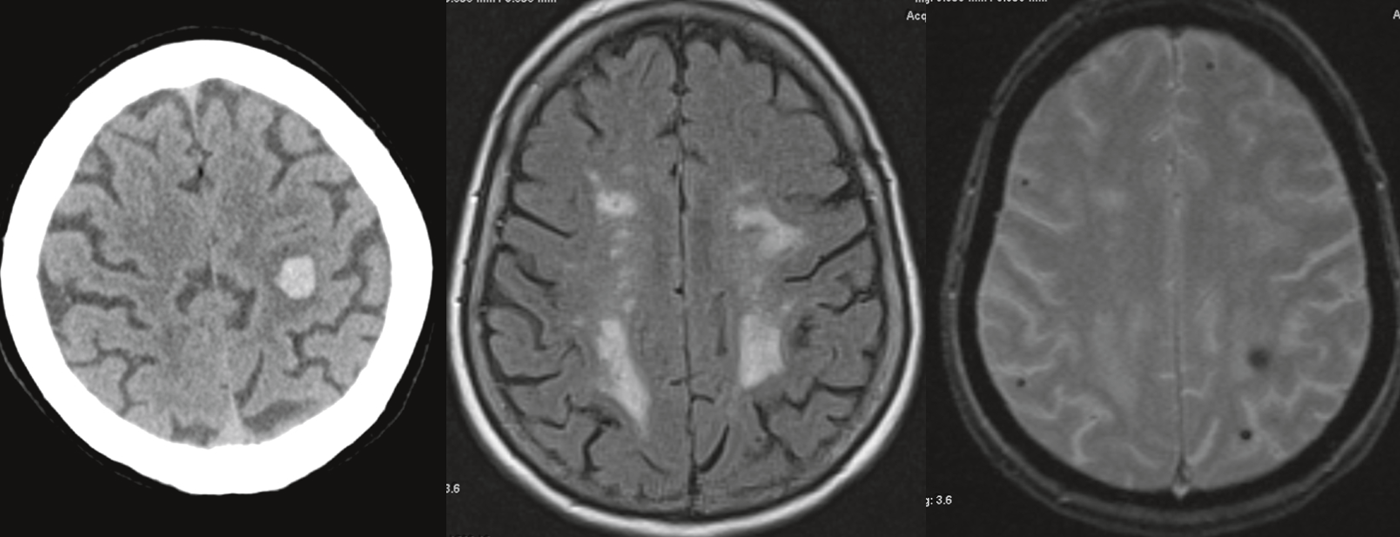
La causa más común de la DVa es la microangiopatía cerebral, que está particularmente asociada a la hipertensión arterial. Además de esta forma esporádica, también existen formas hereditarias más raras de microangiopatía, en las que suele haber antecedentes familiares positivos de ictus cerebrales o trastornos cognitivos, posiblemente sin que existan factores de riesgo vascular. Aproximadamente un tercio de todos los ictus isquémicos están causados por una microangiopatía cerebral. Éstas dan lugar a lesiones cerebrales isquémicas típicas que pueden visualizarse mediante resonancia magnética: Se producen infartos subcorticales lacunares. (Fig. 1a) así como cambios vasculares leucencefalopáticos en la zona del canal medular. (Fig.1b). Además, a veces pueden encontrarse microhemorragias, que en la microangiopatía suelen localizarse en la zona de las estructuras más profundas (por ejemplo, los ganglios basales).
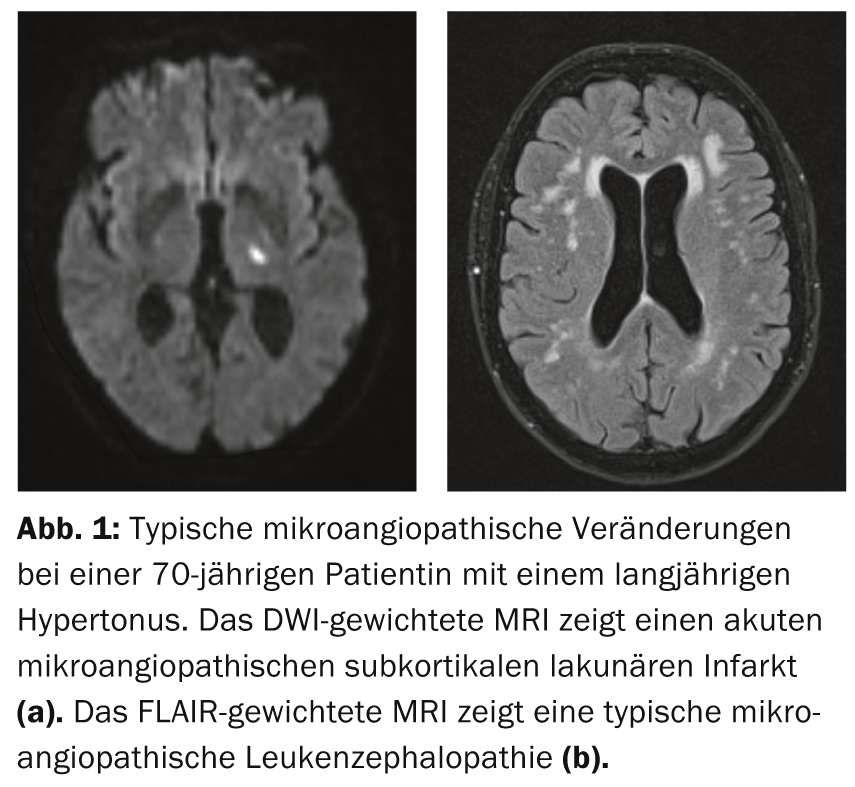
Además de los signos y síntomas clínicos físicos (déficits neurológicos focales, trastornos de la micción, alteraciones de la marcha), los trastornos cognitivos ocupan clínicamente un primer plano en las microangiopatías. A menudo se producen de forma fluctuante e insidiosamente progresiva y no tienen por qué estar asociados a un ictus clínicamente tangible. Debido a la patología en la zona de los pequeños vasos cerebrales arteriales que penetran subcorticalmente, se produce la denominada demencia vascular isquémica subcortical (DIVS) en el contexto de una isquemia medular. Se considera la forma más común de DVa y, por lo tanto, reviste especial importancia en la práctica clínica. En comparación con la EA, se caracteriza mucho menos por el deterioro de la memoria, sino principalmente por alteraciones de las funciones ejecutivas y de la velocidad de procesamiento [10]. Por ello, en su forma pura, suele diferenciarse clínicamente de la EA. En última instancia, la microangiopatía también conduce a la atrofia cerebral, que se asocia a la progresión de los déficits cognitivos [11]. En particular, la hipertensión arterial es un factor de riesgo para la atrofia cerebral debida a la microangiopatía. Esto respalda la importancia clínica de ajustar la presión arterial y los factores de riesgo vascular en general.
Diagnóstico y diagnóstico diferencial
La clasificación diagnóstica de la microangiopatía cerebral y la DVa asociada se basa en parámetros anamnésicos, clínicos y de imagen. Encontrará una visión general en la tabla 3.

A menudo ya es posible realizar una evaluación inicial de los trastornos cognitivos durante la entrevista de la historia clínica. La historia externa de los familiares es de gran importancia en este caso, entre otras cosas en lo que respecta a las posibles limitaciones en la vida cotidiana. En particular, debe indagarse sobre las alteraciones cognitivas que indican trastornos de la atención, la concentración y las funciones ejecutivas. Existen procedimientos de pruebas cortas cognitivas como diagnóstico básico para la evaluación de la orientación inicial y la cuantificación de las deficiencias cognitivas. Se pueden utilizar bien en la rutina clínica y también pueden servir como parámetros de seguimiento en caso necesario. Aquí cabe mencionar, por ejemplo, el Mini-Mental-Test, el DemTect, el TFDD (test para la detección precoz de la demencia con delimitación de la depresión) o la versión en alemán del MoCA (“Montreal Cognitive Assessment”), aunque estos procedimientos de prueba no están dirigidos específicamente a la DVa. Alternativamente, para los trastornos cognitivos vasculares, se proponen dos pruebas más cortas (de 5 y 30 minutos) para uso clínico rutinario [9], que son más capaces de captar los déficits característicos de la microangiopatía antes mencionados. La llamada prueba de creación de rastros también es útil para este fin.
El examen neurológico clínico muestra a menudo reflejos primitivos desinhibidos (reflejo palmomental, reflejo de prensión, etc.) y reflejos posturales alterados. Además de los déficits neurológicos focales relacionados con la isquemia, los trastornos motores extrapiramidales también pueden manifestarse en fases avanzadas de la enfermedad.
El diagnóstico por imagen mediante IRM (tab. 3) tiene como objetivo, por un lado, detectar lesiones vasculares frescas (DWI) o más antiguas (T2/FLAIR) (fig. 1).
En particular, cabe mencionar aquí las lesiones medulares isquémicas típicas que pueden detectarse en la evaluación T2/FLAIR, que pueden presentarse en las formas más variadas hasta una leucoencefalopatía confluente. Tales cambios son un hallazgo común con la edad. Además, está la cuestión de los defectos de la sustancia lacunar (T1) y las hemorragias o microhemorragias (T2*/SWI).
Además, el diagnóstico por imagen se utiliza para excluir otras patologías cerebrales que puedan dar lugar a un síndrome demencial (por ejemplo, NPH, lesiones inflamatorias, tumores, atrofia regional o global en el curso de una enfermedad neurodegenerativa).
Un diagnóstico diferencial importante de la microangiopatía cerebral -especialmente en personas mayores- es la angiopatía amiloide cerebral (AAC) (Fig. 2), que también puede provocar DVa. Una delimitación diagnóstica diferencial es especialmente importante porque la AAC se asocia en particular a hemorragias cerebrales y, por tanto, tiene consecuencias terapéuticas directas, por ejemplo en lo que respecta al uso de inhibidores de la agregación plaquetaria en un paciente con una leucoencefalopatía vascular.
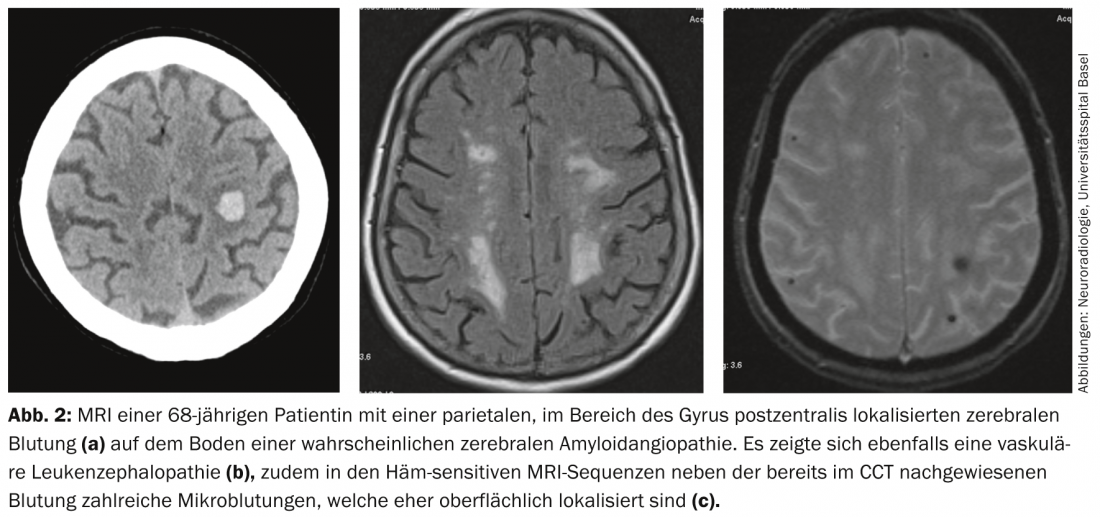
En ocasiones, el diagnóstico diferencial de las lesiones medulares isquémicas microangiopáticas con respecto a otras causas no vasculares de leucoencefalopatía puede resultar difícil.
Los diagnósticos diferenciales importantes se enumeran en la tabla 4. Merecen especial mención aquí las enfermedades inflamatorias y metabólicas. En caso necesario, deben considerarse otras pruebas, en particular de líquido cefalorraquídeo (LCR), de química de laboratorio y serológicas, para el diagnóstico diferencial de una génesis microangiopática-vascular de una leucoencefalopatía.

Terapia
Enfermedades vasculares subyacentes: El tratamiento en la DVa se dirige especialmente al control precoz de las enfermedades vasculares y los factores de riesgo existentes, y en la microangiopatía particularmente al control de la presión arterial. Lo importante aquí es el control de la presión arterial per se, más que el uso de grupos específicos de sustancias, por lo que los antihipertensivos que actúan sobre el sistema renina-angiotensina pueden tener un papel especial en este contexto. Dado que la aparición de un ictus clínicamente manifiesto es de por sí un factor de riesgo para la DVa, es importante el control de los factores de riesgo en el sentido de la profilaxis primaria de las enfermedades cerebrovasculares. Lo mismo se aplica en consecuencia a la prevención secundaria del ictus, ya que el ictus recurrente provoca un nuevo aumento significativo del riesgo de DVa [12]. Así pues, la profilaxis secundaria con medicación según las recomendaciones de las directrices actuales también desempeña un papel importante en relación con los trastornos cognitivos vasculares.
Para el uso profiláctico primario de, por ejemplo, inhibidores de la agregación plaquetaria para la terapia/profilaxis de la demencia, no se dispone hoy en día de datos claros, por lo que actualmente no se recomienda. Esto también se aplica al uso de estatinas. Debe ofrecerse asesoramiento sobre los factores modificables del estilo de vida, especialmente el consumo de alcohol y nicotina y la actividad física. Así pues, la terapia de los factores y las enfermedades vasculares desempeña un papel importante en general en la prevención y el tratamiento de la demencia, sobre todo porque los enfoques terapéuticos de la EA como enfermedad neurodegenerativa son limitados hasta la fecha.
Terapia sintomática: Si existen pruebas de demencia mixta, actualmente se recomienda una terapia sintomática como en la EA, siempre que no existan contraindicaciones vasculares, por ejemplo, para el uso de inhibidores de la colinesterasa. En el caso de síntomas neuropsiquiátricos concomitantes, el uso de neurolépticos atípicos en particular debe revisarse críticamente en el contexto de un riesgo potencialmente mayor de complicaciones cerebrovasculares. También deben evitarse los neurolépticos convencionales debido a sus potenciales efectos secundarios motores anticolinérgicos y extrapiramidales. Los síntomas de depresión no deben tratarse con antidepresivos anticolinérgicos (como los tricíclicos); los inhibidores selectivos de la recaptación de serotonina (ISRS) son una opción en este caso.
Resumen
El término DVa no describe una enfermedad singular, sino un síndrome general de demencia basado en enfermedades cerebrovasculares. La microangiopatía cerebral es la causa más común de la DVa. A menudo se asocia a la hipertensión arterial y conduce en particular a un deterioro cognitivo subcortical. Así pues, el perfil de los trastornos cognitivos es diferente del de la EA, pero no son infrecuentes los solapamientos y los híbridos.
Las imágenes cerebrales desempeñan un papel diagnóstico crucial junto con la evaluación neurológica clínica. El diagnóstico precoz de las causas vasculares del deterioro cognitivo debería conducir al inicio de medidas terapéuticas o preventivas. La microangiopatía cerebral puede tener un impacto negativo significativo en el curso de la enfermedad de Alzheimer existente. Esto subraya la importancia de un diagnóstico y una terapia precoces.
Los ictus isquémicos son un importante factor de riesgo para la aparición de trastornos cognitivos vasculares. Por lo tanto, el control optimizado de los factores de riesgo preventivos primarios, así como la profilaxis secundaria, son de gran importancia terapéutica también en lo que respecta a la DVa.
PD Nils Peters, MD
Literatura:
- Estrategia Nacional contra la Demencia 2014-2017, Oficina Federal de Salud Pública (FOPH) y Conferencia Suiza de Ministros Cantonales de Sanidad (GDK). Berna, noviembre de 2013.
- Roman GC, Kalaria RN: Neurobiol Aging 2006; 27: 1769-1785.
- Stevens T, et al: Br J Psychiatry 2002; 180: 270-276.
- Heyman A, et al: Neurología 1998; 51: 159-162.
- O’Brien JT, et al: Deterioro cognitivo vascular. Lancet Neurol 2003; 2: 89-98.
- Roman GC: Neuroepidemiología 2003; 22: 161-164.
- Snowdon DA, et al: JAMA 1997; 277: 813-817.
- Roman GC, et al: Neurología 1993; 43: 250-260.
- Hachinski V, et al: Ictus 2006; 37: 2220-2241.
- Peters N, et al: Am J Psychiatry 2005; 162: 2078-2085.
- Peters N, et al: Neurology 2006; 66: 1517-1522.
- Pendlebury ST, Rothwell PM: Lancet Neurol 2009; 8: 1006-1018.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2014; 12(3): 18-21