El carcinoma de células renales es uno de los tumores malignos más frecuentes en adultos. En términos de opciones de tratamiento farmacológico, esta entidad tumoral ha experimentado cambios más rápidos en los últimos años que casi cualquier otra enfermedad maligna. Mientras tanto, la atención se centra no sólo en la terapia dirigida para el carcinoma avanzado de células renales, sino también en los tratamientos combinados.
El cáncer de riñón es el tercer cáncer urológico más frecuente. Cada año, casi 1.000 personas desarrollan en Suiza un tumor renal maligno [1]. La mayoría de los tumores pertenecen histológicamente a los carcinomas renales de células claras, que -dependiendo del subtipo- tienen un pronóstico ligeramente mejor que el cáncer renal de células no claras [2]. En las fases avanzadas, sin embargo, el pronóstico es desfavorable para la mayoría de los afectados: tres cuartas partes de ellos tienen un riesgo de medio a alto de que la enfermedad no se detenga [3]. El panorama del tratamiento del carcinoma metastásico de células renales ha cambiado significativamente debido a las numerosas nuevas aprobaciones. A las terapias dirigidas se unieron los inhibidores del punto de control inmunitario, que ahora también pueden utilizarse en combinación [4].
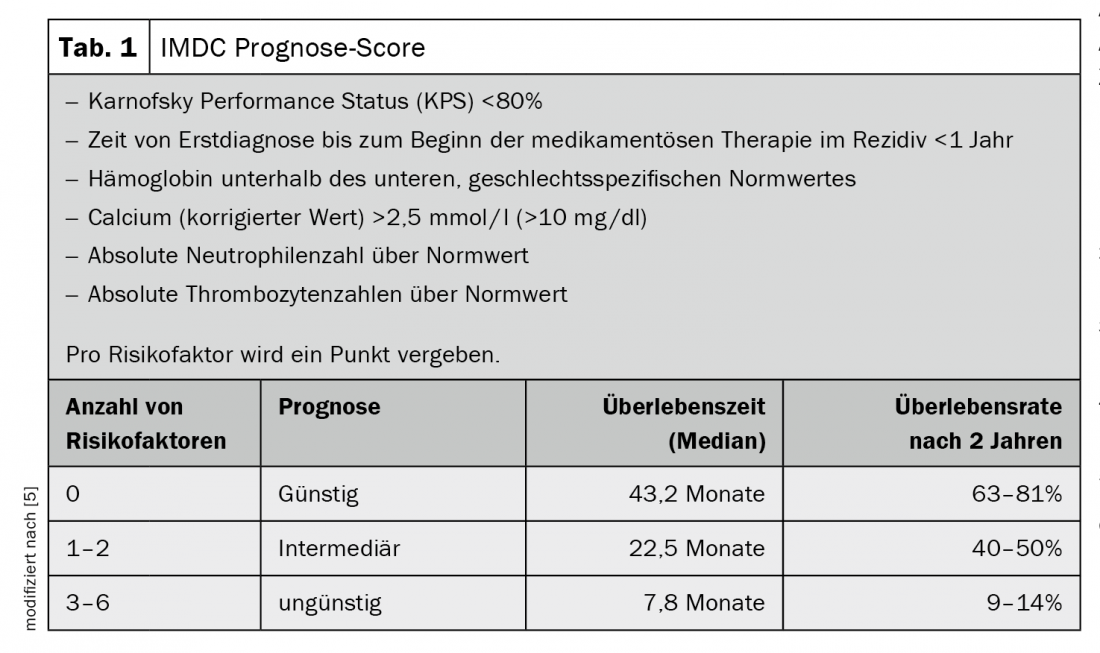
La terapia dirigida con inhibidores de la tirosina quinasa, inhibidores de mTOR o anticuerpos se ha establecido en los últimos años. En particular, la inhibición del VEGFR (receptor del factor de crecimiento endotelial vascular) es la opción estándar para los pacientes con un pronóstico favorable cuyos tumores no han podido ser operados o que han desarrollado metástasis [5]. (Tab. 1). El primer inhibidor del punto de control, dirigido contra la proteína de superficie PD-1, se aprobó entonces como terapia de segunda línea tras el fracaso de una terapia anterior. Recientemente, el bloqueo dual de los puntos de control inmunitarios también se ha podido utilizar antes. Se aprobó la terapia combinada del inhibidor del punto de control nivolumab con el anticuerpo ipilimumab dirigido contra CTLA-4. En comparación con la terapia dirigida, el bloqueo dual de puntos de control muestra ventajas en pacientes con un riesgo basal intermedio o desfavorable. Después de 18 meses, el 75% de los afectados seguían vivos y no se alcanzó la mediana de supervivencia global durante el periodo de observación del estudio. En el 9% de los tratados con inmunoterapia, la enfermedad respondió completamente al tratamiento, lo que significa que el tumor dejó de ser detectable inicialmente tras la terapia [3]. Sin embargo, la posibilidad de una respuesta óptima y una remisión duradera con las nuevas terapias va acompañada de una alta tasa de efectos secundarios. Su tratamiento requiere un equipo de tratamiento interdisciplinar bien coordinado [4].
El futuro: terapias combinadas
Una nueva vía de tratamiento inmuno-oncológico del cáncer renal consiste en combinar las sustancias dirigidas de eficacia probada con los todavía relativamente nuevos inhibidores de los puntos de control. En Estados Unidos ya se ha aprobado el nuevo modo de acción consistente, por ejemplo, en el inhibidor de la tirosina quinasa axitinib con pembrolizumab (anticuerpo anti-PD-1) o axitinib con el también anticuerpo anti-PD-L1 avelumab. En Europa, la aprobación se espera con impaciencia.
Literatura:
- www.krebsliga.ch/ueber-krebs/zahlen-fakten/-dl-/fileadmin/downloads/sheets/zahlen-krebs-in-der-schweiz.pdf (última consulta: 15.30.2020)
- www.krebsinformationsdienst.de/fachkreise/nachrichten/2019/fk17-nierenkrebs-immuntherapie-kombination.php (última consulta: 15.30.2020)
- Motzer RJ, Nizar M, Tannier MD, et al: Nivolumab más ipilimumab frente a sunitinib en el carcinoma avanzado de células renales. N Engl J Med 2018; 378: 1277-1290.
- Zschäbitz S, Ivanyi P, Delecluse S: Revolución en la terapia sistémica del carcinoma metastásico de células renales. El Nefrólogo 2020; 15: 12-19.
- Ivanyi P, Grünwald V: Terapia sistémica del carcinoma de células renales. Oncologist 2019; 25: 517-522.
- Heng DYC, Xie W, Regan MM, et al: Validación externa y comparación con otros modelos del modelo pronóstico del Consorcio Internacional de la Base de Datos del Carcinoma Metastásico de Células Renales: un estudio basado en la población. Lancet Oncol 2013; 14: 141-148.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2020; 8(2): 23