La supervivencia global de los pacientes con leucemia mieloide crónica no puede modificarse optimizando el tratamiento con imatinib. Esto a pesar de que las evaluaciones anteriores pudieron demostrar una influencia en la respuesta.
El imatinib ha revolucionado el tratamiento de la leucemia mieloide crónica (LMC). Como resultado, las tasas de supervivencia han aumentado considerablemente. Los pacientes que responden a los TKI tienen ahora una esperanza de vida casi normal. Por ello, los investigadores estudian ahora si la dosis habitual de 400 mg es adecuada para que todos los pacientes consigan un resultado óptimo. Varios estudios están investigando el beneficio potencial de la terapia con imatinib modificado. Los enfoques con dosis altas (800 mg) o dosis adaptadas de imatinib (o también la combinación con interferón) pueden efectivamente cambiar la respuesta en comparación con la variante estándar, como Hehlmann y sus colegas han demostrado previamente [2,4] (aunque contradiciendo en parte otros estudios aleatorizados [3]). Pero, ¿se traduce este beneficio en una mejor supervivencia, es decir, más prolongada, a largo plazo? Entonces, ¿se pueden conseguir en última instancia tasas de supervivencia más elevadas con diferentes optimizaciones de la terapia?
El estudio CML IV
Entre otras cosas, esta cuestión se investigó en el gran ensayo aleatorizado CML IV, con participación suiza. El objetivo era investigar hasta qué punto puede optimizarse la terapia estándar con 400 mg/d de imatinib. Para ello, 1551 pacientes recién diagnosticados en fase crónica fueron distribuidos aleatoriamente en cinco brazos. Dos brazos, concretamente los que probaban el imatinib en combinación con citarabina o tras el fracaso del interferón, se cerraron al reclutamiento de más pacientes tras una fase piloto. Las tres restantes consistían en la dosis estándar de 400 mg/d, la terapia de dosis alta de 800 mg/d y la combinación de imatinib con interferón. La edad media de los pacientes era de 53 años y el 61% eran varones.
En el congreso de la EHA celebrado en Madrid se debatieron los datos de supervivencia a largo plazo, más concretamente la supervivencia global tras un periodo medio de observación de 9,5 años. Fue del 82% en todos los grupos (supervivencia sin progresión del 80%).
Supervivencia tras una década
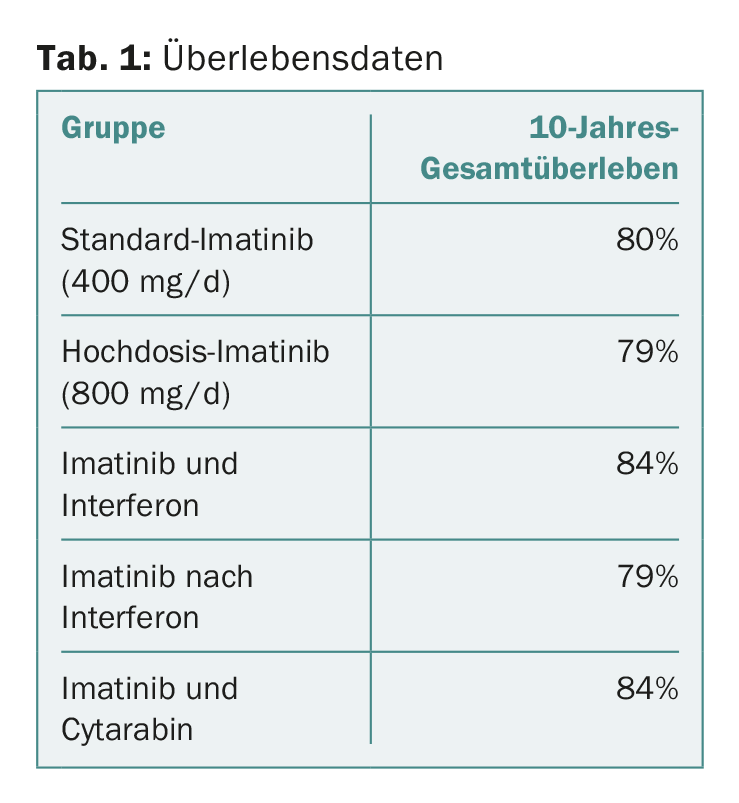
Los detalles de cada grupo se muestran en la tabla 1. Los resultados muestran que no hubo diferencias significativas entre los distintos enfoques u optimizaciones del tratamiento. Esto es así a pesar de que se consiguió una respuesta más rápida con la terapia de dosis altas, como ya demostraron publicaciones anteriores [2]. Sin embargo, lo que sí influyó en la supervivencia a largo plazo fue la consecución de los valores objetivo (“hitos”) en la respuesta molecular a los tres, seis y doce meses, también en consonancia con los datos publicados anteriormente del estudio [2,4]. En el análisis multivariante, las comorbilidades y el hábito de fumar también resultaron ser factores relevantes que influían en la supervivencia. El hecho de que el centro de tratamiento fuera académico o no también desempeñó un papel importante, pero no así el sexo del paciente.
¿Se ha llegado al final de la línea?
La LMC IV ha demostrado en consecuencia: Las tasas de supervivencia de los pacientes con LMC en tratamiento con imatinib son elevadas y no están necesariamente influidas por un régimen de tratamiento inicial con una respuesta más rápida, sino más bien por factores externos como el tabaquismo, el tipo de centro de tratamiento y las comorbilidades del paciente.
El riesgo de morir al cabo de diez años por parámetros independientes de la LMC en lugar de por la propia enfermedad fue significativamente mayor para los participantes, concretamente el doble, en definitiva un efecto esperable con fármacos de buena acción [5]. Además, la denominada puntuación “European Treatment and Outcome Study” (EUTOS) sobre la supervivencia a largo plazo, que evalúa el riesgo de mortalidad asociado a la LMC, también fue un predictor significativo del pronóstico: los grupos con un riesgo alto sobrevivieron menos tiempo que los de riesgo bajo.
Así que, por un lado, la supervivencia es independiente del tiempo hasta la respuesta (al menos en este estudio y entorno de tratamiento o periodo de observación). Por lo tanto, la terapia con dosis altas no provocó una diferencia significativa. Por el contrario, el tiempo hasta la respuesta no es un marcador sustitutivo adecuado para la supervivencia global. Por otro lado, no hay que olvidar que la consecución de los valores objetivo en la respuesta molecular en determinados momentos desempeñó sin duda un papel en el pronóstico, como era de esperar. Los pacientes con BCR-ABLIS <1% a los seis meses tenían una supervivencia a 5 años del 97% frente al 89% con BCR-ABLIS >1% (p<0,001) [6].
¿Es la supervivencia global un indicador adecuado del éxito de una terapia?
Así pues, la presentación de la EHA le deja a uno un tanto perplejo. Aunque más pacientes logran una respuesta (más rápida) con la dosis más alta y esto se asocia a una mejor supervivencia global, las diferencias entre las variantes de dosis no parecen tener un efecto significativo a largo plazo: Todos viven el mismo tiempo, independientemente del régimen de imatinib que hayan recibido. Otros factores no relacionados directamente con la LMC cobran importancia: ¿Está el paciente sano por lo demás? ¿Fuma?
También se puede formular todo al revés: La supervivencia global puede no ser adecuada para evaluar el éxito a largo plazo de tratamientos específicos de la LMC [5]. Si nos guiáramos sólo por esto, el final de la línea se alcanzaría con el imatinib en la dosis estándar.
Por supuesto, los criterios de valoración como lograr una respuesta profunda para poder incluso suspender el TKI (véase el estudio EURO-SKI [7] con actualización en el congreso de la EHA del año pasado [8]), o la protección frente a la progresión también desempeñan un papel central para los pacientes con LMC y no deben olvidarse en este contexto.
Fuente: Congreso 2017 de la Asociación Europea de Hematología (EHA), 22-25 de junio de 2017, Madrid.
Literatura:
- Hehlmann R, et al: Assessment Of Imatinib 400mg As First Line Treatment Of Chronic Myeloid Leukemia: 10 -Year Survival Results Of The Randomized Cml Study IV. EHA 2017; Resumen S424.
- Hehlmann R, et al: Deep Molecular Response Is Reached by the Majority of Patients Treated With Imatinib, Predicts Survival, and Is Achieved More Quickly by Optimized High-Dose Imatinib: Results From the Randomized CML-Study IV. Revista de Oncología Clínica 2014; 32(5): 415-423.
- JE Cortes, et al.: Estudio de fase III, aleatorizado y abierto de 400 mg diarios de mesilato de imatinib frente a 800 mg en pacientes con leucemia mieloide crónica en fase crónica recién diagnosticada y no tratada previamente, utilizando puntos finales moleculares: Estudio de optimización y selectividad de inhibidores de tirosina cinasa. J Clin Oncol 2010; 28: 424-430.
- Hehlmann R, et al: Imatinib adaptado a la tolerancia 800 mg/d frente a 400 mg/d frente a 400 mg/d más interferón-α en la leucemia mieloide crónica recién diagnosticada. Revista de Oncología Clínica 2011; 29(12): 1634-1642.
- Saussele S, et al.: Impacto de las comorbilidades en la supervivencia global en pacientes con leucemia mieloide crónica: resultados del estudio aleatorizado CML IV. Sangre 2015; 126(1): 42-49.
- Hanfstein B, et al.: La respuesta molecular y citogenética temprana es predictiva de la supervivencia global y libre de progresión a largo plazo en la leucemia mieloide crónica (LMC). Leucemia 2012; 26(9): 2096-2102.
- Mahon FX, et al: Análisis provisional de un ensayo paneuropeo de inhibidores de la tirosina cinasa de parada en la leucemia mieloide crónica: el estudio EURO-SKI. Sangre 2014; 124: 151.
- Richter J, et al: Suspensión de los inhibidores de la tirosina quinasa en una cohorte muy amplia de pacientes europeos con leucemia mieloide crónica: resultados del ensayo EURO-SKI. EHA 2016; Resumen S145.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2017; 5(4): 7-8