Las actuales directrices europeas para el tratamiento de la insuficiencia cardiaca recomiendan el uso de puntuaciones de riesgo. Entre ellas, la puntuación MECKI (Datos de la prueba de esfuerzo metabólico combinados con índices cardíacos y renales) ha demostrado ser una de las más precisas. Sin embargo, las puntuaciones de riesgo no se utilizan lo suficiente en la práctica clínica, en parte porque faltan pruebas significativas para su validación externa en diferentes poblaciones.
La insuficiencia cardiaca (IC) es un importante problema de salud pública con una prevalencia actual de más de 23 millones de personas en todo el mundo [2]. A pesar de los grandes avances en la terapia con fármacos y dispositivos, el pronóstico sigue siendo malo. En la cohorte del condado de Olmsted para todos los tipos de pacientes con IC, las tasas de mortalidad a 1 y 5 años entre 2000 y 2010 fueron del 20% y el 53%, respectivamente [3]. En un estudio que combinaba cohortes del Framingham Heart Study y del Cardiovascular Health Study, se halló una tasa de mortalidad del 67% en los cinco años siguientes al diagnóstico [4].
Como consecuencia, está aumentando el número de pacientes con IC que llegan a la fase terminal y requieren asistencia circulatoria mecánica avanzada y/o un trasplante de corazón (TxC), lo que choca con el número limitado de órganos disponibles y una tasa de mortalidad a un año del 20% mientras se está en lista de espera [5]. Las autoridades sanitarias han desarrollado estrategias de priorización destinadas a reducir la creciente discrepancia entre el número de órganos disponibles y los posibles receptores. Decidir qué candidatos son aptos para el THx será aún más frecuente y difícil para el médico implicado en la IC. Esto es especialmente cierto en el caso de los pacientes ambulatorios no inotrópicos, ya que evitar retrasos en el ingreso de pacientes de mayor riesgo debe sopesarse cuidadosamente frente al aplazamiento de pacientes menos enfermos. Por lo tanto, es importante determinar correctamente el pronóstico de los pacientes con IC.
En las últimas tres décadas se han desarrollado una serie de puntuaciones que combinan diversas variables para ayudar al clínico a evaluar el pronóstico del paciente. En 2013, un grupo de trabajo italiano propuso la puntuación MECKI para evaluar el riesgo de mortalidad cardiovascular (CV) y de HTx urgente. Se basa en seis variables: Hemoglobina (Hb), sodio (Na+), función renal mediante la ecuación de la Modificación de la Dieta en la Enfermedad Renal (MDRD), fracción de eyección del ventrículo izquierdo (FEVI) por ecocardiografía, porcentaje del consumo máximo de oxígeno previsto (ppVO2) y pendiente de la ventilación minuto y la producción de dióxido de carbono (VE/VCO2). Las variables anteriores son marcadores pronósticos reconocidos en la IC, que reflejan la complejidad y la afectación multiorgánica de este síndrome: Se determinaron tras análisis multivariantes en grandes poblaciones [6,7].
En comparaciones recientes, la puntuación MECKI mostró un buen poder discriminatorio, superior al de otras puntuaciones utilizadas habitualmente, como la puntuación de supervivencia a la insuficiencia cardiaca (HFSS), el modelo de insuficiencia cardiaca de Seattle (SHFM) y el metaanálisis del Grupo Global en Insuficiencia Cardiaca Crónica (MAGGIC) [8,9]. Otro estudio [10] demostró que la puntuación MECKI también puede utilizarse con la ventaja de que está muy bien calibrada a intervalos de 1 año, lo que permite evitar los escollos de subestimar o sobrestimar el riesgo. Sin embargo, pocas de estas puntuaciones de riesgo se utilizan en la práctica clínica, en parte porque faltan pruebas sólidas que respalden su validación externa en diferentes poblaciones [11]. Por lo tanto, el presente estudio se diseñó como una prueba de validación externa de la puntuación MECKI en un entorno multicéntrico internacional [1].
Población del estudio
Se incluyeron en el estudio 1042 pacientes de ocho centros internacionales (siete europeos y uno asiático). Los criterios de inclusión fueron (i) Síntomas previos o actuales de IC, (ii) Antecedentes de disfunción sistólica ventricular izquierda reducida (FEVI ≤45%), (iii) un estado clínico estable sin cambios en la medicación en los últimos tres meses, (iv) ningún tratamiento o intervención cardiovascular importante previsto; y (v) Realización de una prueba de esfuerzo cardiopulmonar (CPET) máxima, independientemente de la relación de intercambio respiratorio, lograda con un protocolo de carga en rampa (pasos no superiores a un minuto) en la cinta rodante o el cicloergómetro con mediciones continuas de los gases respiratorios y la ventilación. Los criterios de exclusión fueron antecedentes de embolia pulmonar, cardiopatía valvular significativa, enfermedad pulmonar obstructiva grave, angina de pecho inducida por el ejercicio y cambios significativos en el ECG o la presencia de una comorbilidad clínica que merme la capacidad de ejercicio.
Del total de 1042 pacientes, se excluyeron 155 pacientes con una FEVI >45%. De los 887 pacientes elegibles restantes, 43 pacientes fueron excluidos debido a que faltaban variables de la puntuación MECKI, por lo que finalmente se incluyeron en el estudio 844 pacientes.
Por término medio, la muestra del presente estudio estaba formada por una población más joven, con una distribución por sexos comparable, una FEVI y una VO2 máxima inferiores (pero una ppVO2 superior) y una pendiente VE/VCO2 superior. El tratamiento farmacológico también fue diferente: más pacientes recibieron antagonistas de los receptores de mineralocorticoides y menos recibieron digoxina.
Seguimiento de los pacientes y resultados
Se realizó un seguimiento de los pacientes desde 1998 hasta 2019. El seguimiento de los pacientes se realizó según los programas de IC aplicados en cada centro. Los criterios de valoración fueron la mortalidad cardiovascular, la HTx urgente o la implantación de un dispositivo de asistencia ventricular (DAV). Los pacientes se consideraron censurados en el momento del acontecimiento final según los métodos del estudio original [4,5].
Datos de la prueba de esfuerzo metabólico combinados con subgrupos de puntuación del índice cardíaco y renal
Los pacientes se dividieron en tres subgrupos en función de las puntuaciones MECKI calculadas: Puntuación MECKI <10%, 10-20% y ≥20%. El deterioro progresivo de los parámetros clínicos, como una mayor clase funcional de la Asociación Cardiaca de Nueva York (NYHA), fibrilación auricular y pendiente VE/VCO2, y una menor FEVI, VO2 pico y TFGe, se asoció con el aumento de los valores de la puntuación MECKI.
Análisis de la tasa de supervivencia
Hubo 263 acontecimientos en total: 234 se debieron a causas cardiovasculares (89%: 101 muertes, 58 HTx urgentes y 75 implantes de DAV) y 29 a causas no cardiovasculares (11%), siendo estas últimas censuradas en el momento del acontecimiento.
Los criterios de valoración del estudio se registraron en 63 (7,5%), 95 (11,3%) y 122 (14,6%) pacientes al año, a los dos años y a los tres años, respectivamente: Se produjo muerte CV en 12 (1,4%), 19 (2,3%) y 30 (3,6%); HTx en 24 (2,8%), 37 (4,4%) y 43 (5,1%); e implantación de DAV en 27 (3,2%), 39 (4,6%) y 49 (5,8%) al año, dos y tres años, respectivamente. La mediana del tiempo de supervivencia sin eventos de toda la muestra fue de 4168 días (11,4 años).
La comparación del análisis de supervivencia entre los tres subgrupos de puntuación MECKI mostró un peor pronóstico en los pacientes con una puntuación MECKI más alta: la mediana de supervivencia libre de acontecimientos fue de 4396 días (12 años) para una puntuación MECKI <10%, de 3457 días (9,5 años) para una puntuación MECKI 10-20% y de 1022 días (2,8 años) para una puntuación MECKI ≥20% (p<0,0001).
Análisis de las características operativas del receptor
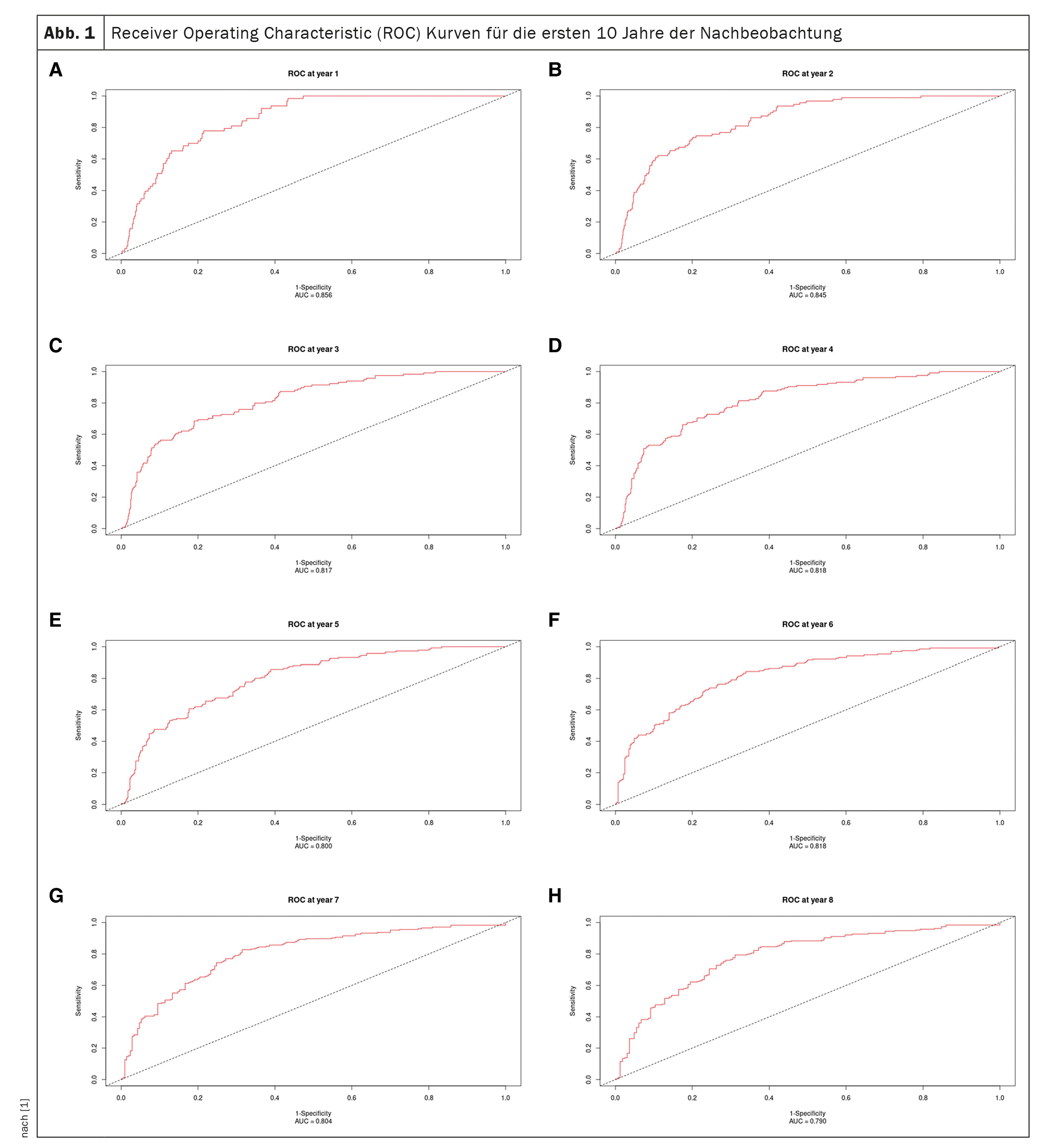
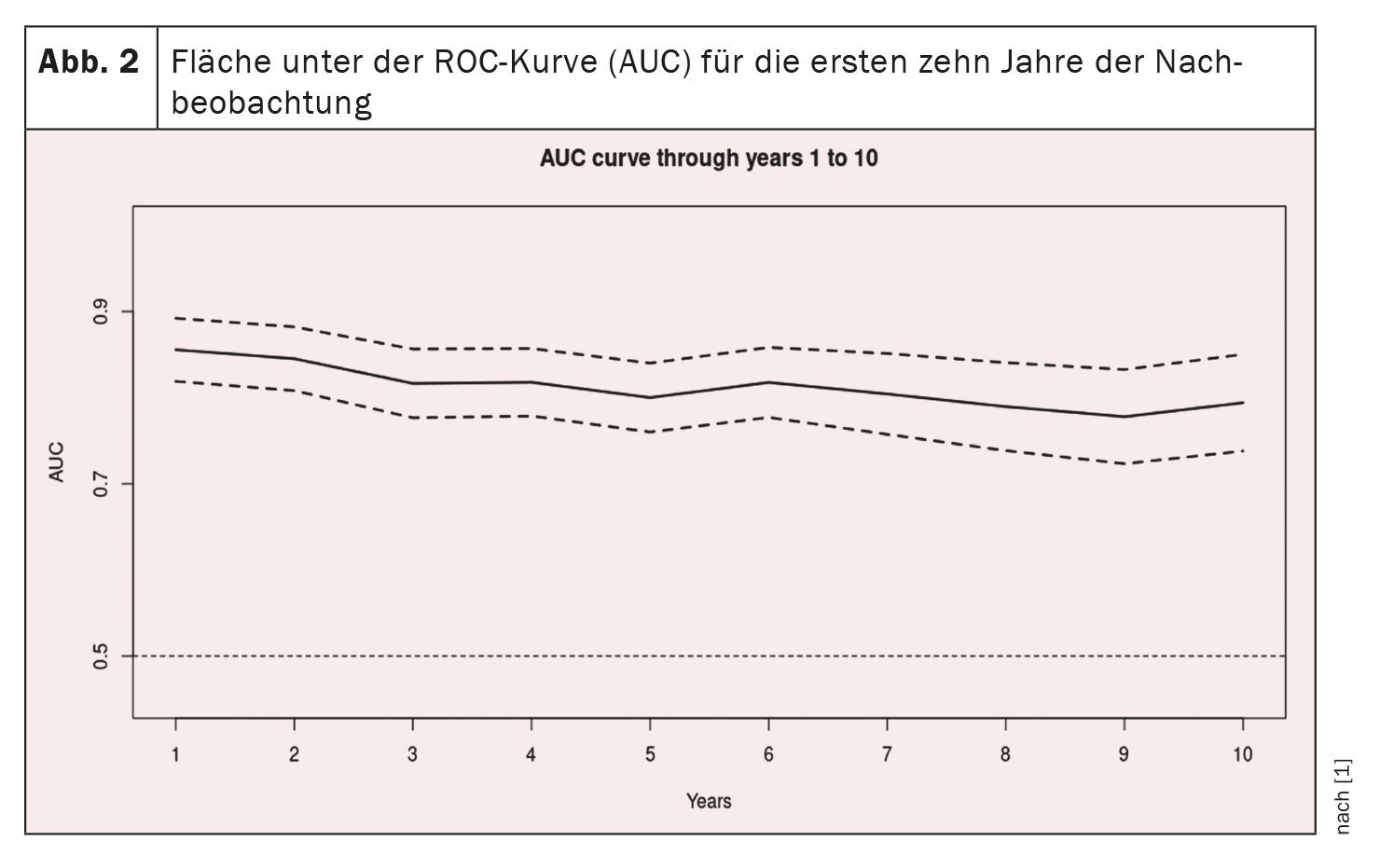
Las curvas receiver operating characteristic de los 10 primeros años de seguimiento se muestran en la figura 1 [1] y la curva AUC en lafigura 2 [1]: La AUC se mantiene en >0,77 para el periodo de 10 años, pero con intervalos de confianza que aumentan progresivamente. Los valores de AUC son similares, si no mejores, que en el estudio original (0,80 ± 0,02, 0,79 ± 0,01 y 0,76 ± 0,01 después de uno, dos y tres años, respectivamente) y en el estudio de validación (0,81 ± 0,04, 0,76 ± 0,04 y 0,80 ± 0,03 después de uno, dos y tres años, respectivamente). [12].
La validación interna y temporal muestra buenos resultados en cuanto a la capacidad de predicción
La estratificación pronóstica en pacientes con IC es esencial para guiar la terapia farmacológica y la implantación de dispositivos. También es una herramienta muy útil para orientar la selección de un HTx. En el pasado, las únicas puntuaciones recomendadas en este contexto eran la SHFM y la HFSS [13]. La sobreestimación y subestimación del riesgo (especialmente en los grupos de mayor riesgo) demostrada recientemente con las puntuaciones anteriores puede tener un impacto significativo en las decisiones de tratamiento, como la selección del THx. En pacientes diagnosticados de IC-FEr, se confirmó que la puntuación MECKI es informativa en términos de pronóstico y estratificación del riesgo, por lo que se apoya su uso tal y como recomiendan las directrices sobre IC.
Mensajes para llevarse a casa
- Los pacientes diagnosticados de insuficiencia cardiaca con fracción de eyección reducida se sometieron a una validación externa de la puntuación de riesgo MECKI (Datos de la prueba de esfuerzo metabólico combinados con índices cardiacos y renales) .
- El poder pronóstico de la puntuación MECKI se confirmó en una amplia población de pacientes de Europa y Asia.
- Estos datos apoyan la introducción de la puntuación MECKI tal y como recomiendan las directrices europeas sobre insuficiencia cardiaca de 2021.
Literatura:
- Adamopoulos S, et al: Validación internacional de la puntuación de la prueba de esfuerzo metabólico combinada con índices cardíacos y renales (MECKI) en la insuficiencia cardíaca. Eur J Prev Cardiol 2023; doi: 10.1093/eurjpc/zwad191.
- Bragazzi NL, et al: Carga de la insuficiencia cardiaca y causas subyacentes en 195 países y territorios de 1990 a 2017. Eur J Prev Cardiol 2021; 28: 1682-1690.
- Gerber Y, et al: Una valoración contemporánea de la epidemia de insuficiencia cardiaca en el condado de Olmsted, Minnesota, 2000 a 2010. JAMA Intern Med 2015; 175: 996-1004.
- Tsao CW, et al: Tendencias temporales en la incidencia y la mortalidad asociadas a la insuficiencia cardíaca con fracción de eyección preservada y reducida. JACC Heart Fail 2018; 6: 678-685.
- Khush KK, et al: Registro Internacional de Trasplante de Órganos Torácicos de la Sociedad Internacional de Trasplante de Corazón y Pulmón: trigésimo sexto informe de trasplante cardíaco en adultos – 2019; tema central: coincidencia de tamaño de donante y receptor. J Heart Lung Transplant 2019; 38: 1056-1066.
- Salvioni E, et al: La iniciativa de puntuación MECKI: desarrollo y estado de la cuestión. Eur J Prev Cardiol 2020; 27: 5-11.
- Agostoni P, et al: Datos de la prueba de esfuerzo metabólico combinados con índices cardíacos y renales, la puntuación MECKI: un enfoque multiparamétrico del pronóstico de la insuficiencia cardíaca. Int J Cardiol 2013; 167: 2710-2718.
- Agostoni P, et al: Puntuaciones pronósticas multiparamétricas en la insuficiencia cardiaca crónica con fracción de eyección reducida: una comparación a largo plazo. Eur J Heart Fail 2018; 20: 700-710.
- Kouwert IJM, et al.: Comparación de las puntuaciones de riesgo MAGGIC y MECKI para predecir la mortalidad tras la rehabilitación cardiaca entre pacientes holandeses con insuficiencia cardiaca. Eur J Prev Cardiol 2020; 27: 2126-2130.
- Freitas P, et al: Análisis comparativo de cuatro puntuaciones para estratificar a los pacientes con insuficiencia cardiaca y fracción de eyección reducida. Am J Cardiol 2017; 120: 443-449.
- Altman DG, et al: Pronóstico e investigación pronóstica: validación de un modelo pronóstico. BMJ 2009; 338:b605.
- Corra U, et al.: Los datos de la prueba de esfuerzo metabólico combinados con la puntuación de los índices cardíaco y renal (MECKI) y el pronóstico en la insuficiencia cardíaca. Un estudio de validación. Int J Cardiol 2016; 203: 1067-1072.
- Mehra MR, et al: The 2016 International Society for Heart Lung Transplantation listing criteria for heart transplantation: a 10-year update. J Heart Lung Transplant 2016; 35: 1-23.
CARDIOVASC 2023; 22(3): 20-22