El síndrome del intestino irritable es una de las disfunciones gastrointestinales más comunes y afecta significativamente a la calidad de vida de los afectados. Cabe suponer que diversos aspectos somáticos, psicológicos y sociales también intervienen en la fisiopatología de la enfermedad. En consecuencia, está indicado un concepto de tratamiento multimodal.
El síndrome del intestino irritable (SII) es un trastorno funcional del aparato digestivo inferior [1] con una prevalencia mundial estimada de alrededor del 11% [2] y una incidencia estimada de alrededor del 1,5% [3], siendo el trastorno más común en mujeres que en hombres [4]. Con una prevalencia del 5-10% en Alemania [2], el SII es una de las disfunciones gastrointestinales más comunes [5]. El SII conlleva un deterioro considerable de la calidad de vida de los afectados [6] y también provoca grandes costes directos (por ejemplo, visitas al médico, medicación, diagnósticos, estancias en el hospital, etc.), así como costes indirectos (en particular a través del absentismo laboral y la reducción de la productividad durante el trabajo) [7]. Este artículo de revisión aprovecha la revisión de la directriz S3 para el SII [7], que se publicará en Alemania en 2021, para presentar las recomendaciones de actuación actuales en relación con el diagnóstico y la terapia del SII. Esta directriz se ha elaborado en colaboración con las sociedades profesionales pertinentes de Alemania, pero también con la participación de la Sociedad Suiza de Neurogastroenterología y Motilidad, y también es válida en Suiza.
Según la directriz actualizada [7], existe SII cuando se cumplen los tres criterios siguientes:
- Molestias crónicas, es decir, que duran más de tres meses o son recurrentes, relacionadas con el intestino (por ejemplo, dolor abdominal, flatulencia), normalmente acompañadas de cambios en las deposiciones;
- las quejas llevan a la persona afectada a buscar ayuda y/o a preocuparse al respecto y las quejas son tan graves que la calidad de vida se ve afectada de forma relevante;
- no hay cambios característicos de otros cuadros clínicos que sean responsables de los síntomas presentes.
Desde el punto de vista pronóstico, los síntomas del SII se resuelven espontáneamente en algunos pacientes, pero suelen ser crónicos, y el SII no parece estar asociado al desarrollo de otras enfermedades gastrointestinales u otras enfermedades graves y no aumenta la mortalidad [8]. Sin embargo, se ha demostrado una elevada comorbilidad con las enfermedades mentales [9]. Debido a la falta de cura, el tratamiento del SII se dirige principalmente a aliviar los síntomas [10]. Las medidas terapéuticas a este respecto con el trasfondo del modelo biopsicosocial son el tema de este artículo.
Nota: El síndrome del intestino irritable es un trastorno funcional del aparato digestivo inferior que se asocia, entre otras cosas, con molestias persistentes, es decir, que duran más de tres meses o son recurrentes, relacionadas con el intestino, como dolor abdominal, flatulencia y cambios en los movimientos intestinales, y que reduce la calidad de vida de los afectados.
en una medida significativa.
Patogénesis
Basándose en un modelo biopsicosocial, cabe suponer que en la fisiopatología del SII intervienen diversos aspectos somáticos (por ejemplo, la [Epi]-genética, las infecciones), psicológicos (por ejemplo, el estrés crónico, el comportamiento ante la enfermedad) y sociales (por ejemplo, el estatus socioeconómico) [11]. Mientras tanto, se han identificado numerosos cambios biológicos asociados a los síntomas del SII [1,10]. Las anomalías más comunes examinadas incluyen, por ejemplo, trastornos de la motilidad, una respuesta inmunitaria entérica alterada y funciones de la mucosa alteradas, que se manifiestan en una barrera intestinal y una secreción perturbadas, así como hipersensibilidad visceral. En cuanto a la hipersensibilidad visceral, podría detectarse a nivel neurológico un procesamiento alterado de las señales en las regiones cerebrales responsables del procesamiento emocional o sensoriomotor de las señales viscerales [12]. Este hallazgo puede proporcionar una explicación plausible de la asociación entre el SII y los factores psicológicos, y también subraya la importancia del eje intestino-cerebro en la fisiopatología del SII [13].
En el sentido de dicha implicación del eje intestino-cerebro, parece detectarse una menor activación parasimpática especialmente en pacientes con SII con diarrea predominante (SII-D), por lo que esta menor activación podría a su vez estar relacionada con la extensión de la dolencia, las experiencias de maltrato y los síntomas de depresión [14]. Un gran número de estudios también muestran una sobreactivación simpática en pacientes con SII [15], que a su vez parece estar asociada a un aumento de los niveles de estrés [16]. Además, en el contexto de un eje intestino-cerebro alterado, los pacientes con SII muestran cambios inducidos por el estrés en la motilidad gastrointestinal, el tono autonómico y la respuesta del eje HPA, entre otros [17].
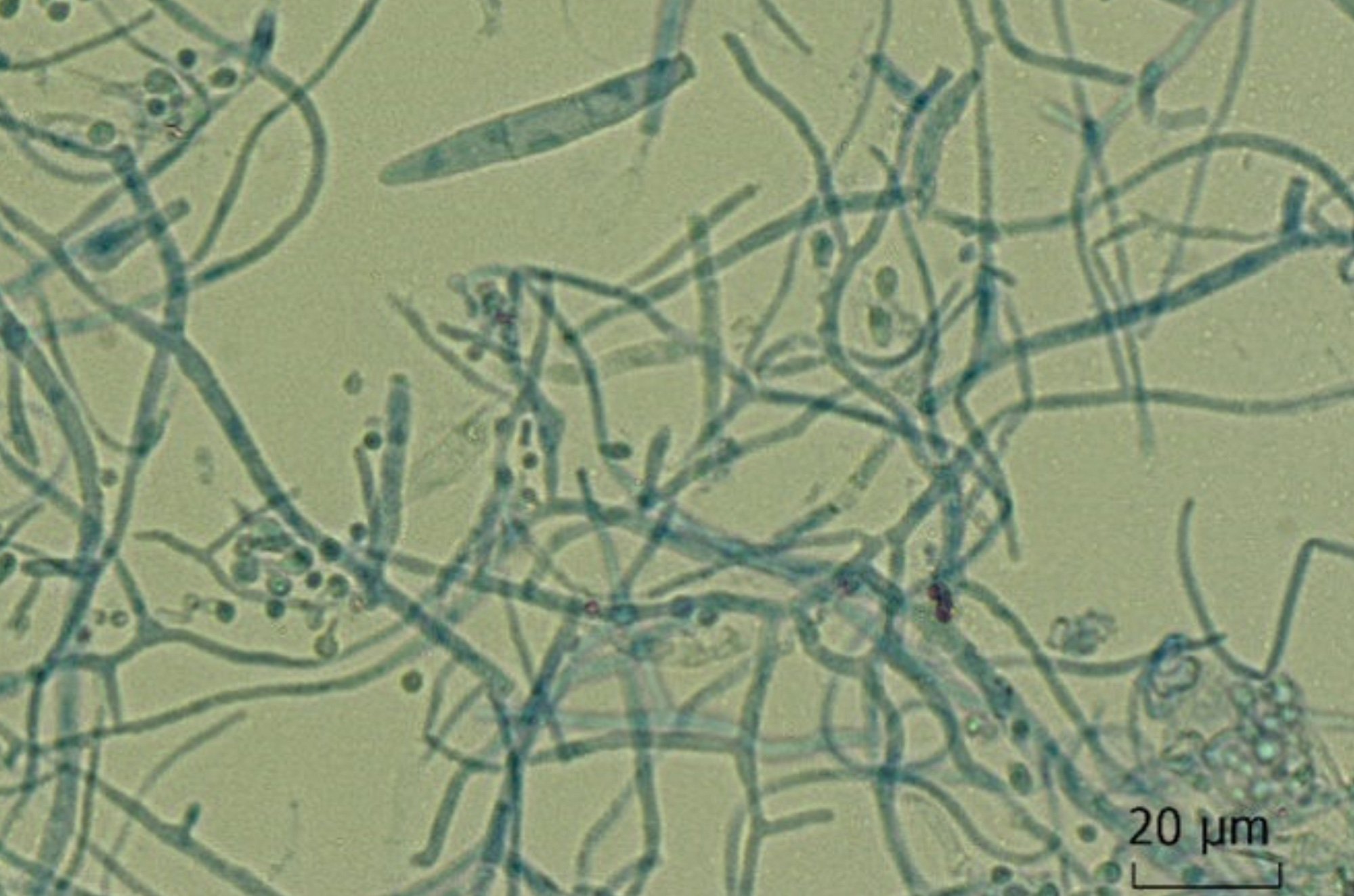
Recientemente, también se ha estudiado con más detalle la influencia del microbioma en el eje intestino-cerebro en relación con el desarrollo y el mantenimiento del SII [18]. Se han encontrado cambios tanto en la cantidad como en la calidad del total de bacterias intestinales en pacientes con SII [18], por lo que el estrés y la flora bacteriana intestinal interactúan a su vez entre sí y pueden influir, por ejemplo, en la percepción del dolor visceral de los pacientes con SII [19]. Los cambios en el microbioma de los pacientes con SII también podrían ofrecer una explicación de los efectos de las infecciones y la terapia antibiótica en el desarrollo del SII.
En cuanto a las predisposiciones genéticas, se ha descubierto que el SII es hereditario, a veces a lo largo de varias generaciones: la probabilidad de desarrollar SII en un familiar de alguien que lo padezca es aproximadamente dos o tres veces mayor [20]. Los resultados de los estudios iniciales también sugieren que los factores epigenéticos pueden estar implicados en la génesis del SII [21].
En el SII está muy bien documentada una elevada comorbilidad con trastornos afectivos, especialmente trastornos de ansiedad y depresivos [22]. El estrés crónico y las comorbilidades psicológicas se consideran factores de riesgo para el desarrollo y el mantenimiento del SII [23]. Por ejemplo, se ha demostrado que el aumento de los síntomas de ansiedad y depresión [24] y la reducción de la calidad de vida [25] son factores predictivos de la manifestación inicial del SII. Además, la prevalencia de acontecimientos vitales estresantes en el pasado (por ejemplo, experiencias de abuso o traumas infantiles) es mayor en comparación con las personas sanas [26]. Además, se ha demostrado que la ansiedad y los síntomas depresivos registrados psicométricamente se correlacionan positivamente con el grado de dolor [27] y pueden tener un efecto negativo sobre la sensación de plenitud y la hinchazón [28]. Sin embargo, la ansiedad y los trastornos depresivos también pueden desarrollarse de forma secundaria como resultado del estrés de los síntomas gastrointestinales crónicos [24]. Además, los aspectos del afrontamiento de la enfermedad o las estrategias de afrontamiento del estrés y los síntomas (especialmente la catastrofización), así como el comportamiento de enfermedad aprendido a través del entorno social (por ejemplo, la interpretación de las percepciones corporales como “síntomas problemáticos”, el comportamiento de evitación desadaptativo, etc.) parecen desempeñar un papel importante en el desarrollo y el mantenimiento del SII [29–31]. La influencia de los rasgos de personalidad también se tiene en cuenta en algunos estudios: por ejemplo, la escala de personalidad neuroticismo, en particular, parece desempeñar un papel y debería investigarse más a fondo en cuanto a la vulnerabilidad para desarrollar el SDR .
En resumen, en el contexto de un modelo biopsicosocial, los complejos procesos de interacción entre el estrés, la comorbilidad psicológica y los síntomas gastrointestinales en el sentido de un círculo vicioso parecen evidentes en la patogénesis del SII [32].
Nota: El modelo biopsicosocial tiene en cuenta diversos factores somáticos y psicosociales dentro de la fisiopatología del SII e integra sus polifacéticos procesos de interacción. Mientras tanto, se han identificado numerosos cambios biológicos asociados a los síntomas del SII. Una explicación plausible de la asociación entre el SII y los factores psicológicos la ofrece sobre todo el eje intestino-cerebro. Aquí parecen evidentes los complejos procesos de interacción entre el estrés, la comorbilidad psicológica y los síntomas gastrointestinales en el sentido de un círculo vicioso.
Terapia
En correspondencia con un cuadro clínico muy heterogéneo en cuanto a la patogénesis, la manifestación de los síntomas y las deficiencias resultantes en la vida cotidiana, existe también un espectro muy amplio de principios de tratamiento potencialmente eficaces en el contexto del modelo biopsicosocial de la enfermedad (Fig. 1). Como resultado de esta heterogeneidad, no es posible nombrar “la” terapia estándar para el SII, sino que cada intervención terapéutica tiene inicialmente un carácter de ensayo. Según la directriz S3, deben considerarse las combinaciones de diferentes sustancias medicinales, así como las combinaciones de tratamientos medicinales y no medicinales, si sólo hay una respuesta parcial a la monoterapia y/o para el tratamiento de diversas molestias sintomáticas [7]. Estos componentes del tratamiento se analizan con más detalle a continuación.
Estilo de vida: Los datos actuales sobre recomendaciones basadas en pruebas para cambios favorables en el estilo de vida (por ejemplo, no fumar, beber poco alcohol, comer de forma consciente, hacer suficiente ejercicio, dormir lo suficiente, reducir el estrés, etc.) son actualmente escasos y (a pesar de algunas observaciones positivas) siguen siendo contradictorios [33]. No obstante, existen pocos estudios de alta calidad que demuestren que el ejercicio físico en particular puede tener un efecto positivo sobre los síntomas del SII durante un periodo de doce semanas (posiblemente también a largo plazo) [34,35].
Nota: Según la directriz S3 actualizada, los conceptos de tratamiento integrador y multimodal deben utilizarse en el tratamiento del SII si sólo hay una respuesta parcial a la monoterapia y/o para el tratamiento de diferentes tipos de síntomas.
Nutrición/dieta: Según la directriz S3, las medidas de medicina nutricional/terapia nutricional son un componente sensato de un concepto terapéutico para pacientes con SII [7]. Por ejemplo, los pacientes con SII con síntomas predominantemente obstructivos (SII-O) pudieron conseguir mejoras de los síntomas como resultado de un aumento de la ingesta de fibra alimentaria (preferiblemente de naturaleza soluble) . Si el dolor, la flatulencia y la diarrea son los síntomas dominantes, debe recomendarse una dieta denominada baja en FODMAP . En este caso, primero deben evitarse los oligo-, di- y monosacáridos y polioles fermentables (FODMAP) en la ingesta de alimentos bajo asesoramiento médico nutricional de acompañamiento (fase de eliminación). Los FODMAP son hidratos de carbono de cadena corta que se absorben mal en el intestino delgado. A más tardar en el intestino grueso, se vuelven entonces osmóticamente activas y se fermentan rápidamente, por lo que pueden aparecer dolores abdominales, flatulencias y heces blandas y voluminosas. Una vez que los síntomas mejoran como resultado de la fase de eliminación, los alimentos con mayor contenido en FODMAP pueden reintroducirse gradualmente [37]. Según este esquema, es posible averiguar qué alimentos desencadenan o empeoran los síntomas y cuáles se toleran (fase de hallazgo de la tolerancia). Todos los alimentos que podrían consumirse sin síntomas se incluyen posteriormente en el plan de nutrición a largo plazo (fase de nutrición a largo plazo). Varios estudios han demostrado una mejora de los síntomas del SII cuando se restringen los FODMAP [38].
Nota: El ejercicio físico puede tener tienen un efecto positivo sobre los síntomas del SII.
Medicación orientada a los síntomas: La farmacoterapia del SII debe estar siempre orientada a los síntomas y tener en cuenta los síntomas dominantes [7]. Para el tratamiento del SII-D, la directriz recomienda la medicación con el inhibidor peristáltico loperamida (agonista de los receptores µ-opioides). A pesar de las buenas pruebas de eficacia, según la directriz actualizada, el agente opiáceo eluxadoline sólo debe considerarse en casos individuales seleccionados de SII-D por lo demás refractario, ya que su uso parece estar asociado, entre otras cosas, a la pancreatitis aguda, y no debe utilizarse en particular en pacientes tras una colecistectomía, con enfermedad de las vías biliares, alcoholismo, cirrosis hepática y disfunción del esfínter-Oddi. El inhibidor de la absorción del colesterol, la colestiramina, debe utilizarse para tratar la diarrea colagenosa. El colesevelam también puede utilizarse en el mismo contexto fisiopatológico. Además, en casos de SII-D por lo demás refractario, debe probarse la terapia fuera de indicación con antagonistas 5-HT3 (por ejemplo, ondansetrón) [7].
Nota: Especialmente la llamada “dieta baja en FODMAP” puede aliviar de forma demostrable los síntomas del SII.
Los laxantes de tipo macrogol deben recomendarse para el tratamiento de los síntomas de estreñimiento. Si no hay respuesta a los laxantes convencionales o no se toleran, debe probarse el tratamiento con el agonista 5-HT4 prucaloprida. Además, el fármaco peptídico linaclotida (agonista de la guanilato ciclasa C) debe recomendarse para el estreñimiento refractario a los laxantes y especialmente para el dolor abdominal y la flatulencia concomitantes, pero el tratamiento no se reembolsa en Alemania. En ausencia de autorización de comercialización y la disponibilidad limitada en Alemania, la lubiprostona del grupo de los activadores de los canales de cloruro sólo debe considerarse en casos individuales seleccionados de SDR-O que de otro modo serían refractarios a la terapia [7].
Según la directriz S3, los espasmolíticos como la butilescopolamina deben recomendarse para el tratamiento del dolor asociado al SII [7]. Además, el aceite de menta piperita del grupo de los fitoterapéuticos ha demostrado su eficacia en el tratamiento de los síntomas del SII de dolor y distensión abdominal, por lo que debe tenerse en cuenta. Otros preparados fitoterapéuticos como la mezcla de plantas STW-5 (Iberis amara, raíz de angélica, flores de manzanilla, frutos de alcaravea, frutos de cardo mariano, hojas de melisa, hojas de menta piperita, celidonia y raíz de regaliz) y STW-5-II (Iberis amara, flores de manzanilla, frutos de alcaravea, hojas de melisa, hojas de menta piperita y raíz de regaliz) lograron aliviar los síntomas, sobre todo del dolor abdominal, y deberían integrarse individualmente en el concepto de tratamiento.
Además, el antibiótico rifaximina, que no está aprobado para esta indicación en Alemania, debería considerarse para el tratamiento de la flatulencia en el SII sin estreñimiento que, por lo demás, es refractario. Sin embargo, la cuestión de un posible desarrollo de resistencia en caso de uso recurrente y/o a largo plazo sigue sin resolverse en la actualidad [7].
Nota: El tratamiento farmacológico del SII debe estar siempre orientado a los síntomas y tener en cuenta los síntomas dominantes. Por ejemplo, los inhibidores peristálticos se utilizan principalmente para el SII-D y los laxantes de tipo macrogol para el tratamiento de los síntomas del estreñimiento. En el tratamiento del dolor asociado al SII, los espasmolíticos como la butilescopolamina son los principales fármacos utilizados.
Probióticos: En cuanto a la eficacia general de los probióticos para el tratamiento de las molestias asociadas al SII, no puede hacerse ninguna afirmación definitiva en este momento debido a la gran heterogeneidad metodológica y cualitativa de la situación de los estudios. Sin embargo, en el caso de las cepas probióticas individuales utilizadas habitualmente en Alemania (por ejemplo, Bifidobacteria, Lactobacillus), así como de los productos multiespecies, se pudieron conseguir mejoras significativas en ensayos clínicos controlados aleatorizados tanto para los síntomas típicos del SII, como el dolor, la flatulencia y los cambios en la frecuencia y consistencia de las heces, como para la calidad de vida y la satisfacción general de los participantes en el estudio. Según la directriz, todo intento de tratamiento con probióticos debe, por tanto, realizarse primero a modo de prueba y sólo continuarse tras un alivio convincente de los síntomas [7].
Nota: Las cepas probióticas individuales, así como los productos multiespecie, ya han demostrado su eficacia, pero aún no se ha demostrado una eficacia general de los probióticos, por lo que todo intento de tratamiento con probióticos tiene inicialmente un carácter de prueba.
Fármacos psicotrópicos: Según la directriz, el antidepresivo tricíclico amitriptilina debe utilizarse en adultos para el tratamiento del dolor, entre otras cosas (con la excepción del estreñimiento), pero no debe utilizarse en pacientes mayores si es posible debido al efecto secundario anticolinérgico [7]. Además, dado que los antidepresivos tricíclicos prolongan el tiempo de tránsito orocecal así como el gastrointestinal total, parece apropiado utilizar tricíclicos en el SDR-D [39]. Por el contrario, los antidepresivos de tipo ISRS acortan el tiempo de tránsito orocecal, por lo que parece razonable utilizarlos en el SDR-O. Sin embargo, dado que los estudios sobre el uso de ISRS en el SII han arrojado hasta ahora resultados inconsistentes y, además, no existe aprobación para el uso de ISRS para el SII en Alemania, según la directriz actualizada, los antidepresivos de tipo ISRS sólo pueden considerarse en casos de comorbilidad psicológica. Además, puede considerarse el uso del inhibidor de la recaptación de serotonina-norepinefrina (IRSN) duloxetina en adultos con ansiedad y trastorno depresivo comórbidos [40].
Nota: El antidepresivo tricíclico amitriptilina en particular se utiliza en adultos para el tratamiento del dolor asociado al SII, entre otras cosas. Según la directriz actualizada, los antidepresivos de tipo ISRS sólo pueden considerarse en casos de comorbilidad mental.
Psicoterapia: Según la directriz S3, los elementos psicoeducativos, como proporcionar información sobre el SII y la conexión entre las emociones estresantes y la aparición de síntomas, son útiles como oferta rentable en el contexto de otro tratamiento [7], ya que han demostrado tener efectos positivos sobre los síntomas y la calidad de vida de los pacientes con SII [9]. Además, las estrategias para afrontar el estrés y/o la enfermedad (afrontamiento) deben recomendarse individualmente como medidas coadyuvantes en el sentido de medidas de autoayuda guiadas [41]. En varios estudios se pudo lograr una reducción de los síntomas del SII y un aumento de la calidad de vida de los afectados, por lo que los resultados iniciales indican que las ofertas en línea(intervenciones de eSalud), en particular, pueden ser un complemento útil [42].
Además, se ofrecerán procedimientos psicoterapéuticos especializados como parte del concepto de tratamiento si están indicados. En cuanto a la indicación básica de la psicoterapia, independientemente del procedimiento respectivo, el deseo del paciente, una calidad de vida significativamente deteriorada debido a los síntomas gastrointestinales así como cualquier comorbilidad psicológica son decisivos [41]. En este contexto, existen pruebas claras de la eficacia de las psicoterapias para el SII, siendo con diferencia la terapia cognitivo-conductual la que más estudios ha publicado. Esto demostró ser eficaz y superior a las condiciones de control [43]. Existen menos estudios sobre los procedimientos psicodinámicos, pero éstos también han demostrado su eficacia [43]. Las terapias basadas en la atención plena también han mostrado efectos positivos de pequeños a moderados en estudios individuales, pero debido al número aún limitado de estudios en la actualidad, las directrices aún no hacen una recomendación concluyente para estas terapias [7].
La hipnosis dirigida al intestino ( HDI) se considera el único método psicoterapéutico órgano-específico para el tratamiento del SII. Varios metaanálisis han informado de efectos positivos en la mejora de los síntomas con tamaños de efecto medios [44,45]. Sin embargo, las enfermedades mentales graves (por ejemplo, la depresión severa y los trastornos de pánico) se consideran una contraindicación relativa.
Según la directriz, la terapia de relajación (por ejemplo, la relajación muscular progresiva según Jacobson, el entrenamiento autógeno) no debe ofrecerse como monoterapia, sino como parte de un concepto de tratamiento multimodal [7]; lo mismo se aplica al yoga basado en la atención plena. Si está indicada la psicoterapia, puede combinarse con psicofarmacoterapia si es necesario .
Nota: Se ha demostrado la utilidad de los elementos psicoeducativos como oferta rentable en el marco de otro tratamiento. Debido a la eficacia demostrada de la psicoterapia para el SII, deben ofrecerse procedimientos psicoterapéuticos especializados como parte del concepto de tratamiento si está indicado (por ejemplo, en caso de comorbilidad psicológica). La hipnosis abdominodirigida se utiliza como procedimiento psicoterapéutico órgano-específico en el tratamiento del SII.
Conclusión
El modelo biopsicosocial tiene en cuenta diversos factores somáticos y psicosociales dentro de la fisiopatología del SII e integra sus polifacéticos procesos de interacción. Además, se pueden identificar e implementar puntos de partida terapéuticos a nivel biológico, psicológico y social. En este contexto, los conceptos de tratamiento integrador y multimodal en la terapia del SII parecen especialmente prometedores y su eficacia debería investigarse más a fondo en la investigación clínica.
Mensajes para llevarse a casa
- El síndrome del intestino irritable es un trastorno funcional
del aparato digestivo inferior, que se asocia, entre otras cosas, a la persistencia,
La enfermedad va acompañada de síntomas relacionados con el intestino, como dolor abdominal, flatulencia y cambios en las deposiciones, y provoca un sufrimiento considerable a los afectados. - Basándose en un modelo biopsicosocial, cabe suponer que en la fisiopatología del SII intervienen diversos aspectos somáticos, psicológicos y sociales. Aquí son evidentes los complejos procesos de interacción entre el estrés, la comorbilidad psicológica y los síntomas gastrointestinales en el sentido de un círculo vicioso.
- En consecuencia, existe una amplia gama de intervenciones terapéuticas para controlar los síntomas del SII y mejorar la calidad de vida de los afectados. Los puntos de partida terapéuticos pueden identificarse y aplicarse a nivel biológico, psicológico y social.
- En este contexto, los conceptos de tratamiento integrador y multimodal en la terapia del SII parecen especialmente prometedores y su eficacia debería investigarse más a fondo en la investigación clínica.
Literatura:
- Mearin F, Lacy BE, Chang L, et al: Trastornos intestinales. Gastroenterología 2016 Feb 18; S0016-5085(16)00222-5.
- Lovell RM, Ford AC: Prevalencia global y factores de riesgo del síndrome del intestino irritable: un metaanálisis. Gastroenterología Clínica y Hepatología 2012; 10(7): 712-721.e4.
- Halder SLS, Locke GR, Schleck CD et al: Natural history of functional fastrointestinal disorders: A 12-year longitudinal population-based study. Gastroenterología 2007; 133(3): 799-807.e1.
- Andrews EB, Eaton SC, Hollis KA, et al: Prevalencia y datos demográficos del síndrome del intestino irritable: resultados de una gran encuesta a través de Internet. Farmacología y Terapéutica Alimentarias 2005; 22(10): 935-942.
- Lacy BE, Patel NK: Criterios de Roma y enfoque diagnóstico del síndrome del intestino irritable. Revista de Medicina Clínica 2017; 6(11): 99.
- Gralnek IM, Hays RD, Kilbourne A, et al: El impacto del síndrome del intestino irritable en la calidad de vida relacionada con la salud. Gastroenterología 2000; 119(3): 654-660.
- Layer P, Andresen V, Allescher H, et al.: Update S3-Leitlinie Reizdarmsyndroms: Definition, Pathophysiologie, Diagnostik und Therapie des Reizdarmsyndroms der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) und der Deutschen Gesellschaft für Neurogastroenterologie und Motilität (DGNM). AWMF 2021.
- Spiller R, Aziz Q, Creed F, et al: Directrices sobre el síndrome del intestino irritable: mecanismos y manejo práctico. Gut 2007; 56(12): 1770-1798.
- Weibert E, Stengel A: El papel de la psicoterapia en el tratamiento del síndrome del intestino irritable. Psychother Psychosom Med Psychol 2019; 69(9-10): 360-371.
- Enck P, Aziz Q, Barbara G, et al: Síndrome del intestino irritable. Nat Rev Dis Primers 2016; 2: 16014.
- Drossman DA: Trastornos gastrointestinales funcionales: historia, fisiopatología, características clínicas y Roma IV. Gastroenterología 2016; 150(6): 1262-1279.e2.
- Mayer EA, Gupta A, Kilpatrick LA, Hong JY: Obtención de imágenes de los mecanismos cerebrales en el dolor visceral crónico. Dolor 2015; 156: S50-63.
- Raskov H, Burcharth J, Pommergaard HC, Rosenberg J: Síndrome del intestino irritable, la microbiota y el eje intestino-cerebro. Microbios intestinales 2016; 7(5): 365-383.
- Mazurak N, Seredyuk N, Sauer H et al: Variabilidad de la frecuencia cardiaca en el síndrome del intestino irritable: una revisión de la literatura. Neurogastroenterología y Motilidad 2012; 24(3): 206-216.
- Liu Q, Wang EM, Yan XJ, Chen SL: Funcionamiento autonómico en el síndrome del intestino irritable medido por la variabilidad de la frecuencia cardiaca: Un metaanálisis. Revista de Enfermedades Digestivas 2013; 14(12): 638-646.
- Heitkemper M, Jarrett M, Cain K, et al: Aumento de catecolaminas urinarias y cortisol en mujeres con síndrome del intestino irritable. Am J Gastroenterol 1996; 91(5): 906-913.
- Chang L: El papel del estrés en las respuestas fisiológicas y los síntomas clínicos del síndrome del intestino irritable. Gastroenterología 2011; 140(3): 761-765.
- Kennedy PJ, Cryan JF, Dinan TG, Clarke G: Síndrome del intestino irritable: ¿un trastorno del eje microbioma-intestino-cerebro? World J Gastroenterol 2014; 20(39): 14105-14125.
- Moloney RD, Johnson AC, O’Mahony SM, et al: El estrés y el eje microbiota-intestino-cerebro en el dolor visceral: relevancia para el síndrome del intestino irritable. CNS Neurosci Ther 2016; 22(2): 102-117.
- Saito YA: El papel de la genética en el SII. Gastroenterol Clin North Am 2011; 40(1): 45-67.
- Dinan TG, Cryan J, Shanahan F et al: SII: Una perspectiva epigenética. Nat Rev Gastroenterol Hepatol 2010; 7(8): 465-471.
- Whitehead WE, Palsson O, Jones KR: Revisión sistemática de la comorbilidad del síndrome del intestino irritable con otros trastornos: ¿cuáles son las causas y las implicaciones? Gastroenterología 2002; 122(4): 1140-1156.
- Tanaka Y, Kanazawa M, Fukudo S, Drossman DA: Modelo biopsicosocial del síndrome del intestino irritable. J Neurogastroenterol Motil 2011; 17(2): 131-139.
- Koloski NA, Jones M, Kalantar J, et al: The brain–gut pathway in functional gastrointestinal disorders is bidirectional: a 12–year prospective population–based study. Gut 2012; 61(9): 1284-1290.
- Ford AC, Forman D, Bailey AG, et al: Síndrome del intestino irritable: una historia natural de 10 años de síntomas y factores que influyen en la conducta de consulta. Am J Gastroenterol 2008; 103(5): 1229-1239; quiz 1240.
- Chitkara DK, van Tilburg MAL, Blois-Martin N, Whitehead WE: Factores de riesgo en la vida temprana que contribuyen al síndrome del intestino irritable en adultos: una revisión sistemática. Am J Gastroenterol 2008; 103(3): 765-774; quiz 775.
- Elsenbruch S, Rosenberger C, Enck P et al: Las alteraciones afectivas modulan el procesamiento neural de los estímulos de dolor visceral en el síndrome del intestino irritable: un estudio fMRI. Gut 2010; 59(4): 489-495.
- Van Oudenhove L, Törnblom H, Störsrud S, et al: La depresión y la somatización se asocian a un aumento de los síntomas posprandiales en pacientes con síndrome del intestino irritable. Gastroenterología 2016; 150(4): 866-874.
- Drossman DA, Leserman J, Li Z et al: Efectos del afrontamiento en los resultados de salud entre las mujeres con trastornos gastrointestinales. Psychosom Med 2000; 62(3): 309-317.
- Van Oudenhove L, Crowell MD, Drossman DA, et al: Aspectos biopsicosociales de los trastornos gastrointestinales funcionales. Gastroenterología 2016; S0016-5085(16)00218-3.
- Lackner JM, Gudleski GD, Thakur ER, et al: El impacto de las quejas físicas, el entorno social y el funcionamiento psicológico en las percepciones de salud de los pacientes con SII: mirando más allá de la gravedad de los síntomas GI. Am J Gastroenterol 2014; 109(2): 224-233.
- Blanchard EB, Lackner JM, Jaccard J et al: El papel del estrés en la exacerbación de los síntomas entre los pacientes con SII. J Psychosom Res 2008; 64(2): 119-128.
- Kang SH, Choi SW, Lee SJ, et al: Los efectos de la modificación del estilo de vida sobre los síntomas y la calidad de vida en pacientes con síndrome del intestino irritable: un estudio observacional prospectivo. Gut Liver 2011; 5(4): 472-477.
- Johannesson E, Simrén M, Strid H, et al: La actividad física mejora los síntomas del síndrome del intestino irritable: un ensayo controlado aleatorizado. Am J Gastroenterol 2011; 106(5): 915-922.
- Johannesson E, Ringström G, Abrahamsson H, Sadik R: La intervención para aumentar la actividad física en el síndrome del intestino irritable muestra efectos positivos a largo plazo. World J Gastroenterol 2015; 21(2): 600-608.
- Zuckerman MJ: El papel de la fibra en el tratamiento del síndrome del intestino irritable: recomendaciones terapéuticas. J Clin Gastroenterol 2006; 40(2): 104-108.
- Hetterich L, Stengel A: Aspectos nutricionales del síndrome del intestino irritable – una actualización. Medicina Nutricional Actual 2020; 45(4): 276-285.
- Rao SSC, Yu S, Fedewa A: Revisión sistemática: la fibra dietética y la dieta restringida en FODMAP en el tratamiento del estreñimiento y el síndrome del intestino irritable. Aliment Pharmacol Ther 2015; 41(12): 1256-1270.
- Hetterich L, Zipfel S, Stengel A: Trastornos somatomorfos gastrointestinales. Fortschr Neurol Psychiatr 2019; 87(9): 512-525.
- Ford AC, Lacy BE, Harris LA, et al: Efecto de los antidepresivos y las terapias psicológicas en el síndrome del intestino irritable: una revisión sistemática y un metaanálisis actualizados. Revista oficial del Colegio Americano de Gastroenterología | ACG 2019; 114(1): 21-39.
- Hetterich L, Stengel A: Intervenciones psicoterapéuticas en el síndrome del intestino irritable. Fronteras de la Psiquiatría 2020; 11: 286.
- Beatty L, Lambert S: Una revisión sistemática de las intervenciones terapéuticas de autoayuda basadas en Internet para mejorar la angustia y el control de la enfermedad entre adultos con enfermedades crónicas. Revista de psicología clínica 2013; 33(4): 609-622.
- Black CJ, Thakur ER, Houghton LA et al: Eficacia de las terapias psicológicas para el síndrome del intestino irritable: revisión sistemática y metaanálisis en red. Gut 2020; 69(8): 1441-1451.
- Webb AN, Kukuruzovic RH, Catto-Smith AG, Sawyer SM.: Hipnoterapia para el tratamiento del síndrome del intestino irritable. Cochrane Database Syst Rev 2007; 4: CD005110.
- Krouwel M, Farley A, Greenfield S et al: Revisión sistemática, metaanálisis con análisis de subgrupos de la hipnoterapia para el síndrome del intestino irritable, efecto de las características de la intervención. Terapias complementarias en medicina 2021; 57: 102672.
InFo NEUROLOGíA Y PSIQUIATRÍA 2023; 21(5): 10-15.