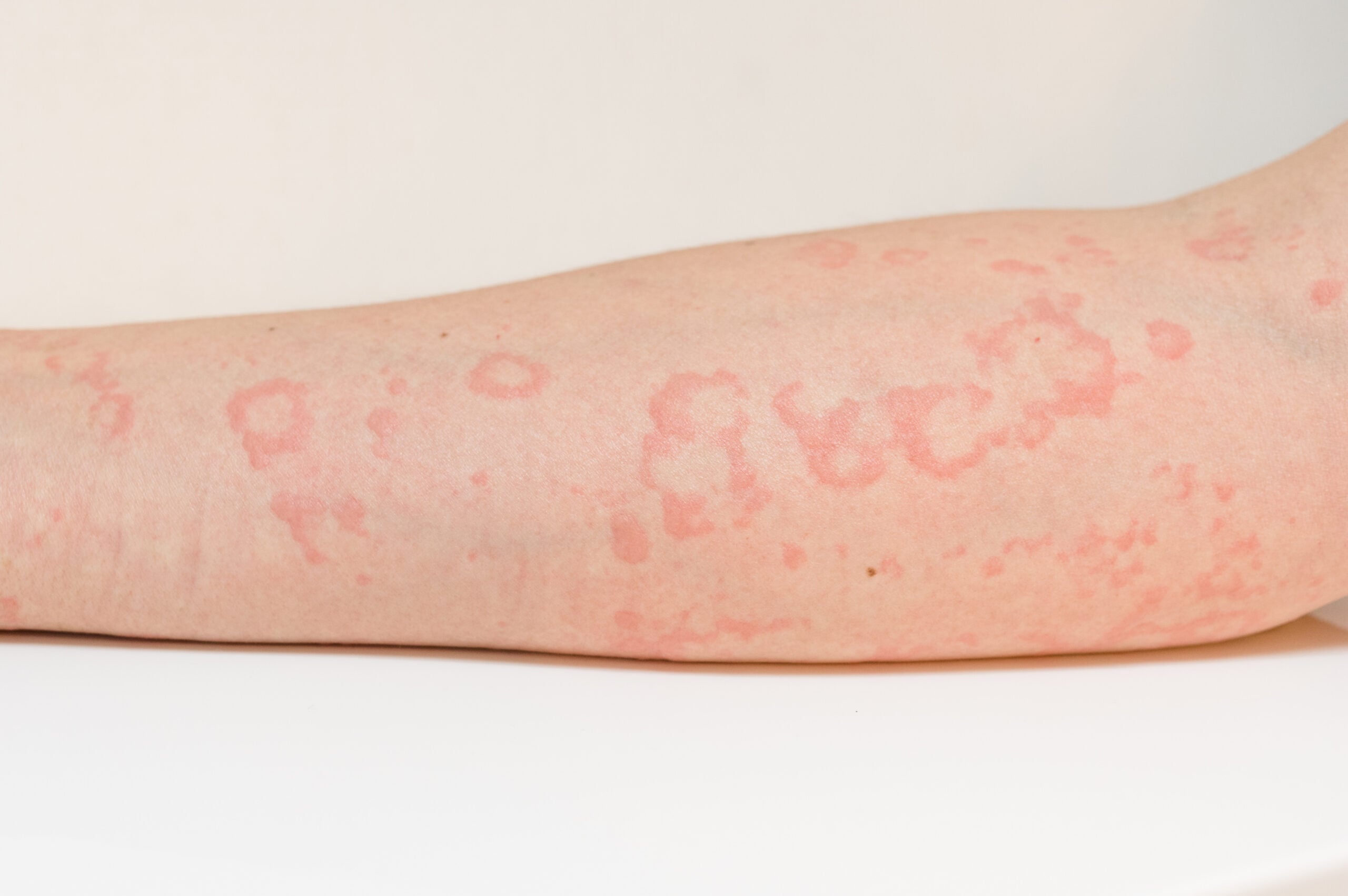
El mieloma múltiple está causado por la degeneración de una única célula plasmática cuyos clones se extienden por toda la médula ósea. En general, la enfermedad se presenta muy raramente. Sin embargo, es uno de los tumores más frecuentes del hueso y la médula ósea. Se está llevando a cabo una intensa investigación en el grupo de los linfomas no hodgkinianos con el fin de mejorar el pronóstico de los afectados a largo plazo.
Trabajos anteriores han demostrado que el deterioro de la maduración de los neutrófilos está asociado a la progresión de la gammapatía monoclonal de significado indeterminado (GMSI) al mieloma múltiple (MM). Las células madre y progenitoras hematopoyéticas (HSPC) participan de diversas formas en la respuesta inmunitaria primaria a diversas afecciones patológicas y sirven de nexo para la acumulación de células supresoras derivadas de los mieloides (MDSC). Recientemente, se encontraron las primeras células progenitoras de neutrófilos en la sangre periférica, caracterizadas por la expresión de CD71 como marcador de las primeras fases de la proliferación de neutrófilos. Estos hallazgos podrían desempeñar un papel biológico y clínico importante en la identificación de los pacientes con MM con peores resultados. Por ello, se investigó si la medición de precursores mieloides en la sangre periférica de pacientes con discrasias de células plasmáticas mediante citometría de flujo podría ser un marcador para identificar a los pacientes con características de displasia mieloide independientemente de la terapia administrada [1].
Se reclutó a 50 pacientes con discrasias de células plasmáticas y se les realizó un seguimiento durante una mediana de 13,8 meses. Se analizaron muestras de 23 donantes sanos como grupo de control. Se observó un aumento progresivo de las células CD15+CD71+CD117+ circulantes en los pacientes con MM en comparación con la GMSI y los donantes sanos. Se observó que los pacientes con una proporción elevada de células CD15+CD71+CD117+ presentaban un ISS más elevado y niveles de hemoglobina más bajos en el momento del diagnóstico, en comparación con los pacientes con una proporción baja de células CD15+CD71+CD117+, y era más probable que presentaran un FISH de alto riesgo. Sin embargo, el análisis de supervivencia univariante no identificó una proporción elevada de células CD15+CD71+CD117+ como factor predictivo de la progresión o la supervivencia global. Esto significa que las células progenitoras mieloides CD15+CD71+CD117+ están aumentadas en los pacientes con GMSI y MM en comparación con los individuos sanos, sin impacto aparente en los resultados clínicos.
El papel de la leptina en el MM
La leptina es producida principalmente por el tejido adiposo y liberada al torrente sanguíneo. La leptina circulante se une al receptor de la leptina (LEPR) en el cerebro, lo que activa vías de señalización que inhiben la ingesta de alimentos y promueven el consumo de calorías. El gen del receptor de la leptina (LEPR, también conocido como Ob-R) está situado en 1p31. La metilación del ADN consiste en la adición de un grupo metilo a la posición 5 del anillo de pirimidina de las citosinas antes de una guanina (dinucleótido CpG), catalizada por las ADN metiltransferasas. La metilación de la citosina en los sitios CpG es una importante modificación epigenética que puede suprimir la expresión génica. Un estudio investigó ahora el papel de los polimorfismos genéticos de la leptina y la LEPR en pacientes con MM [2].
En este estudio se incluyeron un total de 300 pacientes con MM y 170 personas que formaban un grupo de control sano. En el análisis estadístico para investigar los efectos de los polimorfismos de los genes de la leptina y LEPR en la susceptibilidad a la enfermedad, se descubrió que los genotipos GA y AA del gen de la leptina eran significativamente mayores en el grupo de pacientes en comparación con los controles sanos. En cuanto a la metilación de -31 NT y -51 NT del gen de la leptina, se observó que la metilación de -51 NT era significativamente mayor en los controles sanos. El análisis de supervivencia reveló que la supervivencia libre de progresión de los pacientes con el genotipo GG del gen LEPR era significativamente más corta en comparación con otros pacientes, mientras que no había ningún efecto sobre la supervivencia global. En consecuencia, los resultados mostraron que los polimorfismos del MM y la leptina presentan características significativas que afectan tanto a la susceptibilidad a la enfermedad como a la respuesta al tratamiento.
Factores pronósticos bajo el microscopio
El MM es una enfermedad muy heterogénea, en la que casi todos los pacientes recaen y/o se vuelven refractarios al tratamiento en algún momento. Varios estudios han identificado factores que determinan el pronóstico de los pacientes con MMRR. Sin embargo, faltaba una síntesis actualizada de las pruebas disponibles. Esto ya se ha compensado [3]. Los factores más investigados en los 125 estudios incluidos fueron el estadio de la enfermedad, la edad, las líneas de tratamiento previas, la mejor respuesta al tratamiento índice, el riesgo citogenético, la deshidrogenasa láctica, la enfermedad extramedular/plasmocitoma (EMP) y el estado funcional (EF).
La peor supervivencia se asoció a un mayor estadio de la enfermedad, una edad más avanzada, más líneas previas de terapia, peor respuesta, citogenética de alto riesgo, niveles elevados de LDH, presencia de EMP y peor PS. Por el contrario, la peor respuesta se asoció a un estadio más alto de la enfermedad, una edad más joven, más líneas previas de terapia, citogenética de alto riesgo y peor PS.
Congreso: 28º Congreso Anual de la Asociación Europea de Hematología (EHA) 2023
Literatura:
- Parinello NL, Duminuco A, Marino S, et al: Circulating CD71+ myeloid percursors in mgus and multiple myeloma: a prospecitive survey. HemaSphere 2023; 7(S3): 3984-3985.
- Serin I, Oyaci Y, Pehlivan M, et al.: ¿Qué eficacia tienen los polimorfismos y la metilación del gen de la leptina en el curso del mieloma múltiple (MM)? HemaSphere 2023; 7(S3): 3987-3988.
- Kumar S, Leleu X, Weisel K, et al: Revisión sistemática de la literatura sobre los factores pronósticos del mieloma múltiple recidivante/refractario. HemaSphere 2023; 7(S3): 4017-4018.
InFo ONCOLOGY & HEMATOLOGY 2023; 11(4): 22 (publicado el 12.9.23, antes de impresión).