El desarrollo de productos biológicos altamente eficaces fue precedido por esfuerzos de investigación a lo largo de varias décadas. Los avances en los análisis inmunopatogénicos y de genética molecular contribuyeron significativamente a la generación de estos innovadores sistemas terapéuticos. La conferencia en memoria de Guenter Goerz en la reunión anual de este año del Grupo de Trabajo para la Investigación Dermatológica estuvo dedicada a este tema y abarcó desde los hitos en la investigación de la psoriasis hasta los productos biológicos disponibles en la actualidad.
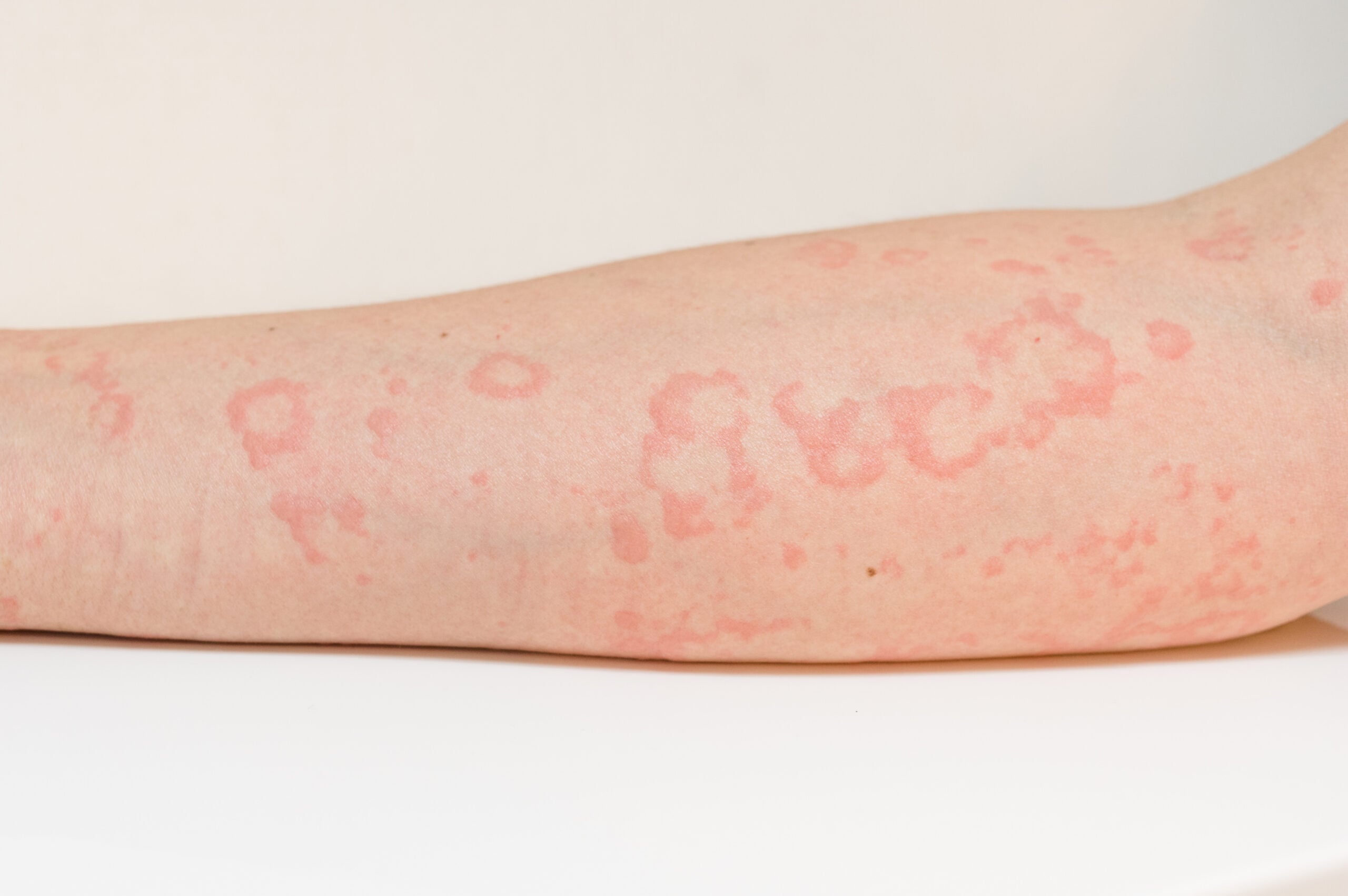
Las pruebas clínicas y experimentales condujeron al descubrimiento de que la psoriasis es una enfermedad inflamatoria de la piel mediada por el sistema inmunitario y genéticamente predispuesta (Fig. 1). El hecho de que las células T desempeñen un papel en la patogénesis de la psoriasis ha quedado cada vez más claro a lo largo de los años, explicó el Prof. Wolf-Henning Boehncke, MD, Médico Jefe del Departamento de Dermatología de los Hôpitaux Universitaires de Genève [1]. El éxito del tratamiento de pacientes con psoriasis con ciclosporina, un inmunosupresor que inhibe la proliferación de células T y la producción de citocinas, fue la primera prueba clínica de un posible papel de las células T en la patogénesis de la psoriasis [2,3]. Otros fármacos dirigidos a las células T, como los anticuerpos monoclonales anti-CD4 y el antígeno 4 asociado a los linfocitos T citotóxicos (CTLA4), también mostraron una eficacia terapéutica significativa en el tratamiento de la psoriasis [4–6]. Un estudio previo in vitro demostró que las células T CD4+ activadas procedentes de lesiones psoriásicas pueden potenciar la proliferación de queratinocitos mediante la secreción de interferón-γ(IFN-γ)8 , y el establecimiento de un modelo de trasplante xenogénico en ratones confirma aún más la importancia de las células T en la psoriasis [4–6].
Descubrimiento de autoantígenos relevantes para la psoriasis
El descubrimiento de que la psoriasis es una enfermedad autoinmune mediada por células T plantea la importante cuestión de cómo se activan las células T patógenas durante el curso de la enfermedad. Durante algún tiempo, se pensó que el péptido antimicrobiano LL37, que se sobreexpresa en la piel psoriásica, desempeñaba un papel en este proceso. Sin embargo, los investigadores no consiguieron aportar pruebas empíricas hasta hace pocos años. En un artículo de 2014 publicado en Nature Communication Lande et al. informaron de que la sobreexpresión crónica de LL37 provoca una activación persistente mediada por ácido nucleico de estos receptores, lo que da lugar a la maduración de las células dendríticas (CD) [7]. Desde entonces, se han descubierto otros tres autoantígenos relevantes para la psoriasis además del LL-37: la catelicidina, el ADAMTSL5, el PLA2G4D y la queratina-17. En numerosos pacientes con psoriasis en placas de moderada a grave se detectaron células T autorreactivas contra estos autoantígenos [8].
| “Células T de memoria residentes en el tejido En la actualidad, la investigación sobre la psoriasis se centra en las células T CD8+ con memoria residentes en los tejidos ( TRM). Se trata de una población específica de células T de memoria en la epidermis y la dermis que mantienen una memoria inmunológica durante años y contribuyen a las lesiones típicas [25]. Incluso en zonas de la piel que nunca se han visto afectadas por lesiones, los pacientes de psoriasis tienen un mayor número de células TRM que los individuos sanos [25]. Una hipótesis, que es objeto de estudios empíricos actuales, se refiere al hecho de que al reducir la acumulación de células TRM en la piel, se puede influir positivamente en el curso a largo plazo de la enfermedad psoriásica [27]. |
Los linfocitos T como desencadenantes de la enfermedad psoriásica
El importante papel de los linfocitos T se ha demostrado en un modelo de trasplante xenogénico [9,10]. La observación de que los injertos de piel no lesional de pacientes con psoriasis en ratones inmunodeficientes daban lugar al desarrollo espontáneo del fenotipo de piel lesional se tomó como prueba de la presencia de células T de memoria residentes en los tejidos (TRM) [11]. Además de los anticuerpos anti-CD4 y la inmunoglobulina antígeno-4 asociada a los linfocitos T, se han desarrollado dos agentes que inhiben las funciones de las células T, el efalizumab y el alefacept [2]. El efalizumab es un anticuerpo monoclonal humanizado que se une a la subunidad CD11a del LFA-1 (antígeno-1 asociado a la función linfocitaria), que se localiza en la superficie de los linfocitos. El efalizumab se aprobó en Suiza y la UE en 2004. Sin embargo, el biológico ha estado fuera del mercado durante varios años debido a una advertencia emitida por la FDA en relación con los riesgos de infección como la sepsis bacteriana, la meningitis vírica, la enfermedad fúngica invasiva y la leucoencefalopatía multifocal progresiva [2]. El alefacept es una proteína de fusión recombinante formada por partes de la molécula de señalización LFA3 de las células presentadoras de antígeno y del anticuerpo IgG1 [2]. El alefacept impide que el LFA3 se una a las células T de memoria activadas, implicadas en el desarrollo de la psoriasis. El alefacept fue aprobado en EE.UU. en 2003, pero no se comercializa desde 2011. Hasta la fecha, el biológico no ha recibido autorización de comercialización en la UE.
Importancia fisiopatológica del eje IL-23/Th17
Que el eje interleucina (IL)-23/células ayudantes (Th)17 desempeña un papel importante en la fisiopatología de la psoriasis y la artritis psoriásica es un hallazgo importante [14]. Pero inicialmente se pensó que la psoriasis implicaba una respuesta Th1 impulsada por las citocinas IFNγ e IL-12 [15]. Sin embargo, la falta de eficacia de las terapias anti-IFNγ para el tratamiento de la psoriasis [16] hablaba en contra. Cuando se descubrió una mayor expresión de p40 en las lesiones psoriásicas, se llegó a la conclusión inicial de que la expresión de IL-12 está aumentada en la psoriasis [17]. Sin embargo, cuando más tarde se demostró que la subunidad p40 de la IL-12 también se encuentra en la IL-23 [18], el Dr. Lee y sus colegas pudieron demostrar que el aumento de la expresión de p40 en la piel psoriásica se debía a la IL-23 y no a la IL-12 [17,19]. Dado que la IL-23 está implicada en el eje Th17, mientras que la IL-12 impulsa el desarrollo de las células Th1, el eje inmunitario IL-23/Th17 se consideró entonces central en la patogénesis de la psoriasis [18,20]. Junto a ésta, la IL-23, el factor de necrosis tumoral (TNF)-α y la IL-17 se han identificado como citocinas patogénicamente significativas en la psoriasis. La IL-23 tiene un efecto regulador sobre el mantenimiento de las células Th17, mientras que la IL-17 y el TNF-α median las funciones efectoras de las células inmunitarias innatas y adaptativas.
| Predisposición: La genética molecular aporta luz a la oscuridad La psoriasis es una enfermedad multifactorial, y la determinación genética parece desempeñar un papel importante. Los estudios de asociación de todo el genoma identificaron 36 loci de susceptibilidad [12,13]. El locus PSORS1 en la región de histocompatibilidad del cromosoma 6p21 es obviamente de especial importancia. Aquí se encuentra el alelo HLA-Cw*0602, que tiene la asociación más fuerte con la psoriasis. Los avances en las tecnologías de genética molecular y los métodos de análisis estadístico han revelado vías biológicas relevantes para la psoriasis, como la barrera epidérmica, los mecanismos asociados al NFκB y las respuestas inmunitarias mediadas por Th17 [2]. |
Biológicos altamente eficaces: un logro moderno
La primera generación de productos biológicos para el tratamiento de la psoriasis dirigidos contra las citocinas se centró en el TNF-α [21]. Sin embargo, los inhibidores del TNF-α son factores de riesgo conocidos de infecciones graves de las vías respiratorias inferiores o de la piel y tejidos blandos. Ustekinumab, otro inhibidor de la interleucina, salió al mercado en 2009 (UE) y 2010 (CH). Ustekinumab se dirige a la subunidad proteínica común p40 de la IL-12 y la IL-23 y bloquea la señalización de sus receptores correspondientes. En el estudio ACCEPT publicado en 2010, ustekinumab demostró ser superior al inhibidor del TNF-α etanercept. Las tasas de respuesta PASI75 y PASI90 en la semana 12 fueron del 73% y el 44%, respectivamente, con ustekinumab, en comparación con el 56% y el 23%, respectivamente, de los pacientes tratados con etanercept. [29]. Sin embargo, en los estudios que compararon el ustekinumab con los inhibidores de la IL-17 secukinumab, brodalumab e ixekizumab, el inhibidor de la IL-12/23 mostró una eficacia terapéutica significativamente inferior. [21]. A la aprobación de los inhibidores de la IL-17 siguió la de los inhibidores de la IL-23 guselkumab, risankizumab y tildrakizumab. En el estudio CLEAR publicado en 2017, se comparó secukinumab cara a cara con ustekinumab [22]. En una muestra de 676 sujetos aleatorizados, el inhibidor de la IL-17A fue significativamente superior al ustekinumab en la semana 52 en términos de tasas de respuesta PASI-90 (76% frente a 61%) e IGA 0/1** (80% frente a 65%) (ambos p<0,0001). Un ensayo cara a cara de secukinumab (n=514) frente a guselkumab (n=534) fue el ensayo ECLIPSE publicado en 2019 [23]. El tratamiento con el inhibidor de IL23p19 dio lugar a una proporción significativamente mayor que logró una respuesta PASI90 en la semana 48 en comparación con secukinumab (84% frente a 70%; p<0,0001). En los estudios con comparaciones indirectas entre el tildrakizumab y el guselkumab, ninguno de los agentes demostró ser superior o inferior [30]. También en 2021, se publicó una comparación directa entre bimekizumab (n=373) y secukinumab (n=370) [24]. El bimekizumab (inhibición dual de la IL17A y la IL17F) no fue ni superior ni inferior al secukinumab (anti-IL17A).
** IGA= Evaluación Global del Investigador (0=sin apariencia, 1=casi sin apariencia)
Congreso: Reunión anual de la ADF
Literatura:
- “Psoriasis – tendencias especulares en biología cutánea”, Conferencia en memoria de Guenter Goerz, Prof. Dr. med. W.-H. Boehncke, 49ª Reunión Anual de la ADF, Innsbruck, 22-25.02.2023.
- Cai Y, Fleming C, Yan J: Nuevos conocimientos sobre las células T en la patogénesis de la psoriasis. Cell Mol Immunol 2012; 9(4): 302-309.
- Mueller W, Herrmann B: Ciclosporina A para la psoriasis. N Engl J Med 1979; 301: 555.
- Nicolas JF, et al: Tratamiento de la psoriasis grave con anticuerpos CD4. Lancet 1991; 338: 321.
- Prinz J, et al: Anticuerpo monoclonal CD4 quimérico en el tratamiento de la psoriasis pustulosa generalizada. Lancet 1991; 338: 320-321.
- Abrams JR, et al: El bloqueo de la coestimulación de linfocitos T con inmunoglobulina del antígeno 4 asociado a linfocitos T citotóxicos (CTLA4Ig) revierte la patología celular de las placas psoriásicas, incluida la activación de queratinocitos, células dendríticas y células endoteliales. J Exp Med 2000; 192: 681-694.
- Lande R, et al: El péptido antimicrobiano LL37 es un autoantígeno de células T en la psoriasis. Nat Commun 2014; 5: 5621.
- Ten Bergen LL, et al: Conocimientos actuales sobre autoantígenos y autoanticuerpos en la psoriasis. Scand J Immunol 2020; 92(4): e12945.
- Boehncke WH, et al: Apretando el gatillo de la psoriasis. Nature 1996; 379: 777.
- Boehncke WH, Brembilla NC: Linfocitos T autoreactivos en las enfermedades inflamatorias de la piel. Front Immunol 2019; 10: 1198.
- Boyman O, et al: El desarrollo espontáneo de psoriasis en un nuevo modelo animal muestra un papel esencial de las células T residentes y del factor de necrosis tumoral alfa. J Exp Med 2004; 199: 731-736.
- Clop A, et al.: Una caracterización en profundidad del locus principal de susceptibilidad a la psoriasis identifica alelos de susceptibilidad candidatos dentro de un elemento potenciador HLA-C. PLoS One 2013; 8(8): e71690.
- Capon F, et al: Psoriasis and other complex trait dermatoses: from loci to functional pathways (Psoriasis y otras dermatosis de rasgos complejos: de los loci a las vías funcionales). J Invest Dermatol 2012; 132(3 Pt 2): 915-922.
- Girolomoni G, et al: El papel de la IL-23 y el eje inmunitario IL-23/TH 17 en la patogénesis y el tratamiento de la psoriasis. J Eur Acad Dermatol Venereol 2017; 31(10): 1616-1626.
- Schlaak JF, et al: Las células T implicadas en la psoriasis vulgar pertenecen al subconjunto Th1. J Invest Dermatol 1994; 102: 145-149.
- Harden JL, et al: AntiIFN-gamma humanizado (HuZAF) en el tratamiento de la psoriasis. J Allergy Clin Immunol 2015; 135: 553-556.
- Yawalkar N, et al: La expresión de la interleucina-12 está aumentada en la piel psoriásica. J Invest Dermatol 1998; 111: 1053-1057.
- Oppmann B, et al.: Novel p19 protein engages IL-12p40 to form a cytokine, IL-23, with biological activities similar as well as distinct from IL-12. Immunity 2000; 13: 715- 725.
- Lee E, et al: Aumento de la expresión de la interleucina 23 p19 y p40 en la piel lesional de pacientes con psoriasis vulgar. J Exp Med 2004; 199: 125-130.
- Aggarwal S, et al: La interleucina-23 promueve un estado distinto de activación de las células T CD4 caracterizado por la producción de interleucina-17. J Biol Chem 2003; 278: 1910- 1914.
- Ten Bergen LL, et al: The TNF/IL-23/IL-17 axis-Head-to-head trials comparing different biologics in psoriasis treatment. Scand J Immunol 2020 Oct; 92(4): e12946.
- Blauvelt A, et al: Secukinumab es superior a ustekinumab en el aclaramiento de la piel de sujetos con psoriasis en placas de moderada a grave hasta 1 año: resultados del estudio CLEAR. J Am Acad Dermatol 2017; 76(1): 60-69.e9.
- Reich K, et al: Guselkumab frente a secukinumab para el tratamiento de la psoriasis de moderada a grave (ECLIPSE): resultados de un ensayo controlado aleatorizado de fase 3. Lancet 2019; 394(10201): 831-839.
- Reich K, et al: Bimekizumab frente a secukinumab en la psoriasis en placas. N Engl J Med 2021; 385(2): 142-152.
- Clark RA: Resident memory T cells in human health and disease. Sci Transl Med 2015; 7(269): 269rv1
- Gallais Sérézal I, et al: Un conjunto sesgado de células T residentes desencadena respuestas tisulares asociadas a la psoriasis en piel nunca lesional de pacientes con psoriasis. J Allergy Clin Immunol 2019; 143: 1444-1454.
- Eyerich K, et al: El bloqueo de la IL-23 con guselkumab modifica potencialmente la patogénesis de la psoriasis: justificación y protocolo de estudio de un estudio de fase 3b, aleatorizado, doble ciego y multicéntrico en participantes con psoriasis en placas de moderada a grave (GUIDE). BMJ Open 2021; 11(9):e049822
- Hu P, et al: El papel de las células T auxiliares en la psoriasis. Front Immunol 2021 Dic 15; 12: 788940. https://www.frontiersin.org/articles/10.3389/fimmu.2021.788940/full,(último acceso 17.05.2023).
- Griffiths CE, et al: Grupo de estudio ACCEPT. N Engl J Med 2010; 362(2): 118-128.
- Ghazawi FM, et al: Front Med (Lausana) 2021; 10 de agosto; 8:702776. fmed.2021.702776.
DERMATOLOGIE PRAXIS 2023; 33(3): 14-15 (publicado el 8.6.23, antes de impresión).