La EoE se reconoce ahora como una enfermedad inmunitaria mediada por el tipo 2 que suele asociarse a enfermedades atópicas como la dermatitis atópica, el asma y las alergias alimentarias. Además de los bloqueantes ácidos (IBP) y los esteroides, ahora también se dispone de un tratamiento biológico, el dupilumab. El dupilumab se dirige específicamente a las citocinas clave de la inflamación de tipo 2. Se siguen recomendando medidas dietéticas. Y si ya se han formado estenosis, debe considerarse la dilatación en caso necesario.
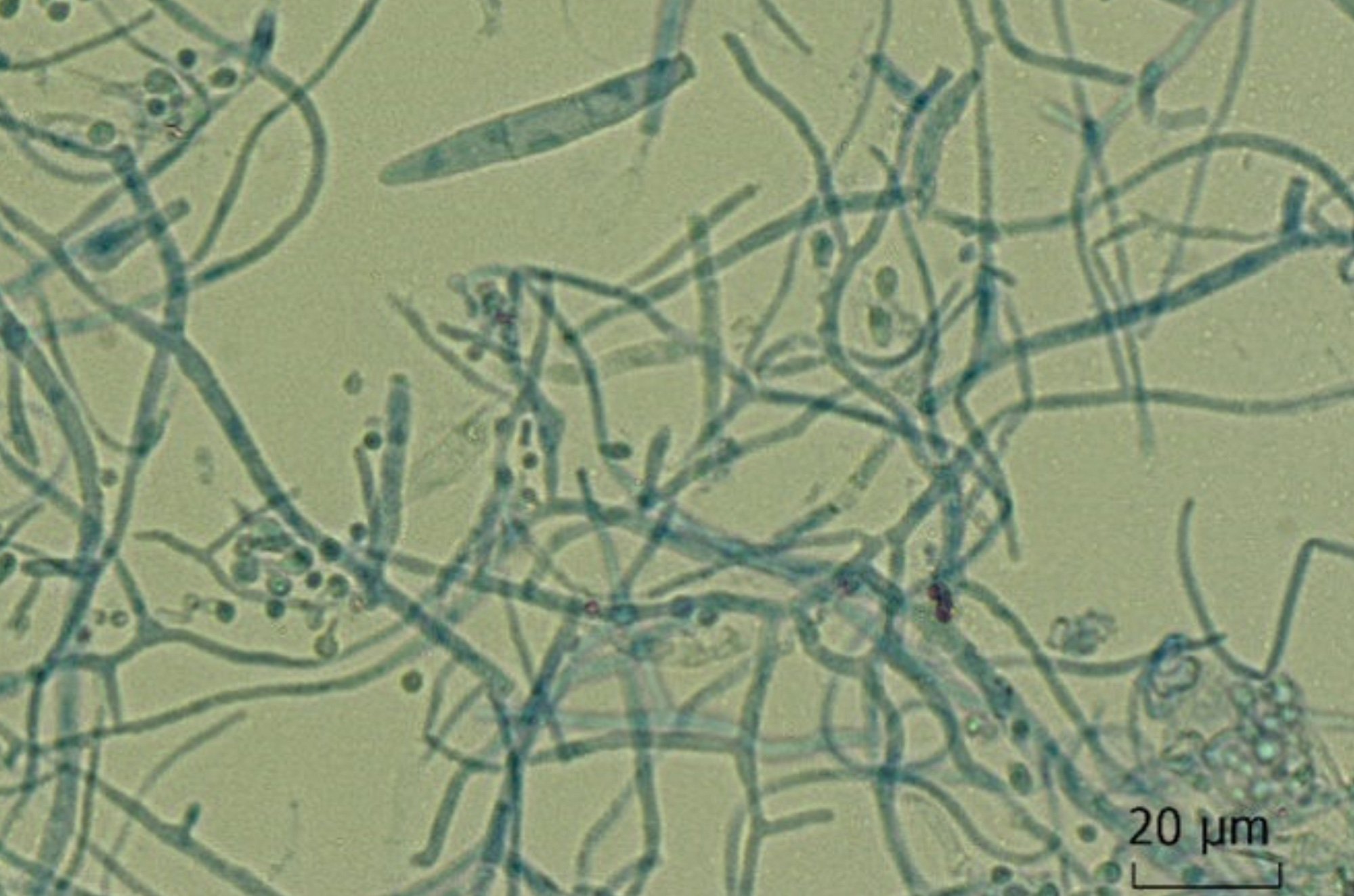
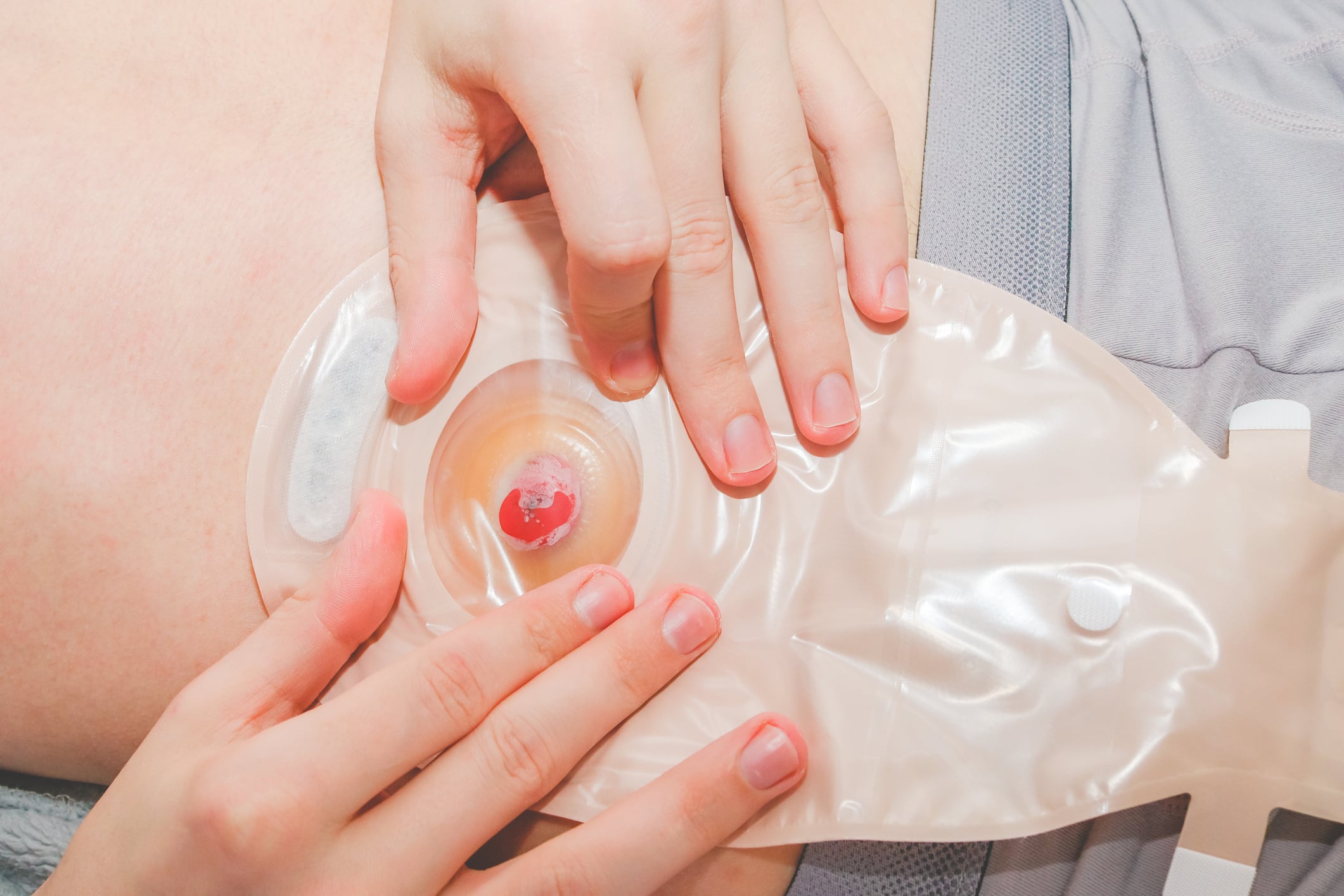
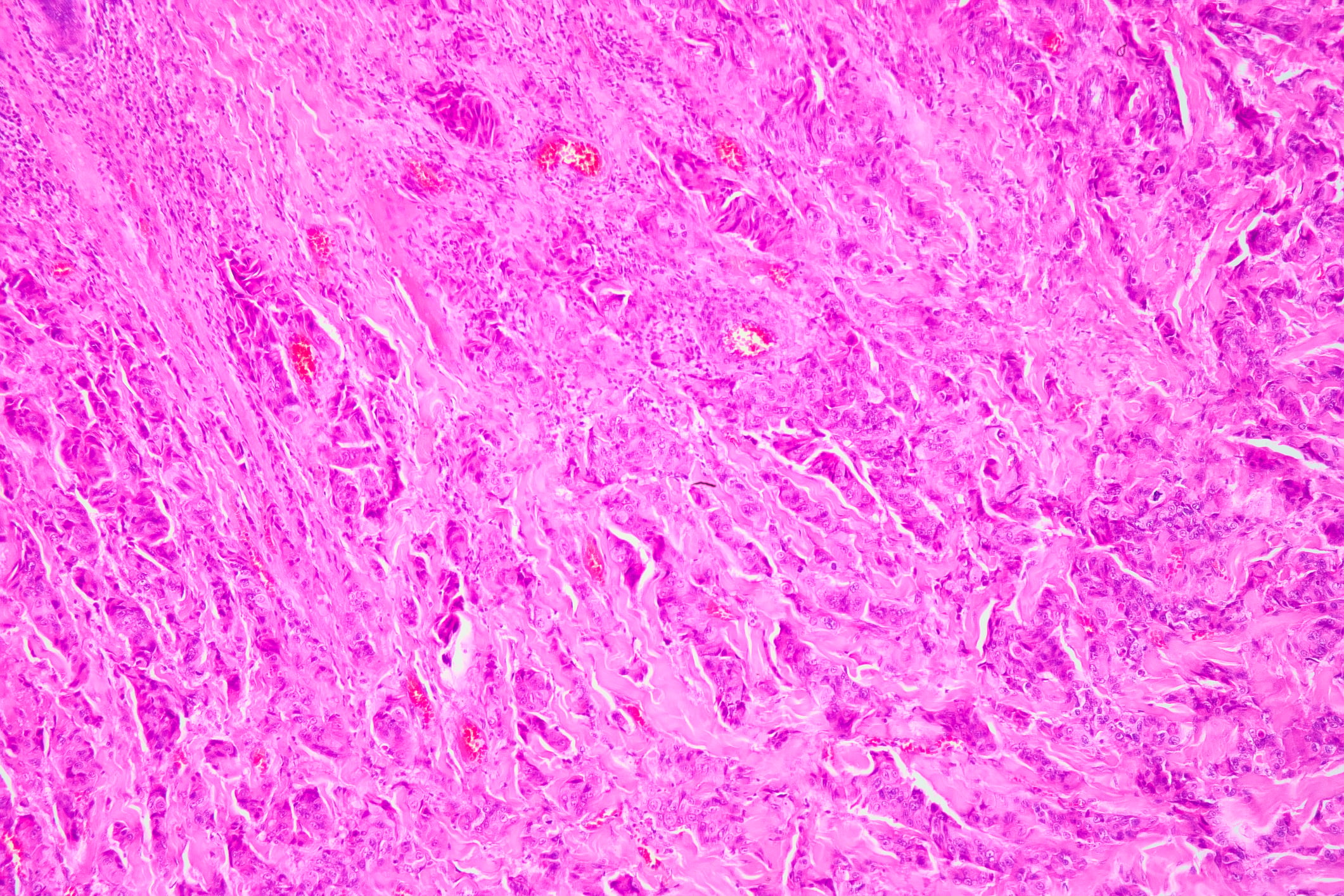
La esofagitis eosinofílica (EoE) (Fig. 1 ) es una enfermedad crónica inmunomediada del esófago caracterizada por síntomas de disfunción esofágica e histológicamente por inflamación eosinofílica. La EoE activa se define como ≥15 eosinófilos por campo de alta potencia (hpf) en los hallazgos de la biopsia de la mucosa esofágica y los síntomas clínicos [1]. Si la EoE no se trata, existe un alto riesgo de fibrosis esofágica, estenosis y obstrucción del bolo . Los estudios han demostrado que la predisposición genética desempeña un papel en la etiopatogenia de la EoE. [6,7]Los familiares de primer grado de pacientes con EoE tienen un riesgo entre 10 y 64 veces mayor de desarrollar la enfermedad en comparación con la población general . Fisiopatológicamente, la EoE da lugar a una respuesta inmunitaria desregulada a los antígenos ambientales y a una alteración de la barrera mucosa, lo que hace que los aeroalérgenos y los componentes alergénicos de los alimentos penetren en el epitelio y activen los receptores y las células inflamatorias (especialmente los eosinófilos). Como resultado, los mastocitos liberan mediadores proinflamatorios y promueven el reclutamiento de eosinófilos y la liberación de proteínas citotóxicas y citoquinas, lo que provoca daños y remodelación tisular [8].
Enfermedad mediada por Th2 con liberación de citoquinas de tipo 2
Se ha demostrado que la EoE está asociada a un aumento de los niveles de citocinas de tipo 2, como la interleucina (IL)-4, la IL-5 y la IL-13, que intervienen en la respuesta inmunitaria desregulada [9]. [10]”La inflamación Th2 tiene un gran impacto en la modificación de las proteínas epiteliales que mantienen la función de barrera”, explicó la doctora Antonella Cianferoni, del Hospital Infantil de Filadelfia y la Facultad de Medicina Perlman de la Universidad de Pensilvania (EE UU) . [8,11]La respuesta inmunitaria Th2 se ve favorecida, entre otras cosas, por la TSLP, una citocina derivada del epitelio que expresan varios tipos de células, al influir en las células dendríticas (CD) . Los alérgenos ambientales y los componentes alergénicos de los alimentos actúan como factores desencadenantes de las respuestas inmunitarias Th2. Cianferoni et al. [12]pudieron demostrar en un estudio que la EoE desencadenada por el consumo de leche no sólo provoca una inflamación Th2 local, sino también sistémica . [10]”La inflamación Th2 suele ser responsable de la desregulación del epitelio”, afirma el ponente .
Estrategia de tratamiento clásica: dieta de eliminación, IBP y esteroides
[10]”Sabemos que las medidas dietéticas son eficaces”, informó la Dra. Cianferoni . En la mayoría de los casos, los pacientes sólo son alérgicos a uno o dos alimentos (por ejemplo, la leche), por lo que una dieta de eliminación selectiva tiene sentido(recuadro) . [14] Además de un cambio en la dieta, el uso de bloqueadores de ácido (inhibidores de la bomba de protones, IBP) y esteroides es una de las medidas de tratamiento probadas para la EoE . Según el ponente, los IBP se utilizan con mayor frecuencia. [14]Las directrices recomiendan utilizar los IBP como monoterapia durante un periodo de 8 a 12 semanas (de 1-2 mg/kg/día a 20-40 mg hasta dos veces al día) . Esta terapia resulta eficaz en aproximadamente un tercio de los pacientes con EoE. La justificación de una dosis elevada de IBP es que no sólo consigue efectos inhibidores del ácido, sino que también puede reducir la producción de STAT-6 y eotaxina-3. [10]”El tratamiento con esteroides, tanto en forma oral como tópica, también ha demostrado su eficacia”, declaró la Dra. Cianferoni . Citó como ejemplos la aplicación tópica de fluticasona y budesonida, así como la budesonida en comprimidos (1 mg, 2×/d). Si no hay respuesta a la monoterapia con IBP o esteroides, puede considerarse la terapia combinada. Si tampoco tiene éxito, puede recurrirse a los biológicos.
“Un alimento” frente a “dieta de eliminación de seis alimentos” En un estudio publicado en la revista Lancet Gastroenterology & Hepatology en 2023, Kliewer et al. demostraron que, en pacientes con EoE, la omisión de un alimento (por ejemplo, la leche) producía una remisión histológica similar al cabo de 6 semanas en comparación con la omisión de seis alimentos (“terapia de dieta de eliminación de seis alimentos”). Los adultos de 18 a 60 años con esofagitis eosinofílica activa y sintomática fueron aleatorizados 1:1 en un brazo de estudio con eliminación de la leche sola (“dieta de eliminación de un alimento”, 1-FED) y un brazo con eliminación de leche, trigo, huevo, soja, pescado y marisco, cacahuetes y frutos secos (“dieta de eliminación de seis alimentos”, 6-FED). La aleatorización se estratificó por edad y sexo. El criterio de valoración primario fue la proporción de pacientes con remisión histológica al cabo de 6 semanas. <La remisión histológica se definió como 15 eosinófilos por campo de alta potencia (hpf). En el grupo de 6-FED, el 40% (n=25) logró la remisión histológica después de 6 semanas en comparación con el 34% (n=23) en el grupo de 1-FED. La diferencia del 6% no fue significativa (IC 95%; -11 a 23; p=0,58). Sin embargo, la proporción de pacientes con remisión completa fue significativamente mayor en el grupo 6-FED que en el grupo 1-FED. |
| a [13] |
Dupilumab como opción terapéutica innovadora y muy eficaz
[10]”Los biológicos dirigidos contra la inflamación Th2 conducen a una normalización o mejora de la función de barrera epitelial”, explicó el Dr. Cianferoni de .
[15]El anticuerpo monoclonal dupilumab se une a la subunidad IL-4Rα de los complejos receptores de IL-4 e IL-13 y, por tanto, inhibe específicamente el efecto proinflamatorio de estas dos citocinas clave .
[16,17]En estudios clínicos de fase II y fase III, el dupilumab demostró mejorar los parámetros histológicos y endoscópicos de la actividad de la enfermedad y, en general, fue bien tolerado .
[17]El dupilumab 300 mg produjo una reducción de los eosinófilos esofágicos tanto con una dosis semanal como a intervalos de 14 días .
En Suiza, el dupilumab (Dupixent®) está autorizado para la indicación EoE a partir de los 12 años de edad.
La dosis recomendada para pacientes con un peso corporal (pc) de al menos
40 kg es de 300 mg de dupilumab una vez a la semana.
Se trata de una terapia a largo plazo; se investigó la administración semanal de 300 mg de dupilumab durante un máximo de 52 semanas.
Recientemente se ha publicado en el New England Journal of Medicine un estudio de fase III sobre el uso de dupilumab en pacientes con EoE de 1 a 11 años.
[18]Muestra que el dupilumab también condujo a la remisión histológica en una proporción significativamente mayor de participantes en el estudio en este grupo de edad en comparación con el placebo .
Otros productos biológicos que se están investigando en estudios en curso para la EoE son el benralizumab (bloqueo del receptor de IL-5), el cendakimib (bloqueo de IL-13) y el lirentelimab (antisiglec-8).
[19,20].
Letzterer erwies sich im Placebovergleich als überlegen hinsichtlich Kontrolle der Entzündung, nicht aber bezüglich Symptomlinderung.
Eine weitere Behandlungsmöglichkeit besteht in der Aufweitung der Speiseröhre (Dilatation).
Diese Therapiemassnahme ist sinnvoll, wenn sich bereits Strikturen gebildet haben.
Congreso: Reunión anual de la EAACI
Literatura:
- Dellon ES, Hirano I: Epidemiología e historia natural de la esofagitis eosinofílica. Gastroenterology 2018; 154(2): 319.e3-332.e3.
- Lucendo AJ, et al: Directrices sobre la esofagitis eosinofílica: declaraciones basadas en la evidencia y recomendaciones para el diagnóstico y manejo en niños y adultos. United European Gastroenterol J 2017; 5: 335-358.
- Schoepfer AM, et al: El retraso en el diagnóstico de la esofagitis eosinofílica aumenta el riesgo de formación de estenosis de forma dependiente del tiempo. Gastroenterología 2013; 145: 1230-1236.e1-2.
- Warners MJ, et al: El curso natural de la esofagitis eosinofílica y las consecuencias a largo plazo de la enfermedad no diagnosticada en una gran cohorte. Am J Gastroenterol 2018; 113: 836-844.
- Shaheen NJ, et al: Historia natural de la esofagitis eosinofílica: una revisión sistemática de la epidemiología y el curso de la enfermedad. Dis Esophagus 2018; 31(8): doy015. doi: 10.1093/dote/doy015
- Kottyan LC, et al: La etiología genética de la esofagitis eosinofílica. JACI 2020; 145: 9-15.
- Alexander ES, et al: Los estudios de gemelos y familias revelan que la heredabilidad de la esofagitis eosinofílica se explica por una fuerte influencia ambiental y una menor influencia genética. JACI 2014; 134: 1084-1092.e1.
- Massironi S, et al: Mechanistic Insights into Eosinophilic Esophagitis: Therapies Targeting Pathophysiological Mechanisms. Cells 2023; 12(20): 2473. https://doi.org/10.3390/cells12202473.
- Rochman M, Azouz NP, Rothenberg ME: Origen epitelial de la esofagitis eosinofílica. JACI 2018; 142(1): 10-23.
- “Manipulación de la disfunción de la barrera en la EoE – el papel de los biológicos y la microbiota”, Antonella Cianferoni, MD, PhD, Congreso EAACI 31.05.-3.06.2024.
- Liu, YJ: TSLP in Epithelial Cell and Dendritic Cell Cross Talk. Adv Immunol 2009; 101: 1-25.
- Cianferoni A, et al. Expresión elevada de células TH2 activadas y células TH2 específicas de la leche en la esofagitis eosinofílica inducida por la leche. Ann Allergy Asthma Immunol 2018; 120: 177-183.
- Kliewer K, et al: Terapia de dieta de eliminación de un alimento frente a seis alimentos para el tratamiento de la esofagitis eosinofílica: un ensayo multicéntrico, aleatorizado y abierto. Lancet Gastro Hepatol 2023; 8: 408-421.
- Dellon ES, et al: Criterios diagnósticos de consenso internacional actualizados para la esofagitis eosinofílica: Actas de la Conferencia AGREE. Gastroenterology 2018; 155(4): 1022-1033.e10.
- Swissmedic: Información sobre medicamentos, www.swissmedicinfo.ch,(última consulta: 28/06/2024)
- Hirano I, et al: Eficacia del dupilumab en un ensayo aleatorizado de fase 2 en adultos con esofagitis eosinofílica activa. Gastroenterología 2020; 158: 111-122 e10.
- Dellon ES, et al: Dupilumab en adultos y adolescentes con esofagitis eosinofílica. N Engl J Med. 2022; 387: 2317-2330.
- Chehade M, et al: Dupilumab para la esofagitis eosinofílica en pacientes de 1 a 11 años de edad. N Engl J Med 2024; 390(24): 2239-2251.
- Nhu QM, Aceves SS: Estado actual de los biológicos en el tratamiento de la esofagitis eosinofílica. Ann Allergy Asthma Immunol 2023; 130(1): 15-20.
HAUSARZT PRAXIS 2024: 19(7): 32-33 (publicado el 22.7.24, antes de impresión)