- El tratamiento a largo plazo con upadacitinib (UPA, RINVOQ®) durante un máximo de 5,5 años no muestra nuevas señales de seguridad [1].
- El AUP tiene un perfil de seguridad consistente en el tratamiento de la dermatitis atópica (DA), la artritis reumatoide (AR), la artritis psoriásica (APs) y la espondiloartritis axial (EA), aunque la incidencia de acontecimientos adversos varía debido a las diferencias en la población de pacientes y las comorbilidades relacionadas con la enfermedad[1].
UPA en la dermatitis atópica
La dermatitis atópica (DA) es la enfermedad inflamatoria crónica de la piel más común en todo el mundo y supone una carga considerable para la vida de los pacientes y sus familias [2]. Además, la EA se asocia a diversas comorbilidades alérgicas, autoinmunes y cardiovasculares [3]. Para los pacientes con EA de moderada a grave que son refractarios al tratamiento tópico, existen terapias sistémicas dirigidas que reducen las recaídas y también mitigan los efectos psicológicos de la enfermedad [1, 4-6]. El UPA es un inhibidor oral reversible de la Janus quinasa (JAK) que actúa específicamente sobre la JAK1 y, en menor medida, también sobre la JAK2, la JAK3 o la TYK2. El UPA se utiliza en una dosis de 15 mg una vez al día para el tratamiento de la EA, la AR, la APs y la EA [7].
El UPA mostró una gran eficacia en los 12 estudios realizados en EA, AR, APs y EA. Sin embargo, un uso seguro es igualmente crucial para el tratamiento [7]. Los datos del estudio de vigilancia ORAL, que comparó el inhibidor de JAK tofacitinib con un inhibidor del factor de necrosis tumoral (TNF) en pacientes ancianos con AR y factores de riesgo cardiovascular, subrayan la necesidad de caracterizar mejor el perfil de seguridad de los inhibidores de JAK, también porque la seguridad de cada uno de ellos difiere en los distintos grupos de pacientes con enfermedades inflamatorias inmunomediadas (IMID) [1]. Una nueva publicación de Burmester et al. muestra ahora el perfil de seguridad a largo plazo del AUP durante un periodo de hasta 5,5 años en diversas enfermedades reumáticas y de hasta 2,75 años en la EA. Durante este periodo no surgieron nuevas señales de seguridad [1].
Tratamiento a largo plazo con UPA
En total, se investigó la seguridad del AUP en 6.000 pacientes con EA, AR, APs y EA con más de 15.000 años-paciente (APs). Los datos de seguridad de 12 estudios de fase IIb/III para cada enfermedad se agruparon en todos los estudios. Tres de estos estudios, con un total de 2.693 participantes, se realizaron en EA. Esto corresponde a 2035,8 PY.
Tabla 1: Datos demográficos básicos y características de la enfermedad de la UPA en pacientes con EA
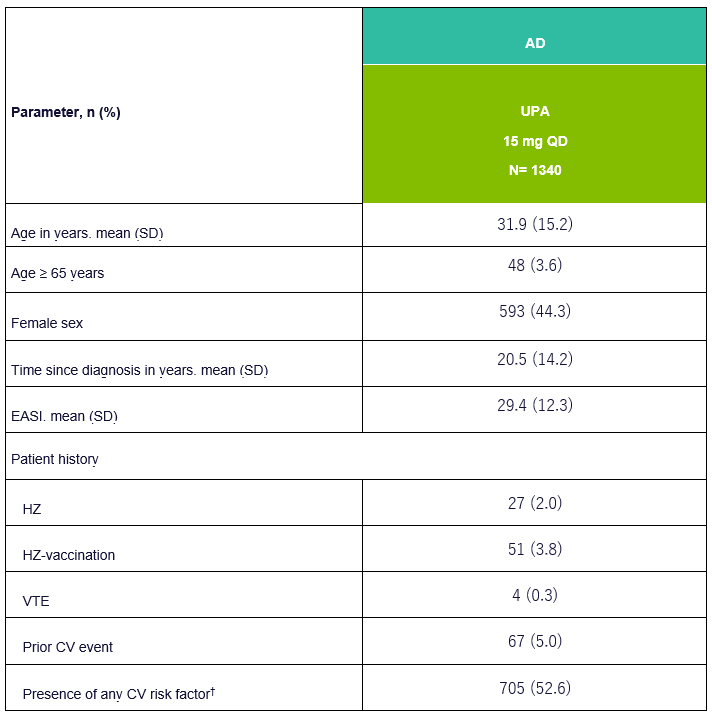
EASI, Índice de Área y Gravedad del Eczema; TEV, Tromboembolismo Venoso; CV, Cardiovascular; HZ, Herpes Zoster; †CV Los factores de riesgo incluyen los acontecimientos cardiovasculares en el historial médico, la hipertensión arterial, la diabetes mellitus, el consumo de tabaco/nicotina, el aumento del valor de LDL-C y la disminución del valor de HDL-C. Adaptado de [1]
No hay nuevas señales de seguridad bajo la UPA en el AD
Las infecciones graves bajo UPA 15 mg se produjeron en AD a una tasa de 2,5 eventos por 100 PY (2,5 E/100 PY) y rara vez condujeron a la interrupción del tratamiento. La infección grave más frecuente en todas las poblaciones estudiadas fue la COVID-19, seguida del herpes zóster en la población de EA. Generalmente fue leve o moderada, sin afectación del sistema nervioso central ni de los órganos internos, rara vez provocó la interrupción de la terapia y normalmente sólo afectó a un dermatoma. Además, no se pudo establecer ninguna correlación entre la duración del tratamiento y la aparición de herpes zóster [1]. Existe una vacuna contra el herpes zóster. La vacuna debe administrarse 4 semanas antes del tratamiento con un agente inmunomodulador activo como el AUP [7]. Otras infecciones oportunistas con UPA 15 mg se cifraron en 1,8 eventos por 100 PY, de los que se notificaron principalmente eczema herpético. La tuberculosis (TB) se registró por separado y la TB activa se registró en 0,03 E/100 PY en los pacientes con EA bajo UPA. El acontecimiento adverso emergente del tratamiento ( AET ) más común asociado a la AUP fue una infección de las vías respiratorias superiores [1].
Los principales acontecimientosadversos cardiovasculares (MACE) incluyeron los siguientes Muerte, infarto de miocardio no mortal y apoplejía no mortal. Usted se han notificado en pacientes con EA en una tasa de 0,03/100 PY. No se encontró correlación entre la duración de la ingesta de AUP y la aparición de MACE. Además, la mayoría de los pacientes que sufrieron un MACE tenían al menos un factor de riesgo cardiovascular [1].
Las trombosis venosas profundas y las embolias pulmonares se registraron como tromboembolias venosas (TEV). Se produjeron a una tasa de 0,04 E/100 PY, y la mayoría de los pacientes tenían al menos un factor de riesgo cardiovascular y/o tromboembólico. No se encontró ninguna correlación entre la duración de la exposición al AUP y la aparición de TEV [1].
Las enfermedades malignas (excluido el cáncer de piel no melanoma, CPNM) se registraron en UPA 15 mg a 0,2 E/100 PY. No hubo cambios significativos en esta tasa durante toda la duración de la ingesta de AUP. Los acontecimientos NMSC no fueron en general graves y no llevaron a la interrupción del tratamiento. En la población UPA 15 mg se notificaron NMSC a 0,3 E/100 PY [1].
Anomalías de laboratorio
También se han notificado efectos secundarios dependientes de la dosis como anemia, neutropenia, linfopenia, disfunción hepática y elevación de la creatina fosfoquinasa (CPK) en pacientes con EA que toman AUP. La mayoría de las anomalías de laboratorio se clasificaron como leves y transitorias en general y sólo unas pocas llevaron a la interrupción de la medicación del estudio [1].
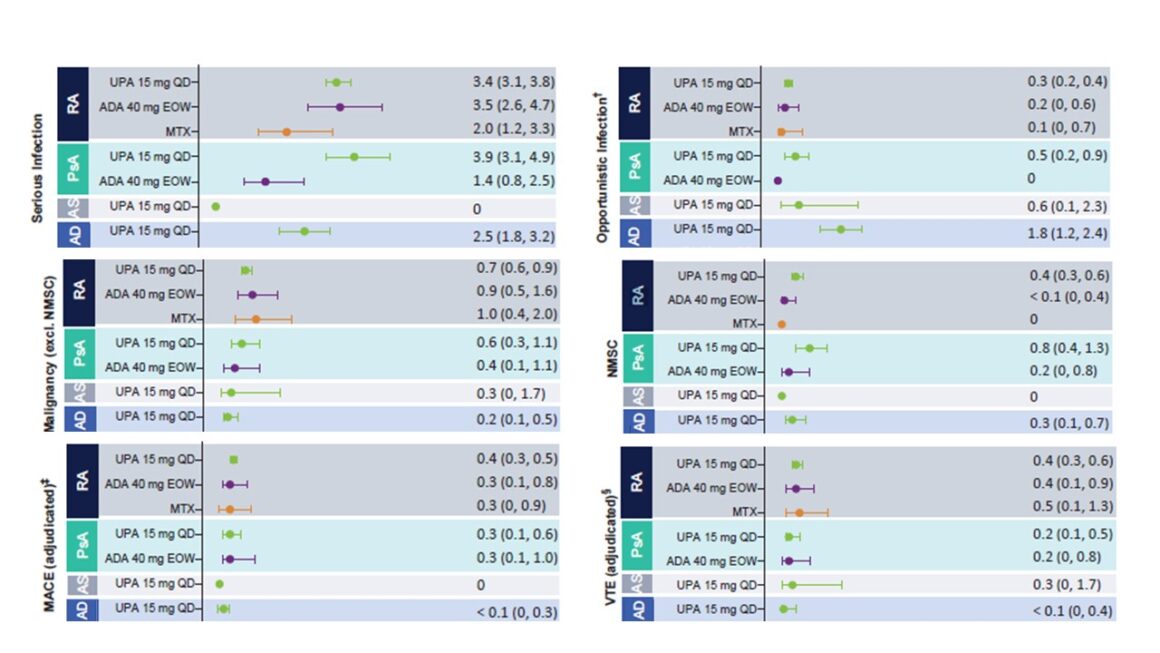
Figura 1: Tasas ajustadas a la exposición de acontecimientos adversos emergentes del tratamiento (AETT) de especial interés. Adaptado de [1]
Este análisis de seguridad no muestra riesgos de seguridad nuevos o inesperados bajo la UPA en comparación con los informes anteriores. Un mayor riesgo de herpes zoster y un aumento de los niveles de CPK se asocian a la inhibición de JAK y son coherentes con el perfil de seguridad general de los inhibidores de JAK. Las infecciones por herpes zóster fueron en su mayoría no graves y limitadas a un dermatoma, mientras que los niveles elevados de CPK fueron en su mayoría asintomáticos y transitorios. Aunque se notificaron casos de TEV en pacientes que recibieron AUP, las tasas fueron coherentes con las tasas de fondo para las afecciones individuales. [1].
Conclusión
En resumen, la UPA fue generalmente bien tolerada. El perfil de seguridad es comparable para la EA, la AR, la APs y la EA, aunque la incidencia de acontecimientos adversos varía debido a las diferencias en la población de pacientes y las comorbilidades relacionadas con la enfermedad. Incluso con un tratamiento a largo plazo con AUP de hasta 5,5 años o 2,75 años en la EA, no se detectaron nuevas señales de seguridad.
La publicación completa de Burmester et al. puede consultarse aquí.
JAK: Janus quinasa; TYK: tirosina quinasa; IMID: enfermedades inflamatorias inmunomediadas; EASI: índice de área y gravedad del eccema; HZ: herpes zóster; MACE: acontecimiento cardiovascular adverso mayor; CPNM: cáncer de piel no melanoma; UPA, upadacitinib; TEV, tromboembolismo venoso; TEAE, acontecimientos adversos emergentes del tratamiento; LDL-C, lipoproteína de baja densidad-colesterol; HDL-C, lipoproteína de alta densidad-colesterol; CPK, creatina fosfoquinasa.
Referencias:
1. Burmester, G.R., et al, Safety profile of upadacitinib over 15 000 patient-years across rheumatoid arthritis, psoriatic arthritis, ankylosing spondylitis and atopic dermatitis. RMD Open, 2023. 9(1).
2 Ali, F., J. Vyas y A.Y. Finlay, Counting the Burden: Dermatitis atópica y calidad de vida relacionada con la salud. Acta Derm Venereol, 2020. 100(12): p. adv00161.
3 Langan, S.M., A.D. Irvine y S. Weidinger, Dermatitis atópica. Lancet, 2020. 396(10247): p. 345-360.
4 Song, A., S.E. Lee, y J.H. Kim, Immunopathology and Immunotherapy of Inflammatory Skin Diseases.Immune Netw, 2022. 22(1): p. e7.
5 Silvestre JF et al. Carga en el mundo real en pacientes con dermatitis atópica candidatos a terapia sistémica y que actualmente no reciben terapia sistémica, ningún tratamiento, terapia tópica sola o terapia sistémica: resultados de un estudio multinacional en el mundo real. EADV, Milán, 7-11 de septiembre de 2022. Sesión oral FC02.02.
6 Megna, M., et al, Tratamiento sistémico de la dermatitis atópica del adulto: una revisión. Dermatol Ther (Heidelb), 2017. 7(1): p. 1-23.
7. información actualizada para profesionales sanitarios RINVOQ® (upadacitinib) en www.swissmedicinfo.ch
Los profesionales pueden solicitar las referencias en medinfo.ch@abbvie.com.
Autor: Dra. Corinne Peter
Breve información técnica RINVOQ
Este artículo ha sido elaborado con el apoyo financiero de AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-RNQD230038_11/2023
Contribución en línea desde el 23.10.2023
Este artículo se publicó en alemán
Puesto actualizado: 17.11.2023












