La nefroprotección incluye intervenciones que ralentizan el declive de la TFG con el tiempo, retrasando así la insuficiencia renal terminal. La última intervención es el uso de inhibidores de SGLT2 en pacientes con nefropatía diabética.
La insuficiencia renal crónica puede diagnosticarse de dos maneras:
- Evidencia de deterioro de la función renal con una tasa de filtración glomerular calculada (eGFR) inferior a 60 ml/min, persistente durante al menos tres meses.
- Evidencia de daño renal crónico (albuminuria, hematuria, pruebas de imagen como riñones poliquísticos) persistente durante al menos tres meses – independientemente del eGFR.
Así pues, el diagnóstico de la insuficiencia renal crónica puede realizarse en la práctica con tres sencillos exámenes: Determinación de la creatinina (calcular el FGe a partir de ésta), estado de la orina con sedimento y proteinuria (orina puntual) y ecografía renal.
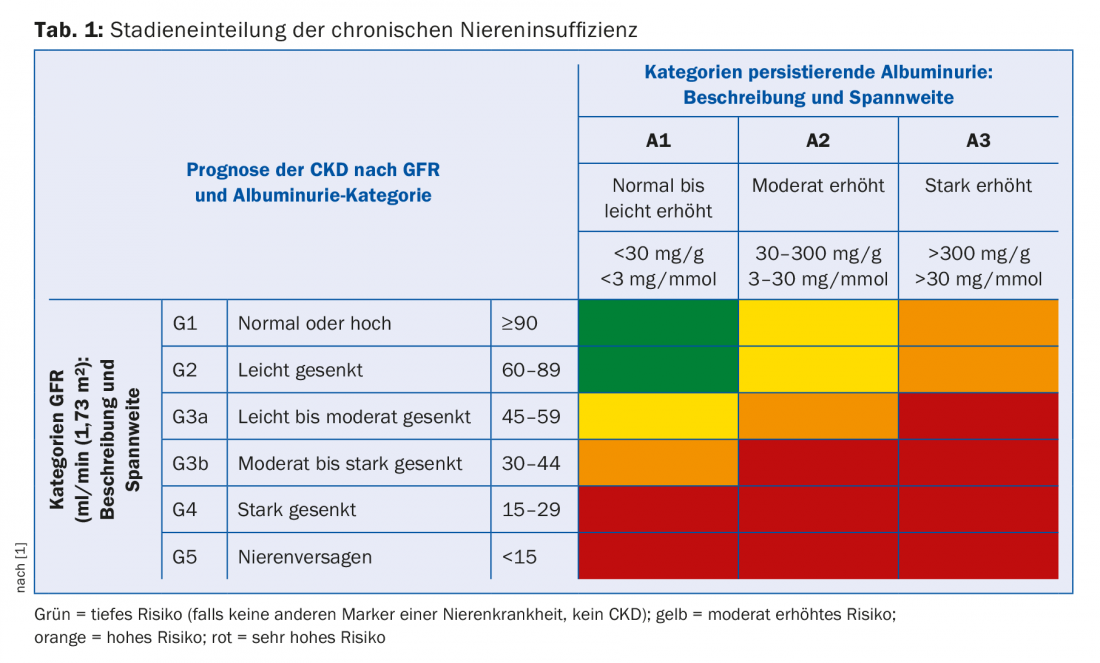
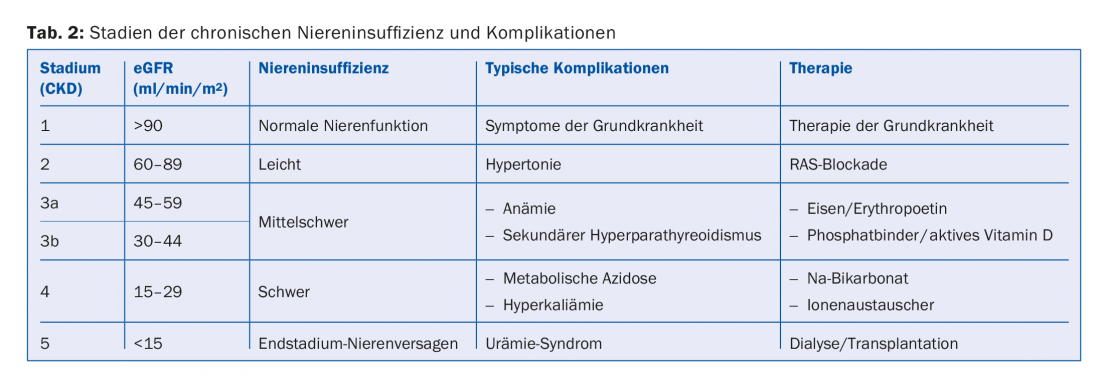
En función del grado de deterioro de la función renal y de la albuminuria, se procede a la estadificación de la insuficiencia renal crónica. El FGe y la albuminuria son factores de riesgo independientes tanto para la mortalidad cardiovascular como para el riesgo de desarrollar insuficiencia renal terminal [1]. Por lo tanto, la estadificación indica la frecuencia con la que debe controlarse a estos pacientes y la agresividad con la que deben tratarse en relación con los riesgos cardiovasculares (tab. 1). Además, el grado de deterioro de la función renal indica qué complicaciones secundarias cabe esperar (tab. 2). Deben buscarse activamente y, si es necesario, tratarse.
Curso
La insuficiencia renal crónica es progresiva a lo largo de los años, independientemente de que la enfermedad subyacente siga activa o no. Este fenómeno se explica por la llamada “hipótesis de Brenner”, que afirma que con la pérdida de un mayor número de nefronas, las nefronas restantes compensan al menos parcialmente la pérdida de función y por tanto hiperfiltran. Esta hiperfiltración, que dura mucho tiempo, provoca daños en las nefronas aún intactas. Histológicamente, puede detectarse primero una hipertrofia glomerular, seguida de una glomeruloesclerosis creciente, que da lugar a una pérdida progresiva de la función y a la aparición de albuminuria.
La progresión de la insuficiencia renal crónica puede describirse individualmente por paciente con la denominada curva de Mitch [2]. Si se traza la TFGe o el valor 1/creatinina a lo largo del tiempo, se obtiene una curva lineal decreciente. Con esta curva, se puede estimar el riesgo de desarrollar insuficiencia renal terminal para un paciente individual (Fig. 1A). Esto facilita la discusión con el paciente y permite hacer los preparativos oportunos para el inicio de un procedimiento de sustitución renal.
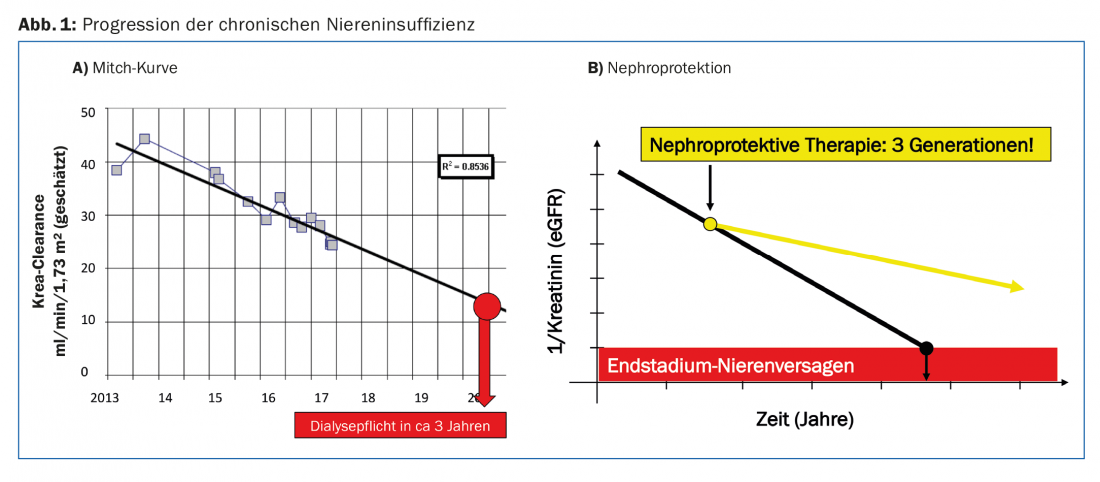
Como médicos, nos gustaría influir favorablemente en la evolución de la insuficiencia renal crónica. Por “medidas nefroprotectoras” entendemos todas las intervenciones que ralentizan el descenso del FGe con el paso del tiempo. Hasta la fecha, no ha habido ninguna intervención para detener por completo este despilfarro. Pero si la caída de la curva Mitch puede aplanarse sólo un poco, el paciente puede ganar varios años de tiempo sin diálisis (Fig. 1B).
Nefroprotección
Primera generación – bloqueo del sistema renina-angiotensina: El sistema renina-angiotensina (SRA) interviene de forma crucial en la regulación del flujo sanguíneo renal y, por tanto, en la perfusión de cada uno de los glomérulos. La angiotensina influye directamente en el tono de los conductos eferentes. Una mayor cantidad de angiotensina provoca la constricción de los conductos eferentes y, por tanto, un aumento de la presión de filtración en el lecho capilar glomerular. Por un lado, esto permite la autorregulación de la filtración glomerular en una amplia gama de fluctuaciones de la presión arterial. Por otro lado, también conduce a la hiperfiltración antes mencionada en el marco de la hipótesis de Brenner. El bloqueo del SRA con inhibidores de la ECA, bloqueantes de los receptores de angiotensina de tipo 1 (sartanes) o inhibidores de la renina provoca la dilatación del vaso eferente en el glomérulo. Esto reduce la presión de perfusión glomerular y protege el lecho capilar glomerular. Al mismo tiempo, sin embargo, la tasa de filtración glomerular por nefrona y global disminuye. Por lo tanto, el inicio del bloqueo del SRA en un paciente con insuficiencia renal siempre conlleva un aumento de la creatinina. Dicho aumento puede tolerarse hasta un 25%, siempre que posteriormente se mantenga estable en este nivel. El aumento de la creatinina es funcional y prueba que la presión de perfusión glomerular podría efectivamente disminuir. Si se interrumpe de nuevo el bloqueo del SRA, la creatinina vuelve a descender en el mismo valor. Si el nivel de creatinina no se estabiliza tras la introducción del bloqueo del SRA, debe suspenderse de nuevo y buscarse una estenosis de la arteria renal.
Varios ensayos aleatorizados realizados en la década de 1990 demostraron que el bloqueo del SRA puede ralentizar la progresión de la insuficiencia renal crónica, tanto en la nefropatía diabética como en la no diabética [3]. Así pues, el bloqueo del SRA es ahora la base de cualquier intervención nefroprotectora y debe ser más agresivo cuanto mayor sea la proteinuria. Las sustancias individuales deben dosificarse al máximo; debe evitarse estrictamente el doble bloqueo del SRA [4].
Segunda generación – corrección de la acidosis metabólica: El riñón es el principal órgano de excreción de los ácidos fijos, y éstos se acumulan con la restricción creciente de la función renal. Por lo tanto, la insuficiencia renal crónica suele asociarse a la aparición de acidosis metabólica, especialmente en los estadios avanzados a partir de la ERC G3b.
La acidosis metabólica tiene varios efectos desfavorables. Deteriora la salud ósea y favorece la aparición de hiperpotasemia, que a su vez aumenta el riesgo de arritmias cardiacas. Sin embargo, durante mucho tiempo no estuvo claro si la acidosis metabólica influye por sí misma en la progresión de la insuficiencia renal crónica. En la década de 2000, se publicaron varios ensayos aleatorios que investigaron el efecto del tratamiento de la acidosis metabólica con bicarbonato sódico en la progresión de la insuficiencia renal crónica. Para sorpresa de muchos nefrólogos, se ha demostrado que en varias fases de la insuficiencia renal crónica (ERC G2, G3 y G4) se puede ralentizar la progresión y retrasar la aparición de la insuficiencia renal terminal con esta sencilla medida [5]. Por ello, actualmente es una recomendación general que la acidosis metabólica con un bicarbonato sérico <20 mmol/l se trate con bicarbonato sódico. Esto también mejora la hiperpotasemia, lo que a su vez permite mantener el bloqueo del SRA más eficaz.
Las limitaciones de esta intervención suelen ser la tolerabilidad (el bicarbonato sódico provoca flatulencia), el elevado número de comprimidos (para conseguir un bicarbonato sérico >20 mmol/l, a veces se necesitan de seis a ocho comprimidos al día) y la carga de sodio, que puede provocar un aumento del edema y/o de la tensión arterial.
Tercera generación – bloqueo del cotransportador de sodio/glucosa SGLT2 en el túbulo proximal : En los últimos años, se ha probado un nuevo grupo de fármacos antidiabéticos orales en varios ensayos aleatorizados: Se trata de inhibidores del cotransportador de sodio/glucosa en el túbulo proximal (SGLT2, “sodium-glucose transporter 2”). Estos fármacos inducen glucosuria. El resultado es una mejor HbA1c y un balance calórico negativo que conlleva una pérdida neta de peso. Sin embargo, al mismo tiempo, el bloqueo de SGLT2 también produce natriuresis. Estas sustancias constituyen así una nueva clase de diuréticos que, a diferencia de los diuréticos de asa y las tiazidas, no actúan en la nefrona distal sino en el túbulo proximal.
Hasta ahora, los inhibidores de SGLT2 se han probado principalmente en pacientes con diabetes de tipo 2 y un perfil de riesgo cardiovascular elevado (a menudo en prevención secundaria). Se demostró un beneficio altamente significativo sobre la mortalidad por todas las causas (empagliflozina) y la mortalidad cardiovascular (empagliflozina, canagliflozina). Debido al efecto diurético, también podrían reducirse significativamente las rehospitalizaciones por insuficiencia cardiaca descompensada [6,7].
Los estudios de seguimiento también han demostrado ahora un efecto positivo altamente significativo sobre los puntos finales renales duros (nueva aparición de macroalbuminuria, duplicación de la creatinina sérica, aparición de insuficiencia renal terminal). ¡El efecto es del mismo orden de magnitud que el bloqueo del SRA en un grupo de pacientes que en su mayor parte ya está tratado con bloqueantes del SRA [8]! El mecanismo de nefroprotección aún no se ha aclarado en detalle. Sin embargo, se postula un efecto a través de la mácula densa con dilatación de los conductos aferentes. Se ha demostrado el mismo aumento de la creatinina funcional al inicio del tratamiento con estabilización posterior de la función renal que con el bloqueo del SRA [9].
Deben señalarse dos efectos secundarios clínicos con esta clase de sustancias: Frecuentes pero inofensivas son el aumento de las infecciones urogenitales, que pueden tratarse fácilmente. Una complicación rara pero grave es la cetoacidosis diabética euglucémica, que puede producirse con deficiencia de insulina y largos periodos de ayuno. Por lo tanto, en las situaciones clínicas enumeradas en la tabla 3, los inhibidores de SGLT2 no deben utilizarse o sólo deben utilizarse con gran precaución o suspenderse temporalmente.

Conclusión
Tras el bloqueo del SRA y la terapia de la acidosis metabólica, disponemos desde hace dos años de una tercera medida nefroprotectora: el uso de inhibidores de SGLT2. Actualmente sólo está aprobado para pacientes con nefropatía diabética (tab. 4) . Dado que lo más probable es que el mecanismo de nefroprotección no tenga nada que ver con la influencia sobre el metabolismo de la glucosa, sino con el efecto diurético de estas sustancias, cabe suponer que también actuarían en la nefropatía no diabética. Los estudios correspondientes están actualmente en curso.

Mensajes para llevarse a casa
- La insuficiencia renal crónica tiene un curso progresivo que puede describirse con la curva de Mitch.
- Por medidas nefroprotectoras entendemos las intervenciones que pueden ralentizar el descenso del FG con el tiempo y retrasar así la insuficiencia renal terminal.
- La base de cualquier nefroprotección es el uso de inhibidores del sistema renina-angiotensina (inhibidores de la ECA, bloqueadores de los receptores AT1, inhibidores de la renina). Deben dosificarse según la tolerancia, pero no combinarse.
- El tratamiento de la acidosis metabólica con bicarbonato sódico es nefroprotector y debe iniciarse con un bicarbonato sérico <20 mmol/l.
- La última intervención es el uso de inhibidores de SGLT2 en pacientes con nefropatía diabética. Tienen un efecto diurético en el túbulo proximal y son cardioprotectores y nefroprotectores.
Literatura:
- Stevens PE, Levin A: Evaluación y tratamiento de la enfermedad renal crónica: sinopsis de la guía de práctica clínica Enfermedad renal: mejora de los resultados globales 2012. Ann Intern Med 2013; 158: 825-830.
- Mitch WE, et al: Un método sencillo para estimar la progresión de la insuficiencia renal crónica. Lancet 1976; 2: 1326-1328.
- Lewis EJ, et al: El efecto de la inhibición de la enzima convertidora de angiotensina en la nefropatía diabética. El Grupo de Estudio Colaborativo. N Engl J Med 1993; 329: 1456-1462.
- Luft FC: Perspective on combination RAS blocking therapy: off-TARGET, dis-CORD, MAP-to-nowhere, low ALTITUDE, and NEPHRON-D. Am J Nephrol 2014; 39: 46-49.
- de Brito-Ashurst I, et al: La suplementación con bicarbonato ralentiza la progresión de la ERC y mejora el estado nutricional. J Am Soc Nephrol 2009; 20: 2075-2084.
- Zinman B, et al: Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015; 373: 2117-2128.
- Neal B, et al: Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med 2017; 377: 644-657.
- Wanner C, et al: Empagliflozina y progresión de la enfermedad renal en la diabetes tipo 2. N Engl J Med 2016; 375: 323-334.
- Anders HJ, et al: Protección de la nefrona en la enfermedad renal diabética. N Engl J Med 2016; 375: 2096-2098.
PRÁCTICA GP 2018; 13(4): 22-25
CARDIOVASC 2019; 18(5): 6-9